基于冠脉CTA成像乳内动脉-前降支吻合口血流动力学数值模拟*
黄信生,周萍,乔瑞国,李海涛,顾承雄,杨俊峰
(首都医科大学附属北京安贞医院-北京市心肺血管疾病研究所心脏外科,北京 100029)
临床上左乳内动脉是冠状动脉旁路移植术的最佳移植血管,但是人们对左乳内动脉-前降支吻合口部位的血液动力学依然知之甚少,而这些血液动力学参数对吻合口远期通畅性有重要意义[1-4]。目前,在人体内进行血液流动特性参数的测量存在较大困难,而应用计算流体力学方法(computational fliud dynamics,CFD)可准确得到移植血管内血流动力学特征参数,对了解吻合口狭窄的发病机制及临床上预防与治疗均具有重要意义[1-8]。随着新型医学成像设备(如螺旋CT等)的快速发展,血管三维重构技术得以实现,可通过重构冠状动脉三维血管模型进行血流动力学特性分析[4-8]。因此,本研究采用CFD方法,建立吻合口三维血管模型,进行相关血流动力学参数分析,为研究吻合口的血流动力学机制,以及血流动力学参数变化与临床的相关性提供实验依据。
1 资料与方法
1.1 模型的建立 将在北京安贞医院行冠状动脉旁路移植术的患者冠脉CTA扫描数据导入到MINICS软件中进行三维重建,经过阈值分割、布尔运算以及三维图像分割等步骤获得搭桥冠状动脉三维实体模型(图1)。然后在3D-matic中对实体模型表面进行优化,并输出STL格式的面网格文件。

图1 三维实体模型
在有限元划分软件ANSYS ICEM中导入STL文件,使用非结构四面体网格进行体网格划分,在靠近壁面处采用三棱柱边界层网格以提高计算精度,体网格数共计130882个(图2a)。边界层近壁面网格宽0.05mm,其后网格宽度以1.06倍速率增长,共 5 层(图 2b)。

图2 a体网格模型

图2 b边界层网格
1.2 边界条件 在ANSYS CFX 17.1中进行搭桥吻合口处血液流动数值模拟。边界条件如图3所示:冠状动脉和移植管均采用入口截面平均脉动速度[7]。入口速度随时间的变化曲线如图4所示,心动周期为0.8s。
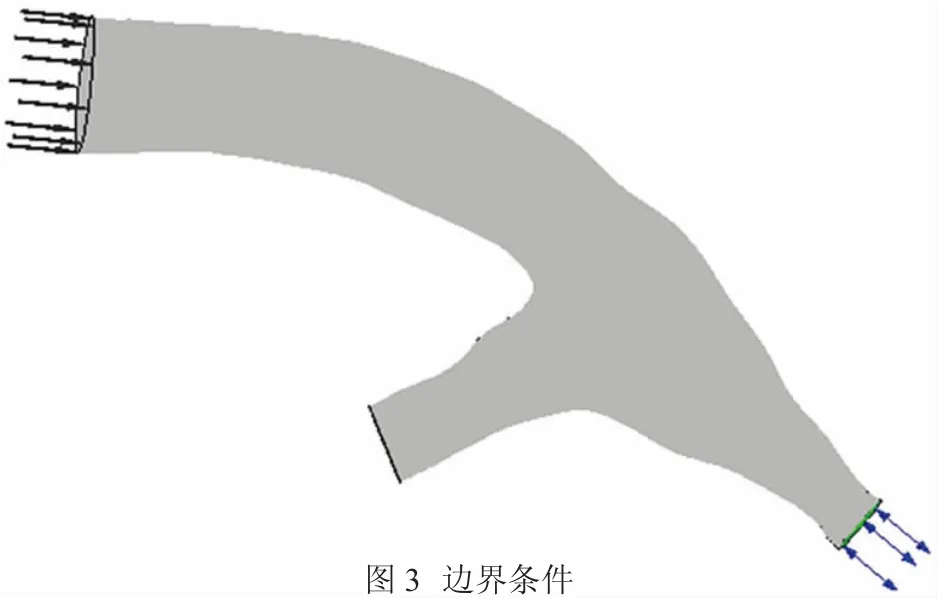
图3 边界条件
数值模拟采用如下假设:血管壁为刚性、无滑移以及无渗透壁面;血液流动为非定常,绝热的层流,自由流出口;入口速度模型如图4所示。心动周期T=0.8s,前0.3s为心脏收缩期,0.3-0.8s为心脏舒张期,且血管中始终有血液流动。

图4 一个心动周期内进口速度
因为生理状态下的血液属于一种粘弹性的悬浮介质,是非牛顿流体,因此采用Carreau模型来表达血液的非牛顿特性。资料显示,Carreau与实验血流环境十分接近[4-6]。
计算采用有限体积法,数值模拟基于满足质量守恒定律和动量守恒定律,即连续方程和Navior-Stroke 方程[2,3]。
数值模拟采用商业软件ANSYS CFX 17.1中完成计算,残差设定为1X10-5,在计算中每个心动周期为0.8s,并均分为100个时间步(每个时间步为8ms),且满足时间无关性要求。待血流在血管模型内充分发展2个心动周期,最后选取第3个心动周期的数据进行分析。
2 数值模拟结果
数值模拟结果分为速度场、压力和壁面切应力。
2.1 吻合口的速度场 图5为模型中乳内动脉的血液流动速度平均值在一个心动周期内随时间变化的曲线。无论是收缩期还是舒张期,模型中搭桥管内的血液始终流向冠脉循环,舒张期血液流动速度值明显大于收缩期,这与冠脉循环中舒张期心脏供血理论一致。由于血管完全阻塞,冠状动脉与移植管的流量差使得血液快速从移植管中流向冠状动脉,在缝合前端位置下血管中心区域出现了高速度区域,最大速度可达到1.07m/s,但缝合前端下游出现了低速度区域,最小速度低至0.07m/s。从图6移植血管速度云图中可看出,冠状动脉的径向速度并不成对称分布,同一径向位置有较大的速度差,缝合前端的低速度区域会出现剧烈粒子停滞,局部回流和紊流等现象,并形成了血流停滞区。
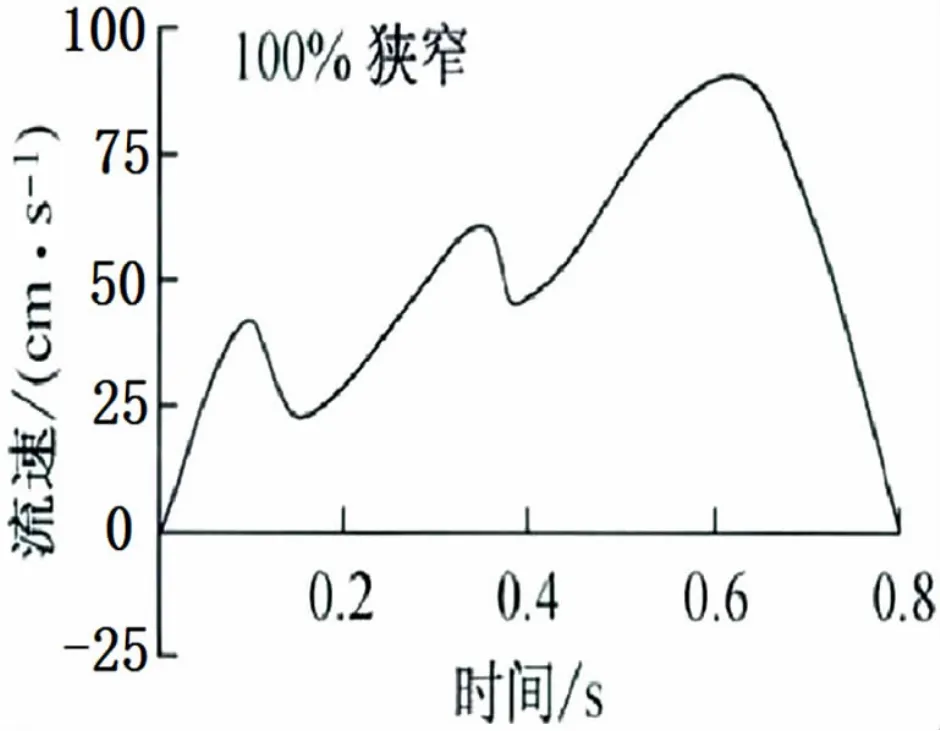
图5 吻合口内血流的心动周期流速图

图6 吻合口流速云图
2.2 压力分布 如图7所示为冠状动脉轴线上压力的时空分布,显示了吻合口模型在一个心动周期不同时刻0.2、0.3和0.8s纵向剖面的压力分布图,由图可见,在整个心动周期中,冠状动脉轴线上的压力随入口流量的增减而增减。在冠状动脉狭窄处,因血液的射流作用,速度较大而压力较低。同理在缝合区,压力也有一定的下降。模型中吻合口两端的压差比较大,吻合口前端部位的压力等值线比较密集,说明大部分的压降主要集中在此处。
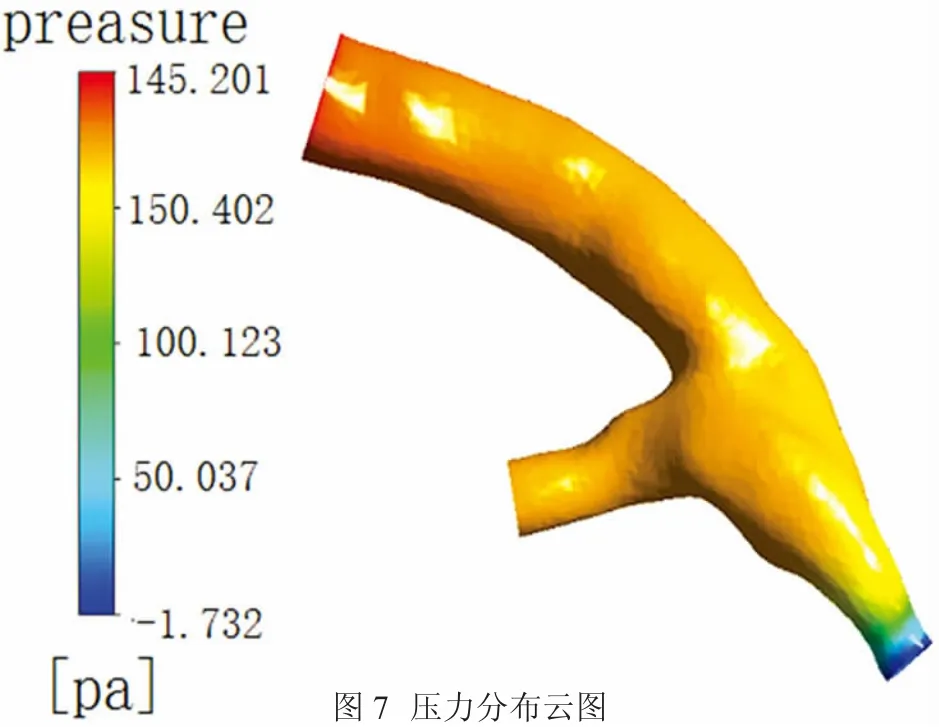
图7 压力分布云图
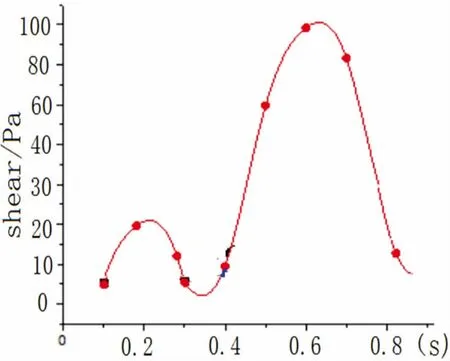
图8 压力随心动周期时间变化曲线图
2.3 壁面切应力 本研究展示了吻合口模型在一个心动周期内不同时刻0.12和0.24s壁面切应力分布云图(图7)。模型中吻合口周围的壁面切应力分布不均匀,约为0.25~60Pa,壁面切应力随吻合区入口速度梯度的增减而增减,高壁面切应力主要集中在前端吻合口附近。
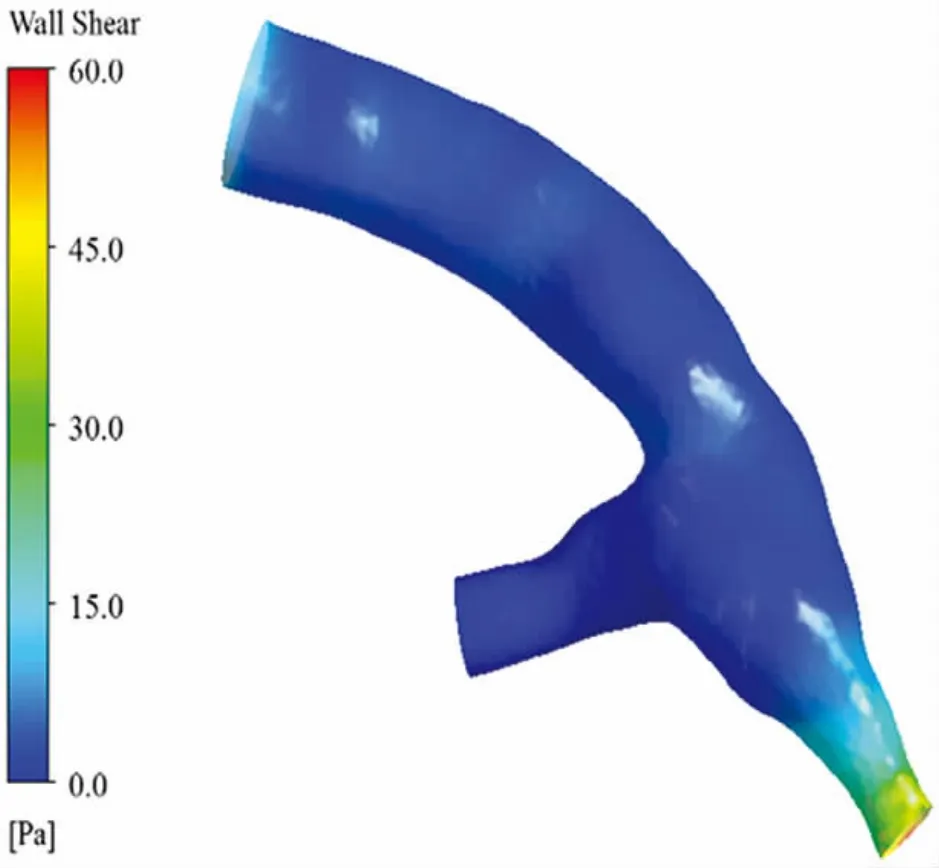
图9 壁面切应力分布云图

图10 壁面切应力心动周期内分布云图
3 讨论
目前CFD数值模拟技术在医学相关研究中已广泛应用,利用计算流体力学的方法对冠脉旁路移植术的血流动力学进行分析,是目前十分常见而且有效的研究方法[2,3,9,10]。 本研究采用该技术,冠状动脉吻合口模型提取于冠脉搭桥术后CT图像,具有个性化的解剖结构,可深刻,更接近于实际情况了解冠状动脉搭桥缝合区的血液流动情况。本研究发现左乳内动脉-前降支吻合口部位血流动力学参数存在变化、波动,并具有明显的区域分布特征,且与搭桥手术后再狭窄主要发生在吻合口缝合处存在临床相关性。
大量研究表明血管再狭窄与血流动力学参数有关[2-5,10-13]。本研究数值模拟结果表明,移植血管吻合口处血液的速度并不成对称分布,同一径向位置有较大的速度差,特别是缝合前端的有低速度区域,存在严重的涡流及二次流的位置;其次压力分布图显示在一个心动周期0.3s和0.6s时刻纵向剖面的压力分布,吻合口两端的压差比较大,大部分的压降主要集中在前端吻合口部位,这与吻合口缝合区下游的血管壁内膜增生,导致冠脉旁路移植术后血管再狭窄和手术失败的临床问题一致[1-6,11-13]。
血流动力学参数以壁面剪应力、压力与流速等指标研究较多,它们被认为与冠状动脉、颈动脉以及周围大动脉的血管分叉及转角处等形态学变化明显处的粥样硬化形成及狭窄密切相关[12-15]。故获得冠状动脉搭桥缝合区的血流动力学特性如血管壁面剪应力、回流、二次流等信息对研究桥血管通畅性的生理和病理机制具有重要意义。在动脉搭桥效果较差位置出现了低壁面剪切应力和高震荡剪切指数,这些血液动力学参数可用来评定搭桥术吻合口疗效的优劣程度[2-5,12-17]。
研究表明计算流体动力学技术在临床影像血管模型重建上一直有很好的应用,可以准确的模拟复杂血管结构的血流状态[7-10,16-17]。 一旦确定了缝合区病变的重要血流动力学参数,外科医生就可以优化吻合口结构来达到最优的血流动力学,保证主动脉流来的血液能顺畅地流入移植血管中,减缓近端吻合区的内膜增生和血小板的活化,进而减缓远端吻合区内膜增生,提高冠状动脉搭桥术的长期通畅率。吻合区血流动力学的研究将有助于改善动脉搭桥术的临床成功率。
(感谢:王宁博士,黄斌教授,北京理工大学流体力学系,提供血流动力学分析)
参考文献
[1]Hofer M,Rappitsch G,Perktold K,et al.Numerical study of wall mechanics and fluid dynamics in end-to-side anastomoses and correlation to intimal hyperplasia[J].J Biomech,1996,29(10):1297-1308.
[2]LeuprechtA,Perktold K,ProsiM,etal.Numericalstudy of hemodynamicsand wallmechanicsin distalend-to-side anastomoses of bypass grafts[J].J Biomech,2002,35(2):225-236.
[3]刘有军,乔爱科,黄伟,等.冠状动脉移植管的血流动力学数值模拟[J].中国生物医学工程学报,2004,(4):370-376+310.
[4]Ballarin F,Faggiano E,Manzoni A,et al.Numerical modeling of hemodynamics scenarios of patient-specific coronary artery bypass grafts[J].Biomech Model Mechanobiol,2017,16(4):1373-1399.
[5]Owida AA,Do H,Morsi YS.Numerical analysis of coronary artery bypass grafts:an over view[J].Comput Methods Programs Biomed,2012,108(2):689-705.
[6]Meirson T,Orion E,Avrahami I.Numerical analysis of Venous External Scaffolding Technology for Saphenous Vein Grafts[J].J Biomech,2015,48(10):2090-2095.
[7]陈亮.冠脉CT成像技术在冠心病诊断中的应用[J].江西医药,2016,51(9):969-971.
[8]蔡小婕,冯蓓莉,江隆福.16层螺旋CT冠状动脉显像和平板运动试验在诊断冠心病中的应用[J].江西医药,2007,42(11):971-973.
[9]Hajati O,Zarrabi K,Karimi R,et al.CFD simulation of hemodynamics in sequential and individual coronary bypass grafts based on multislice CT scan datasets[J].Conf Proc IEEE Eng Med Biol Soc,2012,2012:641-4.
[10]刘赵淼,高立丹,史艺.基于CT成像的冠状动脉搭桥血管的流固耦合分析[J].北京工业大学学报,2013,39(8):1255-1260.
[11]Mortazavinia Z,Arabi S,Mehdizadeh AR.Numerical investigation of angulation effects in stenosed renal arteries[J].J Biomed Phys Eng,2014,8;4(1):1-8.
[12]Chen J,Lu XY.Numerical investigation of the non-Newtonian pulsatile blood flow in a bifurcation model with a non-planar branch[J].J Biomech,2006,39(5):818-832.
[13]罗文香,程云章,胡嵬锋,等.冠状动脉搭桥血流动力学数值模拟[J].生物医学工程学进展,2014,35(3):125-128.
[14]刘有军,乔爱科,黄伟,等.冠状动脉移植管的血流动力学数值模拟[J].中国生物医学工程学报,2004,(4):370-376+310.
[15]乔爱科,刘有军.具有不同移植管-宿主动脉直径比的冠状动脉搭桥术的血流动力学仿真比较 [J].中国生物医学工程学报,2006,(4):453-459+471.
[16]Cecchi E,Giglioli C,Valente S,et al.Role of hemodynamic shear stress in cardiovascular disease[J].Atherosclerosis,2011,214(2):249-256.
[17]Dong J,Inthavong K,Tu J. Image-based computational hemodynamics evaluation of atherosclerotic carotid bifurcation models[J].Comput Biol Med,2013,43(10):1353-1362.

