脯氨酰寡肽酶抑制剂体外对肝星状细胞凋亡、增殖和肝纤维化相关基因表达的影响*
周达,王晶,李冰航,孙超,陈源文,范建高
脯氨酰寡肽酶(prolyloligopeptidase,POP,EC 3.4.21.26)是一种能特异性水解不多于30~40个氨基酸短肽中脯氨酸残基羧基端肽键的丝氨酸蛋白酶,如水解血管紧张素、P物质、胸腺素β4等[1]。POP通过水解酶活性或与其他蛋白间相互作用在体内发挥重要的生理功能,参与多肽的生成与代谢、细胞增殖与分化、体内炎症与代谢等[2,5]。更为重要的是,与其他组织相比,肝脏内POP的活性是最高的,同时肝内还存在如辅酶A这样能够调节POP活性的内源性物质,提示其在肝内可能具有重要的病理生理功能[4,6,7]。已有研究显示POP参与肝内炎症及肝细胞的增殖和分化,肝细胞内POP活力与肝细胞增殖和分化成熟密切相关[7-9],而肝内POP活性降低导致的N-乙酰基-丝氨酸-天冬氨酸-赖氨酸 -脯氨酸(N-acetyl-seryl aspartyl-lysyl-proline,Ac-SDKP)生成不足,是肝内持续炎症反应、肝细胞损伤和细胞外基质过度沉积的关键因素[10-13]。肝脏炎症和纤维化的发生发展机制复杂,至今仍无有效的治疗方法[14]。肝星状细胞(hepatic stellate cell,HSC)是肝纤维化发生发展的关键因素,大鼠HSC-T6细胞系性能稳定,可连续传代,已被广泛应用于实验研究[15]。本研究应用S17092抑制HSC内POP活性,了解POP在HSC生物学功能发挥及其对肝脏炎症和纤维化发生相关基因的影响,以期探索POP在肝脏炎症和纤维化发生发展中的作用。
1 材料与方法
1.1 细胞培养 大鼠HSC-T6细胞购自中国科学院上海生命科学研究院细胞资源中心。根据实验需要,取HSC-T6以适当密度接种于不同大小培养皿中,培养液为10%FBS/DMEM培养基(血清和培养基购自GIBCO,USA),置于含5%CO2孵育箱中,培养细胞处于良好生长状态时进行下列相关实验。选择 S17092(购自 Sigma-Aldrich,USA)作为 POP 酶抑制剂[7]。
1.2 细胞内Ac-SDKP检测 采用ELISA法检测,取HSC-T6 细胞,加入 S17092(0、5、10 μg/ml)共孵育24 h,按试剂盒说明书(购自SPI Bio and CEA,France),先使用 RIPA(含 10 μmol/l卡托普利和 1 mmol/l PMSF)裂解细胞,随后进行HSC内Ac-SDKP浓度测定。通过各组细胞数校正Ac-SDKP终浓度,计算出每 1×106个细胞中 Ac-SDKP的量,以nM/106表示。
1.3 细胞增殖检测 将HSC-T6(约1×103)接种于96 孔板,与不同浓度的 S17092(0、5、10、25、50、100 μg/ml)共孵育24 h和48 h,每个浓度设置5个复孔,每孔加入新鲜培养液100μl,同时设立空白对照组。随后每孔加入CCK-8试剂10μl,避光37℃孵育 2 h,在酶标仪(uQuant,Biotek,USA)测定每孔450 nm处吸光度(OD值)。计算48 h每个浓度下细胞生长抑制率,抑制率=(1-处理组吸光度/对照组吸光度)×100%,所有组别吸光度均先减去空白孔吸光度。
1.4 细胞凋亡检测 取HSC-T6细胞,与S17092(0、5、10μg/ml)共孵育24 h,使用不含EDTA的胰酶(购自GIBCO,USA)消化提取细胞。使用流式细胞仪检测HSC-T6凋亡,具体步骤参照AnnexinVPE/7-AAD凋亡试剂盒说明书(Becton-Dickinson,USA)进行。
1.5 基因转录检测 采用实时定量PCR法检测,取HSC-T6,经 S17092(0、5、10μg/ml)孵育 24 h,采用Trizol(Takara)法提取RNA,并测定其浓度和纯度。应用逆转录试剂盒将其逆转录为cDNA(primescriptRTmaster mix,Takara),采用实时荧光定量 PCR 法(SYBR Premix Ex Taq,Takara,仪器为Biosystems7500 Real-timePCR system)检测转化生长因子 -β1(transforminggrowth factor β,TGF-β1)、α-平滑肌肌动蛋白(α smooth muscle actin,α-SMA)、单核细胞趋化蛋白-1(monocyte chemoattractant protein 1,MCP-1)、Ⅰ型胶原(collagen I,Col I)相关基因mRNA水平,各设3个复孔,各基因引物由生工生物工程(上海)股份有限公司合成(表1),其相对水平(RQ 值)以 2-ΔΔCt表示。

表1 Realtime-PCR引物序列
1.6 蛋白表达检测 采用Western blot法,取HSC-T6,经 S17092(0、5、10μg/ml)孵育 24 h,使用1 mmol/L的RIPA+PMSF提取细胞蛋白(购自碧云天生物技术有限公司),采用BCA法(碧云天生物技术有限公司)测定各组蛋白浓度。随后,进行SDS-PAGE电泳,转膜,5%BSA封闭2 h,加各目的蛋白一抗孵育(4℃过夜),1×TBST洗膜10~15 min×3次,加二抗孵育 1~2 h,1×TBST洗膜 10~15 min×3次,最后使用辣根过氧化物酶法检测(购自 Millipore Corporation,Billerica,USA),使用 Image Lab分析蛋白显影条带。抗POP、抗TGF-β1、抗α-SMA抗体均购自 Sigma-Aldrich公司,抗p-Smad2/3抗体购自巴傲得生物科技有限公司,Smad7和PPAR-γ购自生工生物工程上海股份有限公司,相关二抗和Westernblot相关试剂购自碧云天生物技术有限公司。
1.7 统计学分析 应用SAS(Release 8.02 TS Level 02M0,NC,USA)统计软件进行统计学处理,计量资料以±s表示,两组间比较采用t检验,对方差不齐或非正态分布的计量资料以M(IQR)表示,采用秩和检验。以P<0.05表示差异有统计学意义。
2 结果
2.1 细胞增殖和细胞内Ac-SDKP水平变化 经过不同浓度的S17092抑制POP酶活性后,发现HSC内Ac-SDKP水平较对照组显著下降,其中10μg/ml S17092处理后下降约 50%(图 1A);50 μg/ml和100 μg/ml S17092对HSC-T6细胞呈现明显的细胞毒性,而与对照组相比,低浓度组(5、10、25μg/ml) 则能抑制 HSC-T6 增殖 (图 1B),25μg/ml浓度组作用48 h时HSC增殖抑制率达40%(图 1C)。
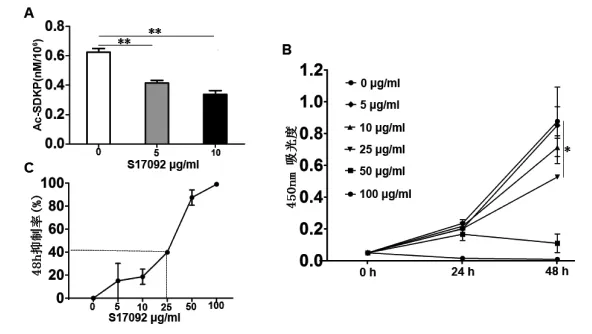
图1 HSC-T6细胞生长抑制率
2.2 POP抑制剂对HSC-T6细胞凋亡及其相关基因水平的影响 经流式细胞仪检测发现,虽然低浓度S17092(5、10μg/ml)组细胞凋亡比例较对照组稍增多,但差异无统计学意义(图2A);HSC-T6经过S17092(5、10μg/ml)处理 24 h 后,发现细胞 MCP-1和α-SMA mRNA水平较对照组明显升高,MCP-1 mRNA在10μg/ml浓度组较对照组升高约1.5倍,α-SMA mRNA在10μg/ml处理组较对照组升高约2倍,各组TGF-β1和Col I基因水平无显著性差异(图2B)。
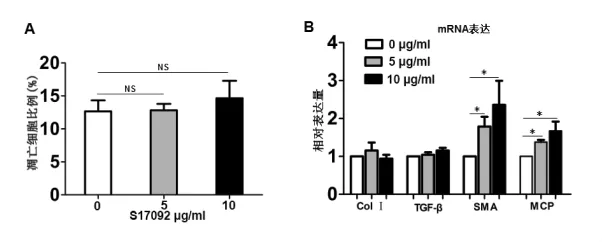
图2 HSC-T6细胞凋亡及其相关基因变化
2.3 POP抑制剂对HSC-T6细胞炎症和纤维化因子蛋白表达的影响 HSC-T6经过 S17092(5、10μg/ml)处理24 h后,发现细胞α-SMA蛋白表达较对照组升高,10μg/ml处理组较对照组表达增加约1.5倍;Smad7和PPAR-γ较对照组显著下降,在10μg/ml处理组分别较对照组下降约50%以上和10%左右,各组细胞POP、TGF-β1和p-Smad2/3蛋白表达无显著性差异(图3)。

图3 HSC-T6细胞炎症和纤维化相关蛋白表达变化
3 讨论
本研究结果提示POP在HSC细胞可能具有重要的病理生理功能,并与肝脏炎症及纤维化发生发展密切相关。POP可调节HSC分泌炎性因子MCP-1及分泌抗纤维化短肽Ac-SDKP,并通过调节Smad7和PPAR-γ的表达调控HSCs内TGF-β-Smad信号通路。
首先,Ac-SDKP为POP水解胸腺素β4(Tβ4)的产物[16]。一方面,POP抑制剂处理组细胞内Ac-SDKP水平显著下降,提示S17092成功抑制了HSC胞内POP酶活性;另一方面,大量研究证实Ac-SDKP抗机体实质器官包括心、肝、肾、肺等纤维化作用显著[10,17-21]。基于此,POP是否通过调节细胞内Ac-SDKP水平而发挥抗肝纤维化作用值得进一步探讨和验证。我们课题组在前期研究工作中已阐明Ac-SDKP在对抗四氯化碳诱导的肝纤维化及对抗胆总管结扎诱导的肝纤维化发病过程中作用显著[10,17]。前期研究结果显示Ac-SDKP可以抑制肝内TGF-β1及Smad2表达,而对Smad7无显著影响,可通过直接调节TGF-β1-p-Smad2/3通路抑制肝纤维化。本研究的靶标为POP,通过直接干预POP酶活性,发现HSC-T6细胞内TGF-β1-p-Samd2/3通路蛋白未发生显著变化,而Smad7表达却显著降低。Smad7的主要作用之一为抑制TGF-β1-pamd2/3信号通路,发挥抗纤维化作用。综合上述结果,提示POP除了酶解作用以外,还存在其他未知功能。已有研究提示POP除了水解酶功能外,还存在非酶功能,如可与其他蛋白相互结合,从而调控基因转录[22,23]。Tenorio-Laranga J et al[4]通过对大鼠体内POP进行长时间抑制,发现抑制组大鼠肝内提取的肽成分与对照组大鼠相比显著不同,这些改变的肽大部分源自线粒体,其功能主要是参与蛋白翻译。因此,以POP为靶向的干预对肝纤维化的调控可能并不依赖于抗纤维化短肽Ac-SDKP。
其次,本研究发现POP被抑制时,HSC-T6细胞生长亦被抑制,即POP调控HSC-T6的增殖生长,可能与肝内POP除了存在于胞质外,还定位于胞核有关。核内POP可能参与核转运和顺反异构酶的调节,进而调控细胞增殖[24]。我们既往的研究提示Ac-SDKP同样可抑制HSCs增殖[10],与本研究结果相反,从侧面反映POP这种直接调控细胞增殖作用与Ac-SDKP无明显关系,更多的是通过其胞内非酶作用调控基因转录所致。近年针对肿瘤细胞研究显示POP抑制剂阻碍细胞生长通过减少pRb和Ki-67蛋白的表达而增加p53、p27kip1和pRb2/p130 的表达[3,25]。因此,POP 抑制剂调控 HSCs增殖的具体机制还值得进一步探索。
肝纤维化主要表现为肝内炎症及细胞外基质沉积,HSCs起着至关重要的作用[26]。我们的研究结果显示,当HSCs胞内POP活性被抑制时可以引起α-SMA和MCP-1表达增高及PPAR-γ下调。α-SMA为活化HSC的标志蛋白,MCP-1为HSC分泌的主要促炎促纤维化的因子[27],同时PPAR-γ为HSCs处于非活化状态即静止储脂状态的标志蛋白,PPAR-γ还可以抑制HSCs的活化[28,29]。上述这些关键蛋白表达的变化提示当HSCs内POP被抑制时可以促进其致纤维化作用,这一效应是由于POP水解活性降低导致其下游产物Ac-SDKP减少所致,还是POP自身通过蛋白-蛋白相互作用所致,仍有待进一步探索,但不管何种机制,都说明POP或其下游产物Ac-SDKP均可抑制HSCs活性而有助于减轻肝纤维化[30]。
总之,POP在肝内的具体功能尚不清楚,尤其是POP自身与其下游产物Ac-SDKP的生物学效应和POP的非酶解功能还需要研究[31]。同时,尚需进一步行体内实验验证以POP为靶向的干预有无改善纤维化的作用。但总得来说,本研究通过POP抑制剂初步揭示了POP这一蛋白酶对HSCs的调节作用,其在抗肝纤维化方面的作用值得进一步探讨。
【参考文献】
[1]Babkova K,Korabecny J,Soukup O,et al.Prolyl oligopeptidase and its role in the organism:attention to the most promising and clinically relevant inhibitors.Future Med Chem,2017,9(10):1015-1038.
[2]Penttinen A,Tenorio-Laranga J,Siikanen A,et al.Prolyl oligopeptidase:a rising star on the stage of neuroinflammation research.CNS Neurol Disord Drug Targets,2011,10(3):340-348.
[3]Suzuki K,Sakaguchi M,Tanaka S,et al.Prolyl oligopeptidase inhibition-induced growth arrest of human gastric cancer cells.Biochem Biophys Res Commun,2014,443(1):91-96.
[4]Tenorio-LarangaJ,Mannisto PT,Storvik M,etal.Fourday inhibition of prolyl oligopeptidase causes significant changes in the peptidome ofratbrain,liver and kidney.Biochimie,2012,94(9):1849-1859.
[5]Maruyama Y,Matsubara S,Kimura AP.Mouse prolyl oligopeptidase plays a role in trophoblast stem cell differentiation into trophoblast giant cell and spongiotrophoblast.Placenta,2017,53:8-15.
[6]Yamakawa N,Shimeno H,Soeda S,et al.Inhibition of proline endopeptidase activity by acyl-coenzyme A esters.Biochim Biophys Acta,1990,1037(3):302-306.
[7]Zhou D,Li BH,Wang J,et al.Prolyl oligopeptidase inhibition attenuates steatosis in the L02 human liver cell line.Plos One,2016,11(10):e0165224.
[8]Yamakawa N,Shimeno H,Soeda S,et al.Regulation of prolyl oligopeptidase activity in regenerating rat liver.Biochim Biophys Acta,1994,1199(3):279-284.
[9]Matsubara Y,Ono T,Tsubuki S,et al.Transient up-regulation of a prolyl endopeptidase activity in the microsomal fraction of rat liver during postnatal development. Eur J Biochem,1998,252(1):178-183.
[10]Chen YW,Liu BW,Zhang YJ,et al.Preservation of basal AcSDKP attenuates carbon tetrachloride-induced fibrosis in the rat liver.J Hepatol,2010,53(3):528-536.
[11]周达,陈源文,范建高.脯氨酰寡肽酶的肝内生物学功能研究进展. 胃肠病学和肝病学杂志,2015,24(1):12-14.
[12]陈源文,董国芳,徐雷鸣,等.内源性AcSDKP及其前体胸腺素β4在四氯化碳致肝纤维化发生早期的变化.胃肠病学和肝病学杂志,2010,19(1):6-9.
[13]Tenorio-Laranga J,Montoliu C,Urios A,et al.The expression levels of prolyl oligopeptidase responds not only to neuroinflammation but also to systemic inflammation upon liver failure in rat models and cirrhotic patients.J Neuroinflamm,2015,12(1):183.
[14]Zoubek ME,Trautwein C,Strnad P.Reversal of liver fibrosis:From fiction toreality.BestPractResClin Gastroenterol,2017,31(2):129-141.
[15]Shang H,Liu X,Guo H.Knockdown of Fstl1 attenuates hepatic stellate cell activation through the TGFbeta1/Smad3 signaling pathway.Mol Med Rep,2017,[Epub ahead of print].
[16]Kumar N,Nakagawa P,Janic B,et al.The anti-inflammatory peptide Ac-SDKP is released from thymosin-beta4 by renal meprin-alpha and prolyl oligopeptidase.Am J Physiol Renal Physiol,2016,310(10):F1026-1034.
[17]Zhang L,Xu LM,Chen YW,etal.Antifibrotic effectof N-acetyl-seryl-aspartyl-lysyl-proline on bile duct ligation induced liver fibrosis in rats.World J Gastroenterol,2012,18(37):5283-5288.
[18]Kanasaki K,Nagai T,Nitta K,et al.N-acetyl-seryl-aspartyl-lysyl-proline:a valuable endogenous anti-fibrotic peptide for combating kidney fibrosis in diabetes. Front Pharmacol,2014,5:70.
[19]Nagai T,Kanasaki M,Srivastava SP,et al.N-acetyl-seryl-aspartyl-lysyl-proline inhibits diabetes-associated kidney fibrosis and endothelial-mesenchymal transition.Biomed Res Int,2014,2014:696475.
[20]Xiaojun W,Yan L,HongX,etal.Acetylated alpha-tubulin regulated by N-acetyl-seryl-aspartyl-lysyl-proline(Ac-SDKP)exerts the anti-fibrotic effect in rat lung fibrosis induced by silica.Sci Rep,2016,6:32257.
[21]Hrenak J,Paulis L,Simko F.N-acetyl-seryl-aspartyl-lysylproline(Ac-SDKP):Potential target molecule in research of heart,kidney and brain.Curr Pharm Des,2015,21(35):5135-5143.
[22]Myohanen TT,Garcia-Horsman JA,Tenorio-Laranga J,et al.Issues about the physiological functions of prolyl oligopeptidase based on its discordant spatial association with substrates and inconsistencies among mRNA,protein levels,and enzymatic activity.J Histochem Cytochem,2009,57(9):831-848.
[23]Di Daniel E,Glover CP,Grot E,et al.Prolyl oligopeptidase binds to GAP-43 and functions without its peptidase activity.Mol Cell eurosci,2009,41(3):373-382.
[24]Myohanen TT,Venalainen JI,Garcia-Horsman JA,et al.Distribution of prolyl oligopeptidase in the mouse whole-body sections and peripheral tissues.Histochem Cell Biol,2008,130(5):993-1003.
[25]Sakaguchi M,Matsuda T,Matsumura E,et al.Prolyl oligopeptidase participates in cell cycle progression in a human neuroblastoma cell line.Biochem Biophys Res Commun,2011,409(4):693-698.
[26]Lee SJ.Mechanisms of fibrogenesis in liver cirrhosis:The molecular aspects of epithelial-mesenchymal transition.World J Hepatol,2014,6(4):207.
[27]Marra F,Tacke F.Roles for chemokines in liver disease.Gastroenterology,2014,147(3):577-594.
[28]Zardi EM,Navarini L,Sambataro G,et al.Hepatic PPARs:their role in liver physiology,fibrosis and treatment.Curr Med Chem,2013,20(27):3370-3396.
[29]Yu J,Zhang S,Chu ES,et al.Peroxisome proliferator-activated receptors gamma reverses hepatic nutritional fibrosis in mice and suppresses activation of hepatic stellate cells in vitro.Int J Biochem Cell Biol,2010,42(6):948-957.
[30]李兵航,李梦婷,何玲楠,等.AcSDKP体外抑制脂多糖诱导的小鼠RAW264.7巨噬细胞促炎功能研究.实用肝脏病杂志,2017,20(2):142-147.
[31]王晶,周达,丁永年,等.慢病毒介导脯氨酰寡肽酶过表达抑制硫代乙酰胺诱导的大鼠肝纤维化.实用肝脏病杂志,2015,18(2):168-172.

