Co3O4的水热法制备及其电化学性能*
尚金艳,吴贤文,唐 悦
(吉首大学化学化工学院,湖南 吉首 416000)
锂离子电池由于电压平台高、循环稳定性好等优点,已经在手机、笔记本等电子通讯领域得到了广泛应用并占据了主导地位[1-4].然而,商业化的锂离子电池电极材料均以碳为负极,其实际比容量较低(约370 mAh/g),无法满足高能量密度锂离子电池的需求.金属氧化物如 Fe2O3和 Co3O4等均具有较高的理论比容量,是新一代高能量密度锂离子电池候选负极材料.[5]在众多金属氧化物中,Co3O4理论比容量高达890 mAh/g,成为一种极具竞争力的锂离子电池负极材料[6-9].然而,阻碍Co3O4实际应用的关键是Co3O4导电性差,在充放电过程中存在较大的体积膨胀而造成电极粉化严重.为了解决以上问题,科研工作者尝试采用溶胶凝胶法、微乳液合成法和水热合成法等来降低材料的微观尺寸,提高材料的导电性.[10-11]水热合成法不仅具有设备和工艺简单、反应条件容易控制等优点,而且煅烧不必经过高温,可直接合成粒径较小、形貌规整且分散性较好的电化学活性材料[12-13].基于此,笔者采用水热法合成Co3O4,研究不同水热反应温度及水热反应时间对材料形貌、结构及电化学性能的影响规律.
1 实验部分
1.1 实验仪器和药品
DF-101S恒温加热磁力搅拌器(巩义市予华仪器有限公司);GZX-9070MBE数显鼓风干燥箱(上海博迅实业有限公司医疗设备厂);SKC-6-12高温管式炉(杭州久立烘箱制造有限公司).硝酸钴(分析纯,天津市科密欧化学试剂研发中心);六次甲基四胺(分析纯,天津市博迪化工有限公司).
1.2 实验方法
1.2.1 水热法制备Co3O4取3.0 g硝酸钴和3.0 g六次甲基四胺分别溶解在30 mL蒸馏水中,混合后并进行磁力搅拌约1 h.将充分混合好的溶液转移到内衬聚四氟乙烯水热反应釜中,将其置于鼓风干燥箱内反应.反应结束后取出,自然冷却可得到墨绿色沉淀,减压过滤除去上层清液,用蒸馏水和酒精反复洗涤后于真空干燥箱中在60 ℃下干燥10 h.最后将所得的产物置于管式炉中于450 ℃下煅烧2 h,即可制备得到Co3O4粉体材料.
1.2.2 材料的表征 采用丹东通达科技公司生产的TD-3700型X射线衍射仪(XRD)对Co3O4的结构进行表征(Cu靶,管压30 kV,管流20 mA,步宽0.02°,扫描范围10°~80°);采用德国蔡司仪器公司生产的SIGMA HD型场发射扫描电子显微镜(FESEM)对Co3O4的形貌进行分析.
1.2.3 电化学性能测试 将活性物质Co3O4、导电剂(乙炔黑)和粘结 (聚偏氟乙烯剂,简称PVDF)按质量比8∶1∶1进行混合,在玛瑙研钵中充分混合后滴加N-甲基吡咯烷酮(简称NMP),然后均匀涂覆在铜箔上,于60 ℃干燥6 h.随后铳成直径为14 mm的圆形电极片.
以Co3O4极片为工作电极,锂片为对电极和参比电极,以1 mol/L LiPF6/ DMC+DEC+EC(体积比1∶1∶1)为电解液,以Celgard 2300为隔膜,在充满氩气的米开罗拉真空手套箱中组装成CR2032纽扣型电池,静置12 h,待用.
恒流充放电测试采用 Neware电池测试系统,充放电电压区间为0.01~3.0 V.循环伏安(CV)测试及交流阻抗(EIS)测试均采用 CHI660E 电化学工作站.其中CV测试电压范围为0.01~2.0 V,扫描速率为0.1 mV/s.EIS 测试频率范围为 10-2~105Hz,振幅为5 mV.
2 结果与讨论
2.1 材料的结构与形貌分析
图1为不同水热反应温度及时间(120 ℃/12 h;120 ℃/24 h;180 ℃/12 h;180 ℃/24 h)合成的Co3O4XRD图谱.
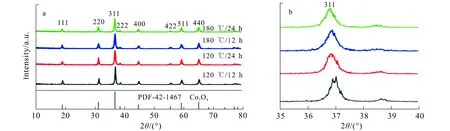
图1 不同水热反应温度及时间合成的Co3O4 XRD图谱Fig.1 XRD of Co3O4 Synthesized at Different Temperature and Time
由图1a可知:4种样品都在(111),(220),(311),(222),(400),(422),(511)和(440)等衍射晶面处具有明显的特征衍射峰,与Co3O4的XRD标准卡片(PDF-42-1467)一致,无其他杂峰.由此说明合成样品的纯度高,都是立方尖晶石型的Co3O4.对(311)峰进一步放大(图1b)可知,当水热反应时间提高到24 h,(311)衍射峰向低角度偏移;当水热反应温度增加到180 ℃时,该(311)衍射峰的半峰宽变窄,且向低角度偏移.因此,水热反应温度和时间增加,有利于提高材料的结晶度,但相应地增加了材料颗粒的大小.
表1列出不同条件下合成的Co3O4的晶胞参数和晶胞体积,由表1可知,随着水热反应温度和时间增加,晶胞体积增加.但晶粒过大将不利于锂离子的传输,提高电极的极化现象.

表1 不同水热合成温度及时间的Co3O4的晶胞参数及晶胞体积Table 1 Cell Parameters and Cell Volume of Co3O4 Synthesized at Different Temperature and Time
结合文献[14],由XRD表征分析可知,六次甲基四胺和金属钴离子借助水热反应形成Co3O4的过程推测如下:

(1)
(2)

(3)
(4)
图2为不同水热反应温度及时间合成的Co3O4SEM照片.

图2 不同水热反应温度及时间合成的Co3O4 SEM照片Fig.2 SEM of Co3O4 Synthesized at Different Temperature and Time
由图2a可见,水热反应温度为120 ℃、水热反应时间为12 h时,Co3O4二次颗粒呈微米花形状,一次颗粒由片状花瓣组成;由图2b可见,当水热反应时间增加到24 h,由零维Co3O4纳米组成的二次颗粒呈一维纳米棒状结构,其纳米棒长度约800 nm,宽度约70 nm:因此,当水热反应时间为120 ℃时,水热反应时间增加,Co3O4材料由微米花变成纳米棒时,更有利于电子的传输和离子的扩散.由图2c、图2d可见,当水热反应温度增加到180 ℃时,Co3O4材料呈纳米片状结构,其长度约3m,且多层堆垛,形貌不规则.仔细观察发现,由无数纳米晶构成的二维纳米片呈疏松多孔结构.总体来说,在低温反应条件下制备的Co3O4形貌更加规则,提高温度,形成的Co3O4虽然呈二维片状结构,但分散性欠佳,颗粒大小不均匀,这将不利于材料性能的发挥.结合XRD分析,本研究仅对120 ℃合成的Co3O4材料的电化学性能进行测试.
2.2 材料电化学性能分析
图3为120 ℃下不同水热反应时间制备的Co3O4电极的循环伏安曲线.由图3a可知,Co3O4的电极的首次阴极扫描过程中在0.82,0.51 V处出现了2个还原峰,在0.51 V处对应于Co3O4还原成金属Co和Li2O的形成,而0.82 V处归因于电解液的不可逆分解和固态电解质相界面膜的形成[15];同时,在首次阳极扫描过程中,在2.05 V处出现了一个宽的氧化峰,对应于金属Co氧化为Co3O4和Li2O的分解.而在第2次扫描过程中位于0.82 V的还原峰消失,电解液的不可逆分解得到了抑制;进一步观察发现,在首次扫描过程中,其还原峰电流较大,而氧化峰电流较小,证实其不可逆过程较大.同时,图3b和图3a对比发现,首次还原峰更加明显,且还原峰电势增加,氧化峰电势降低,由此说明,其电极极化现象降低.因此,当水热反应时间为120 ℃时,水热反应时间增加,Co3O4材料由微米花变成纳米棒时,其极化现象降低,离子的扩散能力提高.
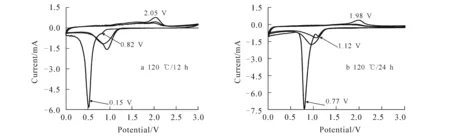
图3 120 ℃下不同水热反应时间制备的Co3O4电极的循环伏安曲线Fig.3 Cyclic Voltammetry of Co3O4 Synthesized at 120 ℃ for Different Time
进一步对120 ℃下不同水热反应时间制备的Co3O4电极的充放电性能进行了测试,结果如图4所示.
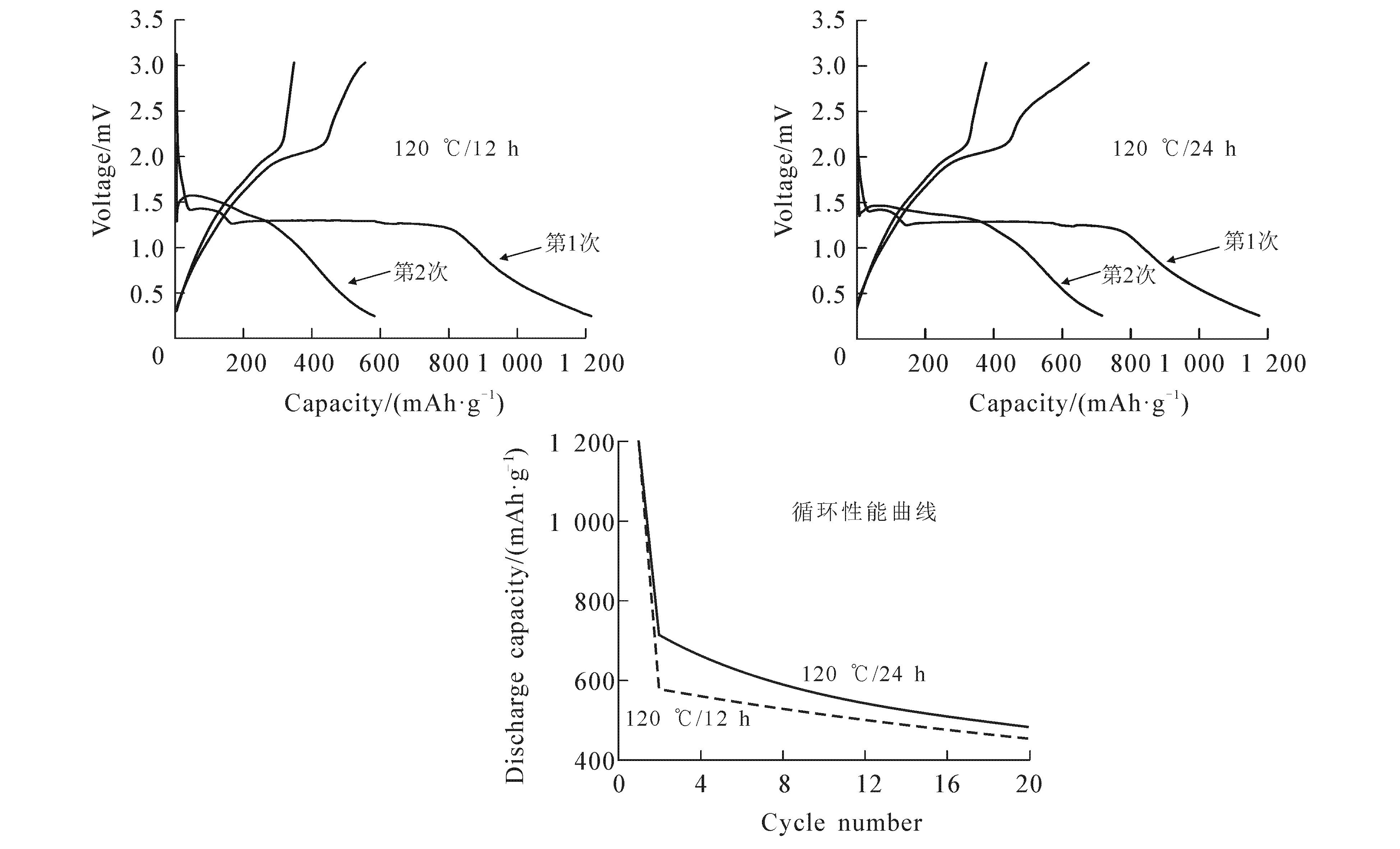
图4 120 ℃下不同水热反应时间制备的Co3O4电极的充放电曲线及循环性能曲线Fig.4 Charge/Discharge Curve of Co3O4 Synthesized at 120 ℃ for Different Time and Its Cycling Performance
由图4可以看出,首次放电曲线上出现了一个短和一个超长的放电电压平台,而充电曲线中出现了一个较陡的充电电压平台,这些现象与循环伏安曲线基本一致.且当水热反应时间为12,24 h时,其首次放电比容量分别为1 216.6,1 176.8 mAh/g,而充电比容量分别为553.2,678.2 mAh/g.前者充放电效率为219.9%,而后者充放电效率为173.5%.经20次循环后,水热反应24 h的样品具有更高的容量保持率,其放电比容量仍为486.9 mAh/g.因此,在同一温度下提高水热反应时间有利于改善材料的电化学性能.
为了进一步揭示其原因,对2种电极在充放电前的交流阻抗进行了测试,并用Zview3.1软件进行了阻抗拟合,如图5和表2所示.由此可以看出,该交流阻抗图谱由高频区的半圆和低频区的直线两部分组成,高频区的半圆对应于电荷转移阻抗,其曲率半径越小,电荷转移速率越快;低频区的直线代表韦伯阻抗,对应于锂离子在材料中的扩散.因此,电池充放电前Co3O4微米花电极和纳米棒电极电荷转移阻抗Rct分别为67.39,41.26 Ω,即在120 ℃下,水热反应24 h比12 h的材料制备的电极电荷转移速率要快.
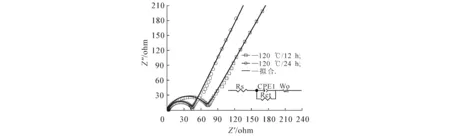
图5 120 ℃下不同水热反应时间制备的Co3O4电极循环前的交流阻抗曲线Fig.5 AC Impedance Curve of Co3O4 Synthesized at 120 ℃ for Different Time
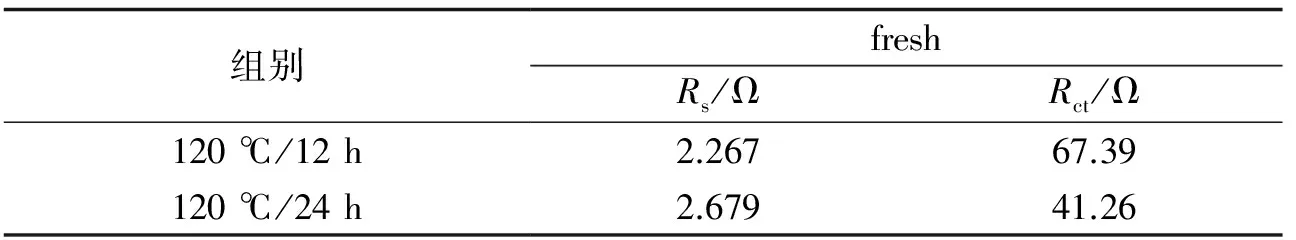
表2 Co3O4电极循环前电池的交流阻抗拟合值Table 2 Fitting Value of AC Impedance of Co3O4 Electrode Before Cycling
3 结论
以六次甲基四胺和硝酸钴为原料,采用水热法合成了Co3O4,结果表明:在180 ℃时六次甲基四胺可以提供均相沉淀剂,但合成的材料形貌不规整;在120 ℃时合成的材料均匀分布,且当水热反应时间为24 h,制备的Co3O4一次颗粒为纳米晶,并相互连接,其二次颗粒呈纳米棒状结构.由此制备的电极具有较高的充放电效率和较低的电荷转移阻抗,该合成工艺可以用于其他金属氧化物负极材料的制备,为新一代高容量锂离子电池以及钠离子电池负极材料的研究提供新的思路.
参考文献:
[1] XIANG Yanhong,SUN Zhen,LI Jian,et al.Improved Electrochemical Performance of Li1.2Ni0.2Mn0.6O2Cathode Material for Lithium Ion Batteries Synthesized by the Polyvinyl Alcohol Assisted Sol-Gel Method[J].Ceramics International,2017,43(2):2 320-2 324.
[2] HE Zhenjiang,WANG Zhixing,HUANG Zimo,et al.A Novel Architecture Designed for Lithium Rich layered Li[Li0.2Mn0.54Ni0.13Co0.13]O2Oxides for Lithium-Ion Batteries[J].Journal of Materials Chemistry A,2015,3(32):16 817-16 823.
[3] ZHENG Junchao,HAN Yadong,SUN Dan,et al.In Situ-Formed LiVOPO4@V2O5Core-Shell Nanospheres as a Cathode Material for Lithium-Ion Cells[J].Energy Storage Materials,2017,7:48-55.
[4] LI,Tao,LI Xinhai.WANG Zhixing,et al.A Novel NiCo2O4Anode Morphology for Lithium-Ion Batteries[J].Journal of Materials Chemistry A,2015,3(22):11 970-11 975.
[5] JI Liwen,LIN Zhan,ALCOUTLABI M,et al.Recent Developments in Nanostructured Anode Materials for Rechargeable Lithium-Ion Batteries[J].Energy & Environmental Science,2011,4(8):2 682-2 699.
[6] FAN Y,SHAO H,WANG J,et al.Synthesis of Foam-Like Freestanding Co3O4Nanosheets with Enhanced Electrochemical Activities[J].Chem Commun (Camb),2011,47(12):3 469-3 471.
[7] CHEN Jiao,XIA Xinhai,TU Jiangping,et al.Co3O4-C Core-Shell Nanowire Array as an Advanced Anode Material for Lithium Ion Batteries[J].Journal of Materials Chemistry,2012,22(30):15 056-15 061.
[8] 黄国勇,徐盛明,李林艳,等.锂离子电池片状四氧化三钴负极的合成及改性[J].物理化学学报,2014,30(6):1 121-1 126.
[9] 黄国勇,徐盛明,王俊莲,等.锂离子电池负极材料用Co3O4及其复合材料研究进展[J].化学学报,2013,71(12):1 589-1 597.
[10] 韩立安,常 琳,牟国栋,等.Co3O4纳米颗粒的溶胶凝胶法制备及磁性[J].西安科技大学学报,2008,28(3):602-604.
[11] 张 强,艾常春,刘 洋,等.四氧化三钴负极材料合成方法研究进展[J].无机盐工业,2014,46(3):67-70.
[12] LI Yehua,WU Xianwen,WANG Suliang,et al.Surfactant-Assisted Solvothermal Synthesis of NiCo2O4as an Anode for Lithium-Ion Batteries[J].RSC Advances,2017,7(59):36 909-36 916.
[13] 张卫民,张 玉,董光明,等.水热-热解法制备具有一维结构的Co3O4多晶[J].高等学校化学学报,2006,27(10):1 791-1 794.
[14] 邓芳泽.不同形貌NiCo2O4的可控合成及其超级电容器性能研究[D].广州:广东工业大学,2014:15-47.
[15] XIONG Lizhi,TENG Yao,WU Yuxia,et al.Large-Scale Synthesis of Aligned Co3O4Nanowalls on Nickel Foam and Their Electrochemical Performance for Li-Ion Batteries[J].Ceramics International,2014,40(10):15 561-15 568.

