杀菌剂恶霉灵的合成新方法
尹 凯
杀菌剂恶霉灵的合成新方法
尹 凯
(绍兴上虞银邦化工有限公司,浙江绍兴 312369)
恶霉灵是新一代内吸性杀菌剂、土壤消毒剂。目前合成恶霉灵的路线较多,但收率均不高。以乙酰乙酸乙酯、盐酸羟胺为起始原料,经羟胺化、环合、中和、结晶等步骤高效合成了恶霉灵原药。此路线在降低成本的同时更加绿色环保。
恶霉灵;合成;新方法
恶霉灵不仅是内吸性杀菌剂,同时也是土壤消毒剂,对腐霉菌、镰刀菌等引起的猝倒病有较好的预防效果。作为土壤消毒剂,恶霉灵能够与土壤中的铁离子、铝离子结合,抑制病菌孢子的萌发。同时能被植物的根系吸收及在根系内移动,在植物体内代谢产生2种糖苷,能调节作物生理作用,从而有效促进植株生长,根毛的增加和根的活力。对水稻生理病害亦有好的药效。该剂对土壤中病原菌以外的细菌、放线菌的影响很小,所以不会对土壤中微生物的生态产生影响,在土壤中可分解成毒性很低的化合物,对环境安全。
近些年来,人们对恶霉灵的制备展开了较多的研究,根据已有的报道归纳起来主要有5条路线:⑴以-氯代巴豆酸乙酯为原料合成;⑵以-丁炔酸乙酯为原料;⑶乙羟肟酸为原料;⑷保护-酮酯合成方法;⑸乙酰乙酸乙酯直接闭环法。其中路线⑴生产安全性较差,腐蚀性较大,氯化物对车间环境要求较高;路线⑵、⑶起始原料较贵,反应条件相对苛刻;路线⑷成本较高,保护试剂回收困难;路线⑸合成简单,反应周期短,收率高,成本低,适合用来工业化生产,但一般采用有机溶剂二氯乙烷、乙醇等作为反应溶剂。
为此,笔者在路线⑸的基础上进行改进设计,开发了一条经济实用且对环境友好的新合成路线——以乙酰乙酸乙酯和盐酸羟胺为起始原料,经羟胺化、环合、中和、结晶等步骤合成了恶霉灵原药。该路线原料易得,操作方便,收率高,成本低,并且更加绿色环保。
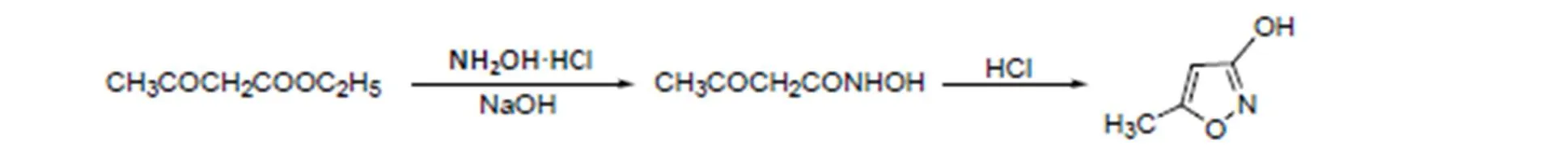
图1 恶霉灵的合成路线
1 试验部分
1.1 仪器
高效液相色谱仪(Agilent1260);气相色谱仪();旋转蒸发仪(RE-52C型,上海亚荣生化仪器厂);数字熔点仪(WRS-1A型,上海精密科学仪器有限公司);循环水式真空泵(SHB-I型,郑州予华仪器厂)。
1.2 试剂
乙酰乙酸乙酯、盐酸羟胺、盐酸、石油醚为分析纯;液碱为公司自制。
1.3 试验方法
1.3.1 羟胺化反应
在1 000 mL四口烧瓶中加入水400 g,搅拌,降温至0 ℃以下,加入盐酸羟胺75 g,加入40%液碱170 g,调pH=12。然后滴加乙酰乙酸乙酯140 g,保持pH=10~11,1.5~2 h滴完,反应温度低于20 ℃。滴加完毕保温反应,得到羟胺化反应液,备用。
1.3.2 环合反应
于1 000 mL四口烧瓶中加入盐酸300 g,将上述反应好的羟胺化液全部加入,在室温下反应20 h,得到环合反应液,备用。
1.3.3 中和、结晶
于1 000 mL四口烧瓶中加入环合反应液,缓慢滴加液碱90 g,控制pH=3,滴完后,冷却降温至5 ℃以下,抽滤得恶霉灵粗品,加石油醚200 g重结晶,降温,抽滤得到恶霉灵原药,白色针状晶体,含量99%,熔点81~83℃。
2 结果与讨论
2.1 pH的影响
当羟胺化反应过程中pH控制在酸性条件下时,在加入盐酸环合反应后,溶液的颜色变为橘黄色,恶霉灵收率很低。当反应过程中pH控制在碱性条件下,加入盐酸环合反应后,溶液的颜色变为红色,恶霉灵收率较高(表1)。
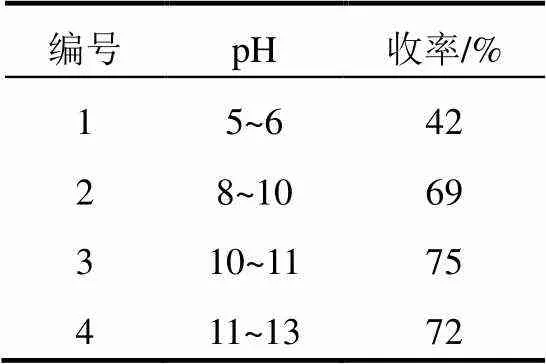
表1 不同pH收率比较
从表1可以看出,当pH为酸性时,收率明显偏低,随着pH增大,收率逐渐升高,但当pH大于11之后,收率又有所下降,最终选择pH为10~11,收率高达75%。
2.2 原料配比对收率的影响
表2为不同配比乙酰乙酸乙酯与盐酸羟胺对反应收率的影响。

表2 原料配比对收率的影响
由表2可知,在相同条件下,乙酰乙酸乙酯与盐酸羟胺的比例为1︰1时,反应收率最高,推测是由于反应保持在碱性条件下;如果盐酸羟胺过量,反应则在酸性条件下进行,使反应不能完全,因而收率降低。
2.3 反应条件的优化
以乙酰乙酸乙酯为起始原料的方法中,大多数文献都采用有机溶剂二氯乙烷、乙醇等作为羟胺化反应的溶剂,文献收率76%左右。笔者经过工艺优化选择,以水为溶剂,收率也能接近文献水平,但避免使用了毒性较大、COD值高、污染严重的有机溶剂,使得工艺路线更加绿色环保。
3 结 论
本合成方法以乙酰乙酸乙酯和盐酸羟胺作为起始原料,在前人的基础上经过优化改进,经羟胺化、环合、中和、结晶成功合成了恶霉灵原药,总收率高达75%。本法与其他文献报道的方法相比具有如下优点:⑴所用原料价廉易得,都是常规化工原料,来源广泛,价格便宜;⑵操作简便易行,本法所有的反应步骤都是工业上较为成熟的单元反应,反应条件较温和,易于实现工业化;⑶收率高,成本低;⑷是符合绿色环保工业化生产的新工艺。
[1] 苏显军, 高树林. 无公害恶霉灵的应用[J]. 农业科技, 2002, 9: 45.
[2] VALKENBURG W V, SUGAVANAM B, KHETAN S K. Pesticide formulation: recent developments and their applications in developing countries[M]. India: New Age International Limited Publishers, 1998.
[3] 陆自强, 周福才, 汪世新. 绿色食品与绿色农药[J]. 世界农药, 2004, 26(2): 1-4.
[4] 刘建超. 化学农药的发展方向--绿色化学农药[J]. 农药, 2005, 44(1): 1-3.
[5] VIJAYARAGHAVAN S JING B W, VRABLIK T, HOU T C,.. Synthesis and in vitro evaluation of quaternary ammonium derivatives of chlorambucil and melphalan, anticancer drugs designed for the chemotherapy of chondrosarcoma[J]. Bioconjugate Chem, 2003, 14 (3): 667-671.
[6] JACQUES K, JEAN-MARIE C. Process for the preparation of 2-benzolone and derivatives from orthonitrophenols and carbon monoxide: US, 4454322 [P]. 1984-06-12.
[7] BANDYOPADHYAY P, SAWKO J Z, REGEN S L. An ion conductor derived from spermine and cholic acid[J]. Chem Soc, 2000, 122 (51): 12888-12889.
[8] MASSAGO H, YOSHKAWA M, FUKADA M, NAKANISHI H. Selective inhibition ofspp on a medium for direct isolation ofspp from soils and plants [J]. Phytopathol, 1977(67): 425-428.
[9] SUTAKE, T. The effect of 3-hydroxy-5-methyl-isoxazole on the promotion of ripening in rice plant [J]. Japan. Crop Sci, 1993, 52 (3): 375-376.
A New Synthetic Method of Hymexazol
YIN Kai
(Shaoxing Shangyu Yinbang Chemicals Co., Ltd., Shaoxing 312369, Zhejiang, China)
Hymexazol is a new generation and systemic fungicide and soil disinfectants. At present, there are many routes for the synthesis of hymexazol, but the yield is not high. In this paper, ethyl acetoacetate and hydrochloricacidare used as starting materials had a series of reactions of hydroxylamine, cyclization, neutralization, crystallization and other steps for efficient synthesis of hymexazol. This synthetic method can reduce the cost of production and are more environmental friendly.
hymexazol; synthesis; new method
10.16201/j.cnki.cn31-1827/tq.2018.02.07
TQ450
A
1009-6485(2018)02-0037-02
尹凯(1983—),男,硕士,浙江宁波人,主要从事农药及中间体的合成研究。E-mail: ykgoals@163.com。
2018-01-12。

