基于加压毛细管电色谱-激光诱导荧光联用技术研究离子强度对维生素B2光解反应的影响
肖 汉, Kevin YAN, 郑怡婷, 王 彦*, 阎 超*(. 上海交通大学药学院, 上海 0040; . University of California, Riverside 95, USA)
维生素B2又称核黄素,是一种人体必需的水溶性维生素。在人体内主要以两种衍生物黄素单核苷酸(FMN)和黄素腺嘌呤二核苷酸(FAD)的形式存在,作为重要的氧化还原酶的辅基参与生物氧化反应及糖、蛋白质等的代谢[1]。核黄素不能在人体内自合成,只能从食物和外源性补充剂中摄取,核黄素的缺乏将导致人和动物能量代谢受阻,引起口角炎、舌炎、角膜血管增生等症状[2]。另外,维生素B2作为一种维生素类药,可用于辅助治疗高血压、冠心病等慢性病,也可用于治疗放化疗所引起皮炎、黏膜炎等[3]。
维生素B2因其结构中含有异咯嗪环,稳定性较差,遇光容易分解[4],很多研究都对维生素B2的光降解特性进行了研究,测定了不同光照条件下维生素B2的含量变化[5,6]。目前对于药物稳定性的研究,包括维生素B2的光稳定性研究,通常是在固定离子强度的情况下进行的。然而,一系列研究表明,离子强度对药物稳定性及光解反应的速率有较大的影响[7-9]。由于液体制剂会加入等渗调节剂等盐类物质,因而在研究维生素B2的光解反应时,不应仅仅考察在水溶液中的分解情况,在盐溶液中的研究将有更实际的参考价值。考察维生素B2在不同离子强度条件下的光照稳定性,首先需要建立维生素B2及降解产物的分析方法。目前,维生素B2多采用紫外-可见分光光度法、高效液相色谱法、荧光比色法等[3,10-12]。UV和HPLC的灵敏度欠佳,荧光分光光度法灵敏度高,但无法测定分解反应产生的有关物质。
加压毛细管电色谱(pressurized capillary electrochromatography, pCEC)是近年发展起来的一种新兴电动微分离技术,它以内含色谱固定相的毛细管为分离柱,利用电渗流结合压力流来推动流动相,既可分离带电物质也可分离中性物质。具有高柱效、高选择性、高分辨度、快速分离、样品和试剂用量少的特点[13]。pCEC已广泛应用于药物分析[14]、食品检测[15]等领域。将具有高效分离能力的pCEC和高灵敏度的激光诱导荧光(laser-induced fluorescence, LIF)检测器联用[16],可显著增加其对痕量物质的分析,非常适合于维生素B2和其有关物质的测定[17]。
本研究将pCEC-LIF微分离平台应用于维生素B2及其荧光性分解产物的分离分析中,建立分析维生素B2及有关物质的新方法,同时将利用此平台考察维生素B2溶液光解反应的速率与离子强度之间的关系。
1 实验部分
1.1 仪器与试剂
TriSep-2100型加压毛细管电色谱仪(美国Unimicro Technologies公司),由激光诱导荧光检测器(型号Trisep-3000)、溶剂输送系统、微流控系统、高压电源及数据采集系统5部分组成;WD-A型药物稳定性检查仪(天津新天光分析仪器技术公司); Sartorius BT224S电子天平(北京赛多利斯仪器系统有限公司); KQ5200DE超声波清洗器(昆山超声仪器有限公司); Molcell 1805V摩尔细胞型纯水机(重庆摩尔水处理设备有限公司); F7000荧光分光光度计(日本Hitachi公司)。
维生素B2(vitamin B2, VB2,批号K1622101,含量98%)购自上海阿拉丁试剂有限公司;光黄素(lumiflavin,含量95%)购自加拿大Toronto Research Chemicals公司,磷酸氢二钠(含量99%)购自上海凌峰化学试剂有限公司;三氟乙酸(trifluoroacetic acid, TFA,含量98%)和氯化钠(分析纯)购自国药集团化学试剂有限公司;甲醇和乙腈(色谱纯)购自美国Tedia公司。
1.2 溶液配制
维生素B2对照储备液的配制:精密称取维生素B218.8 mg置于250 mL容量瓶中,准确配制浓度为2.0×10-4mol/L的储备液。
光黄素对照储备液的配制:精密称取光黄素12.8 mg置于250 mL容量瓶中,准确配制浓度为2.0×10-4mol/L的储备液。
维生素B2系列对照溶液的配制:用超纯水将上述对照储备液逐级稀释为0.25×10-4、0.50×10-4、1.0×10-4和1.5×10-4mol/L的系列对照溶液。
缓冲液和不同离子强度溶液的配制:配制10、20和40 mmol/L磷酸盐缓冲液(phosphate buffer saline, PBS), pH为7.0,并加入氯化钠分别调节其离子强度。
维生素B2/PBS的配制:将维生素B2溶于上述PBS缓冲液中,现用现配。
以上含维生素B2的溶液均用锡箔纸包裹,避光冷藏保存。
1.3 光解反应实验条件
吸取2 mL的维生素B2/水溶液和维生素B2/PBS置于透明玻璃样品瓶中,放入药物稳定性检查仪内,控制检查仪的灯光强度为3 500 Lx,温度保持在室温,开启风扇。开始光照的时间记为t0,在光照不同时间点取样,样品避光冷藏保存。
1.4 维生素B2荧光光谱扫描实验条件
发射光谱测量模式,激发波长488 nm,发射光谱波长测量范围:450~600 nm,激发波长狭缝宽度5 nm,发射波长狭缝宽度5 nm,温度为室温。
1.5 pCEC-LIF实验条件
色谱柱:毛细管色谱柱(150 mm×100 μm, 1.8 μm, C18);流动相A:水(含0.1%(v/v)三氟乙酸),流动相B:乙腈(含0.1%(v/v)三氟乙酸),梯度洗脱(0 min, 30%B; 0-15 min, 30%B上升至90%B; 15-20 min, 90%B),总流速:0.05 mL/min;柱温:室温;分流比:1∶600;进样量:3 nL; LIF激发波长:488 nm,发射波长:520 nm。
2 结果与讨论
2.1 维生素B2在不同离子强度溶液中的荧光光谱
维生素B2溶液为黄色,自身发黄绿色荧光,发生光解后,溶液颜色整体变淡,在离子强度大的溶液中褪色更加明显。通过荧光分光光度计分别测量维生素B2在水和20 mmol/L PBS(离子强度为0.5 mol/L)中光照0.5、1、1.5和2 h后的荧光光谱,见图1。结果显示,维生素B2/水溶液和维生素B2/PBS在光照不同时间后,荧光光谱形状并没有大的改变,但荧光强度发生了改变。维生素B2/水溶液在488 nm处激发产生的荧光强度随光照时间有一定程度的下降,但远低于其在PBS中的下降程度。由此说明离子强度对维生素B2光解反应有直接影响,溶液中离子强度的增加,将加快维生素B2光解反应的速率。

图 1 在不同光照时间下维生素B2荧光光谱的比较Fig. 1 Comparison of fluorescence spectra of vitamin B2 with different exposure time to light a. aqueous solution; b. phosphate buffer saline (PBS)solution.
在图1中看到,维生素B2在水溶液和磷酸盐溶液中的荧光强度有不同程度的下降,这个强度代表的是整个维生素B2反应体系中的总荧光强度,即维生素B2和光降解产物的荧光强度的总和,说明维生素B2的光解产物整体上在488 nm激发时产生的荧光强度不如维生素B2本身,也可能是部分降解产物没有荧光信号导致。为了进一步研究维生素B2和光降解产物的变化,我们需要建立有分离能力的分析方法。
2.2 pCEC-LIF分析维生素B2及其分解产物
pCEC-LIF系统中,毛细管色谱柱的出口端连接负电极,进口端接地,电渗流与压力流方向一致。在毛细管色谱柱中,样品根据各自的分配系数和电泳淌度的不同得到分离。将毛细管色谱柱的窗口直接安装于可变波长LIF中,激光器发射出的488 nm激光由激发滤光片滤光后经二向色镜反射,通过物镜聚焦到色谱柱窗口上,激发被分离的待测物质产生荧光,荧光通过物镜聚焦、滤光片过滤,聚焦到光电倍增管(photomultiplier tube, PMT)前面狭缝处,由PMT采集转化成电信号,然后被信号采集单元转化成数字信号输出。
实验中首先考察了流动相梯度、施加电压等对维生素B2分析的影响。其中电压的影响如图2所示。可看出,随着电压的增加,分离时间缩短。同时,各个物质仍能得到良好的分离,主峰维生素B2与右侧相邻杂质峰的分离度也随电压的增加而增加。其主要原因在于,加压毛细管电色谱兼具HPLC和电泳的双重性质,可通过改变电压来增加分离的选择性。图2中,由于毛细管中电渗流方向和外加电压方向一致,随电压增加,维生素B2等物质的保留时间缩短;同时由于分离对象所带电荷不同,电压对其电泳速度的影响不完全一样,因而维生素B2与右侧相邻降解产物峰的分离度随着电压增加也有所增加,体现了加压毛细管电色谱的双重分离机理。

图 2 电压对pCEC-LIF分离维生素B2及其光解产物的影响Fig. 2 Effects of voltage on separation of vitamin B2 and its photolysis products by pressurized capillary electrochromatography-laser induced fluorescence (pCEC-LIF) detection Column dimension: 150 mm×100 μm, 1.8 μm, C18; mobile phase A: H2O, containing 0.1% (v/v) trifluoroacetic acid(TFA), pH 2; mobile phase B: acetonitrile, containing 0.1% (v/v) TFA. Gradient elution: 0 min, 30%B; 0-15 min, 30%B to 90%B; 15-20 min, 90%B. LIF excitation wavelength: 488 nm; emission wavelength: 520 nm; pump flow rate: 0.05 mL/min.
在pCEC-LIF最优条件下,维生素B2溶液的分离如图3所示。可以看出,维生素B2对照品(见图3a)及光解产物光黄素对照品(见图3b)均显示一个单一的色谱峰。随着光解反应的进行,维生素B2在水溶液(见图3c)和PBS(见图3d)中均开始降解,并有新的降解产物产生,但降解峰的个数和强度有所不同。当光照24 h后,维生素B2在水溶液(见图3e)和盐溶液(见图3f)中的色谱峰基本消失,色谱图中仅存在降解产物的峰。在最优条件下,维生素B2的多种带荧光的光解产物都得到了很好的分离,说明我们建立的pCEC-LIF为维生素B2溶液的光降解产物研究提供了一个很好的分析平台。

图 3 维生素B2、光黄素及维生素B2在水溶液和PBS缓冲液中光解不同时间后的pCEC-LIF谱图Fig. 3 pCEC-LIF electrochromatograms of vitamin B2, lumiflavin and photolysis products of vitamin B2 in aqueous solution and PBS with different exposure time to light (a) vitamin B2 reference standard; (b) lumiflavin reference standard; (c) vitamin B2 in aqueous solution and (d) PBS exposed to light for 2 h, and (e) in aqueous solution and (f) PBS exposed to light for 24 h. Applied voltage: -9 kV. Other conditions are the same to those in Fig. 2.

图 4 维生素B2及光黄素的结构式Fig. 4 Structure of vitamin B2 and lumiflavin
本研究使用的是反相色谱柱。而维生素B2的结构如图4a所示。可以看到,在异咯嗪环的10号位N原子上所连接的基团上有4个极性较大的羟基,在反相色谱中保留较弱。而降解产物光黄素如图4b所示,在其他结构基本不变的情况下,其10号位N原子上的基团部分丢失,虽然相对分子质量变小,但是极性大的羟基也脱去了,因而产物分子在相对分子质量减小同时,极性亦减小,保留增加,符合RPLC的保留规律。
2.3 标准曲线及线性
在pCEC-LIF上分别测定1.2节所述维生素B2系列对照溶液,在该系列对照溶液的浓度范围内,根据色谱图上的峰面积Y对浓度X(mol/L)绘制标准曲线,得到回归方程Y=877 201X-24 602(r>0.999),表明方法的线性关系良好。定量限可低至5×10-8mol/L。连续进样6次,计算得保留时间的RSD为2.1%,峰面积的RSD为3.7%。
2.4 维生素B2在不同离子强度溶液中的降解反应
将维生素B2溶解在不同离子强度的PBS中,在光照不同时间后取样,基于建好的pCEC-LIF平台进行分析。
考察了不同浓度的缓冲液中,维生素B2浓度随光照时间的变化(见图5)。随着光照时间的增加,维生素B2在所有溶液中的浓度都会逐渐降低,但在水溶液中的降低程度最小,且缓冲溶液的浓度越大,维生素B2的降解越快。

图 5 光照时间对水溶液和PBS中维生素B2浓度变化的影响Fig. 5 Effect of exposure time to light on the concen- tration change of vitamin B2 dissolved in aqueous solution and PBS

图 6 光照1 h时不同PBS中维生素B2浓度的变化Fig. 6 Concentration changes of vitamin B2 in different PBS with 1-hour light exposure

2.5 维生素B2光解反应的动力学研究
维生素B2在水溶液中的光解遵从一级反应动力学[10]。故根据动力学方程,维生素B2初始浓度c0与时间t时的浓度ct有以下关系:
ln (c0/ct)=kt
(1)
其中k为表观反应速率常数。

表 1 不同PBS中维生素B2光解的kTable 1 Apparent rate constant of photolysis (k)of vitamin B2 in different PBS
按式(1),基于pCEC-LIF求得维生素B2在不同离子强度溶液中的k,如表1所示。可看出,磷酸盐浓度越高,离子强度越大,维生素B2光解反应的表观反应速率常数越大。
离子强度对溶液中化学反应的影响又称原盐效应。在药物制剂中,往往加入等渗调节剂、抗氧化剂、pH调节剂,而这些多为无机盐[18],产生的离子强度可能会影响药物的降解速度,影响的定量关系可由过渡态理论导出[19]。
离子强度对药物降解速度的影响符合下式[20]:
(2)
式中,ZA、ZB是反应物在溶液中所带电荷,μ是离子强度,k0是无限稀释下的反应速率常数。式(2)适用于μ较小的体系,而在离子强度较大的溶液体系中,式(2)可表示为:
(3)
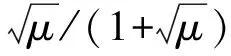
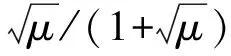

图 7 不同浓度PBS时与log k的关系Fig. 7 Plot of versus log k with different concentrations of PBS
3 结论
本研究基于pCEC-LIF平台,建立了维生素B2及其荧光性分解产物的分析方法,实现了维生素B2及多种光降解产物的分析。用该联用系统研究了维生素B2在水溶液和PBS中的光解反应速率与离子强度之间的关系。发现维生素B2溶液的光解速率与磷酸盐浓度及离子强度呈正相关性,动力学计算表明,该条件下的光解反应是两种带同种电荷的离子之间的反应。因而,在维生素B2液体制剂的运输、保存和使用过程中,应注意控制体系的离子强度。
参考文献:
[1] Murataliev M B, Feyereisen R, Walker F A. Biochim Biophys Acta, 2004, 1698(1): 1
[2] Wang J Y, Zhu S G, Xu C F. Biochemistry. Beijing: Higher Education Press, 2008: 199
王镜岩, 朱圣庚, 徐长法. 生物化学教程. 北京: 高等教育出版社, 2008: 199
[3] Zhang H X, Huang R Q, Xiao B K, et al. Chinese Journal of Pharmaceutical Analysis, 2010, 30(1): 67
张红霞, 黄荣清, 肖炳坤, 等. 药物分析杂志, 2010, 30(1): 67
[4] Zhang W S, Li A L. Medicinal Chemistry. Beijing: Higher Education Press, 2004: 647
仉文升, 李安良. 药物化学. 北京: 高等教育出版社, 2004: 647
[5] Ahmad I, Fasihullah Q, Vaid F H M. J Photochem Photobiol B, 2004, 75(1): 13
[6] Pan D Y, Lan X M. Chinese Journal of Drug Administration and Clinical Medicine, 2010, 10(7): 779
潘代勇, 兰小曼. 中国药物与临床, 2010, 10(7): 779
[7] Shang J, Chen J, Shen Z, et al. Environ Sci Pollut Res Int, 2015, 22(16): 12374
[8] Gong Y, Fu J, O’Reilly S E, et al. J Hazard Mater, 2015, 287: 142
[9] Zhou C, Chen J, Xie Q, et al. Chemosphere, 2015, 138: 792
[10] Zong Y, Zhang S G. Chinese Journal of Pharmaceutical Sciences, 2003, 38(4): 303
宗怡, 张石革. 中国药学杂志, 2003, 38(4): 303
[11] Ahmad I, Anwar Z, Ali S A, et al. J Photochem Photobiol B, 2016, 157(3): 113
[12] Pharmacopoeia Commission of People’s Republic of China. Pharmacopoeia Commission of People’s Republic of China, Part 2. Beijing: China Medical Science Press, 2015: 1232
国家药典委员会. 中华人民共和国药典, 二部. 北京: 中国医药科技出版社, 2015: 1232
[13] Wan Q Y, Ru X, Wang X X, et al. Chinese Journal of Analytical Chemistry, 2015, 43(7): 1063
万青云, 茹鑫, 王晓曦, 等. 分析化学, 2015, 43(7): 1063
[14] Zheng S, Shi W J, Wang X X, et al. Food Science, 2014, 35(20): 105
郑署, 施文君, 王晓曦, 等. 食品科学, 2014, 35(20): 105
[15] Guo Q L, Shi H L, Zhao L, et al. Food Research and Development, 2015(8): 77
郭启雷, 史海良, 赵丽, 等. 食品研究与开发, 2015(8): 77
[16] Lu Q M, Zhang L, Cheng J T, et al. Chemistry, 2010, 73(7): 586
卢巧梅, 张兰, 程锦添, 等. 化学通报, 2010, 73(7): 586
[17] Wu Y M, Wu Q Z, Wang X C, Chinese Journal of Chromatography, 2010, 28(3): 247
吴翊民, 吴庆政, 王晓春, 等. 色谱, 2010, 28(3): 247
[18] Gao P Y, Li J B. Physical Chemistry. Beijing: Science Press, 2007: 220
高丕英, 李江波. 物理化学. 北京: 科学出版社, 2007: 220
[19] Cui F D. Pharmaceutics. Beijing: People’s Health Publishing House, 2012: 72
崔福德. 药剂学. 北京: 人民卫生出版社, 2012: 72
[20] Liu J E. Pharmaceutical Preparation Technology. Beijing: Chemical Industry Press, 2008: 264
刘姣娥. 药物制剂技术. 北京: 化学工业出版社, 2008: 264

