超高效液相色谱-串联质谱法同时检测动物组织中15种保水功能药物
刘洪斌, 姚喜梅, 田亚平, 张 鹭, 蔡英华, 姜艳彬, 李 颖*(. 中国动物疫病预防控制中心, 北京 0609; . 中国标准化协会, 北京 00048)
随着经济的发展和生活水平的提高,人们对动物源食品的需求日益增大,促使畜牧业在近几年得到了长足发展。不同种类兽药的使用对治疗和预防动物疾病、促进动物生长至关重要。目前我国存在养殖规模小而散、科学养殖水平低、盲目用药现象多的现状,导致了养殖环节药物用量超标、不合理休药及人药兽用等问题仍较严重。在经济利益的驱使下,非法添加违禁药物和功能性药物的现象屡禁不止。随着消费者对动物性产品质量安全的日益关注,动物产品中限用及违禁药物的检测对保证食品安全意义重大。
目前动物性产品中药物残留检测方法大多按药物种类分类,如磺胺类[1,2]、喹诺酮类[3]、β-受体激动剂类[4]和大环类脂类[5]等,也有多种类药物同时检测的报道[6,7]。但实际生产中,多类药物往往具有相似的功能或相同的副作用,如部分抗胆碱类、抗惊厥类、肾上腺素类药物均具有口干、钠水潴留、排尿困难等特点[8],这些副作用可间接用于注水增重以达到增收的效果。如果过量使用这些保水功能药物,动物会出现烦躁不安、痉挛等神经兴奋症状,进而出现昏迷、呼吸困难甚至死亡[9,10]。因此建立针对同一功能、特性及副作用的多种类药物同时检测的方法,为更好地保障食品安全、监管药物非法添加具有重要现实意义。
本实验研究了卡马西平、阿托品、哌仑西平和美卡拉明等15种保水功能药物,这些药物的研究大多见于医学领域,内容多为该类药物对人体及动物的治疗效果及药物作用机理[11,12],主要检测方法包括液相色谱法[13,14]、液相色谱-质谱联用法[15,16]和飞行时间质谱法[17]等,然而检测动物组织中这些药物残留方法的报道较少[18],其中多残留同时检测的方法还未见报道。本文建立了液相色谱-串联质谱检测动物组织中这15种保水功能药物残留的方法,较好地满足动物组织中该功能药物残留的检测需求,对更好地警示非法注水、监管动物源性食品安全和打击非法添加提供了技术支撑。
1 实验部分
1.1 仪器、试剂与材料
Acquity UPLC I-CLASS超高效液相色谱仪、TQ-XS三重四极杆质谱仪(美国Waters公司); 3K15型离心机(美国Sigma公司); T25均质机(德国IKA公司); N-EVAP氮吹仪(美国Organomation公司): Milli-Q纯水仪(美国Millipore公司)。
普瑞巴林(pregabalin)、美卡拉明(mecamylamine)、卡马西平(carbamazepine)、卡马西平10,11环氧化物(carbamazepine 10,11-epoxide)、氢溴酸后马托品(homatropine hydrobromide)、托吡卡胺(tropicamide)、阿托品(atropine)、氢溴酸东莨菪碱(scopolamine hydrobromide)、扎来普隆(zaleplon)、双环胺(dicyclomine)、贝那替嗪(benactyzine)、依替唑仑(etizolam)、哌仑西平(pirenzepine)、丁溴酸东莨菪碱(scopolamine butylbromide)和丙哌维林(propiverine)购自百灵威科技有限公司和美仑生物技术公司,纯度均>97%。乙腈、甲醇、甲酸等均为色谱纯,购自美国Fisher公司;Oasis PRiME HLB SPE柱(60 mg/3 mL)购自美国Waters公司。猪肉、牛肉样品购自超市和农贸市场。
称取适量上述标准品,用甲醇配制单标准储备液,并用甲醇配制成质量浓度为10 mg/L的混合标准溶液,于-20 ℃保存;用初始流动相配制系列标准工作液,现用现配。
1.2 样品前处理
提取:准确称取匀浆后的动物组织样品2 g(精确到0.01 g),置于50 mL离心管中,加入10 mL含1.0%(v/v)甲酸的乙腈溶液,以9 500 r/min离心5 min,取上清液于另一50 mL离心管中,再用10 mL含1.0%(v/v)甲酸的乙腈溶液重复提取一次,合并两次提取液,准确量取10 mL,置于15 mL离心管中,待净化。
净化:将提取液上样至用3 mL含1.0%(v/v)甲酸的乙腈溶液活化过的Oasis PRiME HLB SPE柱中,收集全部滤出液,于50 ℃氮气吹至近干,然后用0.5 mL初始流动相定容,以12 000 r/min离心5 min,经0.22 μm滤膜过滤,待上机测定。
1.3 色谱条件
色谱柱:Acquity UPLC BEH C18柱(50 mm×2.1 mm, 1.7 μm);流速:0.3 mL/min;流动相:(A)0.1%(v/v)甲酸水溶液和(B)甲醇。梯度洗脱程序:0~0.5 min, 3%B, 0.5~2.5 min, 3%B~30%B; 2.5~3.5 min, 30%B, 3.5~3.6 min, 30%B~60%B, 3.6~4.5 min, 60%B, 4.5~6.0 min, 60%B~100%B, 6.0~7.5 min, 100%B, 7.5~8.5 min, 100%B~3%B; 8.5~10.5 min, 3%B。进样量:10 μL。
1.4 质谱条件
离子源:电喷雾电离源,正离子模式(ESI+);离子源温度:150 ℃;毛细管电压:3.0 kV;锥孔电压:3 V;透镜电压:0.5 V;脱溶剂温度:250 ℃;锥孔气流速:150 L/h;脱溶剂气流速:600 L/h;碰撞气流速:0.15 mL/min;监测模式:MRM模式。15种保水功能药物的母离子、子离子及其对应的聚焦电压和碰撞能量见表1。

表 1 15种保水功能药物的母离子、子离子、聚焦电压、碰撞能和保留时间Table 1 Precursor ions, product ions, focus voltages, collision energies and retention times of the 15 water-holding functional drugs
* Quantitative ion.
2 结果与讨论
2.1 过滤膜种类的优化

图 1 不同滤膜对15种保水功能药物吸附率的影响Fig. 1 Effect of different filters on the adsorption rates of the 15 water-holding functional drugsGHP: hydrophilic polypropylene; PTFE: polytetrafluoroethylene; PES: polyether sulfone.
滤膜过滤作为前处理过程的最后一道防线,对净化样品、减少基质干扰作用明显。滤膜对药物的吸附作用直接影响检测结果的回收率和准确性。本文考察了Waters GHP膜、Agilent PTFE膜和尼龙膜、聚醚砜(PES)膜(天津津腾实验设备有限公司)等4种适用于绝大多数有机溶剂和水溶液的滤膜对10 μg/L混合标准溶液吸附效果的影响(见图1)。结果显示,4种滤膜对除普瑞巴林、托吡卡胺和阿托品外的其他12种药物均存在不同程度的吸附,吸附率为0.7%~68.7%,其中Waters GHP膜、Agilent PTFE膜对双环胺及丙哌维林的吸附作用较明显;尼龙膜除对丁溴酸东莨胆碱、扎来普隆和卡马西平10,11环氧化物的吸附作用较聚醚砜膜明显外,其他均优于聚醚砜膜。综合滤膜对各药物的吸附率和价格,选取尼龙膜作为实验用过滤膜,但考虑到尼龙膜对部分目标药物也存在吸附,实验用标准溶液也需经滤膜过滤后上机。
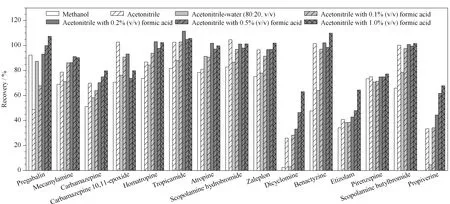
图 2 不同提取溶剂对15种保水功能药物回收率的影响Fig. 2 Effect of different extraction solutions on the recoveries of the 15 water-holding functional drugs
2.2 提取溶剂的选择
在空白动物组织样品中添加10 μg/kg 15种保水功能药物的混合标准溶液,分别选取甲醇、乙腈、80%(v/v)乙腈水溶液、含不同体积分数(0.1%、0.2%、0.5%和1.0%)甲酸的乙腈溶液等7种提取溶剂,考察不同提取溶剂对提取效果的影响(见图2)。结果表明,当采用甲醇和80%(v/v)乙腈水溶液为提取溶剂时,蛋白质变性沉淀不完全,样品整体较为浑浊,且回收率较低。普瑞巴林、卡马西平、依替唑仑、双环胺及丙哌维林5种药物的回收率均随乙腈中甲酸体积分数的升高而增加,当甲酸的体积分数达到1.0%时,双环胺及丙哌维林两种药物的回收率能达到60%以上。因此实验最终选择含1.0%(v/v)甲酸的乙腈溶液作为提取溶剂。
2.3 基质效应(ME)
动物组织含有丰富的脂类、蛋白质、肽类及其代谢产物等各种有机物[19],组织样品经处理后,仍有部分上述物质和待测药物以共流出物的形式同时进入电离源,导致增强或抑制待测药物的电离程度,从而产生不同的基质效应。试验采用提取后添加法[20]测定基质效应。ME=目标化合物在空白动物组织和纯溶剂中的峰面积之比。若ME值小于1.0,说明基质对待测物的响应产生抑制作用;若ME值大于1.0,说明存在增强效应。结果表明,除猪肉中哌仑西平、依替唑仑及牛肉中双环胺的抑制效果不明显外,其他药物在两种基质中均存在不同程度的抑制效果,ME为0.70~1.05; 15种药物在猪肉和牛肉中的基质效应差别不显著(见表2)。但为减少基质效应对结果准确度的影响,应在实际检测中采用空白基质加标溶液。
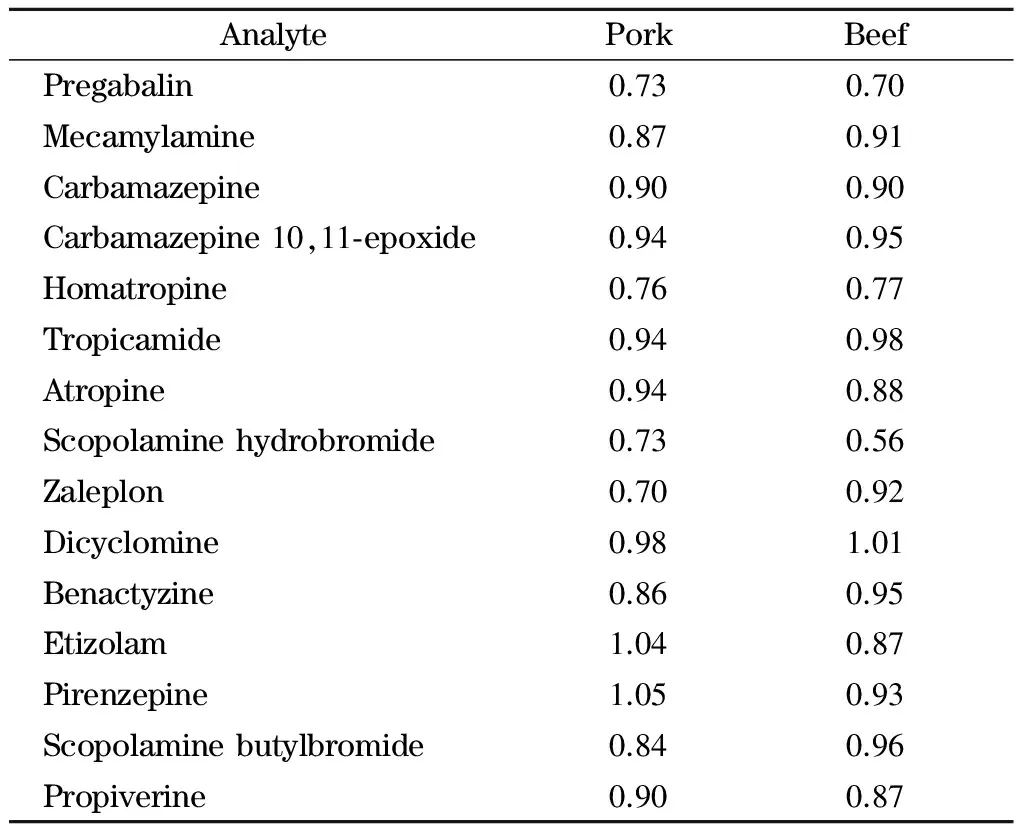
表 2 不同动物组织样品中15种保水功能药物的基质效应Table 2 Matrix effects of the 15 water-holding functional drugs in different animal tissue samples
2.4 线性方程和检出限
采用1.2节方法处理空白组织样品,添加适量15种保水功能药物的混合标准溶液,配制1.0、2.0、5.0、10.0、20.0和50.0 μg/kg基质加标溶液,经UPLC-MS/MS检测,以定量离子色谱峰面积为纵坐标、待测药物的含量为横坐标绘制标准曲线。结果表明,在猪肉和牛肉组织中,15种保水功能药物在1.0~50.0 μg/kg范围内线性关系良好,相关系数(r)均≥0.994 9(见表3)。
用空白基质溶液逐级稀释标准溶液,按3倍和10倍信噪比确定方法的检出限(LOD)和定量限(LOQ), 15种保水功能药物的定量限均低于1.0 μg/kg(见表3)。
2.5 回收率
取空白猪肉、牛肉组织样品,添加含量为1.0、2.0和10 μg/kg 3个水平的混合标准溶液,每个水平平行测定6次,共测定3个批次,按1.2节方法进行添加回收试验(见表4)。猪肉中15种药物的平均回收率为60.0%~108.2%,批内RSD为1.09%~10.5%,批间RSD为2.31%~11.4%;牛肉中15种药物的平均回收率为68.6%~111.0%,批内RSD为0.56%~11.5%,批间RSD为3.65%~14.8%。方法的准确度及精密度均满足GB/T 27404-2008要求。空白猪肉样品中添加15种保水功能药物(10 μg/kg)的提取离子色谱图见图3。
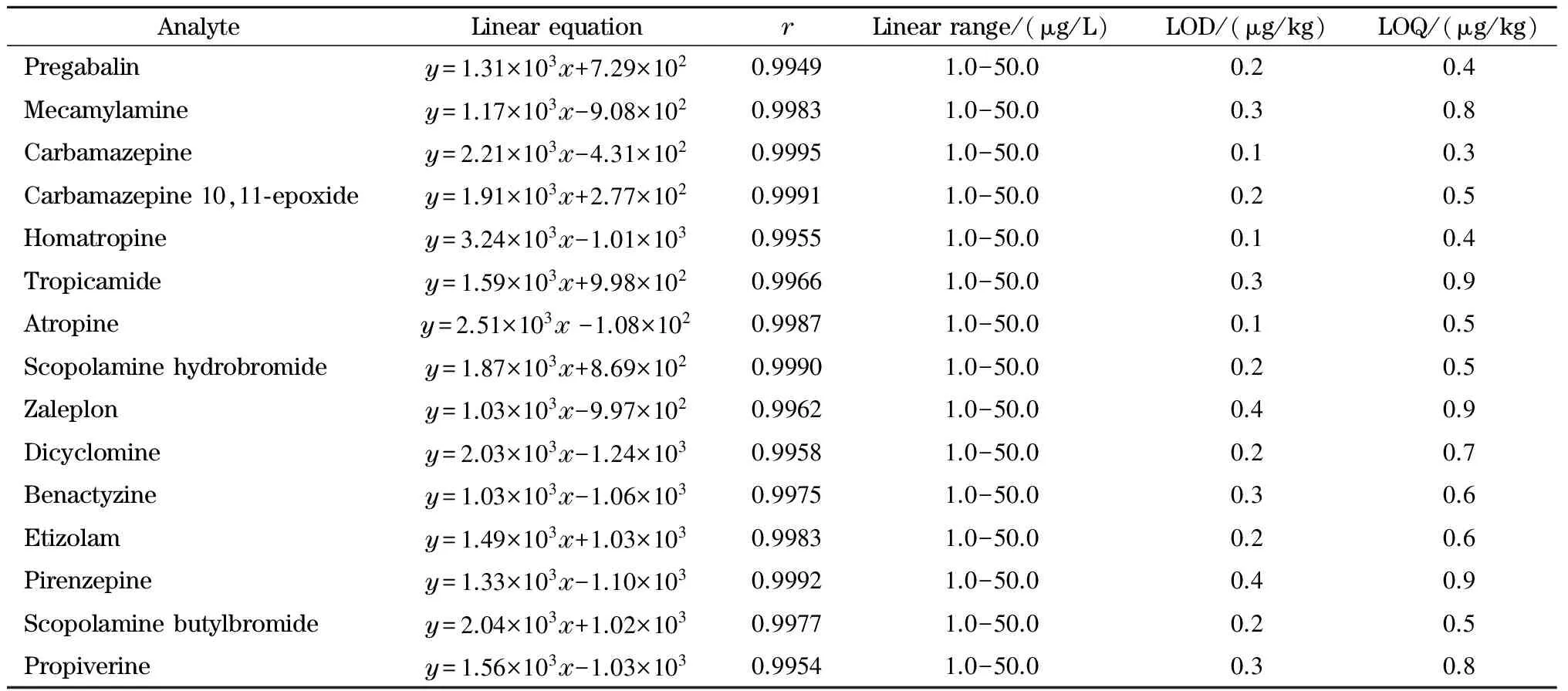
表 3 15种保水抗利尿药物的线性方程、相关系数、线性范围、检出限和定量限Table 3 Linear equations, correlation coefficients (r), linear ranges, limits of detection and limits of quantification of the 15 water-holding functional drugs
y: peak area,x: mass concentration, μg/kg.

表 4 动物样品中15种保水抗利尿药物的加标回收率和相对标准偏差Table 4 Spiked recoveries and RSDs of the 15 water-holding functional drugs in animal samples
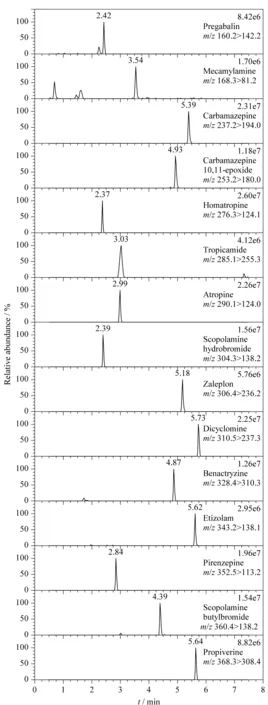
图 3 加标猪肉样品中15种保水功能药物(10 μg/kg)的提取离子色谱图Fig. 3 Extracted ion chromatograms of the 15 water- holding functional drugs in blank pork samples spiked with 10 μg/kg
3 结论
本实验针对具有相同副作用的药物建立了UPLC-MS/MS检测动物组织中15种保水功能药物残留的方法,为应对动物源性食品中风险隐患的筛查和监控提供了新思路。该方法前处理快速简单,灵敏度高,稳定性好,能够较好地满足动物组织中该类药物残留的检测要求,该方法的建立能有效防范药物滥用和非法添加行为,并对打击动物组织中非法注水提供了一定的技术支撑。
参考文献:
[1] Liu H B, Yao X M, Cai Y H, et al. Chinese Journal of Analysis Laboratory, 2015, 34(10): 1141
刘洪斌, 姚喜梅, 蔡英华, 等. 分析试验室, 2015, 34(10): 1141
[2] Xu X, Xiao Y C, Geng D D, et al. Chinese Journal of Chromatography, 2016, 34(4): 422
许旭, 肖远灿, 耿丹丹, 等. 色谱, 2016, 34(4): 422
[3] Yang Y F, Cao X M, Li X L, et al. Chinese Journal of Chromatography, 2016, 34(11): 1063
杨艳菲, 曹旭敏, 李雪莲, 等. 色谱, 2016, 34(11): 1063
[4] Zheng L, Wu Y J, Zhao Y F, et al. Chinese Journal of Chromatography, 2014, 32(8): 867
郑玲, 吴玉杰, 赵永锋, 等. 色谱, 2014, 32(8): 867
[5] Zhang X G, Liu D, Liu H R, et al. Chinese Journal of Chromatography, 2017, 35(10): 1055
张晓光, 刘东, 刘红冉, 等. 色谱, 2017, 35(10): 1055
[6] Luo H D, Xie M T, Huang X L, et al. Chinese Journal of Chromatography, 2015, 33(4): 354
罗辉泰, 谢梦婷, 黄晓兰, 等. 色谱, 2015, 33(4): 354
[7] Wang H, Zhao L, Yang H M, et al. Chinese Journal of Chromatography, 2015, 33(9): 995
王浩, 赵丽, 杨红梅, 等. 色谱, 2015, 33(9): 995
[8] Li W N. [MS Dissertation]. Hangzhou: Zhejiang Gongshang University, 2010
李伟妮. [硕士学位论文]. 杭州: 浙江工商大学, 2010
[9] Wu G S. Chinese Journal of Modern Drug Application, 2010, 4(11): 118
吴桂生. 中国现代药物应用, 2010, 4(11): 118
[10] Jose N, Angela H, Mitchell J B, et al. Am J Geriatr Pharmacother, 2006, 4(1): 42
[11] Modi A R, Casten R, Rovner B W. Am J Geriatr Pharmacother, 2015, 23(3): 109
[12] Machado-Alba J E, Castro-Rodriguez A, Alzate-Piedrahita J A, et al. J Am Med Dir Assoc, 2016, 17(3): 275
[13] Tu J S, Li P M, Yang X Y. et al. J Chromatogr B, 2005, 822(1/2): 300
[14] Ceyhan T, Kartal M, Altun M L, et al. J Pharm Biomed Anal, 2001, 25(3/4): 399
[15] John H, Binder T, Hochstetter H, et al. Anal Bioanal Chem, 2010, 396: 751
[16] Li J L, Zhang Z Q, Ruan J X, et al. J Chromatogr B, 2007, 855: 180
[17] Yu Z H, Wu Z P, Gong F J, et al. J Sep Sci, 2012, 35(20): 2773
[18] Hu X J, Wu N P, Meng L, et al. Chinese Journal of Veterinary Drug, 2014, 48(7): 46
胡兴娟, 吴宁鹏, 孟蕾, 等. 中国兽药杂志, 2014, 48(7): 46
[19] Wang L Q, He L M, Zeng Z L, et al. Journal of Chinese Mass Spectrometry Society, 2011, 32(6): 322
王立琦, 贺利民, 曾振灵, 等. 质谱学报, 2011, 32(6): 322
[20] Matuszewki B K, Constanzer M L, Chavez-Eng C M. Anal Chem, 2003, 75: 3019

