基于L-半胱氨酸功能化的MoS2荧光量子点检测Hg2+
张慧佳, 晋晓勇, 倪 刚, 彭 娟
(宁夏大学化学化工学院,宁夏银川 750021)
MoS2作为一种类石墨烯结构材料,已经应用于电池、催化剂和晶体管等领域[1 - 3]。但是对其光学特性,尤其是利用光致发光特性应用于分析化学方面的相关文献报道较少。具有荧光特性的MoS2量子点(MoS2QDs)在细胞成像和化学传感应用领域有卓越的表现[4 - 5]。为了进一步改进MoS2QDs荧光性能,扩大其应用范围,表面功能化通常是一种很高效的方式。现实生活中含汞产品在人们的生活中随处可见,而环境中的汞能被动植物富集,经生物转化作用转变成毒性更大的有机汞,且各种形态的汞可通过水体及食物链进入人体,对机体产生毒性作用。研究表明长时间暴露在高汞环境中,可以导致脑损伤和死亡[6 - 7]。因此,环境中的痕量汞检测极为重要。传统检测Hg2+的方法如原子吸收光谱法、电感耦合等离子质谱法、气相色谱法和X-射线荧光光谱法等[8]都具有较高的选择性和灵敏度,但是都需要复杂的样品制备和仪器使用。另外这些方法无法对环境中的Hg2+进行实时检测。最近,小荧光有机分子、DNA核酶、蛋白质、贵金属纳米材料及量子点等,已被用于检测Hg2+[9 - 15]。然而,这些策略需要进行多个步骤,其中一些材料甚至会产生严重的毒性。
本研究采用Na2MoO4作为钼源,L-半胱氨酸作为硫源和稳定剂,在水热条件下制备MoS2QDs。在合成时将L-半胱氨酸修饰在MoS2QDs上,而L-半胱氨酸可以与Hg2+发生键合作用,从而可以将MoS2QDs作为荧光探针有选择性的检测Hg2+。而使用MoS2QDs作为荧光探针检测Hg2+可以达到制备简单、灵敏度高、快速响应等优点。
1 实验部分
1.1 仪器与试剂
UV-3600紫外-可见光谱仪(日本,岛津(中国)公司);F-7000荧光光谱仪(日本,高新技术有限公司);JEOL JEM-2010透射电镜(日本,JEOL公司)。
Na2MoO4·2H2O,L-半胱氨酸,ZnSO4,CaCl2,MgCl2·6H2O,BaCl2,NaCl,Cd(NO3)2·4H2O,HgCl2,CuSO4·5H2O,KBr,Ni(NO3)2·6H2O,Al2(SO4)3·18H2O,均购买于阿拉丁试剂公司。所有试剂均为分析纯;实验用水为二次去离子水。
1.2 实验方法
1.2.1MoS2QDs的合成称取0.25 g Na2MoO4·2H2O,溶于25 mL去离子水中,室温下超声5 min后,用0.1 mol/L HCl调节pH至6.5之后,将50 mL 浓度为5 g/L的L-半胱氨酸水溶液加入上述溶液中,继续超声10 min。将混合物转入水热反应釜中在200 ℃下反应36 h。反应结束后过滤,将产物在4 ℃下储存备用。
1.2.2荧光探针检测Hg2+将200 μL MoS2QDs水溶液加入到含有不同浓度Hg2+的磷酸盐缓冲溶液(PBS,pH=7)中,将溶液充分混合后,置于室温下反应5 min。随后在330 nm激发波长下测定溶液的荧光强度。其中激发与发射的狭缝宽度设为10 nm。所有测试平行三次。
2 结果与讨论
2.1 MoS2 QDs的表征
图1(A)和图1(B)分别是MoS2QDs的透射电镜(TEM)和高倍透射电镜(HRTEM)图。从图1(A) 中可以看出:MoS2QDs为形状均一,大小较均匀,尺寸约为8 nm左右的单分散纳米晶体。同时在图1(B)中观察到明显的MoS2晶格条纹。

图1 MoS2QDs的透射电镜(TEM)(A)和高倍透射电镜(HRTEM)(B)图Fig.1 TEM (A) and HRTEM (B) images of MoS2 QDs
2.2 MoS2 QDs的光学性能
图2(A)为MoS2QDs 的荧光激发与发射光谱图。实验确定激发波长为330 nm,发射波长为400 nm。因此在紫外灯照射下观察到MoS2QDs 呈蓝光的现象。图2(B)为不同激发波长下MoS2QDs的发射光谱。考察了激发波长在300~380 nm范围内MoS2QDs 的荧光发射。由图可知,随着激发波长的逐渐增大,荧光强度也逐渐增强。当激发波长为330 nm时,其荧光强度达到最强,继续增大激发波长,荧光强度则逐渐减弱。因此选择330 nm为后续实验中MoS2QDs 的激发波长。在图中还可以观察到荧光发射光谱随着激发波长的逐渐增大产生红移现象,这说明在荧光激发过程中,MoS2QDs 本身发生了一些变化,如团聚现象。

图2 (A) MoS2 QDs 的荧光激发与发射光谱图(插图分别为可见光(左)和365 nm紫外灯照射下(右)的照片);(B)不同激发波长下MoS2 QDs 的荧光发射谱图Fig.2 (A) Fluorescence emission and excitation spectra of MoS2 QDs(Inset is the digital photograph of the MoS2 QDs aqueous solution (200 μL) under daylight (left) and 365 nm UV light (right));(B) Fluorescence emission spectra of MoS2 QDs at different excitation wavelengths
2.3 基于MoS2 QDs荧光猝灭法检测Hg2+

图3 MoS2 QDs红外(FI-IR)光谱图Fig.3 FT-IR spectrum of MoS2 QDs
图3为MoS2QDs的红外光谱图,可见在465 cm-1附近的弱峰归属于Mo-S振动,在2 955 cm-1处的峰为饱和C-H 伸缩振动,在低频区域1 564 cm-1和1 419 cm-1处的峰分别为不饱和碳碳键的伸缩振动和C-N键的伸缩振动,所有结果说明L-半胱氨酸可能包裹于MoS2的表面。
MoS2QDs荧光猝灭法检测Hg2+原理如图4所示。MoS2QDs是表面有L-半胱氨酸修饰的具有蓝色荧光的纳米材料,当MoS2QDs水分散体系加入Hg2+时,Hg2+会与L-半胱氨酸发生键合作用,使MoS2QDs荧光发生猝灭。

图4 基于MoS2 QDs 荧光猝灭法检测Hg2+示意图Fig.4 Schematic illustration of the Hg2+detection based on MoS2 QDs
从图5(A)可以看出,当体系中存在MoS2QDs时,其荧光强度为图中曲线a所示,当向体系中加入2.0×10-5mol/L的Hg2+时,其荧光强度减弱。从图5(B)中可以看出,向体系加入Hg2+时,紫外-可见吸收光谱发生红移。说明Hg2+可以使MoS2QDs的荧光发生猝灭,因此可以用MoS2QDs构建荧光探针检测Hg2+。

图5 MoS2 QDs和MoS2 QD5-Hg2+体系的荧光发射光谱(A)和紫外-可见吸收光谱(B)图Fig.5 The fluorescence emission spectra (A) and UV-Vis absorption spectra (B) of MoS2 QDs and MoS2 QDs-Hg2+ system
2.3.1测定条件优化对MoS2QDs荧光法测定Hg2+的实验条件进行了优化,结果见图6。选取pH范围为4.0~10.0,对MoS2QDs的pH进行优化。结果如图6(A)所示,随着pH的逐渐增大,MoS2QDs的荧光强度呈增加趋势,当pH增大到7.0时,荧光强度值F0达到最大,当pH继续增大时,F0有所减弱。因此,选择pH=7.0为MoS2QDs荧光检测Hg2+的最适宜pH。
在对测定条件反应时间的考察中,选择了MoS2QDs-Hg2+作用的时间范围为1~30 min。由图6(B)可以看出,随着反应时间的逐渐增加,MoS2QDs-Hg2+体系的荧光强度前后差值(F0-F)在2 min内有明显的增加,2 min后趋于平缓,再延长时间到30 min时,(F0-F)值也没有明显的增强。因此,选择反应时间2 min作为MoS2QDs检测Hg2+的最佳条件。
在温度条件的优化中,选择了25 ℃、37 ℃和50 ℃ 3个温度,从图6(C)中可以看出,当温度为37 ℃时,(F0-F)值最大,其他温度下MoS2QDs-Hg2+体系的荧光强度增幅不大,选取37 ℃为检测Hg2+的最佳温度。
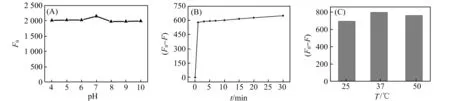
图6 MoS2 QDs溶液在不同pH(A)、反应时间(B)和反应温度(C)下的荧光光谱(F和F0分别是MoS2 QDs体系中有无Hg2+的荧光强度)Fig.6 Fluorescence spectra of MoS2 QDs solutions at different pH values (A),reaction time(B) and reaction temperature (C)(F0 and F are the fluorescence intensity of MoS2 QDs in the absence and presence of Hg2+)
2.3.2线性范围及检测限为了证实方法的可行性,采用MoS2QDs荧光猝灭法检测Hg2+。从图7(A)中可以看出,MoS2QDs的荧光强度随着Hg2+浓度的增加而减弱。此现象表明Hg2+能与MoS2QDs发生相互作用,从而荧光减弱。而图7(B)是Hg2+浓度与(F0-F)/F0的标准曲线。线性范围为5.0×10-7~2.0×10-4mol/L,相关系数R2=0.9983,检测限为2.3×10-7mol/L。

图7 (A) MoS2 QDs在含不同浓度Hg2+的PBS(pH=7.0)中的荧光发射光谱图(激发波长为330 nm);(B)(F0-F)/F0与Hg2+浓度的线性关系图Fig.7 (A) Fluorescence spectra of MoS2 QDs with different Hg2+ concentrations in PBS buffer (pH=7.0) under excitation at 330 nm;(B) Linear plots of the (F0-F)/F0 with Hg2+ concentration
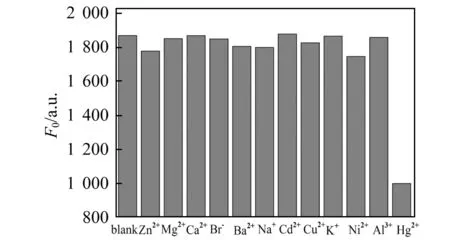
图8 MoS2 QDs 对Hg2+(5.0×10-6 mol/L)的选择性Fig.8 Selectivity of the MoS2 QDs toward 5.0×10-6 mol/L Hg2+ the concentrations of the other metal ions were 5.0×10-3 mol/L;all experiments were performed in pH=7.0 PBS buffer;excitation wavelength was 330 nm.
2.3.3方法的选择性在相同的反应条件下选取了一些常见金属阳离子作为干扰对象,所有物质的浓度均为5.0×10-3mol/L。如图8所示,结果表明只有加入Hg2+的时候荧光强度才会减弱,其余阳离子(如Zn2+、Mg2+、Ca2+、Al3+等)对MoS2QDs 的荧光强度基本上都没有明显影响。这就证明该方法对Hg2+具有较高的选择性。
2.4 实际样品分析
为了研究该方法的实用性,将该方法应用于自来水样品中Hg2+的检测。实验结果表明在自来水样品中未发现Hg2+,然后测量实际样品中Hg2+的回收率(表1)。这些结果表明我们的方法对自来水样品种Hg2+测定的可靠性。

表1 自来水样品中Hg2+的分析结果(n=6)Table 1 Analytical results ofHg2+in tap water samples(n=6)
3 结论
本工作采用水热法制备了L-半胱氨酸功能化的MoS2QDs。该MoS2QDs呈现较强的蓝色荧光性能,并具有较好的水溶性。当有Hg2+存在时,MoS2QDs的荧光发生猝灭,基于该原理发展了一种荧光法来检测自来水中的Hg2+。该方法具有较好的灵敏度和选择性,有望用于环境试样中Hg2+含量的检测。
参考文献:
[1] Wang H T,Lu Z Y,Xu S C,Kong D S,Cha J J,Zheng G Y,Hu P C,Yan K,Bradshaw D.Proceedings of the National Academy of Sciences of the United States of America,2013,110(49):19701.
[2] Mcchesney J L,Bostwick A,Seyller T,Horn K,Rotenberg E.Physical Review Letters,2010,104(13):13680.
[3] Jaramillo T F,Jorgensen K P,Bonde J,Nielsen J H,Horch S,Chorkendorff I.Science,2007,317(5834):100.
[4] Gu W,Yan Y,Cao X,Zhang C,Ding C,Xian Y J.Journal of Materials Chemistry B,2015,4(1):27.
[5] Ou J Z,Chrimes A F,Wang Y,Tang S Y,Strano M S,Kalantar-zadeh K.Nano Letters,2014,14(2):857.
[6] ZENG X D,ZHU L,WANG J G,et al.Journal of Analytical Science(曾晓丹,朱琳,王建刚,等.分析科学学报),2008,26(4):478.
[7] Liu Y,Liu C,Zhang Z.Applied Surface Science,2012,263(6):481.
[8] WU X J,LI Q,FEI J,WANG L F.Journal of Analytical Science(武晓剑,李琼,费玠,王丽芳.分析科学学报),2008,24(5):609.
[9] Wu D,Huang W,Lin Z,Duan C,He C,Wu S,Wang D.Inorganic Chemistry,2008,47(16):7190.
[10] Adhikari B,Banerjee A.Chemistry of Materials,2010,22(15):4364.
[11] Chen P,He C A.Journal of the American Chemical Society,2004,126(3):728.
[12] Guo C,Irudayaraj J.Analytical Chemistry,2011,83(8):2883.
[13] Chen Y,Bai H,Hong Y,Shi G.Analyst,2009,134(134):2081.
[14] Huang C C,Yang Z,Lee K H,Chang H T.Angewandte Chemie International Edition,2007,119(36):6948.
[15] Li T,Dong S J,Wang E.Analytical Chemistry,2009,81(6):2144.

