三七多聚半乳糖醛酸酶抑制蛋白基因的功能分析
关瑞攀,白智伟,王 倩,唐笔锋,崔秀明,刘迪秋
(昆明理工大学 生命科学与技术学院,云南省三七资源可持续利用重点实验室,云南 昆明 650500)
在生长发育过程中植物会受到多种生物和非生物胁迫,其中真菌病害是一类非常严重的生物胁迫。病原真菌在侵染植物的过程中会释放包括多聚半乳糖醛酸酶(Polygalacturonases,PG)在内的果胶降解酶和半纤维素降解酶来水解细胞壁,降低宿主细胞的抗性[1]。相应地,植物形成了特殊的防御机制来抑制真菌的侵染,如生成多聚半乳糖醛酸酶抑制蛋白(Polygalacturonase-inhibiting protein,PGIP)结合并抑制真菌分泌的PG活性[2]。PGIP蛋白属于富含亮氨酸重复(Leucine-rich repeats ,LRRs)蛋白超家族,包含了一个由10个不完整的LRR组成的功能性结构域,每个LRR由24个保守的氨基酸残基(xxLxLxx.NxLx..GxIPxxLxxL.xxL)组成,该序列是PGIP蛋白家族的共有序列,介导蛋白之间的相互作用[3]。
PGIP响应逆境胁迫,作为重要的植物防御蛋白在植物的防卫反应过程中起重要作用。壳聚糖(Chitosan)和茉莉酸甲酯(Methyl jasmonate,MeJA)处理草莓(Fragariachiloensis)能减少其被灰葡萄孢(Botrytiscinerea)侵染引起的灰霉病,在此过程中,FcPGIP1和FcPGIP2表达上调[4]。棉花(Gossypiumhirsutum)GhPGIP1的转录水平受MeJA、水杨酸(Salicylic acid ,SA)、过氧化氢(H2O2)、伤害处理以及黄萎病菌(Verticilliumdahlia)、枯萎病菌(F.oxysporumf. sp.vasinfectum)侵染的诱导[5]。烟草(Nicotianatabacum)NtPGIP响应低温(4 ℃)、SA、脱落酸(Abscisic acid,ABA)、盐(NaCl)处理以及疫霉菌(Phytophthoranicotianae)侵染[6]。将菜豆(Phaseolusvulgaris)PvPGIP2转化入小麦(Triticumaestivum)过量表达,在转基因小麦一叶期叶片接种根腐病菌(Bipolarissorokiniana)的孢子悬液,接种后72 h转基因小麦与非转基因小麦相比,病斑数少且病斑面积也小,表明PvPGIP2在小麦中的过量表达增强了小麦对根腐病菌的抗性,并且转基因小麦J82-23aT株系还提高了对禾谷镰刀菌(Fusariumgraminearum)的抗性[7-8]。在水稻(Oryzasativa)中过表达OsPGIP1增强了转基因水稻对立枯丝核菌(Rhizoctoniasolani)的抗性[9]。大豆(Glycinemax)GmPGIP3在小麦中的表达提高了敏感型小麦对根腐病菌的抗性[10]。
三七(Panaxnotoginseng(Burk.) F.H. Chen)为五加科人参属多年生植物,主要产自云南省文山州,具有“生打熟补”的功效,是我国传统的名贵中药。三七中主要的活性成分是三七总皂苷,研究表明,三七皂苷有改善记忆损伤模型动物的学习记忆功能、抗肿瘤、抗病毒、降低胆固醇及提高机体免疫力等多种生物活性,是预防心脑血管疾病的重要药物[11-14]。三七生长周期长,性喜温暖阴湿,对光敏感,需要在遮阳网下栽培,其独特的生长环境易诱发病虫害的发生,尤其是根腐病等真菌病害。在前期研究中,笔者从三七中克隆得到一个PGIP基因PnPGIP,表达分析结果表明,PnPGIP响应MeJA、乙烯(Ethylene,ETH)、H2O2和SA的处理,MeJA预处理三七接种茄腐镰刀菌(Fusariumsolani)后,PnPGIP的表达量呈现出先逐渐降低后缓慢升高又急速下降的趋势[15]。
为了研究PnPGIP的功能,本研究构建了PnPGIP的原核表达载体以获得PnPGIP的原核表达蛋白,并分析在体外的抑菌活性,进一步构建了PnPGIP的植物表达载体,通过根癌农杆菌介导产生转基因烟草并分析了转基因烟草对茄腐镰刀菌的抗性。
1 材料和方法
1.1 试验材料
野生型(Wild type,WT)烟草种子经表面消毒后播种在1/2 MS培养基上,萌发的无菌幼苗培养5周后用于转化遗传试验。试验中用到的病原真菌胶孢炭疽菌(Colletotrichumgloeosporioides)、核盘菌(Sclerotiniasclerotiorum)、茄腐镰刀菌和轮枝状镰刀菌(F.verticillioides)均保存于-4 ℃,使用前从斜面取出少量菌丝接种于PDA培养基上活化。
1.2 试验方法
1.2.1PnPGIP原核表达载体构建及His-PnPGIP重组蛋白的诱导表达和纯化 本试验采用pET-32(a)为原核表达载体。在扩增PnPGIPORF的1对特异引物的5′端分别添加限制性内切酶EcoR Ⅰ和SalⅠ的识别位点,合成特异性引物5′-GAATTCATGTTGTTAC
TCCTCTTCTTGATCT-3′和5′-GTCGACTCAAAATTTCC
AAGGATCAAGTG-3′用于扩增PnPGIP的ORF。扩增产物先连接至克隆载体pMD-18T(TaKaRa,Japan),然后提取pMD-18T-PnPGIP质粒,经限制性内切酶EcoR Ⅰ和SalⅠ消化后获得PnPGIP的ORF,pET-32(a)空载体经过同样的限制性内切酶消化后与PnPGIP的ORF连接。连接产物转化入大肠杆菌DH5α中,提取pET-32(a)-PnPGIP质粒,转化入大肠杆菌BL21(DE3)中,通过PCR筛选阳性菌株。
吸取1 mL BL21阳性单克隆菌液转接于100 mL LB液体培养基(含100 μL/mL 氨苄Ampicillin,Amp)中,于37 ℃、200 r/min振荡培养至OD600达到0.6~0.8。后将菌液冰上静置30 min左右,加入IPTG(Isopropyl β-D-1-thiogalactopyranoside,IPTG)至终浓度为1 mmol/L,之后分别在30,37 ℃诱导外源蛋白表达,7 h后取样。取未添加IPTG的菌液和加入相同浓度IPTG的空载体菌株为阴性对照进行SDS-PAGE以分析重组蛋白的最适诱导温度。最后加大培养量,在最适条件下诱导重组蛋白表达,取500 mL菌液收集菌体,加入结合Buffer和溶菌酶后超声30 min以破碎菌体,然后低温离心40 min,收集上清。重组蛋白的分离和纯化参考Chen等[16]的方法进行。
1.2.2 重组蛋白的体外抑菌试验 将4种供试真菌活化后接种于PDA培养基上,28 ℃倒置培养2~3 d。在菌落边缘均匀摆放无菌滤纸片(直径6 mm),依次将纯化的重组蛋白液点在放好的滤纸片上,点样量依次为10,25,50,100 μg,使用无菌水和溶解蛋白的Buffer为阴性对照。将真菌置于28 ℃培养2~3 d,记录重组蛋白对几种病原真菌菌丝生长的影响。
1.2.3PnPGIP植物过表达载体的构建 在扩增PnPGIPORF的1对特异引物的5′端分别添加限制性内切酶BamH Ⅰ和EcoR Ⅰ的识别位点,上下游引物的序列分别为5′-GGAAGACCAATGTTGTTACTCCTCT-3′和5′-TCCATTGAGTACTAGGGAAACCATG-3′。扩增产物首先连接到pGEM-T载体上用BamH Ⅰ和EcoR Ⅰ消化pGEM-T-PnPGIP质粒获得PnPGIP的ORF,然后与双酶切过的植物表达载体pCAMBIA2300S连接。将连接产物转化入大肠杆菌DH5α中,通过PCR挑选阳性单克隆。提取阳性克隆的质粒,采用冻融法将pCAMBIA2300S-PnPGIP质粒转化入根癌农杆菌(Agrobacteriumtumefaciens)LBA4404菌株中,筛选获得阳性克隆。
1.2.4 农杆菌介导的烟草遗传转化 活化携带pCAMBIA2300S-PnPGIP质粒的农杆菌菌株,在无菌条件下侵染WT烟草无菌苗的叶盘,侵染结束吸干叶盘上的菌液,将叶盘置于共培养培养基上暗培养2 d,之后叶盘转移到分化培养基上进行光照培养(25 ℃,光照16 h/d)。将叶盘分化再生出的幼苗移至含有50 mg/L卡那霉素和100 mg/L头孢霉素的生根培养基中诱导幼苗生根。用CTAB法提转基因烟草植株叶片的DNA,以转基因植株基因组DNA为模板,用扩增PnPGIP的特异性引物进行PCR,筛选获得转基因阳性植株。随机挑选10个T0转基因单株通过套袋自交结合PCR分析获得T2转基因株系。
1.2.5 荧光定量PCR(Quantitative reverse transcription-PCR,qRT-PCR) 用总RNA试剂盒(Gene Star,康润)提取T2转基因烟草叶片的RNA,逆转录合成第1链cDNA。后取0.2 μL逆转录产物为模板,PnPGIP特异性引物(5′-CATACCTCAAGAGACTTCGGCTTC-3′和5′-AGGGAGAGTGGAATTGAGCCAT-3′)进行Real-time PCR,以分析PnPGIP在T2转基因烟草中的表达水平。反应条件为:50 ℃ 2 min,95 ℃ 10 min;95 ℃ 15 s,60 ℃ 1 min,40个循环,之后进行熔解曲线分析,qRT-PCR中每个反应均设置3次重复,以烟草NtACT基因(GenBank登录号AB158612.1)作为内参基因。将Ct值最大的转基因株系中PnPGIP的表达值设置为1,采用2-ΔΔCT法计算得出其他株系中PnPGIP的相对表达水平。采用SPSS软件中Duncan′s multiple range test分析转基因株系与WT之间的差异显著性。
1.2.6 转基因烟草抗病性分析 选择表达水平较高的4个T2转基因烟草株系进行抗病性分析。取大小均一且完全伸展的转基因烟草和WT烟草叶片,分别用灭菌的枪头造成伤口并在伤口处接种200 μL的茄腐镰刀菌孢子悬液。将接种好的叶片放置在湿润的滤纸上,用保鲜膜包裹后置于光照培养箱(25 ℃,光照16 h/d)中。接种7 d后收集叶片,观察叶片的发病情况。
2 结果与分析
2.1 PnPGIP原核表达蛋白的SDS-PAGE分析及纯化
在前期研究中,从三七中克隆得到1个多聚半乳糖醛酸酶抑制蛋白基因PnPGIP,表达特性分析表明,PnPGIP受三七根腐病菌茄腐镰刀菌侵染的诱导,还响应茉莉酸甲酯、水杨酸等胁迫相关信号分子的处理。为了分析PnPGIP蛋白的活性,本研究构建了PnPGIP的原核表达载体pET-32(a)-PnPGIP,并转入大肠杆菌BL21菌株中表达。添加1 mmol/L IPTG条件下分别在30,37 ℃诱导PnPGIP蛋白的表达,SDS-PAGE检测结果如图1所示,重组蛋白分子量约为46 ku,30 ℃,1 mmol/L IPTG、200 r/min的诱导条件下重组蛋白有较高的表达量。根据这个条件大量诱导表达重组蛋白后纯化蛋白,SDS-PAGE分析结果表明,纯化的蛋白液中重组蛋白的浓度和纯度都很高。

M.蛋白Marker;1,2. 1 mmol/L IPTG、200 r/min条件下,分别在37,30 ℃诱导重组蛋白表达;3.未添加IPTG的蛋白表达条带;4.添加1 mmol/L IPTG诱导空载体转化菌体蛋白表达条带;5.镍柱纯化后的重组蛋白。
M.Protein Marker;1,2.The expression of recombinant protein induced at 37,30 ℃,1 mmol/L IPTG and 200 r/min,respectively;3.Band of the expression of recombinant protein without IPTG;4.Band of cell protein expression of cells with no-load body added 1 mmol/L IPTG;5.Band of recombinant protein purified from nickel column.
图1PnPGIP原核表达重组蛋白的诱导和纯化
Fig.1InductionandpurificationofprokaryoticexpressionrecombinantproteinofPnPGIP
2.2 PnPGIP重组蛋白明显抑制4种病原真菌菌丝的生长
分别将10,25,50,100 μg PnPGIP重组蛋白依次点在滤纸片上,培养2 d后观察,发现滴有ddH2O的滤纸片对胶孢炭疽菌、核盘菌、茄腐镰刀菌和轮枝镰刀菌菌丝生长几乎没有任何抑制作用,而滴有磷酸缓冲液的滤纸片表现出极轻微的抑制效果(图2)。相对于这2个阴性对照,PnPGIP重组蛋白对4种供试真菌的生长均具有很明显的抑制作用,并且随着蛋白量的增加,抑制活性也逐渐增强(图2),尤其是100 μg PnPGIP蛋白液对胶孢炭疽菌和茄腐镰刀菌菌丝的生长具有很强的抑制作用。
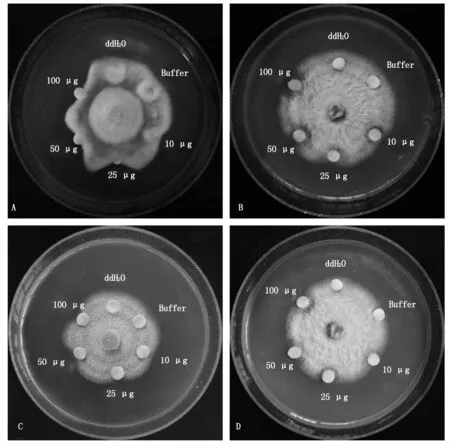
ddH2O.无菌双蒸水;Buffer.磷酸缓冲液;A.胶孢炭疽菌;B.核盘菌;C.茄腐镰刀菌;D.轮枝镰刀菌。ddH2O.Double distilled water;Buffer.Phosphate Buffer;A. C. gloeosporioides;B.S. sclerotiorum;C.F. solani;D. F. verticillioides.
2.3 PnPGIP转基因烟草的产生和筛选
为了深入研究PnPGIP的生物学功能,本试验构建了植物过表达载体pCAMBIA2300S-PnPGIP,采用根癌农杆菌介导分4批侵染了100多个烟草叶盘。再生的烟草幼苗首先经过卡那霉素筛选,再挑选生长正常的植株提取基因组DNA。使用扩增PnPGIP的特异引物以转基因烟草的基因组DNA为模板进行PCR,筛选出56棵阳性转基因植株,其中部分烟草PCR筛选结果如图3所示。将烟草种在温室中,PnPGIP转基因烟草和野生型烟草在生长过程中没有可见的形态差异。随机挑选10个生长正常的T0转基因单株通过套袋自交结合PCR分析获得T2转基因株系。
2.4 PnPGIP在T2转基因烟草中大量表达
为了确保PnPGIP在转基因烟草中稳定遗传并表达,本研究利用qRT-PCR分析T2转基因植株中PnPGIP的表达量。结果表明,在这10个T2转基因株系中均检测到PnPGIP转录物的积累,而在WT烟草中没有发现PnPGIP的转录产物(图4)。在P9株系中,PnPGIP的表达量较其他转基因株系高,是P23的30多倍。P1、P6和P17中的外源基因表达量也很高,在P23株系中,PnPGIP的表达量最低。由此可见,过表达载体上的CaMV 35S启动子正常指导PnPGIP在转基因植株中的表达,且表达稳定。挑选表达量较高的4个转基因株系进行下一步试验。
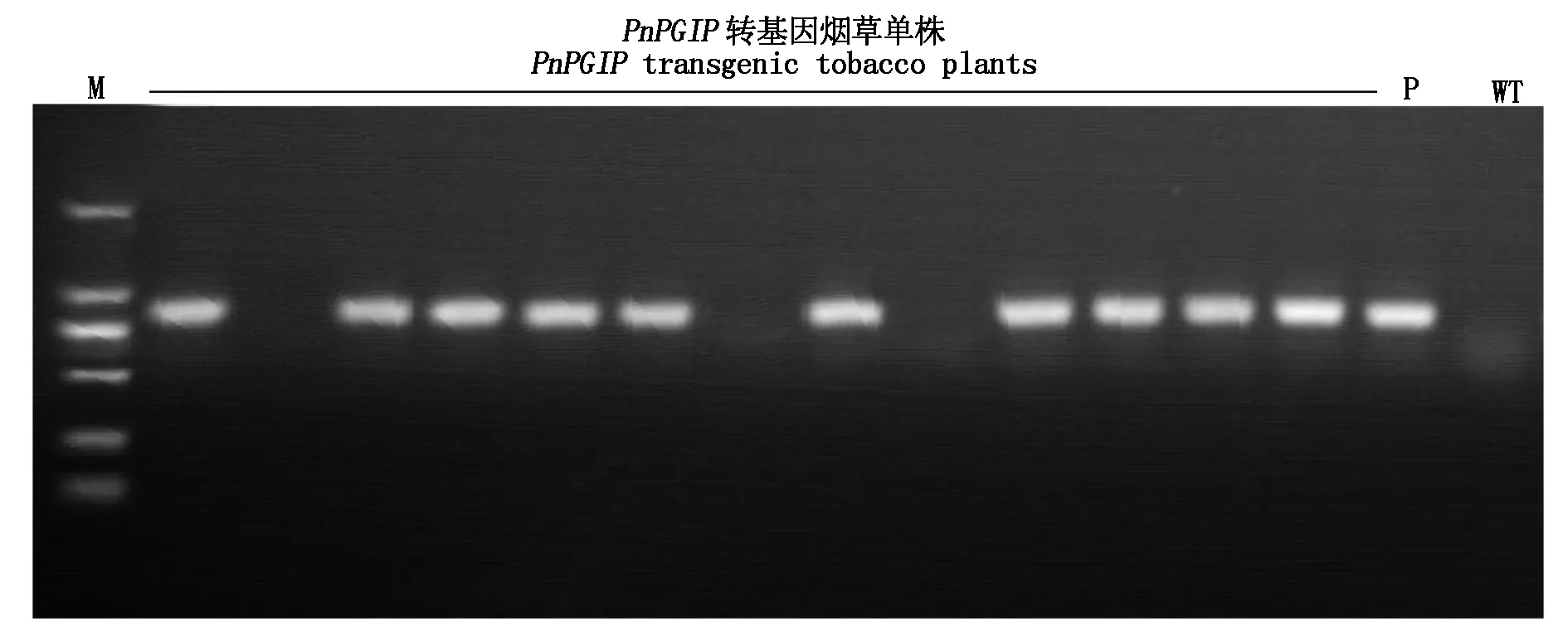
P.阳性对照pCAMBIA2300S-PnPGIP质粒;WT.野生型烟草;M.DL2000 Marker。P.Positive control pCAMBIA2300S-PnPGIP plasmid;WT.Wild type tobacco;M.DL2000 Marker.
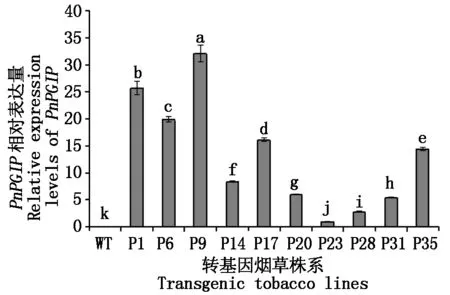
WT.野生型烟草;P1、P6、P9、P14、P17、P20、P23、P28、P31、P35.PnPGIP转基因烟草株系;图中不同小写字母表示差异有显著性(P<0.05)。
WT.Wild type tobacco;P1,P6,P9,P14,P17,P20,P23,P28,P31,and P35. Lines ofPnPGIPtransgenic tobacco;The letters a,b,c,d,e,f,g,h,i,j and k,showed the significant difference (P<0.05).
图4T2PnPGIP转基因烟草的表达水平分析
Fig.4ExpressionlevelanalysisofPnPGIPT2transgenictobaccolines
2.5 PnPGIP超表达显著增强了转基因烟草对茄腐镰刀菌的抗性
为了评价PnPGIP转基因烟草的抗性水平,株系P1、P6、P9、P17以及WT烟草的幼嫩叶片受伤处理后接种茄腐镰刀菌的孢子悬液,接种7 d后叶片的发病情况如图5所示,WT叶片在接种7 d后出现了严重的黄化、腐烂现象,而转基因株系的叶片只在接种的伤口附近出现了轻微腐烂以及叶片局部的黄化。显然,PnPGIP在烟草中的超表达大大增强了转基因烟草对茄腐镰刀菌的抗性,表明PnPGIP是三七中参与抵抗根腐病菌侵染的一个重要防卫基因。

WT.野生型烟草叶片;P1、P6、P9、P17.PnPGIP转基因烟草。WT. Leaves of wild type tobacco;P1,P6,P9,P17.Leaves of PnPGIP transgenic tobaccos.
3 讨论
因其化学成分具有多种多样的生物活性,三七已经成为中草药基础和应用研究的焦点之一。然而,三七的生长周期长、病害多发,农药的大量使用对三七药材安全性的影响引起了广泛的关注。而三七抗病遗传育种方面的探索研究鲜见报道,遗传育种研究的滞后已成为三七产业健康可持续发展的限制因素。云南省三七资源可持续利用重点实验室发现,外源茉莉酸甲酯能显著诱导三七对根腐病菌的抗性,进而通过转录组测序获得了大量响应茉莉酸甲酯的抗病相关基因,并对PnPGIP、PnNAC1等基因进行了克隆和表达特性分析[15,17]。为了深入认识三七的抗病机制并挖掘抗病功能基因,本研究采用反向遗传学方法验证了PnPGIP的功能。
PGIP是一类富含亮氨酸重复序列蛋白,属于植物胞外的富含亮氨酸重复序列蛋白超家族,是植物防御系统的一部分[18]。病原真菌侵染植物的过程中释放PG水解植物细胞壁及胞间层的果胶物质,在此过程中PGIP通过与PG结合形成寡聚半乳糖醛酸(Oligogalacturonides,OGs),从而抑制PG活性,且OGs能激发植物体内的防御反应从而增强植物的抗性[19-21]。将烟草基因NtPGIP转入大肠杆菌表达,得到的重组蛋白明显抑制辣椒(Capsicumannuum)疫霉(P.capsici)的PG活性[6]。辣椒CaPGIP1、CaPGIP2和CaPGIP3的重组蛋白对烟草链格孢菌(Alternariaalternata)和烟草炭疽病菌(C.nicotianae)的PG活性有明显的抑制作用[22]。然而,PGIP蛋白的直接抑菌活性却鲜有报道。将深绿木霉(Trichodermaatroviride)带有几丁质结合域的chit42和菜豆基因PG1P2转入油菜(Brassicanapus)中共表达,从阳性转基因油菜叶片中提取的粗蛋白具有很高的几丁质酶活性和PGIP活性,平板抑菌实验表明,粗蛋白还抑制核盘菌菌丝的生长,抑制率约为44%[23]。将火把梨(Pyruspyrifolia)PpPGIP基因转入烟草中过量表达,转基因烟草粗蛋白对茎点霉菌拟茎点霉(Phomopsissp.)、链格孢菌(Alternariasp.)、青霉属(Penicilliumsp.)和黑曲霉(Aspergillusniger)菌丝的生长有不同程度的抑制作用[24]。本研究构建了三七PnPGIP的原核表达载体,诱导表达PnPGIP重组蛋白,用纯化的重组蛋白进行平板抑菌实验,结果发现,PnPGIP重组蛋白对胶孢炭疽菌、核盘菌、茄腐镰刀菌和轮枝镰刀菌的菌丝体生长均有非常明显的抑制作用,体外的抑菌活性表明,PnPGIP蛋白可能作为一种抑菌蛋白直接参与三七抵抗病原真菌侵染的防御过程。
反向遗传学研究提供了PGIPs是抗病功能基因的更多证据。与非转基因小麦相比,PvPGIP2转基因小麦的花穗在受禾谷镰刀菌侵染后的赤霉病症状较WT减少25%以上,可见,PvPGIP2的表达增强了小麦对禾谷镰刀菌的抗性[25]。Atpgip1或者Atpgip2在拟南芥(Arabidopsisthaliana)中过量表达显著减轻了由灰葡萄孢引起的病害症状,用禾谷镰刀菌接种Atpgip1或Atpgip2转基因拟南芥花序,死花序百分比分别较WT降低了30%和50%[8,26],而利用反义基因沉默AtPGIP1基因的表达,增加了拟南芥对灰葡萄孢的敏感性[27]。葡萄(Vitisvinifera)VvPGIP1转入烟草中表达,阳性转基因株系叶片接种灰葡萄孢菌孢子悬液后的感病率较WT降低了47%~69%[28]。辣椒CaPGIP1的表达使转基因烟草受链格孢菌侵染引起的症状降低54.4%~62.7%,并且转基因烟草的炭疽病感病率降低了54.6%~57.7%[22]。除此之外,CaPGIP1转基因烟草的病斑数量和平均病斑面积较WT也显著减少,而CaPGIP1基因沉默的辣椒接种疫霉菌后产生的病斑是WT和转空载体辣椒的3倍。本研究中,三七PnPGIP的过量表达增强了转基因烟草对茄腐镰刀菌的抗性,表明PnPGIP在三七受茄腐镰刀菌的侵染过程中起重要作用。
综上所述,三七PnPGIP的原核表达蛋白对多种植物病原菌具有很强的体外抑菌活性,在模式植物烟草中的过量表达大大提高了转基因烟草对茄腐镰刀菌的抗性,PnPGIP无疑是三七中参与根腐病菌防卫反应的重要抗病基因。随着基因工程技术的广泛应用,来源于名贵中药材三七中的重要抗病功能基因PnPGIP将成为植物抗病基因工程中新的候选基因。
参考文献:
[1] Juge N. Plant protein inhibitors of cell wall degrading enzymes[J]. Trends in Plant Science,2006,11(7):359-367.
[2] De Lorenzo G,D′Ovidio R,Cervone F. The role of polygalacturonase-inhibiting proteins (PGIPs) in defense against pathogenic fungi [J]. Annual Review of Phytopathology,2001,39:313-335.
[3] Kobe B,Kajava A V. The leucine-rich repeat as a protein recognition motif[J]. Current Opinion in Structural Biology,2001,11(6):725-732.
[4] Saavedra G M,Sanfuentes E,Figueroa P M. Independent preharvest applications of methyl jasmonate and chitosan elicit differential upregulation of Defense-related genes with reduced incidence of gray mold decay during postharvest storage ofFragariachiloensisfruit[J]. International Journal of Molecular Sciences,2017,18(7):e1420.
[5] Liu N A,Zhang X E,Sun Y,et al. Molecular evidence for the involvement of a polygalacturonase-inhibiting protein,GhPGIP1,in enhanced resistance toVerticilliumandFusariumwilts in cotton[J]. Scientific Reports,2017,7:39840.
[6] Zhang C,Feng C,Wang J,et al. Cloning,expression analysis and recombinant expression of a gene encoding a polygalacturonase-inhibiting protein from tobacco,Nicotianatabacum[J]. Heliyon,2016,2(5):e110.
[7] Janni M,Sella L,Favaron F,et al. The expression of a bean PGIP in transgenic wheat confers increased resistance to the fungal pathogenBipolarissorokiniana[J]. Molecular Plant-microbe Interactions,2008,21(2):171-177.
[8] Ferrari S,Sella L,Janni M,et al. Transgenic expression of polygalacturonase-inhibiting proteins inArabidopsisand wheat increases resistance to the flower pathogenFusariumgraminearum[J]. Plant Biology,2012,14(S1):31-38.
[9] Wang R,Lu L,Pan X,et al. Functional analysis ofOsPGIP1 in rice sheath blight resistance[J]. Plant Molecular Biology,2015,87(1/2):181-191.
[10] Wang A Y,Wei X,Rong W,et al. GmPGIP3 enhanced resistance to both take-all and common root rot diseases in transgenic wheat[J]. Functional & Integrative Genomics,2015,15(3):375-381.
[11] 赵文萃,张 宁,周慧琴,等. 三七总黄酮对高血脂大鼠血脂的影响[J]. 中国实验方剂学杂志,2016(8):143-147.
[12] 张玉清,王 帅,景 娇,等. 5种中药总黄酮成分体外抗病毒作用观察[J]. 南京农业大学学报,2012,35(4):105-109.
[13] 刘艳娥,刘丽丽,房国涛. 三七抗肿瘤的实验研究概况[J]. 时珍国医国药,2008,19(4):1015-1016.
[14] 张小超,何 波,陈 鹏,等. 三七皂苷Rg1对学习记忆功能障碍的影响[J]. 中药药理与临床,2008,24(3):13-16.
[15] 陈 瑞,刘迪秋,李金晶,等. 三七多聚半乳糖醛酸酶抑制蛋白基因的克隆及表达分析[J]. 中草药,2016,47(24):4420-4427.
[16] Chen R,He H,Yang Y,et al. Functional characterization of a pathogenesis-related protein family 10 gene,LrPR10-5,fromLiliumregaleWilson[J]. Australasian Plant Pathology,2017,46(3):251-259.
[17] 王国东,李金晶,白智伟,等. 三七NAC转录因子基因PnNAC1的克隆及表达特性分析[J]. 华北农学报,2017,32(4):91-97.
[18] 李文娴,刘迪秋,葛 锋,等. 多聚半乳糖醛酸酶抑制蛋白的结构、功能以及应用研究进展[J]. 生物学杂志,2010,27(5):77-80.
[19] Di Matteo A,Federici L,Mattei B,et al. The crystal structure of polygalacturonase-inhibiting protein(PGIP),a leucine-rich repeat protein involved in plant defense[J]. Proceedings of the National Academy of Sciences of the United States of America,2003,100(17):10124-10128.
[20] Ridley B L,O′neill Ma,mohnen D.Pectins:structure,biosynthesis,and oligogalacturonide-related signaling[J]. Phytochemistry,2001,57(6):929-967.
[21] Ferrari S,Savatin D V,Sicilia F A,et al. Oligogalacturonides:plant damage-associated molecular patterns and regulators of growth and development[J]. Frontiers in Plant Science,2013,4(49):49.
[22] Wang X,Zhu X,Tooley P,et al. Cloning and functional analysis of three genes encoding polygalacturonase-inhibiting proteins fromCapsicumannuumand transgenicCaPGIP1 in tobacco in relation to increased resistance to two fungal pathogens[J]. Plant Molecular Biology,2013,81(4/5):379-400.
[23] Ziaei M,Motallebi M,Zamani M R. Co-expression of chimeric chitinase and a polygalacturonase-inhibiting protein in transgenic canola (Brassicanapus) confers enhanced resistance toSclerotiniasclerotiorum[J]. Biotechnology Letters,2016,38(6):1021-1032.
[24] Liu D Q,Li W X,He X,et al. Characterization and functional analysis of a novelPGIPgene fromPyruspyrifoliaNakai cv Huobali[J]. Acta Physiologiae Plantarum,2013,35(4):1247-1256.
[25] Tundo S,Janni M,Moscetti I,et al. PvPGIP2 accumulation in specific floral tissues but not in the endosperm limitsFusariumgraminearuminfection in wheat[J]. Molecular Plant-Microbe Interactions,2016,29(10):815-821.
[26] Ferrari S,Vairo D,Ausubel F M,et al. Tandemly duplicatedArabidopsisgenes that encode polygalacturonase-inhibiting proteins are regulated coordinately by different signal transduction pathways in response to fungal infection[J]. Plant Cell,2003,15(1):93-106.
[27] Ferrari S,Galletti R,Vairo D,et al. Antisense expression of theArabidopsisthalianaAtPGIP1 gene reduces polygalacturonase-inhibiting protein accumulation and enhances susceptibility toBotrytiscinerea[J]. Molecular Plant-Microbe Interactions,2006,19(8):931-936.
[28] Joubert D A,Slaughter A R,Kemp G,et al. The grapevine polygalacturonase-inhibiting protein (VvPGIP1) reducesBotrytiscinereasusceptibility in transgenic tobacco and differentially inhibits fungal polygalacturonases[J]. Transgenic Research,2006,15(6):687-702.

