肝硬化合并门静脉血栓形成的危险因素分析
吕笑娟,孙亚星,冯永星,李东颖,李建生
郑州大学第一附属医院消化内科,河南 郑州 450052
门静脉血栓(portal vein thrombosis,PVT)是指形成在门静脉主干或累及肠系膜上静脉、脾静脉及肠系膜下静脉的血栓,在一般人群中是一种罕见疾病,但在肝硬化患者中出现概率很高,可能引起肠系膜缺血坏死等严重并发症,甚至危及生命。在肝硬化患者中PVT的发病率为0.6%~26%[1]。PVT的发病率随肝脏疾病严重程度的增加而增加,可根据年龄、肝脏疾病、门静脉血流速度、抗凝状态等的变化而变化。Child-Pugh A级和B级的肝硬化患者1年和5年后的新诊断PVT发生率为4.6%~10.7%[2]。PVT也是影响肝移植预后的危险因素[3]。在一项肝移植患者的大型评估性研究中显示,约6.3%的肝硬化患者被诊断为PVT。在晚期肝硬化接受肝移植的患者中,PVT发病率为5%~16%[4]。本研究旨在探讨肝硬化合并PVT形成的危险因素,以早期发现及预防PVT的形成,早期治疗,改善患者预后。
1 资料与方法
1.1一般资料选取2014年8月至2016年8月郑州大学第一附属医院收治的具有完整资料的肝硬化患者712例,其中肝硬化合并PVT患者57例,选取同时期肝硬化无PVT患者63例。肝硬化患者诊断标准:按照慢性乙型肝炎防治指南[5]和酒精性肝病诊疗指南[6]诊断,PVT或非PVT患者均经彩色多普勒或增强CT或MRI成像诊断。排除标准:肝癌及其他恶性肿瘤、肝移植、非肝脏疾病并发PVT、布-加综合征、服用抗凝或抗血小板药物、外周血管疾病等病例。
1.2研究方法采用回顾性分析,统计收集PVT组和对照组病例资料,一般资料包括性别、年龄、脾切除史、糖尿病史、肝硬化病因(乙肝、丙肝、自免肝、酒精性)、Child-Pugh分级,实验室检查资料包括白细胞(white blood cell, WBC)、血红蛋白(hemoglobin, HB)、血小板计数(platelet count, PLT)、白蛋白(albumin, ALB)、总胆红素(total bilirubin, TBIL)、凝血酶原时间(prothrombin time, PT)、活化部分凝血酶原时间(activited partial thomboplastin time, APTT)、D-二聚体(D-dimer),彩超检查资料:门静脉主干直径(main portal vein width, MPV)、脾脏厚度、门静脉血流速度。

2 结果
2.1一般资料PVT组患者57例,男32例,女25例,年龄32~67岁,平均年龄56岁;对照组患者63例,男40例,女23例,年龄32~67岁,平均年龄54岁。PVT组与对照组在性别、年龄、肝硬化病因、脾切除史方面相比,差异无统计学意义(P>0.05),但在糖尿病史、Child-Pugh分级方面相比,差异有统计学意义(P<0.05)(见表1)。
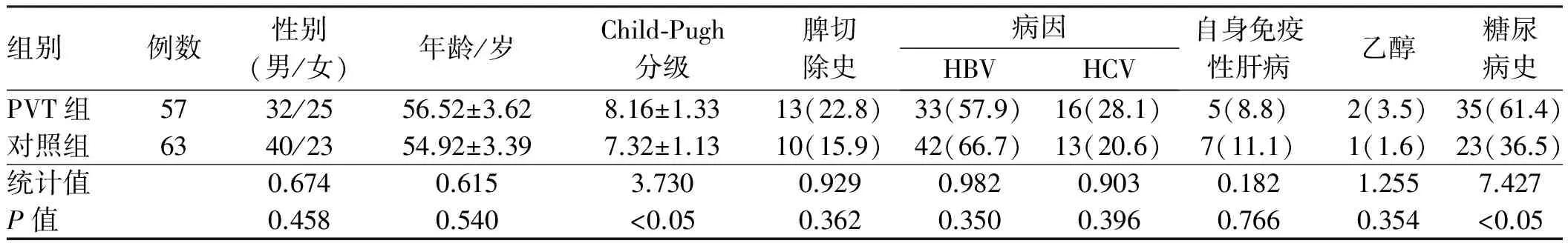
表1 患者一般资料Tab 1 General clinical data of patients
2.2实验室和影像学检查PVT组与对照组在WBC、ALB、TBIL、APTT、PT之间差异无统计学意义(P>0.05);PVT组HB、PLT、门静脉血流速度均较对照组低,差异有统计学意义(P<0.05),D-二聚体、MPV、脾脏厚度数值偏高,与对照组相比,差异有统计学意义(P<0.05)(见表2)。
2.3非条件性Logistic回归分析结果将单因素分析差异有统计学意义指标进行非条件性Logistic回归分析,结果显示,糖尿病史、Child-Pugh分级、D-二聚体升高、门静脉血流速度减慢是肝硬化合并PVT的危险因素(见表3)。
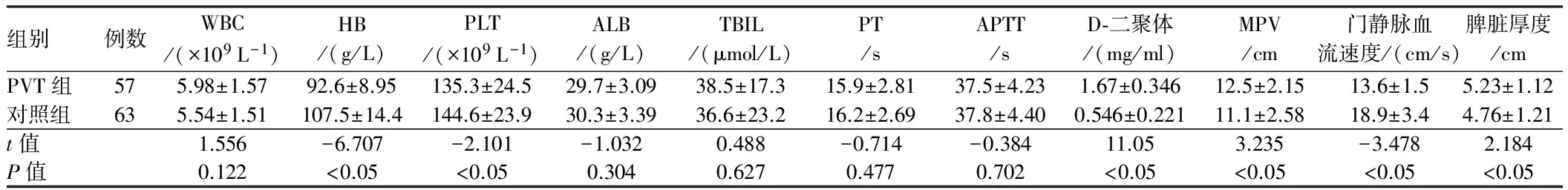
表2 患者检验及检查资料Tab 2 Patients with laboratory examination and inspection data
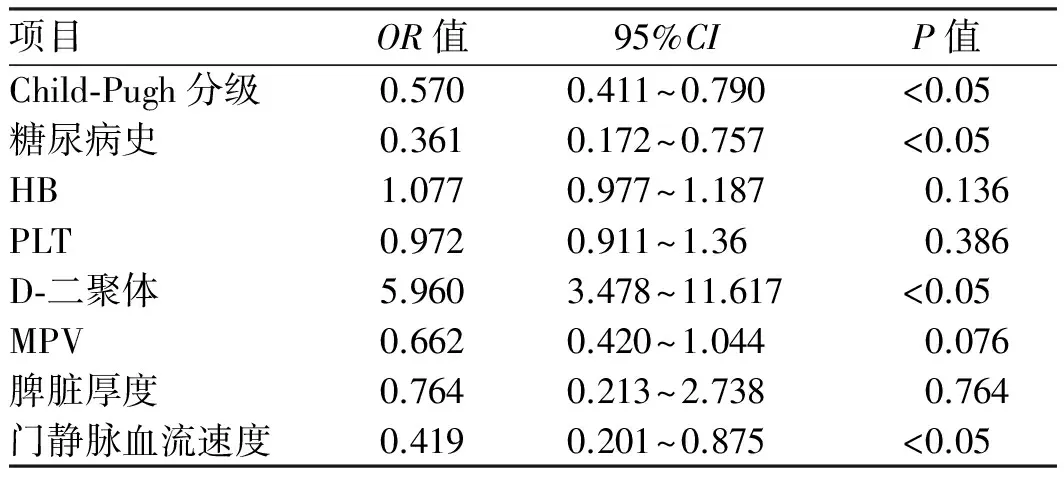
表3 非条件Logistic回归分析结果Tab 3 Non-conditional Logistic regression analysis
3 讨论
在肝硬化患者中,PVT常在随访筛查过程中被超声诊断,临床症状不特异[7]。通常难以解释具体症状,更准确地说,PVT可定义为一组临床综合征。PVT与病情严重程度没有必然的因果关系,但PVT的出现可能加速病情演变。临床病情加重可能是新发PVT或肝硬化进展引起失代偿的结果。临床上需要掌握肝硬化患者并发PVT的高危因素,进而从根本上预防和治疗PVT,以提高患者生存质量,改善肝硬化合并PVT患者的预后。
本研究结果显示,糖尿病史是肝硬化合并PVT的独立危险因素。这与ABDEL-RAZIK等[8]的研究结果相同。长期高血糖可导致体内NO合成减少,从而使血管内皮舒张功能降低,同时高血糖介导的炎症反应也在糖尿病大血管病变的发生、发展中起重要作用。Child-Pugh分级是综合评价肝硬化患者肝功能的常用指标,越高的Child评分表明肝功能损伤越重,肝脏又是维持机体凝血系统和纤溶系统动态平衡的重要脏器,肝硬化患者肝功能受损可导致凝血与抗凝失衡,这可能是Child-Pugh分级成为肝硬化合并PVT危险因素的原因,且有研究[9]表明,增加凝血因子Ⅷ水平、ALB减少更易使凝血系统平衡向高凝状态倾斜,从而促进PVT的形成。D-二聚体是纤维蛋白降解过程中的产物,对深静脉血栓及肺栓塞的阴性诊断有较高的敏感性,ZHANG等[10]的一项回顾性研究表明,D-二聚体水平的升高可能诱发肝硬化患者PVT的形成,此结论与本研究结果一致。
超声下门静脉血流速度下降到<15 cm/s,被证实为PVT的重要风险因素[11]。由于肝硬化患者肝实质硬化和血管反应性改建,肝内血管阻力增加导致门静脉血流减少、门静脉增宽,都会使门静脉血流动力学改变。STINE等[12]的一项匹配研究认为,门静脉血流速度的降低预示着门静脉血栓的发生。有研究[13]发现,使用非选择性β-受体阻滞剂在降低门脉压的同时也可以通过进一步减少门静脉血流量来促进PVT的发展,但仍存在争议。
肝硬化的病因对PVT发病的影响未得到充分证实,本研究中,HBV、HCV引起的肝硬化患者中是否合并PVT不具有统计学意义。当然,这需要进一步的数据来证实这些结果。有趣的是,有研究[14]证实,在肝移植患者中,当患者之前肝硬化病因与非酒精性或脂肪性肝炎相关时,常可检测到PVT。ABU EL-MAKAREM等[15]的一项研究发现,在丙肝患者中单核细胞组织因子(TF)表达增强可能在丙肝肝硬化患者的PVT发展中起到预测作用。
肝硬化合并PVT临床常用治疗方案是低分子肝素及口服维生素K拮抗剂,抗凝实现再通率为42%~75%[9],使用尿激酶或重组组织型纤溶酶原激活剂进行溶栓治疗的安全性和有效性仍存在争议,需要进一步探讨。在内科治疗无效情况下,可考虑行TIPS治疗,但PVT的治疗目前尚无统一的指南及共识,因此应根据患者不同临床特点采用个体化治疗。
综上所述,肝硬化合并PVT可促进或加重肝功能恶化,导致临床并发症并影响预后,也增加了肝硬化患者肝移植失败的风险。因此,对肝硬化患者应早期进行评估[16],早发现,早治疗,改善肝功能,减少PVT的发生。
[1] VON KOCKRITZ L, DE GOTTARDI A, TREBICKA J, et al. Portal vein thrombosis in patients with cirrhosis [J]. Gastroenterol Rep (Oxf), 2017, 5(2): 148-156. DOI: 10. 1093/gastro/gox014.
[2] NERY F, CHEVRET S, CONDAT B, et al. Causes and consequences of portal vein thrombosis in 1,243 patients with cirrhosis: results of a longitudinal study [J]. Hepatology, 2015, 61(2): 660-667.DOI: 10. 1002/hep.27546.
[3] STINE J G, PELLETIER S J, SCHMITT T M, et al. Pre-transplant portal vein thrombosis is an independent risk factor for graft loss due to hepatic artery thrombosis in liver transplant recipients [J]. HPB (Oxford), 2016, 18(3): 279-286.DOI: 10.1016/j.hpb.2015.10.008.
[4] HARDING DJ, PERERA M T, CHEN F, et al. Portal vein thrombosis in cirrhosis: controversies and latest developments [J]. World J Gastroenterol, 2015,21(22):6769-6784.DOI:10.3748/wjg.v21.i22.6769.
[5] 中华医学会肝病学分会, 中华医学会感染病学分会. 慢性乙型肝炎防治指南(2010年版) [J]. 中华肝脏病杂志, 2011, 19(1): 13-24. DOI: 10.3760/cma.j.issn.1007-3418.2011.01.007.
Chinese Society of Hepatology and Chinese Society of Infectious Diseases, Chinese Medical Association. The guideline of prevention and treatment for chronic hepatitisB (2010 version) [J]. Chin J Hepatol, 2011, 19(1): 13-24. DOI: 10.3760/cma.j.issn.1007-3418.2011.01.007.
[6] 中华医学会肝病学分会脂肪肝和酒精性肝病学组. 酒精性肝病诊疗指南(2010年修订版) [J]. 中华肝脏病杂志, 2010,18(3): 163-166. DOI: 10.3760/cma.j.issn.1007-3418.2010.03.003.
The Chinese National Workshop on Fatty Liver and Alcoholic Liver Disease for the Chinese Liver Disease Association. Guidelines for management of alcoholic liver disease: an updated and revised edition [J]. Chin J Hepatol, 2010, 18(3): 167-170. DOI: 10.3760/cma.j.issn.1007-3418.2010.03.003.
[7] 池添雨, 张玫. 肝硬化并发静脉血栓形成的危险因素分析 [J]. 胃肠病学和肝病学杂志, 2017, 26(1): 17-19. DOI: 10.3969/j.issn.1006-5709.2017.01.005.
CHI T Y, ZHANG M. Analysis of the risk factors of patients with cirrhosis and venous thrombosis [J]. Chin J Gastroenterol Hepatol, 2017, 26(1): 17-19. DOI: 10.3969/j.issn.1006-5709.2017.01.005.
[8] ABDEL-RAZIK A, MOUSA N, ELHELALY R, et al. De-novo portal vein thrombosis in liver cirrhosis: risk factors and correlation with the model for end-stage liver disease scoring system [J]. Eur J Gastroenterol Hepatol, 2015,27(5):585-592.DOI:10.1097/MEG.0000000000000325.
[9] CHAWLA Y K, BODH V. Portal vein thrombosis [J]. J Clin Exp Hepatol, 2015, 5(1): 22-40.DOI: 10.1016/j.jceh.2014.12.008.
[10] ZHANG D, HAO J, YANG N. Protein c and d-dimer are related to portal vein thrombosis in patients with liver cirrhosis [J]. J Gastroenterol Hepatol, 2010, 25(1): 116-121.DOI: 10.1111/j.1440-1746.2009.05921.x.
[11] ZOCCO M A, DI STASIO E, DE CRISTOFARO R, et al. Thrombotic risk factors in patients with liver cirrhosis: correlation with meld scoring system and portal vein thrombosis development [J]. J Hepatol, 2009, 51(4): 682-689.DOI: 10.1016/j.jhep.2009.03.013.
[12] STINE J G, WANG J, SHAH P M, et al. Decreased portal vein velocity is predictive of the development of portal vein thrombosis: a matched case-control study [J]. Liver Int, 2018, 38(1): 94-101.DOI: 10.1111/liv.13500.
[13] QI X S, BAI M, FAN D M. Nonselective β-blockers may induce development of portal vein thrombosis in cirrhosis [J]. World J Gastroenterol, 2014, 20(32): 11463-11466.
[14] STINE J G, SHAH N L, ARGO C K, et al. Increased risk of portal vein thrombosis in patients with cirrhosis due to nonalcoholic steatohepatitis [J]. Liver Transpl, 2015, 21(8):1016-1021.DOI:10.1002/lt.24134.
[15] ABU EL-MAKAREM M A, EL-AKAD A F, ELIAN M M, et al. Non-neoplastic portal vein thrombosis in HCV cirrhosis patients: is it an immuno-inflammatory disorder? [J]. Ann Hepatol, 2017, 16(4): 574-583.DOI: 10.5604/01.3001.0010.0296.
[16] 李丽, 刘潇, 陈东风. 肝硬化门静脉血栓形成的临床研究进展[J]. 胃肠病学和肝病学杂志, 2015, 24(11): 1303-1306. DOI:10.3969/j.issn.1006-5709.2015.11.006.
LI L, LIU X, CHEN D F. Advances in the clinical management of portal vein thrombosis in cirrhosis [J]. Chin J Gastroenterol Hepatol, 2015, 24(11): 1303-1306. DOI: 10.3969/j.issn.1006-5709.2015.11.006.

