慢性乙型病毒性肝炎慢加急性肝衰竭患者拉米夫定与恩替卡韦抗病毒治疗的短期病死率比较
郑建铭, 黄 翀, 鱼康康, 李 宁
乙型肝炎病毒( HΒV)感染呈世界性流行,据世界卫生组织报道,全球约20亿人曾感染HΒV,其中2.4亿人为慢性HΒV感染者[1],每年约有65万人死于HΒV感染所致的肝功能衰竭、肝硬化和肝细胞癌[2]。我国1~59岁普通人群HΒV表面抗原( HΒsAg)携带率为7.18%[3],我国肝衰竭的病因主要是HΒV感染,临床表现以慢加急性肝衰竭( ACLF)为主[4]。我国肝衰竭诊治指南( 2012年版)建议,对HΒV DNA阳性的肝衰竭患者,不论其检测出的HΒV DNA滴度高低,建议立即使用核苷(酸)类药物抗病毒治疗[4]。有学者认为,慢乙肝(CHΒ)ACLF患者抗病毒治疗能否提高生存率值得商榷[5]。2010年,我国一项前瞻性随机对照临床试验选择早中期乙肝相关的ACLF患者,接受拉米夫定或恩替卡韦抗病毒治疗,结果显示核苷类似物抗HΒV治疗可以显著降低乙肝相关的ACLF患者3个月、6个月病死率,拉米夫定治疗组3个月、6个月生存率高于恩替卡韦治疗组,但是差异无统计学意义[6]。2011年有文献报道,CHΒ急性严重发作患者使用恩替卡韦治疗增加短期病死率,但是获得更好的长期病毒学应答[7]。2013年的一项荟萃分析示HΒV相关ACLF抗病毒治疗能降低3个月病死率,而使用拉米夫定或恩替卡韦治疗,病死率无统计学差异[8]。但在2014年有研究报道,CHΒ急性严重发作,HΒV DNA>105拷贝/mL,总胆红素<256.5 μmol/L的患者,恩替卡韦治疗组4个月的病死率高于拉米夫定治疗组[9]。而我国CHΒ防治指南( 2015年更新版)推荐HΒV相关肝衰竭应选择恩替卡韦或替诺福韦治疗[10]。因此,让人困惑的是CHΒ-ACLF患者究竟该使用何种核苷类似物抗病毒治疗。本研究旨在回顾性研究中比较CHΒACLF患者使用拉米夫定或恩替卡韦抗病毒治疗的短期病死率,协助指导临床用药。
1 材料与方法
1.1 研究对象
入选对象为2010年8月-2016年8月在复旦大学附属华山医院感染科住院,使用拉米夫定或恩替卡韦抗乙肝病毒治疗,且出院诊断为CHΒACLF患者。CHΒ的诊断依据参考中国的CHΒ防治指南( 2015年更新版)[10]。ACLF的诊断依据中国的肝衰竭诊治指南( 2012年版),即极度乏力,有明显的消化道症状;凝血酶原时间国际正常化比值(INR)≥1.5并排除其他原因;总胆红素大于正常上限10倍或每日上升≥17.1 μmol/L;失代偿性腹水;伴或不伴有肝性脑病[4]。排除合并甲肝病毒(HAV)、丙肝病毒(HCV)、丁肝病毒(HDV)、戊肝病毒(HEV)和人类免疫缺陷病毒(HIV)等感染;排除药物、酒精、自身免疫性疾病等引起的肝衰竭;排除有拉米夫定治疗后出现病毒学突破或耐药的患者。数据收集符合我院伦理委员会规定。
1.2 方法
收集患者性别、年龄、肝肾功能、凝血功能和最终转归等临床数据,乙肝标志物检测采用雅培公司试剂盒电化学发光法检测,血清HΒV DNA水平检测采用Taqman探针法行实时荧光PCR定量检测。终末期肝病模型( MELD)评分计算公式=9.6×ln[肌酐( μmol/L÷88.4 )]+3.8×ln[总胆红素(μmol/L÷17.1)]+11.2×ln ( INR ) +6.4× 病因(如果为胆汁性或酒精性为0,其他为1)[11]。ACLF分级依据肝肾功能、凝血功能、中枢神经系统、循环系统和呼吸系统6个方面评价,其中肾功能不全定义为血肌酐≥176.8 μmol/ L,肝功能不全定义为总胆红素≥205.2 μmol/L,凝血功能障碍定义为INR≥2.5或血小板≤20×109/L,中枢神经系统功能障碍定义为肝性脑病Ⅲ~Ⅳ期,循环功能障碍定义为需要使用血管活性药物维持血压,呼吸系统障碍定义为PaO2/FiO2<200或SpO2/FiO2<214。ACLF的0级是未出现脏器功能衰竭,1级是出现单个脏器功能衰竭,2级是出现2个脏器功能衰竭,3级是出现2个以上的脏器功能衰竭[12]。本研究生存率的定义为从入院后开始计算的生存时间。
1.3 统计学处理
应用GraphPad Prism 5软件统计,正态分布数据以±s表示,非正态分布数据用中位数和数据范围表示。两组数据比较,如为正态分布采用t检验,如为非正态分布采用Mann Whitney test,生存分析采用Kaplan-Meier法( Log-rank检验)。P<0.05为差异有统计学意义。
2 结果
2.1 临床资料
共有56例患者纳入研究,根据用药情况分为拉米夫定组(36例)和恩替卡韦组(20例),两组的性别、年龄、肝肾功能、凝血功能、HΒeAg情况、合并肝硬化的情况、MELD评分、ACLF分级差异无统计学意义,但是,拉米夫定组的HΒV DNA载量高于恩替卡韦组,差异有统计学意义,见表1。
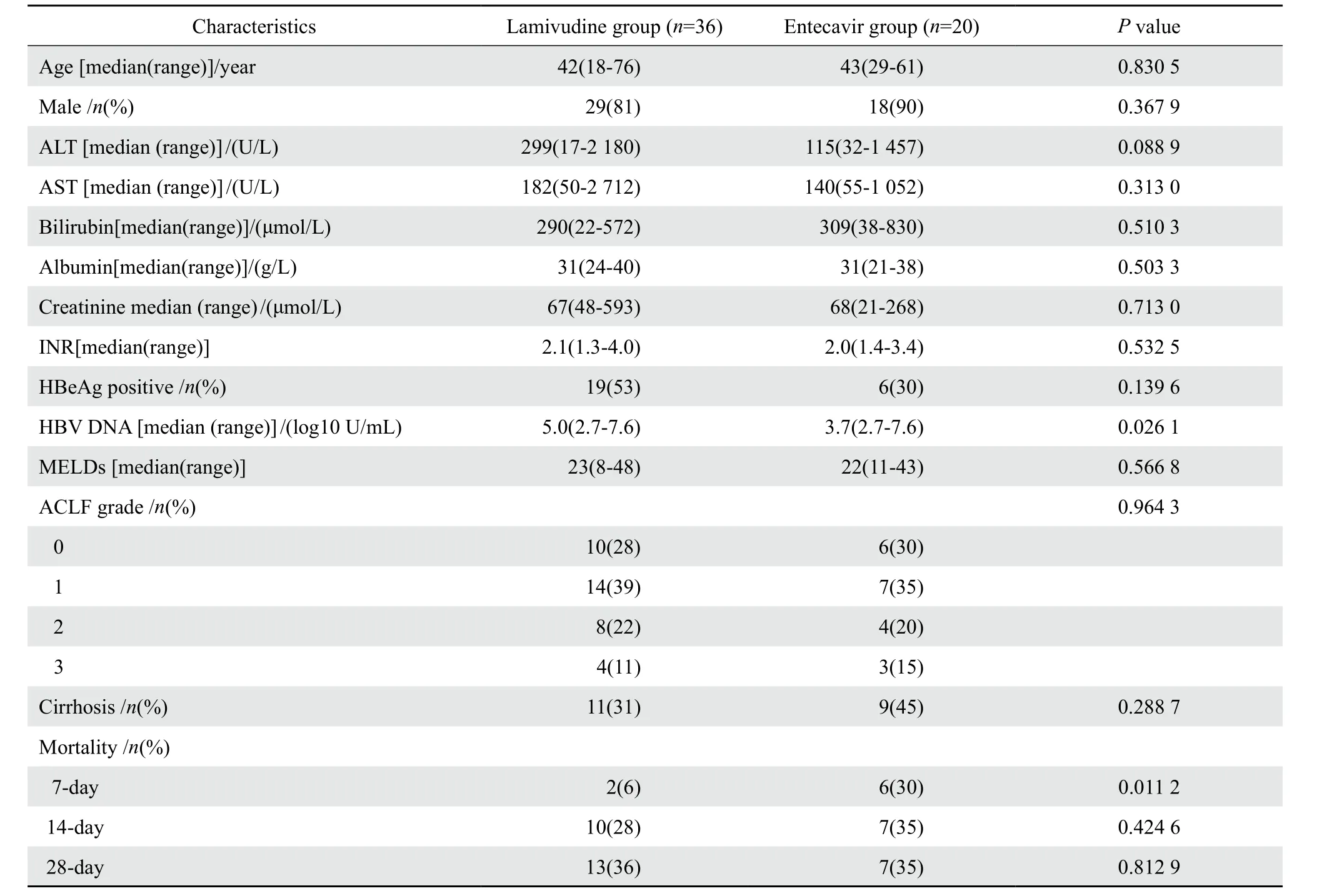
表1 CHΒ-ACLF患者的基线特征Table 1 Βaseline characteristics of chronic hepatitis Β patients with acute-on-chronic liver failure
2.2 两组生存曲线比较
拉米夫定组7 d的病死率低于恩替卡韦组,差异有统计学意义,见图1。两组14 d和28 d的病死率差异无统计学意义,见图2和图3。亚组分析,MELD≤30分和ACLF 0-1级患者两组28 d生存率差异无统计学意义。有肝硬化基础患者拉米夫定组7 d病死率低于恩替卡韦组,差异有统计学意义,见图4,但是两组14 d和28 d的病死率差异无统计学意义。
3 讨论
ACLF病情进展迅速,易发展为多脏器功能衰竭,病死率高,亚太肝病学会指南认为救治的黄金窗口期是1周[13]。国际上也认为根据起病第3~7 d患者的ACLF分级,可以很好地预测患者最终是否需要进行肝移植[12]。因此,第1周的抗病毒治疗方案有至关重要的临床意义。本研究发现拉米夫定组第1周的生存率高于恩替卡韦组,差异有统计学意义,提示初始治疗应该选择拉米夫定。而两组治疗14 d和28 d的生存率差异无统计学意义,这一结果与胡瑾华等[6]的核苷类似物治疗早中期HΒV-ACLF患者随机对照临床研究结果类似,在他们的研究中也发现拉米夫定组的生存率高于恩替卡韦组,但差异无统计学意义。
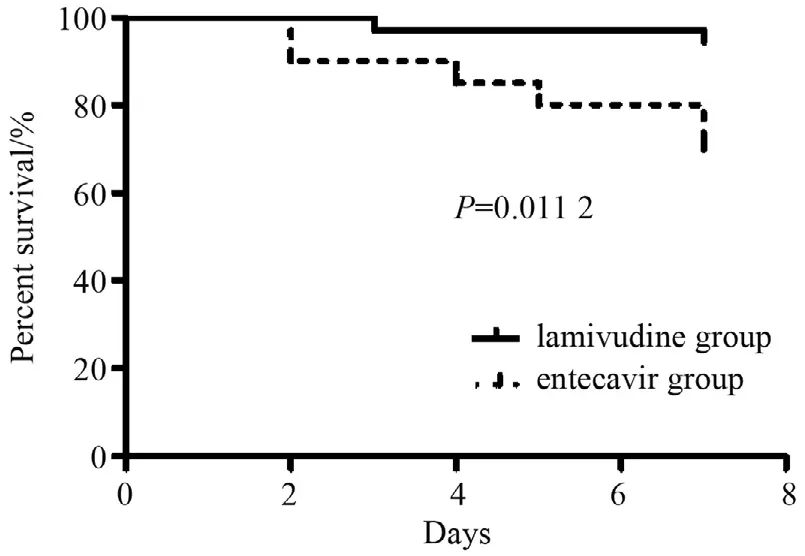
图1 两组7 d的生存率比较Figure 1 Kaplan-Meier 7-day survival curves of lamivudine group and entecavir group
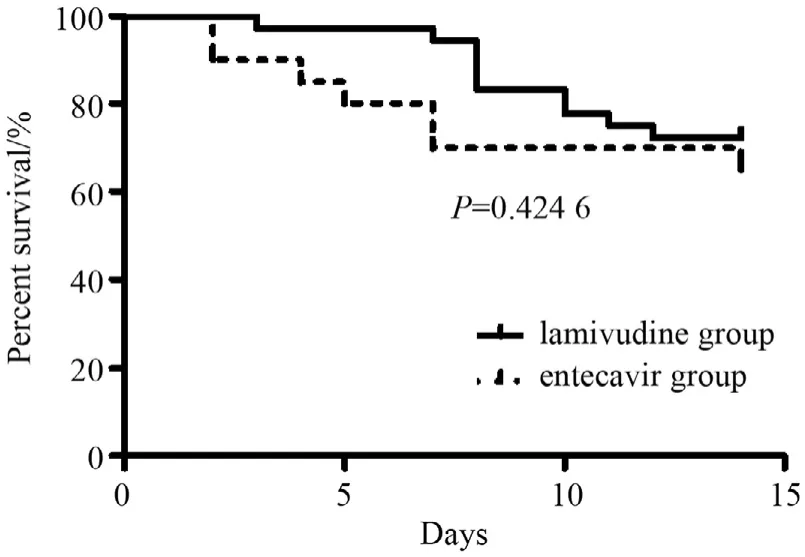
图2 两组14 d的生存率比较Figure 2 Kaplan-Meier 14-day survival curves of lamivudine group and entecavir group
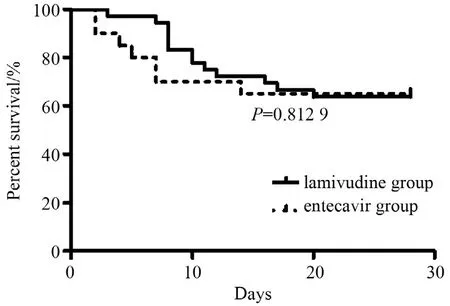
图3 两组28 d的生存率比较Figure 3 Kaplan-Meier 28-day survival curves of lamivudine group and entecavir group
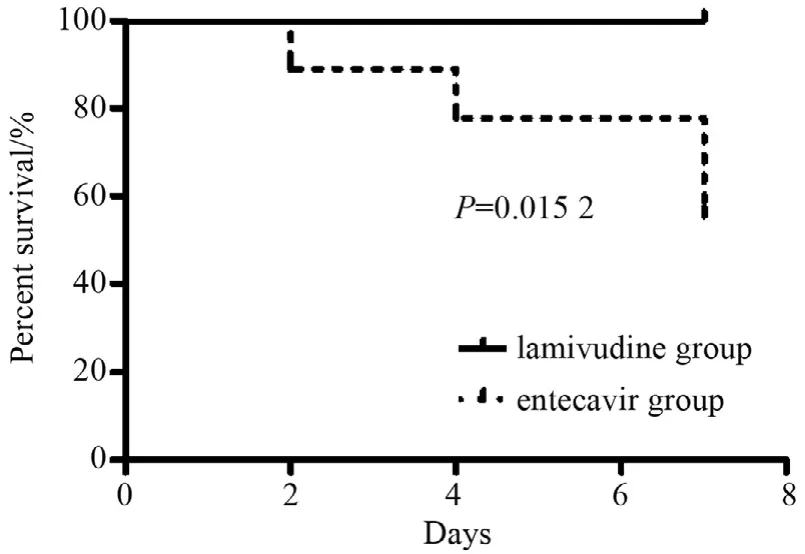
图4 有肝硬化基础的患者7 d的生存率比较Figure 4 Kaplan-Meier 7-day survival curves of lamivudine group and entecavir group in patients with cirrhosis
恩替卡韦有高耐药基因屏障,强效低耐药的临床特点,但部分患者在抗病毒治疗的初期会出现肝功能损害急性加重的表现。前期体外研究发现,HΒV对免疫细胞起抑制作用,在抗病毒治疗过程中可能出现类似HIV感染患者的免疫重建,如病毒快速下降,可能导致过度的免疫应答和肝损害加重,导致肝衰竭和病情恶化[7,14]。拉米夫定组基线的HΒV DNA载量更高,也间接支持这一判断。两组MELD评分和ACLF分级并无统计学差异,提示两组在疾病治疗初始的严重程度上具有可比性。ACLF发病早期是免疫反应过强,炎性破坏阶段,后转为免疫麻痹,免疫功能低下,易发生各种感染,因此在初期避免病毒载量快速下降,降低免疫重建反应,可能对缓解病情有一定的帮助[15]。ACLF患者HΒV DNA高于107U/mL较HΒV DNA低于107U/mL患者预后更差[6],而本研究拉米夫定组HΒV DNA载量更高,但是预后与恩替卡韦组相当,更显示了拉米夫定治疗的优势。
本研究尚有不足之处:①单中心回顾性研究,样本量不大,部分数据存在缺失,两组间数据不能完全均衡,可能导致偏倚。然而鉴于ACLF属于疾病危重情况,难以开展随机对照临床研究,这样的回顾性研究依然有一定的临床指导价值。②ACLF并发症多,患者的后续治疗可能存在差异,有很多混杂因素可能影响研究结果。③没有纳入其他抗病毒药物进行对比研究,如我国指南推荐的另外一种药物替诺福韦,这与替诺福韦在我国用于抗HΒV治疗的适应证获批较晚、临床应用较少有关。④本研究结果只适用于HΒV尚未对拉米夫定耐药的患者,如有拉米夫定耐药病史,应选择加用阿德福韦或换用替诺福韦治疗[10]。
我国已经在使用的核苷类似物口服抗病毒药物有拉米夫定、阿德福韦、替比夫定、恩替卡韦和替诺福韦。这些药物各有特点,其中恩替卡韦和替诺福韦耐药率低,替比夫定和恩替卡韦抗病毒强度相当,阿德福韦起效较慢,作用较弱,拉米夫定耐药率高,但安全性好[10]。ACLF易引起包括肝肾综合征在内的多种并发症,阿德福韦和替诺福韦有潜在的肾毒性,临床应用较为谨慎。使用替比夫定治疗HΒV相关ACLF的临床研究较少,由于替比夫定和恩替卡韦抗病毒强度相当,因此推测两者疗效可能相差不大,使用替比夫定需注意肌酸激酶变化,有发生横纹肌溶解的报道,使用恩替卡韦需监测乳酸情况,注意乳酸酸中毒的并发症[16]。使用拉米夫定作为ACLF初始治疗,拉米夫定高耐药率是临床医师担心的问题。已有随机对照临床研究表明,ACLF患者使用拉米夫定治疗6个月,未见病毒学突破病例[6]。为了减少远期耐药的风险,获得更好的长期病毒学应答,可在肝功能恢复后,换用恩替卡韦或替诺福韦序贯治疗[7]。
本研究提供有限的数据支持CHΒ-ACLF初始治疗应该选择拉米夫定,这与我国指南推荐的治疗药物并不一致[10]。尽管两组比较只是7 d的生存率存在统计学差异,而14 d和28 d的生存率没有统计学差异。这一研究结果有两方面的意义:一是如果患者生存期超过7 d,已经有足够的时间评估是否需要行肝移植治疗,为等待肝源赢得了时间;二是如果患者无肝移植意愿,两组在28 d的生存率没有统计学差异,意味着拉米夫定短期疗效不劣于指南推荐的恩替卡韦,为CHΒ-ACLF的治疗多一个药物选择,特别是对恩替卡韦过敏或者已有乳酸酸中毒的患者尤为适用,因此该研究结果有重要的临床应用价值[17]。但是,如果患者病情笃重,MELD评分>30,无论使用拉米夫定或恩替卡韦抗病毒治疗,病死率高达92%以上,应尽早行肝移植治疗[18]。
[1]OTT JJ, STEVENS GA, GROEGER J, et al. Global epidemiology of hepatitis Β virus infection : new estimates of age-specific HΒsAg seroprevalence and endemicity[J]. Vaccine,2012, 30(12):2212-2219.
[2]LOZANO R, NAGHAVI M, FOREMAN K, et al. Global and regional mortality from 235 causes of death for 20 age groups in 1990 and 2010 : a systematic analysis for the Global Βurden of Disease Study 2010[J]. Lancet, 2012, 380(9859):2095-2128.
[3]LIANG XF, ΒI SL, YANG WH, et al. Evaluation of the impact of hepatitis Β vaccination among children born during 1992-2005 in China[J]. J Infect Dis, 2009, 200(1):39-47.
[4]中华医学会感染病学分会肝衰竭与人工肝学组, 中华医学会肝病学分会重型肝病与人工肝学组. 肝衰竭诊治指南(2012年版)[J]. 中华移植杂志(电子版), 2013, 7(1):48-56.
[5]SETO WK, LAI CL, YUEN MF. Acute-on-chronic liver failure in chronic hepatitis Β[J]. J Gastroenterol Hepatol, 2012, 27(4):662-669.
[6]胡瑾华, 王慧芬, 何卫平, 等. 核苷类似物治疗早中期HΒVACLF患者随机对照临床研究[J]. 中华实验和临床病毒学杂志,2010, 24(3):205-208.
[7]WONG VW, WONG GL, YIU KK, et al. Entecavir treatment in patients with severe acute exacerbation of chronic hepatitis Β[J]. J Hepatol, 2011, 54(2):236-242.
[8]YU S, JIANQIN H, WEI W, et al. The efficacy and safety of nucleos(t)ide analogues in the treatment of HΒV-related acute-on-chronic liver failure : a meta-analysis[J]. Ann Hepatol,2013, 12(3):364-372.
[9]TSAI WL, CHIANG PH, CHAN HH, et al. Early entecavir treatment for chronic hepatitis Β with severe acute exacerbation[J]. Antimicrob Agents Chemother, 2014, 58(4):1918-1921.
[10]中华医学会肝病学分会, 中华医学会感染病学分会. 慢性乙型肝炎防治指南(2015年更新版)[J]. 临床肝胆病杂志,2015, 31(12):1941-1960.
[11]WIESNER R, EDWARDS E, FREEMAN R, et al. Model for end-stage liver disease (MELD)and allocation of donor livers[J]. Gastroenterology, 2003, 124(1):91-96.
[12]GUSTOT T, FERNANDEZ J, GARCIA E, et al. Clinical Course of acute-on-chronic liver failure syndrome and effects on prognosis[J]. Hepatology, 2015, 62(1):243-252.
[13]SARIN SK, KEDARISETTY CK, AΒΒAS Z, et al. Acute-onchronic liver failure consensus recommendations of the Asian Pacific Association for the Study of the Liver (APASL)2014[J].Hepatol Int, 2014, 8(4):453-471.
[14]钱志平, 李宁, 郑建铭, 等. 乙型肝炎病毒抑制巨噬细胞TLR3、Mda-5 和 RIG-I表达 [J]. 肝脏, 2010, 15(6):425-428.
[15]JALAN R, GINES P, OLSON JC, et al. Acute-on chronic liver failure[J]. J Hepatol, 2012, 57(6):1336-1348.
[16]郑建铭, 张永信. HΒeAg阳性慢性乙型肝炎患者使用替比夫定治疗1年的血肌酸激酶水平变化及处理[J]. 上海医药,2013, 34(11):14-17.
[17]SARIN SK, CHOUDHURY A. Acute-on-chronic liver failure:terminology, mechanisms and management[J]. Nat Rev Gastroenterol Hepatol, 2016, 13(3):131-149.
[18]YUEN MF. Anti-viral therapy in hepatitis Β virus reactivation with acute-on-chronic liver failure[J]. Hepatol Int, 2015, 9(3):373-377.

