肺结核患者利福喷丁血药浓度监测研究
彭明丽,陈 明,温筱煦,赵冠人(解放军第309医院药剂科,北京 100091)
结核病是由结核分枝杆菌引起的慢性呼吸道传染病,严重威胁人类的健康。WHO报告显示2015年全球新发结核病例高达1040万,而中国是新发结核最多的六个国家之一,结核病在全部死亡原因中仍排位前十[1]。结核病的治疗主要依赖于针对结核分枝杆菌的长期联合化疗[2],如何更好的利用现有的抗结核药物成为临床关注的焦点。
利福喷丁是一种新合成的长效利福霉素类抗生素,半衰期为11 h,其抗菌作用是利福平的4 ~ 5倍,对结核分枝杆菌,尤其对生长期结核分枝杆菌作用强,临床上广泛用于替代利福平抗结核治疗[3]。利福喷丁的抗结核分枝杆菌作用强,其治疗窗为8 ~ 30 μg·mL-1[4],有文献表明利福喷丁的血药浓度个体差异较大,药物过量时临床不良反应肝毒性较明显[5]。因此,对利福喷丁开展治疗药物监测(therapeutic drug monitoring,TDM)具有一定的临床意义。其目的是保证利福喷丁抗结核分枝杆菌疗效的同时尽量降低其不良反应发生率,从而使利福喷丁的临床应用更为安全有效。为了进一步探讨对结核病患者应用利福喷丁进行TDM的临床意义,本研究选取我院服用利福喷丁的结核患者,对其血药浓度进行测定,并对数据进行汇总分析。
1 材料
1.1 临床资料
选取2016年7月– 2017年3月期间在我院门诊或病房治疗的结核患者共计67例,进行利福喷丁峰浓度(Cmax)的测定。其中男性31例,女性36例,均为汉族,年龄14 ~ 67岁,平均年龄(32.1±9.4)岁,平均体质量(57.3±17.1)kg。
1.2 仪器与试药
API3200型三重四级杆串联质谱仪,配有离子喷雾离子化源(ESI)以及Analyst 1.4.1数据处理软件(美国Applied Biosystem公司);Prominence LC-20A超快速高效液相色谱系统,包括CBM-20A系统控制器,LC-20AD二元输液泵,DGU-20A3脱气装置,SIL-20AHT自动进样器(日本Shimadzu公司);VDRTEX-5型旋涡混合器(其林贝尔仪器制造有限公司);5420型台式高速离心机(德国Eppendorf公司);MG-2200型氮气吹干仪(东京理化器械株式会社)。利福喷丁对照品(中国药品生物制品检定所,批号:130541-200401);对乙酰氨基酚对照品(内标,中国药品生物制品检定所,批号:100018-200408);甲醇、乙腈为色谱纯(Dikma公司);水为Millipore制备超纯水,电阻率为18.2 MΩ·cm。患者血浆样品由解放军第309医院结核病研究所提供。
2 方法与结果
2.1 给药方案
67例结核患者治疗方案如下:异烟肼300 mg·d-1,qd(67例);利福喷丁450 mg·d-1,biw(67例);吡嗪酰胺1500 mg·d-1,tid(62例);乙胺丁醇750 mg·d-1,qd(24例人);1000 mg·d-1,qd(38例)。纳入连续服药7 d以上的患者,并进行血药浓度监测。
2.2 血样采集
采血时间为服用利福喷丁4 h后,取静脉血2 mL,置EDTA-Na真空抗凝管中,当日测定血浆中利福喷丁浓度。
2.3 血药浓度测定方法
2.3.1 色谱条件 分析柱:Agilent Poroshell 120SB C18色谱柱(4.6 mm×50 mm,2.7 µm);保护柱:ZORBAX SB C18柱(2.1 mm×12.5 mm,5 µm);流动相:甲醇-0.2%醋酸溶液;进样量:5 µL;流速:0.5 mL·min-1;梯度洗脱:0.01 ~ 3.00 min,25%甲醇;3.01 ~7.00 min,80%甲醇;7.01 ~ 10.00 min,25%甲醇。
2.3.2 质谱条件 离子源:离子喷雾离子化源(Ion spray);离子喷射电压(IS):5000 V;离子源温度(TEM):350 ℃;源内气体1(GS1,N2):25;源内气体2(GS2,N2):45;气帘气体压力(Cur Gas):30。正离子方式检测;扫描方式为多重反应监测(MRM);DP:67;EP:67;CE:36;CXP:7;用于定量分析的离子反应分别为m/z 877.5→845.5(利福喷丁)和m/z 152.0→110.0(对乙酰氨基酚)。
2.3.3 溶液的配制 精密称取利福喷丁对照品适量,加50%甲醇溶解,定量配制成300 µg·mL-1的对照品储备液。精密称取内标对乙酰氨基酚适量,加甲醇溶解,定量配制成161.60 µg·mL-1的内标储备液,利福喷丁与内标储备液置于– 20 ℃冰箱保存,临用时用50%甲醇稀释至30 µg·mL-1作为工作液。
2.3.4 血浆样品的处理 取血浆样品100 µL于1.5 mL离心管中,加入内标溶液10 µL,加入甲醇300 µL,涡旋混合1 min,离心12 min(13 200 r·min-1,4 ℃),取上清液200 µL,加入去离子纯化水400 µL,涡旋混合1 min,取上清液5 µL进样分析。
2.4 方法专属性
分别取空白血浆,加入利福喷丁对照品溶液和对乙酰氨基酚内标溶液的样品血浆(利福喷丁终浓度15.00 µg·mL-1,对乙酰氨基酚终浓度16.16 µg·mL-1)以及加入对乙酰氨基酚内标溶液的服用利福喷丁的患者血浆,按“2.3.4”项下方法处理,依“2.3.1”项下色谱条件进样分析,结果显示,利福喷丁及内标对乙酰氨基酚有对称的色谱峰和良好的分离度,其测定不受血浆中杂质峰及其他合用药品的干扰,具有较高的专属性。详见图1。
2.5 标准曲线与线性范围
平行取人空白血浆6份各90 μL,分别加入利福喷丁工作液适量,精密配制0.60、1.50、3.00、6.00、15.00、24.00、30.00 µg·mL-1的血浆样品,按“2.3.4”项下方法处理,“2.3.1”项下色谱条件进样分析。以样品与内标峰面积比值(Y)对浓度(C)进行回归计算,结果表明利福喷丁在0.60 ~ 30.00 µg·mL-1内线性关系良好,回归方程为:Y = 0.118 C + 0.029 5,r = 0.996 2。在上述条件下测得血浆中利福喷丁最低检测浓度为0.60 µg·mL-1。
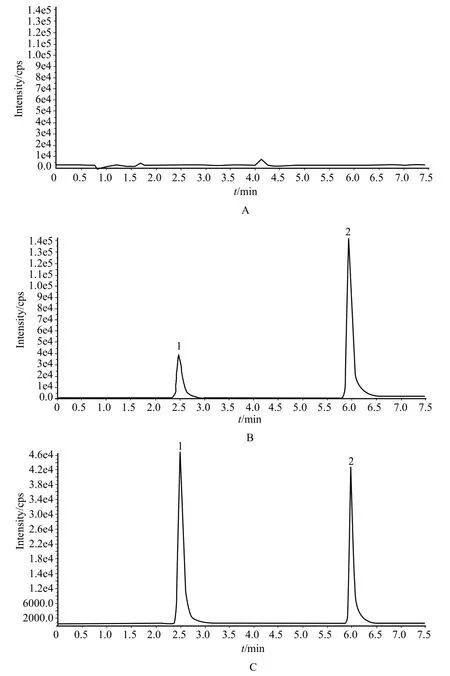
图1 HPLC色谱图Fig 1 HPLC chromatograms
2.6 基质效应考察
取空白血浆90 μL于1.5 mL离心管内,按“2.3.4”项下方法处理,向获得的上清液中分别加入适量对照品溶液,配制低、中、高3个浓度水平的样品,每个浓度3个样品。另于流动相溶液分别加入适量对照品溶液,同样配制低、中、高3个浓度各3个样品。按“2.3.1”项下色谱条件进样分析,测定各色谱峰面积,求出对应浓度前者与后者峰面积的比值即为基质效应,结果表明,利福喷丁在人血浆中的基质效应为(97.01±2.89)%,定量过程不受基质效应影响。
2.7 准确度和精密度实验
平行取3份各90 μL的空白血浆,分别加入利福喷丁工作液适量,精密配制成低、中、高3种浓度(1.50、6.00、24.00 µg·mL-1)的血浆样品,每个浓度6份样品,按“2.3.4”项下方法处理,按“2.3.1”项下色谱条件进样,依法测定日内与日间(3 d内)精密度,结果见表1。
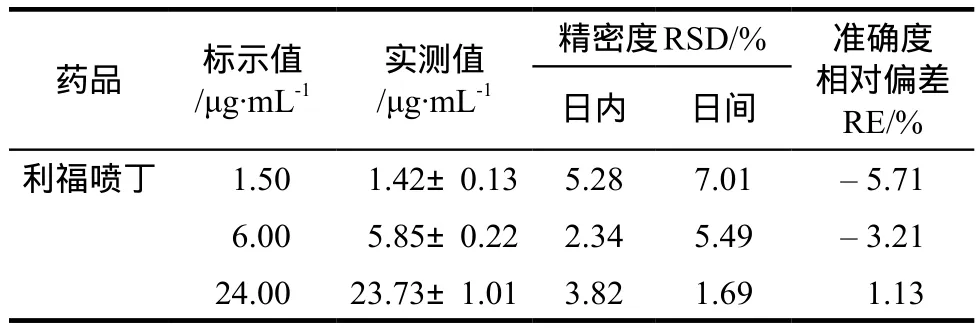
表1 准确度与精密度. n = 6Tab 1 Precision and accuracy. n = 6
2.8 提取回收率与稳定性实验
平行取3份各90 μL的空白血浆和经过“2.3.4”项下方法处理的血浆空白基质,分别加入利福喷丁工作液适量,精密配制成低、中、高3种浓度(1.50、6.00、24.00 µg·mL-1),其中每个浓度3个样品。按“2.3.1”项下色谱条件进样分析,测定各色谱峰面积,对应浓度前者与后者峰面积的比值即为其提取回收率。结果表明利福喷丁平均回收率均> 90%,RSD均< 5%,见表2。
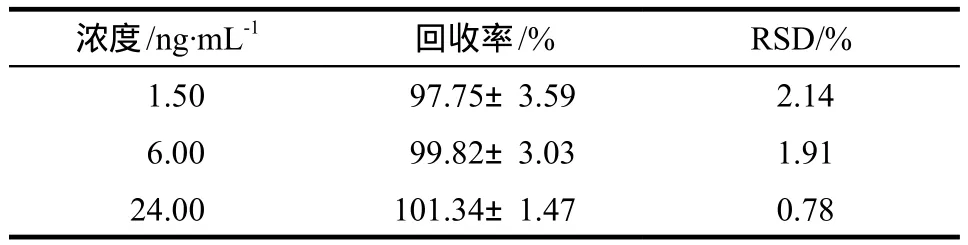
表2 利福喷丁的提取回收率Tab 2 The extraction recovery of rifapentine
取已知利福喷丁浓度血浆样品,分别置室温条件下存放0、1、2、4、8、16、24 h后,按“2.3.4”项下方法处理,按“2.3.1”项下色谱条件进样,测定利福喷丁浓度,考察样品放置稳定性。结果表明血浆样品在室温放置4 h稳定,RSD均< 15%,同时又考察了样品在-20 ℃冰箱中存放1个星期的稳定性,结果表明样品稳定,RSD均< 15%,符合规定。
2.9 利福喷丁血浆峰浓度测定结果
对67例服用利福喷丁的肺结核患者按照“2.2”项下要求采血,按“2.3.4”项下方法处理,按“2.3.1”项下色谱条件进样分析,另取利福喷丁低、中、高浓度(1.50、6.00、24.00 µg·mL-1)的血浆样品各3份,作为质控随行测定,RSD均< 5%,根据内标法加校正因子法计算利福喷丁浓度。
肺结核患者利福喷丁血浆峰浓度(Cmax)测定结果为1.59 ~ 39.79 µg·mL-1,测定值分布情况见表3。峰浓度与利福喷丁抗结核分枝杆菌疗效密切相关,由表3可见,按治疗窗为8 ~ 30 µg·mL-1[4]计,其有效率为59.70%。
3 讨论
肺结核是一种由结核分枝杆菌引起的感染性疾病,其治疗主要是以异烟肼和利福平为基石的一线抗结核药联合化疗为主。其中,利福喷丁作为利福霉素类药物的代表,相较于利福平表现出更强的抗结核疗效和更好的安全性[6-7],且一周只需服用两次,病人依从性更好,临床上常用于替代利福平治疗肺结核。但在长期的对主要抗结核药物血药浓度的临床监测中发现,服用利福喷丁的个体间血药浓度差异过大,这已成为肺结核患者合理使用利福喷丁的一个难点。因此对其开展TDM具有重要的临床意义。

表3 利福喷丁血浆峰浓度(Cmax)测定值的分布Tab 3 Range distribution of Cmax about rifapentine in plasma
基于临床需要,本文建立了一种简便、快速测定血浆中利福喷丁浓度的HPLC-MS/MS法,可用于肺结核患者常规血药浓度的监测。本研究结果表明,按单一剂量服用利福喷丁,血药浓度的个体差异较大,因此对于服用利福喷丁的患者进行TDM具有更重要的临床意义。笔者观察到当利福喷丁血药浓度在8.01 ~29.99 µg·mL-1时,在1个月内有77.50%(31/40)的患者临床症状出现明显改善,表现为咳嗽咳痰症状缓解,痰菌转阴,病灶明显吸收等;当利福喷丁血药浓度≤ 8.00 µg·mL-1时,84.21%(16/19)的患者症状得不到有效的控制,当利福喷丁血药浓度≥30 µg·mL-1时,75.00%(6/8)的患者出现了恶心、呕吐、白细胞降低、皮疹等药品不良反应。提示对利福喷丁进行TDM在肺结核的个体化治疗中可能具有一定指导作用,但由于本研究样本量较少,对于利福喷丁在肺结核治疗中的最佳血药浓度尚有待于收集大样本病例进行更深入的分析。
[参考文献]
[1] World Health Organization. Global tuberculosis report 2016[S].Geneva: World Health Organization, 2016.
[2] Kwon YS, Jeong BH, Koh WJ. Tuberculosis: clinical trials and new drug regimens[J]. Curr Opin Pulm Med, 2014, 20(3): 280-286.
[3] 李相杰.利福喷丁、利福平治疗菌阳肺结核的疗效观察[J].临床肺科杂志,2006,11(3):380.
[4] Choi R, Jeong BH, Koh WJ, et al. Recommendations for optimizing tuberculosis treatment: therapeutic drug monitoring,pharmacogenetics, and nutritional status considerations[J]. Ann Lab Med, 2017, 37(2): 97-107.
[5] Alsultan A, Peloquin CA. Therapeutic drug monitoring in the treatment of tuberculosis: an update[J]. Drugs, 2014, 74(8): 839-854.
[6] 叶春瑛,刘勇,郭小军.利福喷丁、利福平治疗肺结核药效及安全性对比[J].临床医药文献杂志,2016,3(48):9635,9637.
[7] 蔡灵芝.利福喷丁和利福平治疗肺结核患者的疗效比较[J].中华全科医学,2016,14(8):1414-1416.

