两种菊科中药材挥发油成分的GC-MS分析研究
刘瑜霞,邓仕明,林健
(湖北民族学院,湖北 恩施 445000)
羽叶千里光(SeneciojacobaceaL.)为菊科千里光多年生草本植物,全草可作药用[1],具有清肝明目、清热解毒等功效,常用于治疗结膜炎、咽喉炎、蛇虫咬伤、外敷治疮疖痈肿等[2-3]。目前文献报道了西藏双花千里光花精油、麻叶千里光挥发油及恩施产羽叶千里光全草的挥发油GC-MS化学成分分析,鉴定出多种化合物[4-6]。羽叶千里光挥发油的药理学报道目前还未见到,但其植物资源的药理学已有较多的报道,主要药理学作用表现在:抗氧化作用、抗菌作用、抗肿瘤作用[7-9]。
野菊花(Dendranthemaindicum)为菊科菊属多年生植物,药用部位为干燥头状花序,具有消炎解毒、疏风散热、凉血止血、平肝明目、降血压的功效,可治老年慢性支气管炎、扁桃体炎、风热感冒、乳腺炎、外伤出血等疾病。目前文献报道了湖北、河北、河南3个地区的野菊花挥发性化学成分分析,鉴定出多种化合物[10],不同产区的野菊花之间存在一定的差异[11]。野菊花挥发油具有保护血管内皮和抗微生物作用, 这可能是药物发挥舒张血 管内皮细胞、降低血压的作用机理之一[12-14]。其挥发油体外对金色葡萄球菌、大肠杆菌、白喉杆菌、 结核杆菌及白色念珠菌等有一定的抑能[15]。从野菊花中分离出的木犀草素能明显抑制大鼠晶状体醛糖还原酶活性[16]。
本试验以恩施本地野生的羽叶千里光和野菊花的花为材料,提取挥发油,GC-MS获得其挥发油各成分进行分析。
1 仪器与药材
1.1 仪器
Agilent Technologies GC-MS联用仪,Xcalibur,NIST标准质谱图库(美国Fininhag公司)
1.2 药材
羽叶千里光于2015年10月中旬采自湖北省恩施市龙凤坝镇,新鲜植株叶片洗净待用。野菊花同期采于湖北巴东县野三关镇药农种植田间,取头状花序部分,烘干备用。
2 方法与结果
2.1 挥发油的提取
羽叶千里光挥发油类成分的提取:取新鲜药材123g,粉碎,置于2000mL圆底烧瓶中,加1.5倍体积蒸馏水,加热水蒸汽蒸馏提取挥发油成分,提取4h,油状物用乙醚萃取3次,合并萃取液,用无水Na2SO4干燥,过滤,N2气保护下挥干乙醚,得黄色油状物(0.15 mL),待检测。
野菊花挥发油类成分的提取:取新干野菊药材97 g粉碎,置于2000 mL圆底烧瓶中,加1.5倍体积蒸馏水,加热水蒸汽蒸馏提取挥发油成分,提取3h,油状物用乙醚萃取2次,合并萃取液,用无水Na2SO4干燥,过滤,N2气保护下挥干乙醚,得蓝色油状物(0.20 mL),待检测。
2.2 测试条件
羽叶千里光,GC条件:色谱柱DB-5MS(30 m×0.25 mm,0.25 μm),柱流速:1 mL/min;柱温:40 ℃恒温2 min;程序升温:10℃/min升至120℃,保持1 min;5 ℃/min升至270 ℃,保持5 min;95%甲基聚硅氧烷,载气为高纯度氦气,气化温度:280 ℃。MS条件:电离电压70eV,质量范围30~400 amu,EI离子源,分流进样,分流比为30∶1。溶剂延缓时间4 min,全波长扫描,离子温度240 ℃,扫描周期1 s。
野菊花,GC条件:色谱柱为HP-5(30 m ×250 μm ×0.25 μm),弹性石英毛细管柱,柱流速:1 mL/min;升温程序的初温是60 ℃,保持1 min,以15 ℃/min的速率升到200 ℃,保持5 min,以5 ℃/min的速率升到280 ℃,保持20 min;进样口温度:240 ℃,载气为氦气,流速:1.2 mL/min,进样量:0.2 μL。MS条件:离子源为EI;离子源温度230 ℃;接口温度270 ℃;扫描质量范围为40~550 amu;进样方式为不分流进样;采样延迟时间为5 min。溶剂延缓时间4 min,全波长扫描,离子温度240℃,扫描周期1s。
2.3 结果
将“2. 1” 项所得羽叶千里光挥发油按“2. 2” 项条件进行分析,得总离子流色谱图(图1)。GC-MS检测,其成分的质谱图经计算机质谱数据库检索,按各色谱峰的质谱裂解碎片图与文献核对,对基峰、 质荷比和相对丰度等进行比较,并结合有关图谱解析,分别对各色谱峰加以确认,从而鉴定羽叶千里光挥发油中的化学成分。采用峰面积归一化法测得各组分的相对百分含量,分析鉴定结果见表1。
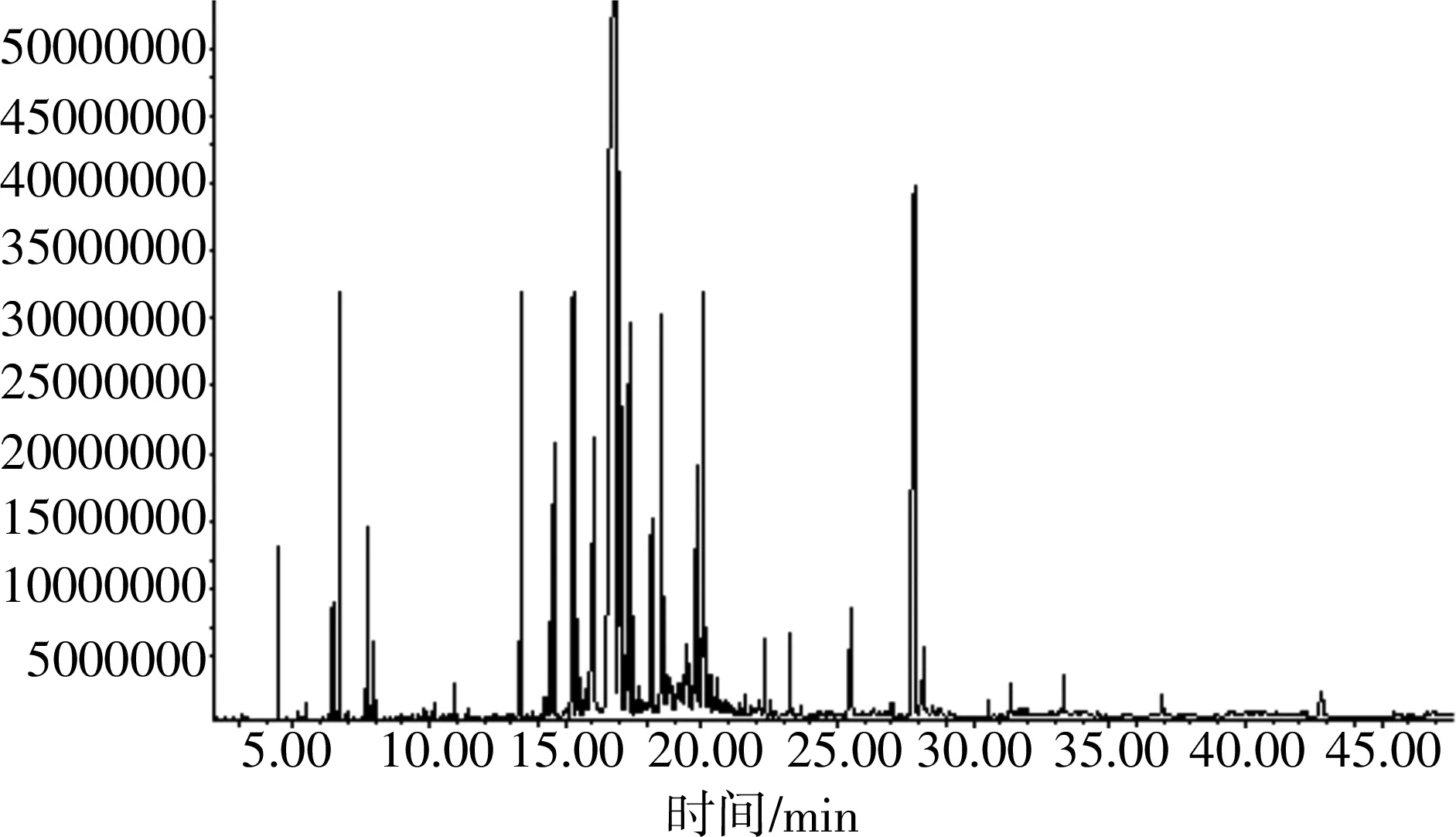
图1 羽叶千里光挥发油总离子流色谱图
共鉴定出顺-3-已稀醇等77种挥发性成分,其它峰未能鉴定。实验分离的化合物占挥发油类成分总量的94.28%,其中含量在10%以上的成分为1-甲基-5-亚甲基-8-(1-甲基乙基)-1,6-环癸二烯(32.8%)、叶绿醇(10.6%),含量在5%以上的成分为1-石竹烯(5.29%),含量在3%以上的成分为α-依兰油烯(4.98%)、1-羟基-1,7-二甲基-4-异丙基-2,7-环癸二烯(4.61%)、6,8-二甲基-9-亚甲基-3-(1-甲基乙基)双环[4.3.0]-2,7-壬二烯(3.85%)、3,7-二甲基-1,3,6-辛三烯(3.79%)、丁香烯(3.52%)、(1S,cis)-4,7-二甲基-1-(1-甲基乙基)-1,2,3,5,6,8a-六氢化萘(3.46%)。

表1 羽叶千里光挥发油化学成分GC-MS分析结果
续表1-1

编号保留时间/min化合物名称分子量/amu相对含量(%)匹配度(%)76.0691⁃甲基⁃4⁃(1⁃甲基乙基)⁃1,3⁃环己二烯136.1250.01949786.331右旋萜二烯136.1250.03939996.449(3E)⁃3,7⁃二甲基⁃1,3,6⁃辛三烯136.1250.678596106.7283,7⁃二甲基⁃1,3,6⁃辛三烯(罗勒烯)136.1253.798397116.9721⁃甲基⁃4⁃(1⁃甲基乙基)⁃1,4⁃环己二烯136.1250.056894127.583异松油烯136.1250.033997137.7191⁃十一烯154.1721.261994147.915芳樟醇154.1360.460297158.028壬醛142.1360.120391168.544(4E,6Z)⁃2,6⁃二甲基⁃2,4,6⁃辛三烯136.1250.035097179.826(⁃)⁃4⁃萜品醇154.1360.0659971810.171α⁃松油醇154.1360.1280941910.9252⁃异丙基⁃5⁃甲基茴香醚164.120.2696952011.393香叶醇154.1360.0756952111.7676⁃甲基⁃1,2,3,4⁃四氢化萘146.110.0044962212.4912⁃甲基萘142.0780.0581962412.996(E,E)⁃2,4⁃癸二烯醛152.120.0444942513.3946,8⁃二甲基⁃9⁃亚甲基⁃3⁃(1⁃甲基乙基)双环[4.3.0]⁃2,7⁃壬二烯204.1883.8459972613.613α⁃荜澄茄烯204.1880.0342972714.13(+)⁃环苜蓿烯204.1880.0586962814.331(E)⁃1⁃(2,6,6⁃三甲基⁃1,3⁃环己二烯⁃1⁃基)⁃2⁃丁烯⁃1⁃酮190.1360.0522972914.397(1S,2S,4R)⁃1⁃甲基⁃1⁃乙烯基⁃2,4⁃二亚丙基环己烷204.1880.1065993014.581β⁃榄香烯204.1882.4038913115.0912,6⁃二甲基⁃6⁃(4⁃甲基⁃3⁃戊烯基)双环[3,1,1]⁃2⁃庚烯204.1880.1116943215.2931⁃石竹烯204.1885.2960993315.342,7⁃二甲基萘156.0940.0549963415.928(Z)⁃β⁃金合欢烯204.1880.8785953516.041丁香烯204.1883.5165973616.81⁃甲基⁃5⁃亚甲基⁃8⁃(1⁃甲基乙基)⁃1,6⁃环癸二烯204.18832.7765963716.892,6⁃二甲基⁃6⁃(4⁃甲基⁃3⁃戊烯基)双环[3,1,1]⁃2⁃庚烯204.1880.5334933916.984α⁃依兰油烯204.1884.9785944017.115β⁃红没药烯204.1880.1187974117.2524,7⁃二甲基⁃1⁃(1⁃甲基乙基)⁃1,2,4a,5,6,8a⁃六氢化萘204.1880.5913984217.352(1S,cis)⁃4,7⁃二甲基⁃1⁃(1⁃甲基乙基)⁃1,2,3,5,6,8a⁃六氢化萘204.1883.4616934317.436[S⁃(R∗,S∗)]⁃3⁃(1,5⁃二甲基⁃4⁃己烯基)⁃6⁃亚甲基环己烯204.1881.2016964417.6141,6⁃二甲基⁃4⁃(1⁃甲基乙基)⁃1,2,3,4,4a,7⁃六氢化萘204.1880.1761994517.691[1S⁃(1α,4aβ,8aα)]⁃4,7⁃二甲基⁃1⁃(1⁃甲基乙基)⁃1,2,4a,5,6,8a⁃六氢化萘204.1880.2344984617.8632,3,5⁃三甲基萘170.110.0931974718.023雅榄蓝烯204.1880.1352914818.172γ⁃榄香烯204.1881.7254914918.5631⁃羟基⁃1,7⁃二甲基⁃4⁃异丙基⁃2,7⁃环癸二烯222.1984.6090965018.7(⁃)⁃蓝桉醇222.1980.3205975118.878α⁃古芸烯204.1880.5080965219.169柏木脑222.1980.303995
续表1-2

编号保留时间/min化合物名称分子量/amu相对含量(%)匹配度(%)5319.4891,6⁃二甲基⁃4⁃(1⁃甲基乙基)⁃1,2,3,4,4a,7⁃六氢化萘204.1880.7087905419.94α⁃毕橙茄醇222.1980.1805915520.9262⁃甲基芴180.0940.0907945621.899肉豆蔻酸228.2090.1231995722.9441⁃甲基⁃9,10⁃二氢菲194.110.0248955823.3356,10,14⁃三甲基⁃2⁃十五烷酮268.2770.0741935923.638邻苯二甲酸二异丁酯334.2140.1086906024.1317⁃十五碳炔208.2190.0228966124.2912⁃甲基菲192.0940.0497976224.6294H⁃环五菲190.0780.0471946324.7781⁃甲基菲192.0940.0379976425.519十六酸256.242.0212996526.2323,6⁃二甲基菲206.110.0238956627.537亚麻酸甲酯292.240.0320996727.828叶绿醇296.30810.5865956828.178亚麻酸278.2250.6593996928.517硬脂酸284.2720.1395967028.76硬脂酰胺283.2880.1373917131.033脱氢枞酸甲酯314.2250.0653927231.36(Z)⁃9⁃十八烯酸酰胺281.2720.3772997331.93二十四烷338.3910.1204997433.1881⁃十九烯266.2970.1384997533.313二十五烷352.4070.4400997636.933二十七烷380.4380.2923987742.791二十九烷408.470.546499
将“2. 1” 项所得野菊花挥发油按“2. 2” 项条件进行分析,得总离子流色谱图(图2)。GC-MS检测,其成分的质谱图经计算机质谱数据库检索,按各色谱峰的质谱裂解碎片图与文献核对,对基峰、 质荷比和相对丰度等进行比较,并结合有关图谱解析,分别对各色谱峰加以确认,从而鉴定野菊花挥发油中的化学成分。采用峰面积归一化法测得各组分的相对百分含量,分析鉴定结果见表2。

图2 野菊花挥发油总离子流色谱图
共鉴定出3β-羟基-5-胆烯酸等64种挥发性成分,其它峰未能鉴定。本实验分离的化合物占挥发油类成分总量的95.36%,其主要成分为氧化石竹烯(10.3%),右旋樟脑(4.64%)、二十烷(3.89%)、棕榈酸(3.67%)、亚油酸(3.02%)等成分。
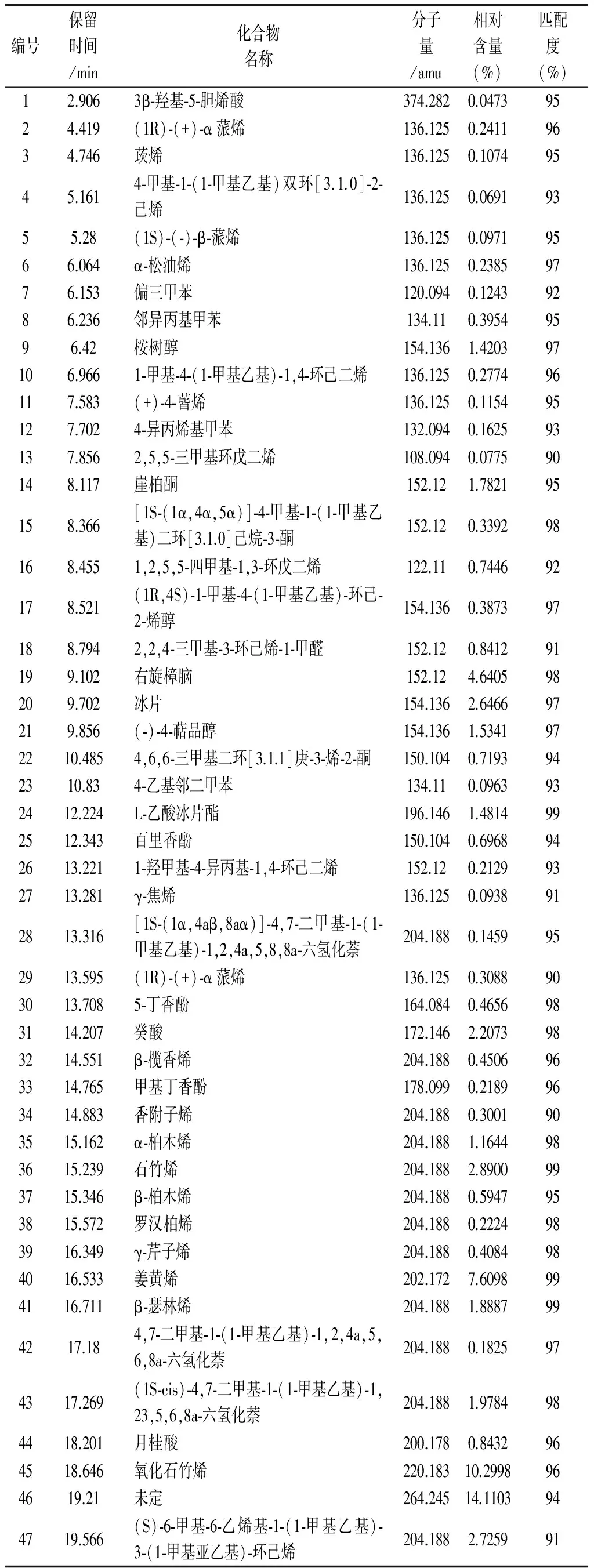
表2 野菊花挥发油化学成分GC-MS分析结果
续表2
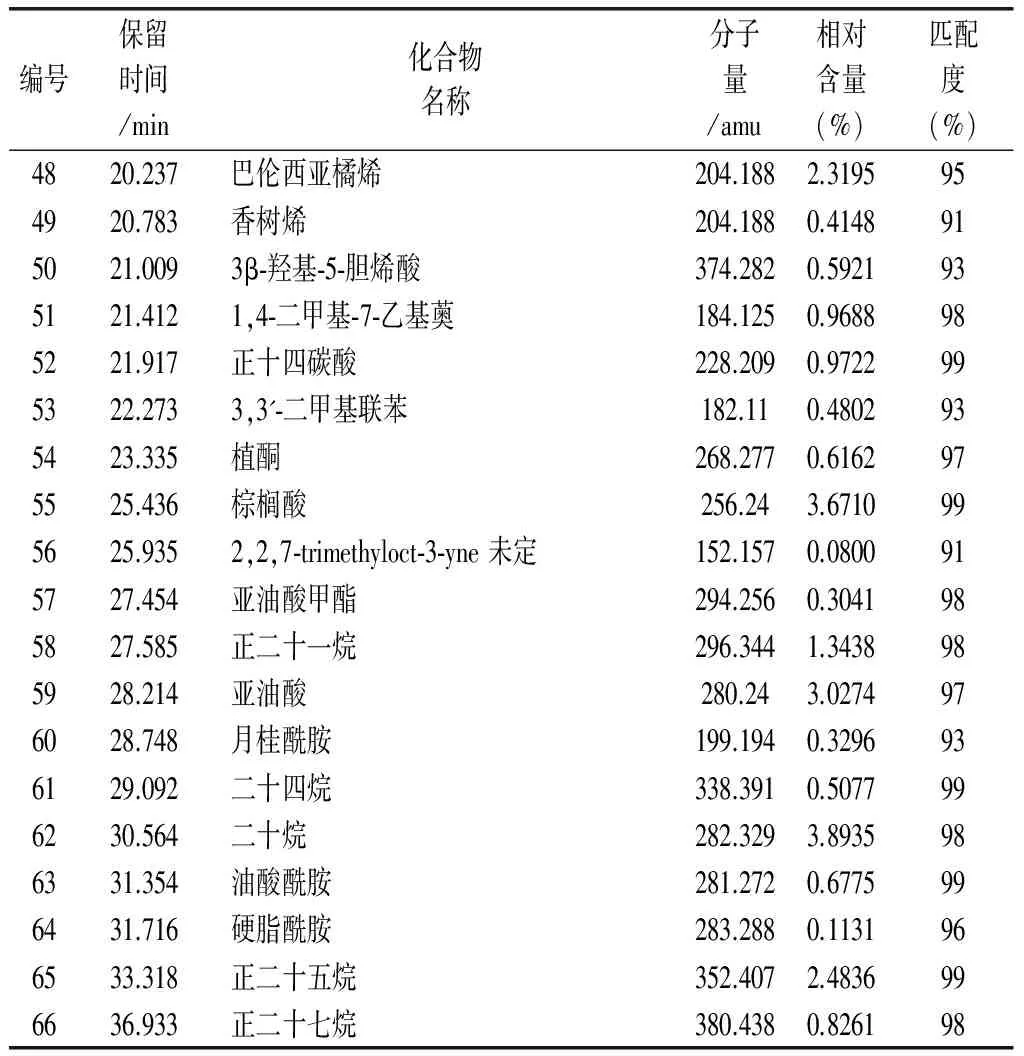
编号保留时间/min化合物名称分子量/amu相对含量(%)匹配度(%)4820.237巴伦西亚橘烯204.1882.3195954920.783香树烯204.1880.4148915021.0093β⁃羟基⁃5⁃胆烯酸374.2820.5921935121.4121,4⁃二甲基⁃7⁃乙基薁184.1250.9688985221.917正十四碳酸228.2090.9722995322.2733,3'⁃二甲基联苯182.110.4802935423.335植酮268.2770.6162975525.436棕榈酸256.243.6710995625.9352,2,7⁃trimethyloct⁃3⁃yne未定152.1570.0800915727.454亚油酸甲酯294.2560.3041985827.585正二十一烷296.3441.3438985928.214亚油酸280.243.0274976028.748月桂酰胺199.1940.3296936129.092二十四烷338.3910.5077996230.564二十烷282.3293.8935986331.354油酸酰胺281.2720.6775996431.716硬脂酰胺283.2880.1131966533.318正二十五烷352.4072.4836996636.933正二十七烷380.4380.826198
3 讨论
本研究以湖北恩施产羽叶千里光和野菊花为研究对象,通过GC-MS对其进行了挥发油类成分的研究,并结合己知化学谱库进行分析,从羽叶千里光中共鉴定出顺-3-已稀醇等77种挥发性成分,实验分离的化合物占挥发油类成分总量的94.28%,主要成分有:1-甲基-5-亚甲基-8-(1-甲基乙基)-1,6-环癸二烯、叶绿醇、1-石竹烯等成分;从野菊花中共鉴定出3β-羟基-5-胆烯酸等64种挥发性成分,实验分离的化合物占挥发油类成分总量的95.36%,主要成分有:氧化石竹烯、右旋樟脑、姜黄烯、棕榈酸、亚油酸、二十烷等成分。
从羽叶千里光鉴定的结果来看,其挥发油中的叶绿醇是合成维生素K及维生素E的原料;石竹烯可作为食品香料;3,7-二甲基-1,3,6-辛三烯(罗勒烯)是日用化工香料的主要配方;β-榄香烯是一种新兴的抗增殖药物,现在有一部分专家将目光转移到应用于眼部肿瘤及视网膜新生血管上来;芳樟醇等萜烯类化合物,对变形杆菌、大肠杆菌、葡萄球菌、肠炎膜杆菌、酿酒酵母菌、黑曲霉菌、白色含球菌、等有很好的抗菌活性。
从野菊花挥发油鉴定的结果来看,其挥发油中的桉树醇可减轻慢性气道炎症、降低气道上皮损伤,且对急性肺炎有很好的治疗效果;右旋樟脑、石竹化合物都具有杀虫止痒、消炎杀菌的作用,氧化石竹烯还具有杀细菌、抗真菌作用;亚油酸具有软化血管、降低血脂、降低血压、促进微循环的作用,可预防或减少心血管病的发病率;4-松油醇也具有抗菌消炎的作用,它们是野菊花对治疗痈疮疖肿有显著作用的主要药效成分,对照相关文献,表明我国各地野菊花的分布相对比较广泛,都含有较为相似的活性挥发油成分,都可以作为中药材来使用。然而,这些活性成分在不同的产区,含量有较大的差异,这可能是由于不同产区栽培技术、生态环境、炮制技术和储运条件等方面的原因所造成的;所以,对野菊花进行深度开发利用时,要根据用途和适用人群,对来自不同产区的野菊花进行药效鉴定和系列检测,成分发挥野菊花的药用和食用价值。
随着这些活性成分逐步应用于临床,市场需求越来越大,而这些成分在植物中的含量往往很低,羽叶千里光和野菊花很有可能成为这些成分新的植物资源。对羽叶千里光和野菊花挥发油成分和药效作进一步探讨,具有很大的研究意义和经济价值。
[1]马成亮. 野菊花的价值与加工[J]. 特种经济动植物, 2002(09) : 25.
[2]江苏新医学院. 中药大辞典下册[M]. 上海: 上海科技出版社, 1997: 4402.
[3]江苏新医学院. 中药大辞典上册[M]. 上海: 上海人民出版社, l977: 549.
[4]周欣, 赵超, 杨小生, 等. 气相色谱-质谱分析黔产千里光挥发油的化学成分[J]. 中草药, 2001, 32(10): 880-881.
[5]陈梅荣, 丁惠堂, 王晖, 等. 千里光不同方法提取物抑菌作用的研究[J]. 江西中医学院学报, 2002, 14(04): 15.
[6]Susana Abdo, Maria de Bernardi. Furanoeremophilanes and Other Constituents from Senecio canescens[J]. Phytochemstry, 1992, 31(11): 3937.
[7]李艳辉, 格桑索朗,等. 双花千里光精油的GC-MS分析[J]. 分析实验室,2006, 25(07): 42-45.
[8]何忠梅, 孟祥颖, 鲍永利, 等. 麻叶千里光挥发油抗病毒性及成分分析[J]. 分析化学研究简报, 2007, 10(10): 1513-1516.
[9]夏新中, 肖静,夏庭君. 湖北五峰野菊花挥发性化学成分的GC-MS分析[J]. 中国实验方剂学杂志, 2013, 19(21): 132-137.
[10]孙曙光, 韩永成,刘伟,等. 不同产地野菊花挥发油化学成分GC-MS比较分析[J]. 河南农业科学,2014, 43(07): 116-120.
[11]袁炎, 陈超,鞠海,等. 不同产地野菊花挥发油化学成分比较研究[J]. 中国实验方剂学杂志中国实验方剂学杂志, 2009, 15(11): 31-33.
[12]张永明, 黄亚非,陶玲,等. 不同产地野菊花挥发油化学成分比较研究[J]. 中国中药杂志,2002, 27(04): 265-267.
[13]刘航, 杨晓燕,侯相民. 羽叶千里光化学成分及生物活性研究进展[J]. 安徽农业科学,2011, 39(01): 106-113.
[14]张忠, 程富胜, 张霞, 等. 野菊花提取物对小鼠血清NO、NOS的影响[J] . 中兽医医药杂志, 2006, 25(01): 21-23.
[15]胡浩斌, 郑旭东. 子午岭野菊花挥发油的化学成分及抑菌活性[J] . 新疆大学学报(自然科学版), 2005, 22(03): 295-298.
[16]王志东. 中药野菊花的药理作用研究进展[J]. 医学综述, 2009, 15(06): 906-909.

