基于化学核心素养发展的教学设计
——以《盐类水解》第一课时为例
刘 伟
(深圳市华侨城中学 深圳 518053)
一、教材分析
本课程为高中化学选修新课程4第三章第三节《盐类的水解》(第一课时)。盐的水解是基于化学平衡的原理,学生已经学会讨论电解质在水溶液中的电离行为,进而探讨水溶液中酸碱度的规律,有助于促进学生的认知发展。同时,盐类水解是后续电化学学习的必要基础。从知识结构来看,盐水解平衡是继弱酸、弱碱和水的电离平衡系统之后,电解质溶液的另一种平衡系统,它便于学生形成完整的电解质溶液平衡系统。因此,这一节的内容在过去和未来的教学中起着一定的作用,它是理论教学的重点和难点。[1]
二、学生分析
在研究本节内容之前,学生有一定的离子反应、强弱电解质电离、建立化学平衡、水电离、溶液酸碱度等基础,并具有分析溶液中离子水解平衡的能力。[2]
三、教学目标
1.知识与技能
⑴能够知道哪些盐在溶液中发生水解,知道盐类水解的本质;
⑵能够判断盐溶液的酸碱性;
⑶能够书写简单的盐类水解的离子方程式。
2.过程与方法
通过盐类水解规律的学习帮助学生构建电解质溶液的平衡体系,培养学生提出问题、分析问题和解决问题的科学探究能力;
3.情感态度价值观、
学会依据本质推现象,透过现象看本质,感受化学世界的奇妙与和谐,培养学生科学探究精神,在学习中感受合作学习的乐趣。
四、教学重、难点
教学重点:盐类的水解的实质和规律
教学难点:盐类的水解的实质
五、教学策略
问题导学,实验探究
六、教学流程
[新课引入]
1.新闻链接:被蜜蜂蛰了下,差点要了命!设问:当蜜蜂叮咬后应如何利用家庭常用物质加以处理?
2.工业上焊接金属为何用硫酸铵溶液清洗金属表面?
[点评]以生活、生产实例设疑,激发学生兴趣。
[活动与探究1]盐溶液的酸碱性
测定食盐(NaCl)、纯碱(Na2CO3)、除锈剂(NH4Cl)、小苏打(NaHCO3)、硫酸铵、醋酸钠(NaAC)溶液的pH,并将实验结果填入下表

物质pH(<、=、>7)物质pH(<、=、>7)NaCl NaHCO3 Na2CO3(NH4)2SO4 NH4Cl NaAC
[点评]小组探究实验,用pH试纸测定不同盐溶液的酸碱性,并派代表对实验结果进行汇报。通过让学生亲自动手测定不同盐溶液的酸碱性,为寻找盐类的水解的规律、探寻盐类的水解的本质设悬念。通过自主、合作、探究学习,进一步培养学生实验探究与创新意识的核心素养。
[活动与探究2]盐溶液呈现不同酸碱性的原因
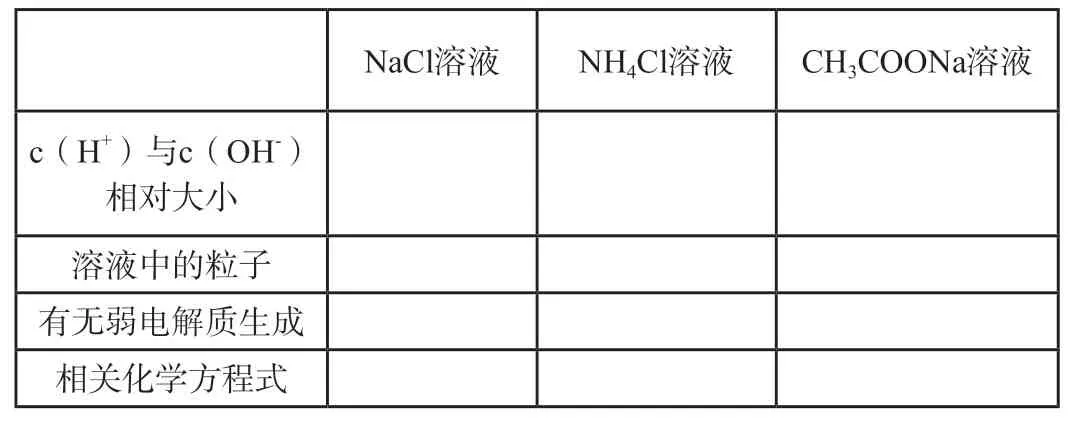
NaCl溶液NH4Cl溶液CH3COONa溶液c(H+)与c(OH-)相对大小溶液中的粒子有无弱电解质生成相关化学方程式
[点评]从微观角度对盐溶液呈现不同酸碱性进行分析以期得出原因,锻炼学生的归纳思维,归纳总结出盐类水解的本质,进一步培养学生宏观辨识与微观探析、变化观念与平衡思想的核心素养。
[活动与探究3]盐的类别与盐溶液酸碱性
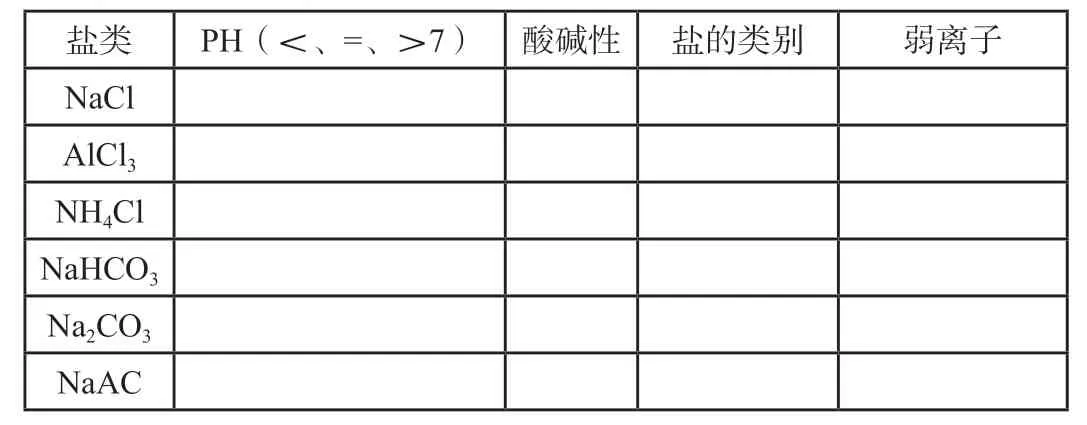
盐类PH(<、=、>7)酸碱性盐的类别弱离子NaCl AlCl3 NH4Cl NaHCO3 Na2CO3 NaAC
[点评]从盐的类别与盐溶液酸碱性的关系总结盐类水解的基本规律:有弱才水解,谁弱谁水解;谁强显谁性,同强显中性。同时规范水解方程式和离子方程式的书写。一方面激发学生兴趣从盐类别去认识和掌握盐类水解规律,培养学生逻辑思维能力,另一方面通过盐类水解方程式和离子方程式书写,学生进一步体会盐类水解的本质,学会盐类水解的表达方式,培养学生规范应用化学用语的能力,从而进一步培养学生证据推理与模型认知的核心素养。
[知识应用]
1.请设计一个合理而比较容易进行的方案证明某酸HA是弱电解质(应用水解原理,做简明扼要表述)
2.Na2CO3、NaHCO3和肥皂水溶液能减轻蜜蜂蛰后带来的痛楚说明了什么?
3.食用纯碱大量用于面条、面包等食品加工中,主要成分Na2CO3,它明明是盐为何要称为“碱”?
4.工业上焊接金属为何用硫酸铵或氯化铵溶液溶液清洗金属表面?
5.为何草木灰(K2CO3)和铵态氮肥(NH4NO3)不能混用?
6.家庭小实验:用pH试纸测试家中食盐、味精、苏打、小苏打溶液的酸碱性
[点评]巩固本节所学内容,强调盐类水解在日常生活、实验室和工农业生产中实际应用;培养学生学以致用的意识,感受所学内容的价值;从而进一步培养学生科学精神与社会责任的核心素养。
七、板书设计(略)
八、教学反思
通过本节课学习,激发了学生的学习兴趣,达到了师生间的双向活动,学生取得了较好的学习效果;此外,“活动探究”、“交流研讨”的设置,能更好地调动学生的学习主动性,更有利于实现“过程与方法”的三维目标,能帮助学生掌握解决问题的方案,达到迁移和应用的目的。实验的设置可以使抽象问题具体化,有利于“情感态度与价值观”目标的实现。本节课基本上能从五个方面(宏观辨识与微观探析、变化观念与平衡思想、证据推理与模型认知、实验探究与创新意识、科学精神与社会责任)培养学生化学核心素养。

