PBS基共聚酯P(BS-co-PeD)和P(BS-co-GA)的降解差异性研究
张 敏, 马晓宁, 李成涛, 赵 冬
(1.陕西科技大学 教育部轻化工助剂化学与技术重点实验室, 陕西 西安 710021; 2.陕西科技大学 环境科学与工程学院, 陕西 西安 710021)
0 引言
由于传统塑料在自然界中不能降解,带来了日益严重的环境问题,因此开发新型可生物降解材料势在必行[1,2].在众多的脂肪族聚酯材料中,由丁二酸和丁二醇缩合聚合的聚丁二酸丁二醇酯(PBS)具有良好的成型加工性,力学性能和生物相容性[3-5],被广泛应用于农用地膜、包装塑料,医用材料等[6-9].但是,由于PBS具有较高的结晶性因而生物降解速度缓慢,因此共聚物的改性从而提高其降解性能已经成为目前的研究热点[10-12].脂肪族聚酯的酶降解受几个因素影响,如聚酯的化学结构,亲水-疏水平衡,固态形态,结晶度等[13,14].
本研究分别通过在PBS分子主链结构引入二元醇和二元酸,采用南极假丝酵母脂肪酶B(Candida antarctica lipase B)[15,16]降解PBS基共聚物,研究共聚物的热性能、结晶性对降解性能的影响,为脂肪族共聚酯材料的应用提供理论指导和基础数据.
1 实验部分
1.1 实验试剂与仪器
(1)主要试剂:丁二酸(SA)、1,4-丁二醇(BDO),均购于国药集团化学试剂有限公司;戊二醇(PeD)、戊二酸(GA),均购于Alfa Aesar 化学试剂有限公司;钛酸四丁酯(TBT),购于天津天力化学试剂有限公司;南极假丝酵母脂肪酶B(CALB),酶活力为10 000 PLU/g,购置于Novozymes (中国)投资有限公司.
(2)主要仪器:核磁共振波谱仪(NMR),ADVANCE Ⅲ 400MHz,德国Bruker公司;X射线衍射仪,AD/Max-3c型,日本理学株式会社;差示扫描量热仪,Q2000型,美国TA公司;热重分析仪,Q500型,美国TA公司;开放式塑炼机,SK-160型,上海齐才液压机械厂机械有限公司;水浴恒温振荡器,SHZ-C型,上海浦东光学仪器厂.
1.2 实验过程
1.2.1PBS共聚物的合成
通过熔融缩聚法自主合成共聚酯聚丁二酸丁二醇酯(PBS);聚(丁二酸丁二醇-co-丁二酸戊二醇酯) [P(BS-co-PeD)];聚(丁二酸丁二醇-co-戊二酸丁二醇酯) [P(BS-co-GA)].在100 mL三口烧瓶中按照酸醇物质的量之比为1.0∶1.1投入二元酸和二元醇,其中第三单体PeD和GA的摩尔分数分别为0%、10%、20%、30%,在N2氛围下升温至170 ℃进行脱水反应,至理论值;随后,升温至220 ℃,抽真空,在真空条件下反应,体系粘度达到要求后,停止反应.将反应物用氯仿溶解,在甲醇溶液中进行纯化可得共聚酯产物,提纯后的产物在真空干燥箱中彻底干燥用以后续研究.
1.2.2降解实验
将共聚酯于开放式塑炼机熔融炼制成薄膜,将共聚酯薄膜裁剪成10×25×0.03 mm 的规则矩形,置于KH2PO4-K2HPO4(pH=7.2± 0.01,0.1 mol/L)缓冲液中,在45 ℃的恒温水浴摇床中进行CALB降解,周期5 d,每组设置不含脂肪酶的空白对照组1个,平行实验3个,以24 h为时间间隔进行取样,样品用蒸馏水清洗降解样并在真空条件下干燥至恒重,其质量损失率计算如公式(1)所示:
Wloss=(W0-Wt)/W0×100%
(1)
式(1)中:Wloss为质量损失率,W0为薄膜酶降解前的质量,Wt为降解时间为t的薄膜质量.
1.2.3分析与测试
TGA测试:升温速率为10 ℃/min,温度范围25 ℃~500 ℃,N2作为保护气;DSC测试:N2氛围下,以10 ℃/min从室温加热至150 ℃以消除热历史,随后以5 ℃/min降温至60 ℃,再以10 ℃/min加热至150 ℃;WAXD测试:扫描速度为6 °/min,步长0.02 °,扫描范围5 °~40 °,电压40 kV,电流30 mA,入射X射线的波长0.154 nm.
2 结果与讨论
2.1 共聚物的合成与表征
通过熔融缩聚法合成不同结构的共聚物,图1为共聚物PBS,P(BS-co-PeD),P(BS-co-GA)的1H NMR谱图.图1(a)中有3组质子峰,δ4.12和δ1.71为BDO链段亚甲基上的H,δ2.1为SA链段亚甲基的H,如图1(b)所示,除SA和BDO链段上亚甲基上H的化学位移外,还有PeD的k,l,m处亚甲基的氢,同样在图1(c)中,出现GA链段上g,h,i处亚甲基的峰.通过核磁谱图可以证明所合成的共聚物为预期产物.

(a)PBS

(b)P(BS-co-PeD)

(c)P(BS-co-GA)图1 PBS基无规共聚物的核磁共振氢谱图
同时,采用分子模拟方法模拟了PBS及其共聚物的空间结构如图2所示.图2(a)为PBS的空间螺旋结构,2(b)为共聚物PBS-co-20PeD的空间结构图,2(c)为共聚物PBS-co-20GA的空间结构图.从图中可以看出,未经改性的PBS,其分子链在空间的排布较为规整,并且呈现出高度螺旋状;经PeD和GA单体改性共聚物主链结构呈现不规则性,链段的卷曲缠绕更加无规柔顺,链段运动性较高.

(a)PBS (b)PBS-co-20PeD (c)PBS-co-20GA图2 三种共聚物的空间结构模型
2.2 共聚物的结晶性能
共聚物的结晶性能影响其降解性能.图3为共聚物P(BS-co-PeD)和P(BS-co-GA)的X射线衍射谱图.PBS为单斜晶系,从图3可以看出,加入PeD和GA的共聚物,共聚物的特征衍射晶面(020)(110)均出现,说明共聚物的晶体构型并未发生改变,同时其结晶衍射峰对应的2θ略向小角度偏移,说明晶面间距变大,同时从图中可以明显看出结晶峰衍射强度下降,说明第三组分的引入改变了共聚物的结晶性能,由Jade6 软件对X射线衍射峰强度2θ在19.6 °~19.8 °和22.5 °~22.8 °处的特征峰进行计算,得到聚合物的结晶度如表1所示.
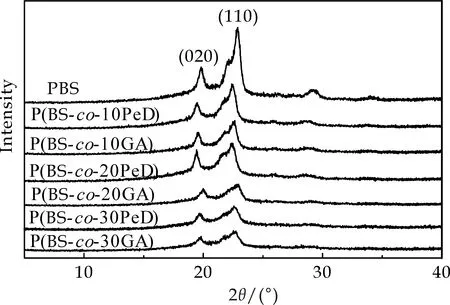
图3 PBS基共聚物的WAXD图谱
P(BS-co-PeD)和P(BS-co-GA)共聚物的结晶度较PBS有明显的下降,随着PeD和GA含量的增加,共聚物的结晶度呈现下降趋势,同时由Jade分析共聚物的半峰可知,共聚物的半峰宽值变小,即晶粒尺寸变大,分子链折叠堆砌不紧密,晶格缺陷明显.对比P(BS-co-PeD)和P(BS-co-GA)可知,P(BS-co-GA)的结晶度均略低于(BS-co-PeD).这可能是因为P(BS-co-GA)分子链无规性更高,分子运动性较高,在接下来的DSC分析中会加以证明.
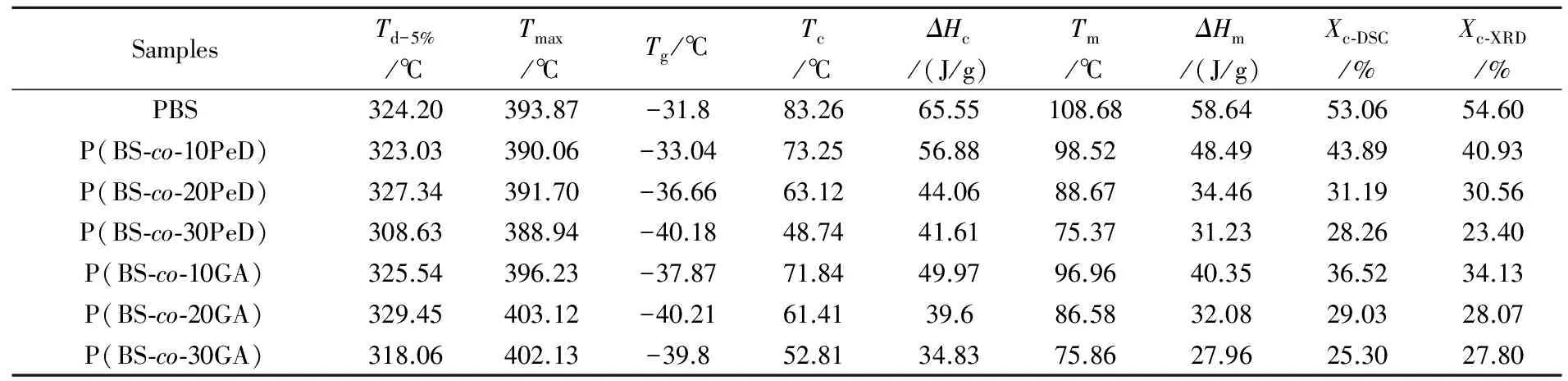
表1 PBS基共聚物的热性能参数
2.3 共聚物的热性能
为了进一步说明PBS及其共聚物的结晶和热性能,测试了PBS基共聚物的熔融结晶和再加热过程的DSC曲线,如图4所示,相关参数列于表1.从图4可以看出,加入PeD和GA后,与纯PBS相比较,共聚物的玻璃化转变温度(Tg)均程现下降趋势,同时共聚物的结晶温度(Tc),熔融温度(Tm)也大大降低,并且随着PeD和GA组分含量的增加,下降幅度增大.

(a)熔融,10 ℃/min
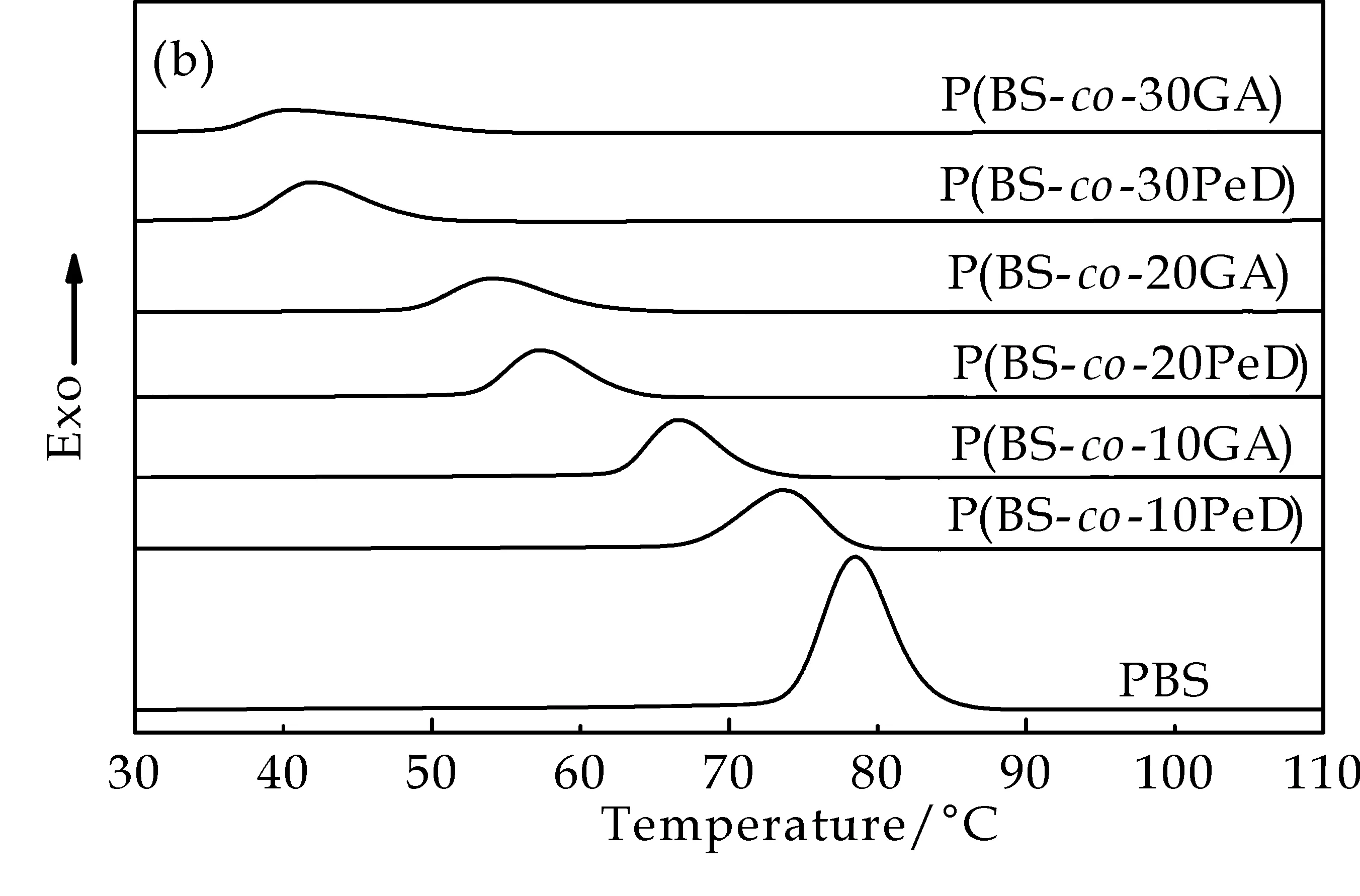
(b)冷却,5 ℃/min图4 三种共聚酯的DSC曲线图
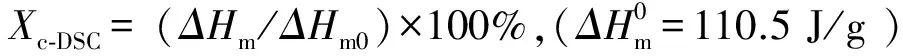

a:PBS; b:PBS-co-10PeD; c:PBS-co-20PeD; d:PBS-co-30PeD; e:PBS-co-10GA; f:PBS-co-20GA; g:PBS-co-30GA图5 PBS基共聚酯的TGA曲线图
2.4 共聚物的降解性能
共聚物的降解率因其结构而异,水相体系中,不同组分的共聚物在CALB酶催化降解的质量损失率如图6所示.从图6(a)可以看出,经过五天的酶降解,两种PBS基共聚物的质量损失率远高于纯PBS.由于P(BS-co-30PeD)和P(BS-co-30GA)在一天内降解率均达到100%,所以对其进行了24 h的降解,取样间隔为4 h,如图6(b)所示,P(BS-co-30GA)的质量损失率低于P(BS-co-30PeD).综上,随着第三组分单体添加量的增加,共聚物的质量损失率随之增加,添加量为30%时,两种共聚物均可实现完全降解,添加量为20%时,降解五天后,共聚物(BS-co-20PeD)的质量损失率为85%,P(BS-co-20GA)的质量损失率高达93%,添加量为10%时,降解五天后,共聚物P(BS-co-10PeD)的质量损失率为21%,P(BS -co-10GA)的质量损失率为27%.共聚物降解速率大幅提高主要是因为引入第三组分单体时,主链分子结构发生改变,打破了PBS规整的双螺旋结构,在空间结构上呈现出分子链不规整的现象,从而使得共聚物的结晶度下降,非晶态部分的增加有利于被酶进攻,从而实现快速降解.对比两种共聚物的降解性能,P(BS-co-GA)优于P(BS-co-PeD).共聚物热分析和结晶性能分析已经指出,P(BS-co-GA)的结晶度均低于P(BS-co-PeD),且前者Tg也低于后者,非晶相是被酶侵蚀的第一个区域,结晶度低,Tg越低,流动相越多,侵蚀过程越容易,越有利于酶的降解.

(a)单体摩尔比为10%,20%的PBS基共聚物

(b)单体摩尔比为30%的PBS基共聚物图6 不同单体比例PBS基共聚物的质量损失率
酶对聚酯的降解是一个亲核加成反应.对比两种共聚物的主链结构,酸段亚甲基的引入可以分散羰基碳上的电荷,使得羰基碳的正电性提高,有利于CALB对羰基碳正离子的进攻,确保亲核加成反应的有效进行.而醇段亚甲基的引入并不能起到分配羰基碳上电荷的作用,因此无法促进酶促反应.
3 结论
(1)以第三组分为PeD和GA改性的PBS基无规共聚物P(BS-co-PeD)和P(BS-co-GA),均具有良好的热稳定性,随着PeD和GA含量的增大,两种共聚物的晶体构型未发生变化,但结晶度降低,Tg降低,质量损失率大幅提高,与对P(BS-co-PeD)比较,P(BS-co-GA)分子链更加柔顺,因此降解性能比P(BS-co-PeD)好.
(2)酸段亚甲基的引入,起到分配羰基碳电荷的效应,促进催化反应的进行,醇段亚甲基的引入无此效应,因此P( BS-co-PeD)降解速率小于P(BS-co-GA).
[1] Marc A Hillmyer,Willian B Tolman.Aliphatic polyester block polymers:Renewable,degradable,and sustainable[J].Accounts of Chemical Research,2014,47(8):2 390-2 396.
[2] 徐亚鹏,李继航,陈明清,等.可生物降解聚酯P(DHCA-co-LA)的合成与表征[J].高分子学报,2010(3):300-307.
[3] 张敏,张驰,盛思丽,等.氮化硼改性两种脂肪族聚酯复合材料耐热性差异[J].陕西科技大学学报(自然科学版),2015,33(2):69-73.
[4] Huaiyu Wang,Ming Xu,Zhangwei Wu,et al.Biodegradable poly(butylene succinate) modified by gas plasmas and their in vitro functions as bone implants[J].Applied materials & interfaces,2012,8(4):4 380-4 386.
[5] 何小全, 赵彩霞, 邹国享,等.聚(丁二酸丁二醇-co-二聚酸丁二醇)酯的合成及等温结晶行为[J].高分子材料科学与工程,2016,32(6):6-11.
[6] Leura Genovese,Nadia Lotti,Massimo Gazzano,et al.Novel biodegradable aliphatic copolyesters based on poly(butylene succinate) containing thioether-linkages for sustainable food packaging applications[J].Polymer Degradation & Stability,2016,13(2):191-201.
[7] 宋洁,延小雨,张敏,等.五倍子/PBS复合材料的性能研究[J].陕西科技大学学报(自然科学版),2016,34(4):65-70.
[8] Alessandro Jäger,Daniel Gromadzki,Eliézer Jäger,et al.Novel "soft" biodegradable nanoparticles prepared from aliphatic based monomers as a potential drug delivery system[J].Soft Matter,2012,16(8):4 343-4 354.
[9] 周卫东,张维,王小威,等.聚丁二酸丁二醇酯作为生物材料的应用及研究进展[J].化工新型材料,2012,40(7):145-147.
[10] Matteo Gigli,Macro Govoni,Nadia Lotti,et al.Bio-compatible multiblock aliphatic polyesters containing ether-likages:Influence of molecular architecture on solid-state properties and hydrolysis rate[J].RSC Advances,2014,62(4):32 965-32 976.
[11] 王国利,徐军,郭宝华,等.可生物降解聚丁二酸丁二醇酯及其共聚物的合成及改性研究进展[J].高分子通报,2011(4):99-109.
[12] 郝瑞,周艺峰,聂王焰.聚(丁二酸丁二醇酯癸二酸丁二醇酯)的合成与表征[J].高分子材料科学与工程,2012,
28(3):33-37.
[13] 张敏,李成涛,许小玲,等.在不同溶剂体系中PC脂肪酶对PBS基共聚物的催化降解和分子模拟[J].高分子通报,2014(12):141-148.
[14] Matteo Gigli,Andrea Negroni,Michelina Soccio,et al.Influence of chemical and architectural modifications on the enzymatic hydrolysis of poly(butylene succinate)[J].Green Chemistry,2012,14(10):2 885-2 893.
[15] Sangeeta Naik,Aditya Basu,Rakhi Saikia,et al.Lipases for use in industrial biocatalysis:Specificity of selected structural groups of lipases[J].Journal of Molecular Catalysis B:Enzymatic,2010,65(1):18-23.
[16] Qi Wu,Pankai Soni,Manfred T Reetz.Laboratory evolution of enantiocomplementary candida antarctica lipase B mutants with broad substrate scope[J].Journal of the American Chemical Society,2013,135(5):1 872-1 881.

