体表神经调控对功能性消化不良患者胃容受及胃电图的影响
汤净 陈军 谭安萍 谭琰
海南医学院第一附属医院消化内科(海口 570102)
功能性消化不良(functional dyspepsia,FD)是临床最常见的功能性胃肠病,但其病因和发病机制仍然不完全清楚,治疗很棘手。严重影响人们的生活质量。因此对FD发病机制的深入研究及探索新的治疗方法是当前消化系疾病研究中最引人注目的领域。FD病理生理机制表现其胃容受性(gastric accommodation,GA)下降,胃电节律紊乱,餐后胃电图(EGG)主波频率的百分率明显减少,主功率下降,自主神经系统失平衡等。GA障碍是FD病理生理机制的重要组成部分,40%~70%的FD患者存在GA障碍[1-2],因此对GA障碍的研究成为目前研究FD发病机制的一个重要切入点。
循证医学证实,足三里(ST36)、内关(PC6)穴位刺激治疗能改善FD患者上腹痛、反酸、嗳气、腹胀、纳差等症状[3-6]。在过去几十年用针灸疗法也作了大量研究,但是关于针灸治疗FD及其可能机制研究还是很少,因此探索针刺疗法对FD的潜在治疗作用有着很重要的临床意义。陈建德教授研究团队应用体表针灸穴位神经调控(transcutane⁃ous electroacupuncture,TEA)治疗糖尿病胃轻瘫,可以改善患者上腹部饱满、腹胀、恶心等症状,完全无不良反应[7]。以及其前期的动物研究表明TEA能改善FD动物模型的胃容受性、胃电节律紊乱,自主神经系统失衡[8-10]。OUYANG等[11]报道,电针刺激(electroacupuncture,EA)足三里(ST36)能改善狗迷走神经切除术后胃容受的损害。近年一些研究[12-14]显示无针经皮神经调控(transcutaneousneuromodulation,TN)、TEA方法对胃慢波、胃容受性、餐后胃主功率有改善作用,与EA一样有效。
本课题主要观察体表穴位无针经皮神经调控(TEA)治疗功能性消化不良患者对其胃容受和胃动力的作用效果,多维度地探讨的FD病理生理机制。TEA治疗FD的特色在于是非药物、非侵入性、安全且价格较便宜的医疗方法,可为治疗FD探索安全有效的创新疗法。
1 资料与方法
1.1一般资料入组病例均为2015年4月至2017年5月我院消化科的门诊患者,其中男49例,女57例,年龄25~60岁,平均(43.25±6.12)岁,平均病程(26.8±7.5)个月。以上病例符合罗马Ⅲ中FD的诊断标准。入组前6个月经胃镜、B超和实验室检查排除食管炎、消化性溃疡和肝胆胰等器质性疾病;无糖尿病、肾病、结缔组织病等全身性疾病和精神疾病史;无腹部手术史,年龄18~65岁。10例健康对照。入组的FD患者按序号随机分成两组,双盲交叉进行两组实验,每一位患者分别进行TEA治疗和假性TEA(Sham⁃TEA)治疗。两组患者在年龄、性别、病程、临床症状积分方面差异无显著性(P>0.05)。本课题通过海南医学院第一附属医院伦理委员会。受试者在试验前签署知情同意书。
1.2方法
1.2.1试验方案治疗穴位取足三里(ST36)和内关(PC6)。每个受试者按照随机顺序参加TEA和假-TEA(Sham⁃TEA)两个研究。一组先用TEA连续治疗4周,一天2次,早晚各1次,每次治疗30 min,刺激参数:2 s⁃on,3 s⁃off,25 Hz,0.6 ms。随后1周洗脱,然后再进行4周假-TEA治疗作为对照;另一组流程同第一组,但治疗期和对照期顺序颠倒。比较两组治疗前后胃容受性、胃电图及临床症状变化。便携式神经调控刺激器(SNM⁃FDC0,宁波迈达医疗设备有限公司研发)分别放FD患者在足三里(ST36)和内关(PC6)。ST36位于腓骨和胫骨之间,从外膝下4指宽,胫骨旁1指宽处。假⁃TEA组(Sham⁃TEA):假电针穴位是位于足三里(ST36)外侧往下10~15 cm不在任何经络线上的部位;另一假电针穴位是位于远离内关PC6 15~20 cm没有任何经络线的部位。10例健康对照者不进行TEA或Sham⁃TEA治疗,只测试胃容受作为FD患者的基线对照。
1.2.2检测方法禁食1夜后于清晨进行检测。采用体表4通道胃电图监测仪(MEGG⁃04A,宁波迈达医疗设备有限公司)检测。患者取仰卧位,除去放置电极部位的体毛,用磨擦剂清洁皮肤,电极中央放导电糊,沿胃窦轴线方向放置检测电极,电极3置于腹部正中线上、剑突与脐连线中点线的中点处;电极4置于电极3右侧水平距离5 cm处;电极2置于电极3左上角约5 cm,电极1置于电极2左上角约5 cm处。参考电极置于剑突部位。受试者在记录期间不允许说话、阅读或睡觉。先空腹查30 min,继而让患者进食液体试餐(0.95 kCal/mL)的标准餐,进行饱腹测试。餐后再检查30 min。观察指标:主频率(DF)、主功率(DP)及正常慢波节律百分比(PSR)。
1.2.3胃容受测试受试者能摄入的最多液体体积表示胃容受。禁食12 h,受试者按照指示以30 mL/min喝下试餐(0.95 kCal/mL)直至受试者报告已经达到最大饱腹感。受试者每隔5 min完成一个饱感评分,使用标准:0,没有症状;1,轻微;2,轻度;3,中度;4,明显;5,最大或难以忍受的饱腹感。当达到5分时,受试者停止喝试餐。受试者摄入的总胃液体容量记录下来,这反映胃的容受(GA)。
1.2.4评估消化不良的症状消化不良的症状主要通过胃主要症状积分来评估,包括基线值和TEA或假-TEA治疗后的症状指数。这些症状包括上腹痛、上腹部不适、餐后饱胀感、上腹部胀满、早饱、恶心、呕吐、过度打嗝、胃烧心感等。每个症状分级根据严重程度计分:0分,无症状;1分,轻微;2分,中度;3分,严重。症状最高总分36分。
1.3统计学方法结果表示为平均值±标准差。采用t和U检验,P<0.05表示差异有统计学意义。
2 结果
2.1TEA对胃容受性的影响正常对照组胃容受性结果:初始容积量(367±42.3)mL,最大胃容积量即胃容受(GA)(725±46)mL。FD患者胃容受性结果:初始容积量(235±38.5)mL(t=9.90,P<0.001),最大容受量(基线值)(539±36)mL(t=15.24,P<0.001)。见图1A。
TEA治疗增加了FD患者的胃容受(715±32)mL,与基线比较差异有统计学意义(U=37.62,P<0.001);假-TEA并没有增加患者的GA(549±38)mL,与基线相比差异无统计学意义(U=1.96,P=0.065)。FD患者胃容受在TEA和假⁃TEA治疗后两者有明显差异(U=34.4,P<0.001)。见图1B。
2.2TEA减少FD的症状积分FD患者治疗前平均症状积分(基线值)为24.5±2.9,TEA治疗后平均症状积分为11.9±2.1(U=36.23,P<0.001)。假⁃TEA治疗后平均症状积分为23.8±4.3,与基线比较差异无统计学意义(U=1.39,P=0.15)。TEA组与假⁃TEA组的症状积分比较差异有统计学意义(U=25.6,P<0.001)。见图2。
2.3TEA对FD患者胃电图的影响
2.3.1空腹及餐后(最大饱腹状态)的胃电图正常慢波百分比FD患者空腹时的胃慢波百分比为(52.6±8.3)%;餐后胃慢波百分比为(50.2±7.3)%。TEA组:空腹胃慢波百分比为(70.9±2.4)%,餐后胃慢波百分比为(68.2±3.1)%,与治疗前比较不管空腹或者餐后,差异均有统计学意义(空腹U=21.8,餐后最大饱腹U=23.36,P< 0.001)。假⁃TEA组:空腹时胃慢波百分比为(54.7±9.4)%,餐后胃慢波百分比为(52.3±10.4)%,与治疗前比较差异无统计学意义(空腹U=1.72,餐后U=1.7,P=0.07)。TEA组与假⁃TEA组比较差异有统计学意义(空腹U=17.19,餐后U=14.2,P< 0.001)。见表1。
2.3.2空腹及餐后(最大饱腹状态)的主功率FD患者空腹时胃主功率(30.25±3.76)db,餐后胃主功率(28.71±2.85)db;TEA组:空腹时主功率(35.35±1.53)db,餐后主功率(46.23±4.03)db,与治疗前相比不管什么状态差异均有统计学意义(空腹U=13.37,餐后U=36.54,P< 0.001)。假⁃TEA组:空腹时主功率(30.52±2.35)db,餐后主功率(29.81±3.67)db,与治疗前相比不管什么状态差异均无统计学意义(空腹U=0.62,餐后U=1.97,P>0.05)。TEA组FD患者餐后EEG主功率明显高于假⁃TEA组(U=15.1,P< 0.001)。见表1。

图1 A 胃容受Fig.1A The gastric accommodation in normal controls and patients with FD
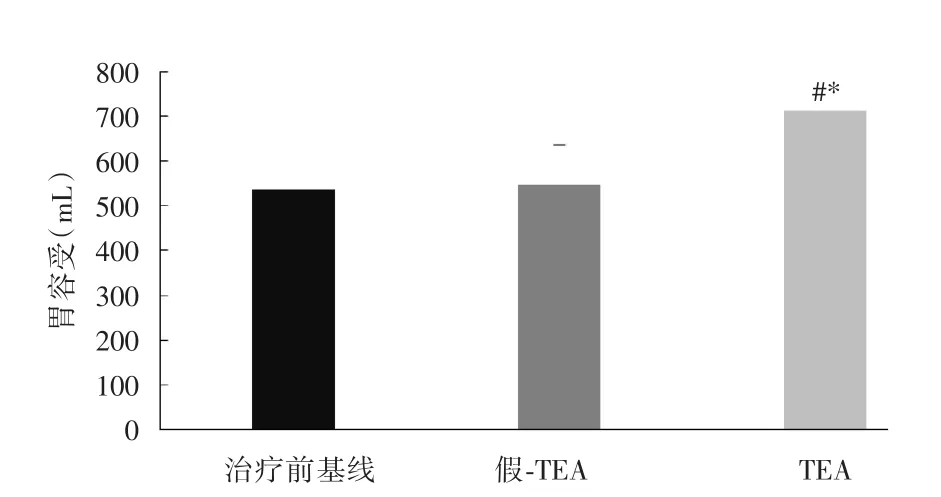
图1 B TEA和Sham⁃TEA治疗后胃容受变化Fig.1B The maximum tolerable volume after TEA and sham⁃TEA
3 讨论
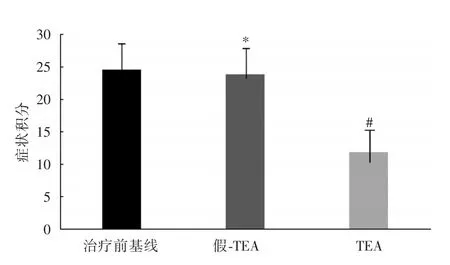
图2 TEA和Sham⁃T治疗后临床症状积分变化Fig.2 The clinical symptom scores in FD patients after TEA and sham⁃TEA treatment
表1 TEA治疗对FD患者胃电图的影响Tab.1 Effects of TEA treatment on EGG in patients with functional dyspepsia ±s
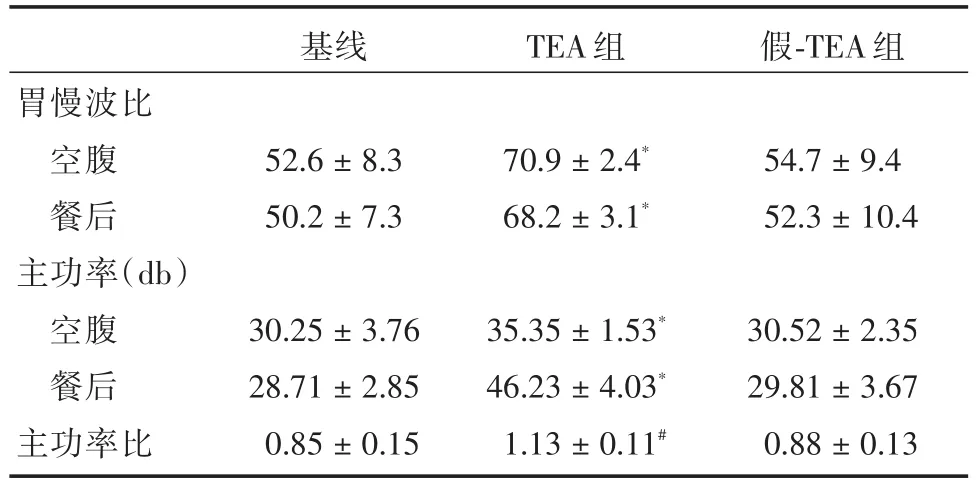
表1 TEA治疗对FD患者胃电图的影响Tab.1 Effects of TEA treatment on EGG in patients with functional dyspepsia ±s
注:TEA组 vs.治疗前(基线),*P <0.001;TEA组 vs.Sham⁃TEA组,#P<0.001
基线TEA组 假⁃TEA组胃慢波比空腹餐后主功率(db)空腹餐后主功率比52.6±8.3 50.2±7.3 70.9±2.4*68.2±3.1*54.7±9.4 52.3±10.4 30.25±3.76 28.71±2.85 0.85±0.15 35.35±1.53*46.23±4.03*1.13±0.11#30.52±2.35 29.81±3.67 0.88±0.13
本课题研究结果显示:用无针经皮电刺激神经调控(TEA)作用体表穴位足三里(ST36)和内关(PC6)可以明显改善FD患者的胃容受性,增强患者的餐后胃慢波比例和餐后主功率加强;明显缓解FD患者常见的顽固的临床症状:上腹痛、上腹部不适、餐后饱胀感、上腹部胀满、早饱、恶心、呕吐、过度打嗝、胃烧心感等。通常认为电刺激(EA)对动力学紊乱调节取决于刺激位点,中医学中电针刺激或针灸体表穴位ST36、PC6一直用于治疗胃部疾病,也常用于实验研究[13]。本团队在前期临床研究中也选择ST36和PC6,结果表明该位点可用于治疗功能性消化不良症状,改善胃动力[14]。
近端胃舒张功能受损是产生消化不良症状,尤其是早饱的病理基础,也是功能性消化不良的重要发病机制之一。因此如何改善消化不良患者的胃容受性功能,是治疗功能性消化不良的关键,也是研究热点。笔者前期研究结果显示:针灸穴位神经调控能改善消化不良动物模型的胃容受性下降,改善胃电节律紊乱,并可以调节自主神经系统失平衡[15]。
内脏高敏感认为是FD的发病机制之一[16]。内脏高敏感包括:(1)低阈值刺激即可引起反应或不适感;(2)正常人不被感知的生理刺激,在疾病下被感知,引起腹胀、早饱及疼痛不适等;(3)对伤害性刺激反应强烈,引起剧烈疼痛。目前,针灸对FD患者内脏敏感性的研究国内外均很少报道。胃的初始容量、最大耐受容量、初始压力、最大耐受压力等指标可以反映近端胃的感觉阈值。本课题研究显示,FD患者的症状积分显著高于正常人,FD患者胃容受检查其初始感觉阈值和最大感觉阈值均低于正常人,说明FD患者存在内脏高敏感性。经TEA治疗的FD患者症状积分明显下降,胃容受性增加,这与国外相关研究报道相似[17]。说明TEA可以降低FD患者的内脏高敏感,对治疗功能性消化不良有临床应用价值。
EEG的重要分析参数包括胃电慢波比例,主功率和主功率比,反映餐后胃动力。胃慢波在调节胃动力的多因素中起着重要作用。研究表明胃电图是研究胃电慢波准确可靠的方法[18]。传统的有创穴位电针刺激已经应用于治疗胃动力紊乱。之前的研究也提示电刺激(EA)可以改善胃慢波比例。笔者应用胃电图(EEG)记录受试者的胃电活动,可以客观反映FD患者胃电的节律和功率。本课题研究结果表明,TEA能改善FD的胃慢波紊乱和提高餐后主功率;TEA通过调整异常胃肌电活动,促进胃动力和胃排空,为临床治疗FD特别是难治性消化不良提供了一种独特的新方法,这是一种创新的具有广泛临床应用前景的治疗手段。本研究为日后开展应用TEA治疗功能性消化不良提供理论基础。那么,体表神经调控治疗可成为处置胃肠动力、胃容受等功能受损的可行方法;说明研发家庭便携式神经调控治疗仪具有良好的临床应用前景。
本研究观察,TEA治疗FD可能是通过调节自主神经发挥作用的,其治疗作用机制还需进一步深入研究。补充和替代性医疗方法作为功能性胃肠疾病的治疗模式正成为当今关注的热点。TEA也是一种当前比较推荐的替代性治疗,下一步笔者将继续探讨TEA治疗其他类别的功能性胃肠病的疗效和机制,作为本课题的拓展研究。
[1]KLAUS B,ASHOK T,SALMAN N.Disorders of gastrointesti⁃nal hypomotility Versionl[J].F1000 Res,2016.doi:10.12688/f1000research.8658.1
[2]马忠金,王淑芳.茯苓神志爽心丸联合全面干预治疗功能性消化不良的疗效[J].实用医学杂志,2014,30(14):2318⁃2320.
[3]许良锋,王启仪,沙卫红.电刺激治疗功能性消化不良的研究进展[J].实用医学杂志,2011,27(15):2874⁃2876.
[4]张洪领,杨春敏.功能性消化不良的脑肠轴机制研究进展[J].实用医学杂志,2010,26(17):3265⁃3266.
[5]黄伟锋,欧阳守.体表胃肠起搏治疗功能性胃肠道疾病的研究[J].实用医学杂志,2012,28(7):1077⁃1080.
[6]PARK Y C,KANG W,CHOI S M,et al.Evaluation of manual acupuncture at classical and nondefined points for treatment of functional dyspepsia:a randomized⁃controlled trial[J].Altern Complement Med,2009,15(8):879⁃884.
[7]IRENE S,GENG QING S,YAN S,et al.Central and peripher⁃al effects of transcutaneous acupuncture treatment for nausea in patients with diabetic gastroparesis[J].Neurogastroenterol Motil,2017,23(2):245⁃253.
[8]YIN J Y,CHEN J D.Gastrointestinal motility disorders and acupuncture[J].Auton Neurosci,2010,28,157(1⁃2):31⁃37.
[9]SONG J,YIN J Y,CHEN J D.Needleless transcutaneous elec⁃troacupuncture improves rectal distension⁃induced impairment in intestinal motility and slow waves via vagal mechanisms in dogs[J].Int J Clin Exp Med,2015,8(3):4635⁃4646.
[10]ZHANG Z H,YIN J Y,CHEN J D.Ameliorating effects of au⁃ricular electroacupuncture on rectal distention⁃induced gastric dysrhythmias in rats[J].PLoS One,2015,10(2):e0114226.
[11]OUYANG H,XING J,CHEN J.Electroacupuncturerestores im⁃paired gastricaccommodation in vagotomized dogs[J].Dig Dis Sci,2004,49(9):1418⁃1424.
[12]CHEN J D Z,YIN J Y,HOU X H,et al.Complementary and alternative therapies for functional gastrointestinal diseases 2016[J].Evid Based Complement Alternat Med,2017,2017:2089165.
[13]LI H,HE T,XU Q,et al.Acupuncture and regulation of gas⁃trointestinal function[J].World J Gastroenterol,2015,21(27):8304⁃8313.
[14]XU F,TAN Y,HUANG Z H,et al.Ameliorating effect of transcutaneous electroacupuncture on impaired gastric accommo⁃dation in patients with postprandial distress syndrome⁃predomi⁃nant functional dyspepsia :a pilot study[J].Evid Based Com⁃plement Alternat Med,2015,2015:168252.
[15]SUN Y,TAN Y,SONG G,et al.Effects and mechanisms of gastricelectricalstimulation on visceralpain in a rodentmodel of gastrichyperalgesiasecondary to chemicallyinducedmucosalulcer⁃ation[J].Neurogastroenterol Motil,2014,26(2):176⁃186.
[16]RITA B,BRADEN K.Functional dyspepsia[J].TherapAdv⁃Gastroenterol,2010,3(3):145⁃164.
[17]HUANG Z,ZHANG N,XU F,et al.Ameliorating effect of transcutaneous electroacupuncture on impaired gastric accommo⁃dation induced by cold meal in healthy subjects[J].Gastroen⁃terol Hepatol,2016,31(3):561⁃566.
[18]ZHANG N,SONG G,CHEN J,et al.Ameliorating effects and autonomic mechanisms of needle⁃less transcutaneous electrical stimulation at ST36 on stress⁃induced impairment in gastric slow waves[J].Gastroenterol Epatol,2015,30(11):1574⁃1581.

