Haynes 282镍基合金在600~700 ℃超临界水中的氧化特性
, ,,, ,
(华北电力大学1.能源动力与机械工程学院;2.电气与电子工程学院,北京 102206)
0 引 言
为满足经济增长的需求,并进一步提高电力生产效率、降低污染物排放量,燃煤电厂的主蒸汽参数不断提高,已达到了620 ℃、30 MPa的超超临界(USC)水准[1]。欧洲、美国、日本等国家已在逐步推进蒸汽参数为700 ℃先进超超临界(A-USC)技术的研发工作,我国也于2011年1月启动了“国家700 ℃超超临界燃煤发电关键技术和设备研发及应用示范”项目,计划自主完成700 ℃超超临界燃煤机组的发电总体设计方案[2]。美国计划将蒸汽参数提高至760 ℃、35 MPa,从而使亚临界机组的热效率由37%提升至45%,双回热系统的热效率达到47%,CO2的减排量有望达到7×105t·a-1[3]。然而,蒸汽在超过临界点后其物性将发生较大的变化,对结构材料具有更强的腐蚀性[4],因此700 ℃先进超超临界机组候选材料的耐腐蚀问题得到了重视。目前,700 ℃先进超超临界机组的候选材料主要为镍基合金[5],其高温强度和耐腐蚀性均优于超超临界机组采用的耐热钢的,这对提高机组运行的安全性和可靠性有着重要的作用。
Haynes 282合金是一种时效强化型镍基合金,具有高温强度高、抗氧化性强、热稳定性好、可加工性良好等特点[6-7],是700 ℃先进超超临界机组候选材料之一。目前,对Haynes 282合金在高温环境下的氧化行为已进行了一些研究。PEREZ-GONZALEZ等[8]研究了Haynes 282合金在800~1 000 ℃静态空气环境中的短时氧化行为,结果发现在150 h氧化过程中,氧化膜的生长速率遵循抛物线规律,形成了内层为Cr2O3、外层为TiO2的双层结构,同时在氧化膜与合金界面处存在Al2O3。唐丽英等[9]研究了Haynes 282合金在750 ℃高温蒸汽环境中的氧化行为,发现经过2 000 h的高温蒸汽氧化后,板状和管状Haynes 282合金表面均形成了外层为连续的Cr2O3、TiO2、(Mn, Fe, Cr)3O4混合物和内层为沿晶界和亚晶界呈网状分布的Al2O3的双层结构。李江等[10]研究发现,在650 ℃烟气环境中Haynes 282合金表面形成了Cr2O3氧化层,700~750 ℃时合金表面形成了含有第二类硫酸盐腐蚀产物的双层结构。综上可知,在不同环境中,温度对Haynes 282合金表面氧化膜的形成具有重要的影响。此外,国内外学者对Haynes 230、Inconel 617、Inconel 625镍基合金在高温蒸汽环境中的氧化特性[11-13]以及对镍基合金在超临界水中的氧化特性也进行了相关研究。CHANG等[14]研究发现,Inconel 625镍基合金在400~600 ℃超临界水动态环境中的氧化动力学曲线基本符合抛物线规律。ZHONG等[15]研究了Inconel690镍基合金在450~550 ℃、25 MPa超临界水中的氧化特性,发现氧化膜外层含有NiFe2O4尖晶石、NiO和Ni(OH)2,内层含有Cr2O3和NiCr2O4尖晶石。ZHANG等[16]研究了Hastelloy C-276合金在500~600 ℃超临界水中的氧化特性,发现随着温度的升高,氧化膜的生长速率增大且更易于剥落。然而,对Haynes 282镍基合金在超临界水中氧化特性的研究很少。
为此,作者在600~700 ℃、25 MPa超临界水中对Haynes 282镍基合金进行了氧化试验,研究了不同温度下合金的氧化动力学和氧化膜的表面形貌、微观结构及物相组成等,为我国700 ℃先进超超临界机组候选材料的选用提供试验参考。
1 试样制备与试验方法
试验采用氢电导率小于0.1 mS·cm-1的超纯水为工质。通过超纯水机制备超纯水后,采用氮气鼓泡法和添加联氨的化学方法对其进行除氧,直至溶解氧质量浓度小于10 μg·L-1。采用超纯水溶解氧仪和电导率仪分别对超纯水的溶解氧含量和电导率进行测试,以确保其满足试验要求。
Haynes 282合金由美国哈氏公司生产,其化学成分如表1所示。截取尺寸为20 mm×10 mm×2 mm的试样,用200#,400#,600#,800#,1000#砂纸依次打磨,金刚石抛光剂抛光,丙酮清洗,烘干待用。

表1 Haynes 282镍基合金的化学成分(质量分数)Tab.1 Chemical composition of Haynes 282 nickel-based alloy (mass) %
超临界水氧化试验装置参考文献[17],氧化温度分别为(600±3) ℃,(650±3) ℃,(700±3) ℃,压力为(25±0.5) MPa,氧化时间为1 000 h。在试验过程中,每200 h暂停试验,取出部分试样,再加入部分新试样,然后继续进行试验。采用精度为0.01 mg的METTLER TOLEDO电子天平称取不同时间氧化前后试样的质量,计算氧化质量增加,称量前保证试样在干燥箱内充分干燥。氧化质量增加与氧化时间的关系可用下式进行拟合[18]:
Δm=kptn
(1)
式中:Δm为单位面积氧化质量增加,mg·cm-2;kp为氧化速率,mg·cm-2·h-n;t为氧化时间,h;n为氧化时间指数。
采用JSM 6490LV型扫描电镜(SEM) 观察氧化后试样表面形貌,采用背散射电子成像观察截面形貌,用附带的能谱仪(EDS)分析微区成分。测试前,采用环氧树脂将试样固定,对其氧化层进行保护。采用XPert Powder型 X射线衍射仪(XRD)分析氧化膜的物相组成。用ESCALAB 250Xi型X射线光电子能谱仪(XPS)对氧化膜进行成分分析。
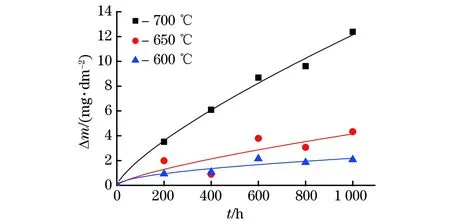
图1 在不同温度超临界水中Haynes 282合金的氧化动力学曲线Fig.1 Oxidation kinetics curves of Haynes 282 alloy in supercritical water at different tempertatures
2 试验结果与讨论
2.1 氧化动力学
由图1可知:Haynes 282合金的Δm随温度的升高和时间的延长而增大;700 ℃时,合金的Δm大约为650 ℃时的3倍,为600 ℃时的6倍;通过式(1)拟合得到600~700 ℃下合金的n分别为0.52,0.72,0.75,600 ℃时合金的氧化动力学曲线遵循抛物线规律,而650,700 ℃时合金的氧化动力学曲线介于抛物线与直线之间。通常,合金在蒸汽或超临界水中的氧化动力学与氧化速率的控制因素有关。当氧化温度为600 ℃时,由于氧化过程中离子扩散速率较低,此时合金的氧化速率由离子扩散速率决定,因此氧化动力学曲线基本遵循抛物线规律。当氧化温度为650,700 ℃时,在氧化初期,由于离子扩散速率升高,氧化反应速率低于离子扩散速率,此时的氧化动力学曲线符合直线规律;但随着氧化过程的进行,保护性氧化膜覆盖试样表面导致离子扩散速率降低,此时氧化速率的控制因素逐渐由氧化反应速率转变为离子扩散速率。因此,650,700 ℃时合金的氧化动力学曲线介于直线与抛物线之间。TAN等[19]也发现了相似的现象。
2.2 氧化膜物相组成和表面形貌
由图2可知:在氧化初期,即氧化时间为200 h时,不同温度下合金表面的氧化物相均不明显,基体镍的特征峰十分突出,随着氧化时间的延长,氧化物特征峰均有所增强,表明氧化物含量逐渐增大;当氧化时间为1 000 h时,600 ℃时合金表面氧化膜由Cr2O3和TiO2组成,650 ℃时氧化膜中除了存在Cr2O3和TiO2外,还存在少量MnCr2O4,700 ℃时氧化膜由NiCr2O4、Cr2O3、MnCr2O4组成,但并没有检测到TiO2。此外,图中Haynes 282合金基体镍的特征峰要明显强于氧化物相的,这表明形成于合金表面的氧化膜较薄。

图2 在不同温度超临界水中氧化不同时间后Haynes 282合金 表面的XRD谱Fig.2 XRD patterns of the surface of Haynes 282 alloy after oxidation in supercritical water for different temperatures and times
由图3可以看出:Haynes 282合金表面的氧化膜具有双层结构,外层为松散的多面体形状的微米尺寸氧化物颗粒,内层为由细小晶粒组成的致密氧化膜;氧化膜外层的氧化物颗粒尺寸和疏松程度均随温度升高和时间延长而增大,在700 ℃氧化600 h后,外层氧化膜的氧化物呈细小的菜花状,当氧化时间达到1 000 h后,外层氧化膜比600 ℃氧化1 000 h的更加平整。由此可见,在氧化过程中,温度和时间对氧化物膜形貌具有重要的影响。

图3 在不同温度超临界水中氧化不同时间后Haynes 282合金的表面形貌Fig.3 Surface morphology of Haynes 282 alloy after oxidation in supercritical water for different temperatures and times
由图4(a)~(c)可以看出:在600 ℃氧化400 h后,一些较大颗粒氧化物镶嵌于合金表面;位置A处的颗粒状氧化物主要含有钛元素,位置B处氧化膜较致密,主要含有铬、镍元素。由图4(d)~(f)可知,在700 ℃氧化400 h后,氧化膜中的钛元素含量比较低。由此可推测,600 ℃氧化后,合金表面氧化膜外层为颗粒状TiO2,内层为致密Cr2O3膜,TiO2分散于Cr2O3膜表面,而700 ℃氧化后,合金表面氧化膜的主要组成为MnCr2O4和NiCr2O4。
2.3 氧化膜横截面形貌及元素分布
由图5可知,在650,700 ℃氧化1 000 h后,合金表面氧化膜的厚度分别约为0.43,0.89 μm,氧化膜很薄。图6为不同扫描时间下氧化膜中不同元素的分布,由氧化膜外层向内层方向扫描,可以发现,氧化膜中主要含有铬、氧以及少量的铁、锰、镍等元素。综上可知,在650,700 ℃氧化后,合金表面氧化膜外层主要为富镍和锰的氧化物,而内层主要为富铬的氧化物,这是由金属离子与氧之间不同的亲和力而导致的。
2.4 氧化膜成分
通常,氧离子沿氧化膜内的短程扩散通道(如微型孔洞或晶界)向内扩散[15,20],并与铬发生反应,形成内层氧化膜;同时,阳离子向外扩散并在氧化膜/环境界面与氧发生反应,形成外层氧化膜。由图7~图9可知,600,650 ℃氧化后合金氧化膜中出现Ni0特征峰,700 ℃时合金在溅射初期,先出现Ni2+特征峰,随着溅射时间的延长,Ni2+的特征峰逐渐消失并出现Ni0特征峰;600~700 ℃时合金氧化膜中铬、锰、氧元素的特征峰均分别为Cr3+、Mn2+、O2-特征峰。结合XRD与XPS分析结果可以推断:600 ℃时合金表面形成的氧化膜内层主要为Cr2O3,外层则为零散的TiO2;650 ℃时氧化膜外层由TiO2与MnCr2O4组成,而内层由Cr2O3和少量的MnCr2O4组成;700 ℃时氧化膜外层由NiCr2O4与MnCr2O4组成,而内层由Cr2O3和少量的MnCr2O4组成。PEREZ-GONZALEZ等[8]从热力学平衡的角度分析,认为TiO2比Cr2O3更易形成。因此,合金表面氧化膜外层中通常含有TiO2,但由于合金中钛含量较低,因而TiO2的含量也较低。另外,由于锰元素在铬中具有较大的溶解度,能够扩散至氧化膜外层[19],因此随着温度的升高,更多的锰元素向外扩散并形成MnCr2O4。
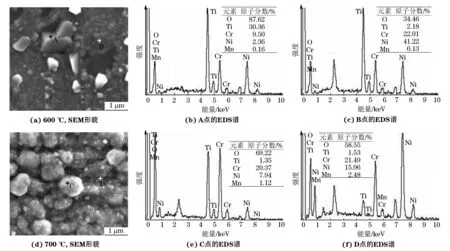
图4 在600,700 ℃超临界水中氧化400 h后Haynes 282合金表面的SEM形貌和EDS谱Fig.4 Surface morphology (a, d) and EDS spectrum (b, c, e, f) of Haynes 282 alloy in supercritical water at 600 (a-c), 700 ℃ (d-f) for 400 h

图5 在650,700 ℃超临界水中氧化1 000 h后Haynes 282合金横截面背散射电子形貌及元素线扫描结果Fig.5 Backscattered electron morphology and linear scanning results of elements of the cross section of Haynes 282 alloy in supercritical water at 650 (a), 700 ℃(b) for 1 000 h
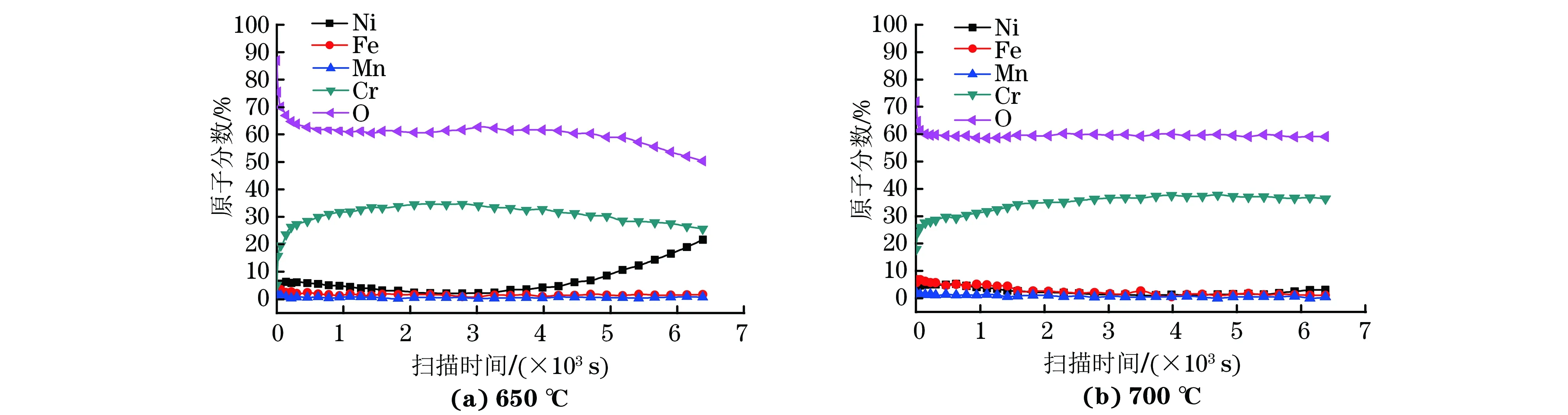
图6 在650,700 ℃超临界水中氧化1 000 h后Haynes 282合金氧化膜沿厚度方向的元素分布Fig.6 Elements distribution of the oxide film of Haynes 282 alloy along the thickness direction in supercritical water at 650 (a), 700 ℃ (b) for 1 000 h
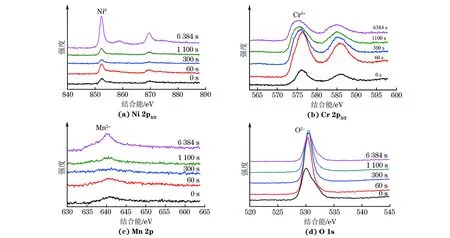
图7 在600 ℃超临界水中氧化1 000 h后Haynes 282合金表面在不同溅射时间下的XPS谱Fig.7 XPS spectra of the surface of Haynes 282 alloy oxided in supercritical water at 600 ℃ for 1 000 h after sputtering for different times
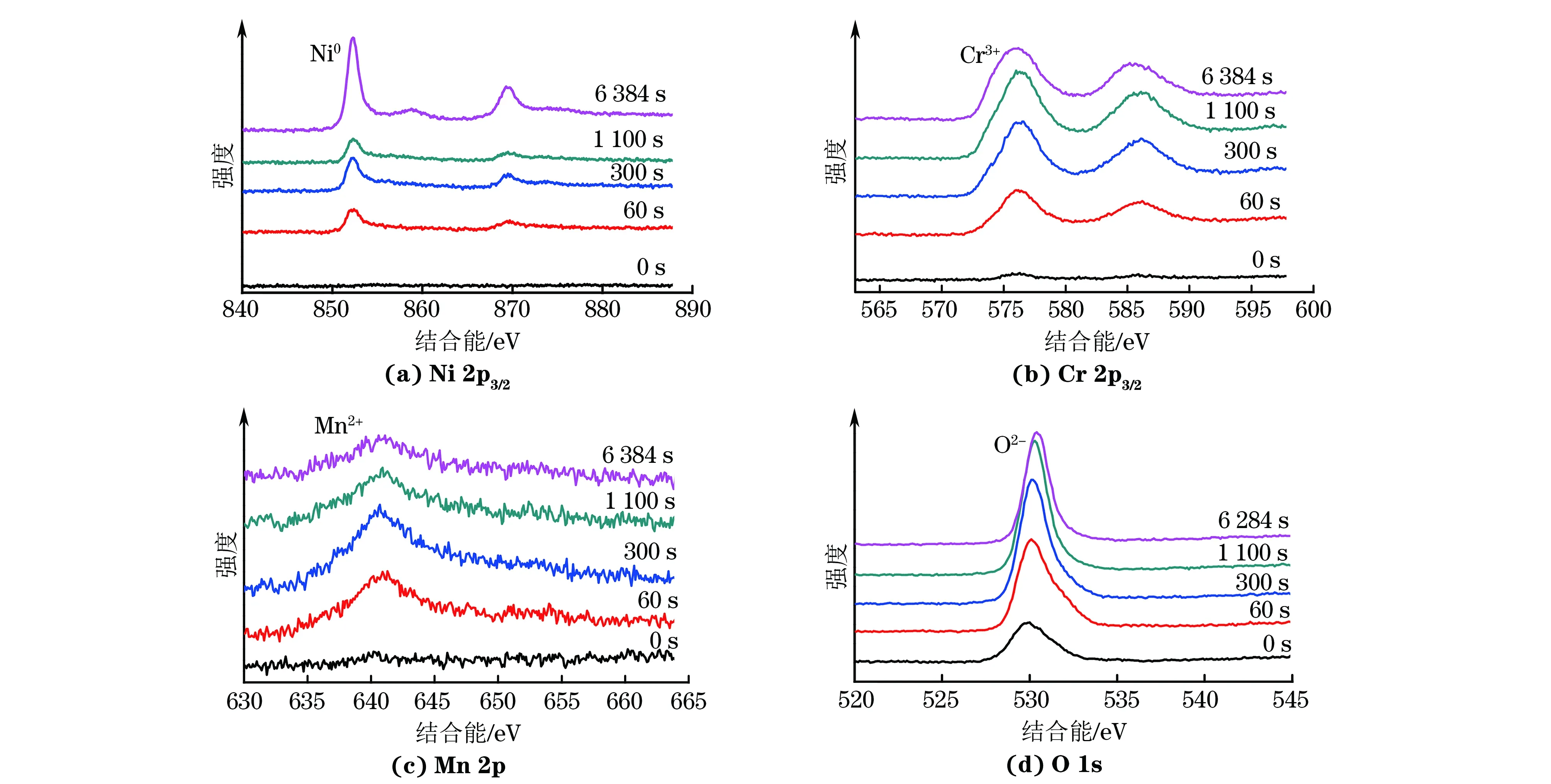
图8 在650 ℃超临界水中氧化1 000 h后Haynes 282合金表面在不同溅射时间下的XPS谱Fig.8 XPS spectra of the surface of Haynes 282 alloy oxided in supercritical water at 650 ℃ for 1 000 h after sputtering for different times

图9 在700 ℃超临界水中氧化1 000 h后Haynes 282合金表面在不同溅射时间下的XPS谱Fig.9 XPS spectra of the surface of Haynes 282 alloy oxided in supercritical water at 700 ℃ for 1 000 h after sputtering for different times
CHANG等[14]与ZHONG等[15]研究发现,在超临界水中,镍基合金表面氧化膜外层含有NiO,这主要是因为在Cr2O3氧化膜中镍离子向外扩散的速率大约为铬离子的两倍,因此镍离子可以穿过Cr2O3氧化膜并在外层形成NiO[20]。BRIKS等[21]研究发现,金属缺陷型氧化物NiO和Cr2O3的形成与生长过程的控制因素主要为阳离子的向外扩散,而氧化物生长的驱动力为金属离子与氧反应所产生的吉布斯自由能[22]。因此,与Cr2O3相比,形成NiO需要更高的氧分压,这也是NiO只形成于外层氧化膜的原因。700 ℃时合金表面的氧化膜以及由超临界水分解出的溶解氧导致氧化膜/环境界面处产生更高的氧分压,进而使镍氧化成Ni2+。SENNOUR等[23]研究发现,氧化物按热稳定性由强到弱的顺序为Cr2O3、NiCr2O4、NiO,这表明在高温超临界水中NiCr2O4比NiO具有更高的热稳定性。因此,为形成更加稳定的氧化物,NiO与Cr2O3发生反应形成NiCr2O4尖晶石,反应式为

(2)
综上可知,NiO仅在氧化过程中的较短时间内形成,之后便形成NiCr2O4,因此在700 ℃超临界水中,合金表面氧化膜中仅检测出NiCr2O4,并没有发现NiO的存在。
温度对Haynes 282镍基合金在超临界水中氧化速率的影响关系式[17]为
(3)
式中:Ea为氧化激活能,J·mol-1;k0为常数;R为理想气体常数;T为氧化温度,K。
单位面积氧化质量增加与时间的关系可以表示为
(4)
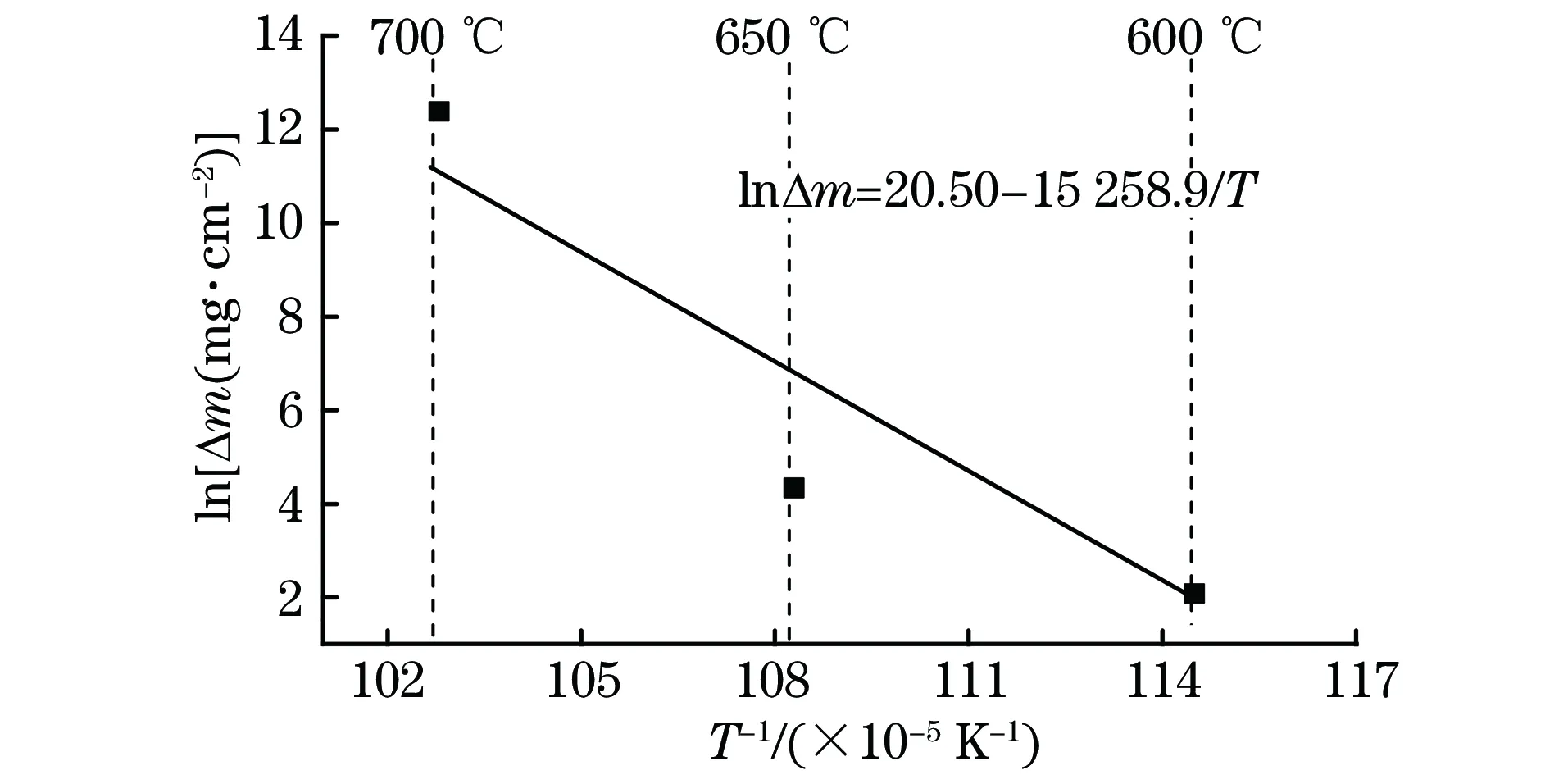
图10 在600~700 ℃超临界水中Haynes 282合金的 lnΔm-T-1关系曲线Fig.10 Relationship curves of lnΔm-T-1 of Haynes 282 alloy in supercritical water at 600-700 ℃
根据图1中不同温度氧化1 000 h的试验结果,得到如图10所示的氧化温度的倒数与单位面积氧化质量增加对数之间的关系,进而通过计算图10曲线的斜率获得Haynes 282合金在600~700℃温度范围内的氧化激活能,为253.72 kJ·mol-1,这与铬离子在Cr2O3膜中的扩散激活能相同[24],说明Haynes 282合金的氧化过程可能受到铬离子向外扩散的控制。
3 结 论
(1) Haynes 282合金的单位面积氧化质量增加随着温度的升高和时间的延长而增大;600 ℃时合金的氧化动力学曲线遵循抛物线规律,650,700 ℃时合金的氧化动力学曲线介于抛物线和直线之间。
(2) Haynes 282合金表面的氧化膜具有双层结构,外层为松散的多面体形状的微米尺寸氧化物颗粒,内层为由细小晶粒组成的致密氧化膜。600 ℃氧化后合金表面氧化膜内层主要为Cr2O3,外层则为TiO2;650 ℃氧化后氧化膜外层由TiO2与MnCr2O4组成,内层由Cr2O3和少量的MnCr2O4组成;700 ℃氧化后氧化膜外层由NiCr2O4与MnCr2O4组成,内层由Cr2O3和少量的MnCr2O4组成。
[1] PATEL S J, DEBARBADILLO J J, BAKER B A,etal. Nickel base superalloys for next generation coal fired AUSC power plants[J].Procedia Engineering, 2013, 55(12): 246-252.
[2] 张涛, 郝丽婷, 田峰, 等. 700 ℃超超临界火电机组用高温材料研究进展[J]. 机械工程材料, 2016, 40(2): 1-6.
[3] VISWANATHAN R, COLEMAN K, RAO U. Materials for ultra-supercritical coal-fired power plant boilers[J]. International Journal of Pressure Vessels and Piping, 2006, 83(11/12): 778-783.
[4] YAMAGUCHI T. Structure of subcritical and supercritical hydrogen-bonded liquids and solutions[J]. Journal of Molecular Liquids, 1998, 78(1/2): 43-50.
[5] 陈石富, 秦鹤勇, 张文云, 等. 700 ℃超超临界锅炉用镍基合金管材的研究进展[J]. 机械工程材料, 2012, 36(11): 1-4.
[6] PIKE L M. Haynes®282TMalloy: A new wrought superalloy designed for improved creep strength and fabricability[C]∥Proceedings of GT2006 ASME Turbo Expo 2006: Power for Land, Sea, and Air. Barcelona: ASME, 2006: 1031-1039.
[7] PIKE L M. Low-cycle fatigue behaviour of Haynes®282®and other wrought gamma-prime strengthened alloys[C]∥Proceedings of GT2007 ASME Turbo Expo 2007: Power for Land, Sea, and Air. Montreal: ASME, 2007: 161-169.
[9] 唐丽英, 周荣灿, 侯淑芳, 等. 两种表面状态的Haynes 282在750 ℃高温蒸汽中的氧化行为[J]. 中国电机工程学报, 2016, 36(10): 2728-2733.
[10] 李江, 周荣灿, 唐丽英, 等. 模拟燃用高硫煤锅炉烟气环境中Haynes 282合金的腐蚀行为[J]. 热力发电, 2017, 46(10): 30-35.
[11] KIM D, SAH I, LEE H J,etal. Hydrogen effects on oxidation behaviors of Haynes 230 in high temperature steam environments[J]. Solid State Ionics, 2013, 243(4): 1-7.
[12] GORMAND M, HIGGINSON R L, DU H,etal. Microstructural analysis of IN617 and IN625 oxidised in the presence of steam for use in ultra-supercritical power plant[J]. Oxidation of Metals, 2013, 79(5/6): 553-566.
[13] KIM D, KIM D, LEE H J,etal. Corrosion characteristics of Ni-base superalloys in high temperature steam with and without hydrogen[J]. Journal of Nuclear Materials, 2013, 441(1/2/3): 612-622.
[14] CHANG K H, HUANG J H, YAN C B,etal. Corrosion behavior of Alloy 625 in supercritical water environments[J]. Progress in Nuclear Energy, 2012, 57(5): 20-31.
[15] ZHONG X Y, HAN E H, WU X. Corrosion behavior of Alloy 690 in aerated supercritical water[J]. Corrosion Science, 2013, 66(1): 369-379.
[16] ZHANG Q, TANG R, YIN K,etal. Corrosion behavior of Hastelloy C-276 in supercritical water[J]. Corrosion Science, 2009, 51(9): 2092-2097.
[17] ZHANG N Q, ZHU Z L, XU H,etal. Oxidation of ferritic and ferritic-martensitic steels in flowing and static supercritical water[J]. Corrosion Science, 2016, 103: 124-131.
[18] CHANG K H, CHEN S M, YEH T K,etal. Effect of dissolved oxygen content on the oxide structure of Alloy 625 in supercritical water environments at 700 ℃[J]. Corrosion Science, 2014, 81: 21-26.
[19] TAN L, ALLEN T R, YANG Y. Corrosion behavior of alloy 800H (Fe-21Cr-32Ni) in supercritical water[J]. Corrosion Science, 2011, 53(2): 703-711.
[20] LOGNIG R E, SCHMIDT H P, HENNESEN K,etal. Diffusion of cations in chromia layers grown on iron-base alloys[J]. Oxidation of Metals, 1992, 37(1/2): 81-93.
[21] BRIK S N, MEIER G H, PETTIT F S. Introduction to the high-temperature oxidation of metals[M]. New York: Cambridge University Press,2006.
[22] PAN G Q, WU G H, XIU Z Y,etal. Microstructure, oxidation resistance and high-temperature strength of a new class of 3D open-cell nickel-based foams[J]. Materials Characterization, 2012, 70(4): 125-136.
[23] SENNOUR M, MARCHETTI L, MARTIN F,etal. A detailed TEM and SEM study of Ni-base alloys oxide scales formed in primary conditions of pressurized water reactor[J]. Journal of Nuclear Materials, 2010, 402(2/3): 147-156.
[24] ENGLAND D, VIRKAR A V. Oxidation kinetics of some nickel-based superalloy foils and electronic resistance of the oxide scale formed in air: Part 1[J]. Journal of the Electrochemical Society, 2015, 146(9): 3196-3202.

