螺环化合物的合成研究进展
陈炎钊
(绍兴文理学院 化学化工学院,浙江 绍兴 312000)
螺环化合物是一种具有特殊性能的有机中间体,其具有刚性结构,结构稳定,存在异头效应、螺共轭以及螺超共轭等一般有机化合物不具备的特殊性质。它们独特的结构特征和生物活性引起了人们的广泛关注。螺环化合物在不同领域可有不同的作用,在医药方面可作为镇痛药等[1]、在生活中可作为阻燃剂和灭火剂[2-3]等。
1 合成研究
1.1 含异噁唑结构的螺环化合物
对于螺异噁唑化合物,在已有的合成中来说,是一种比较新型的化合物,并且于1997年冯亚青和张晓东[4]等,利用氧化腈与4,4-亚甲基-1-甲基哌啶的1,3-偶极环加成反应生成了杂螺(4,5)葵烷化合物,产物经LiAlH4还原成了γ-氨基醇,最后经插入C-1单元扩环生产了新的杂螺(5,5)十一烷化合物。其氧化腈为偶极体,亚甲基哌啶为亲偶极体1,3-偶极环加成反应合成了一类新的杂环体系及一系列新的螺异噁唑衍生物,此杂螺化合物经还原开环后,再与合适的试剂环合可得到另一类扩展的新的杂螺环体系及螺(5,5)环化合物。如图1。
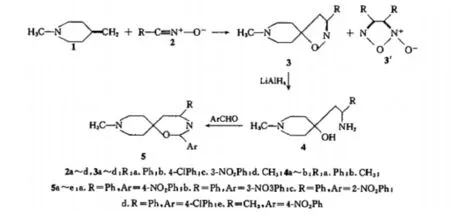
图1 杂螺环体系及螺(5,5)环化合物的合成
1.2 含多个手性中心的呋喃型螺环化合物
我国早期已有的报道是在2000年,由张淅芸和陈庆华等,通过改进已有的方法,利用5-(l-孟氧基)-3-溴-2(5H)-呋喃新手性源合成子与乙醇发生串联的不对称双Michael加成和分子内新核取代反应,合成了含有多个手性中心的螺(1-溴-4-l-孟氧基-5-氧杂-6-氧代双环(3.1.0)乙烷-2,3-(4'-乙氧基-5'-孟氧基丁内酯))。早期人们尝试利用炔醇环化异构化合成二氢呋喃类化合物,但这些方法涉及多步反应且繁琐,所得的最终产物的产率也较低。但于2014年,经过不断探索,邹建峰和李新生[5]设计出了更加简单方便的合成方法。他们在辛可宁的作用下,利用迈克(Michael)加成方法,在手性碱的作用下,以靛红衍生物(N-甲基-3-烃基-2-吲哚酮)和氰基苯乙烯衍生物为原料,1,3,5-三甲苯为溶剂,合成了一系列的新型的手性吲哚螺-2,3-二氢化呋喃衍生物。该反应产率高(90%~99%),选择性好,而且操作简单、后处理方便,是近年来一个很成功的设计改进的合成方法。如图2。
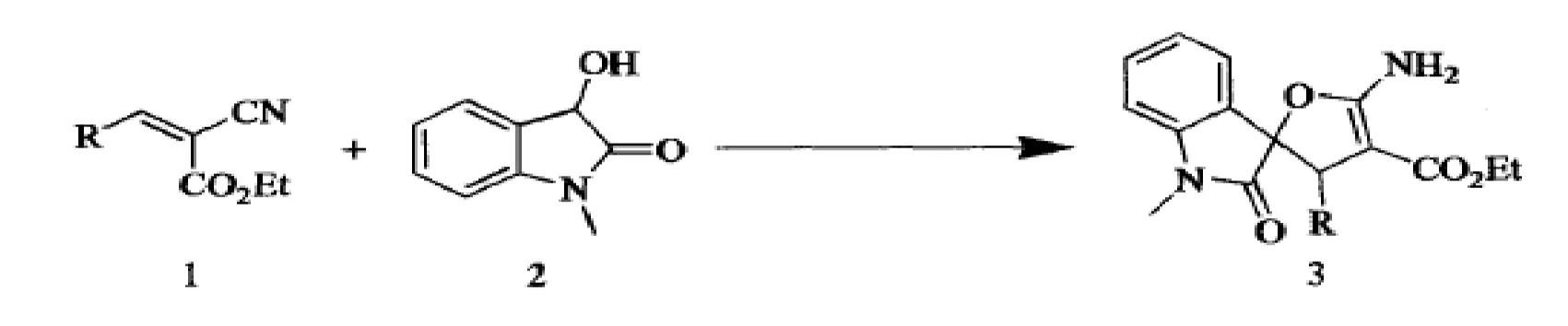
图2 手性吲哚螺-2,3-二氢化呋喃衍生物的合成
1.3 含吲哚型结构的螺环化合物
螺环氧化吲哚是一类非常重要的核心结构,它存在于大量具有生物活性的化合物中。兰州大学新药临床前研究甘肃省重点实验室王锐小组[6]发展了这类化合物与缺电子烯烃的Michael加成反应,使其与合适的Michael受体在手性胺-硫脲双功能催化剂的控制和催化下发生加成环化,以高的产率与对映体选择性快捷高效地构建了含有三个连续手性中心的螺环氧化吲哚结构。
光致变色现象是一种从1952年起受到重视的化学现象,其在信息储存、光控开关原件、光敏性磁性材料等领域显得越发重要,该研究领域取得的进展使其在其他领域的应用也日益受到重视,例如在服装材料与装饰材料等。刘振东、崔明等[7]于2004年合成了螺环类光致变色中间体-吲哚啉盐中间体,可用于光致变色化合物与高分子的共聚与嫁接,以获得功能性的光致变色高分子。如图3。
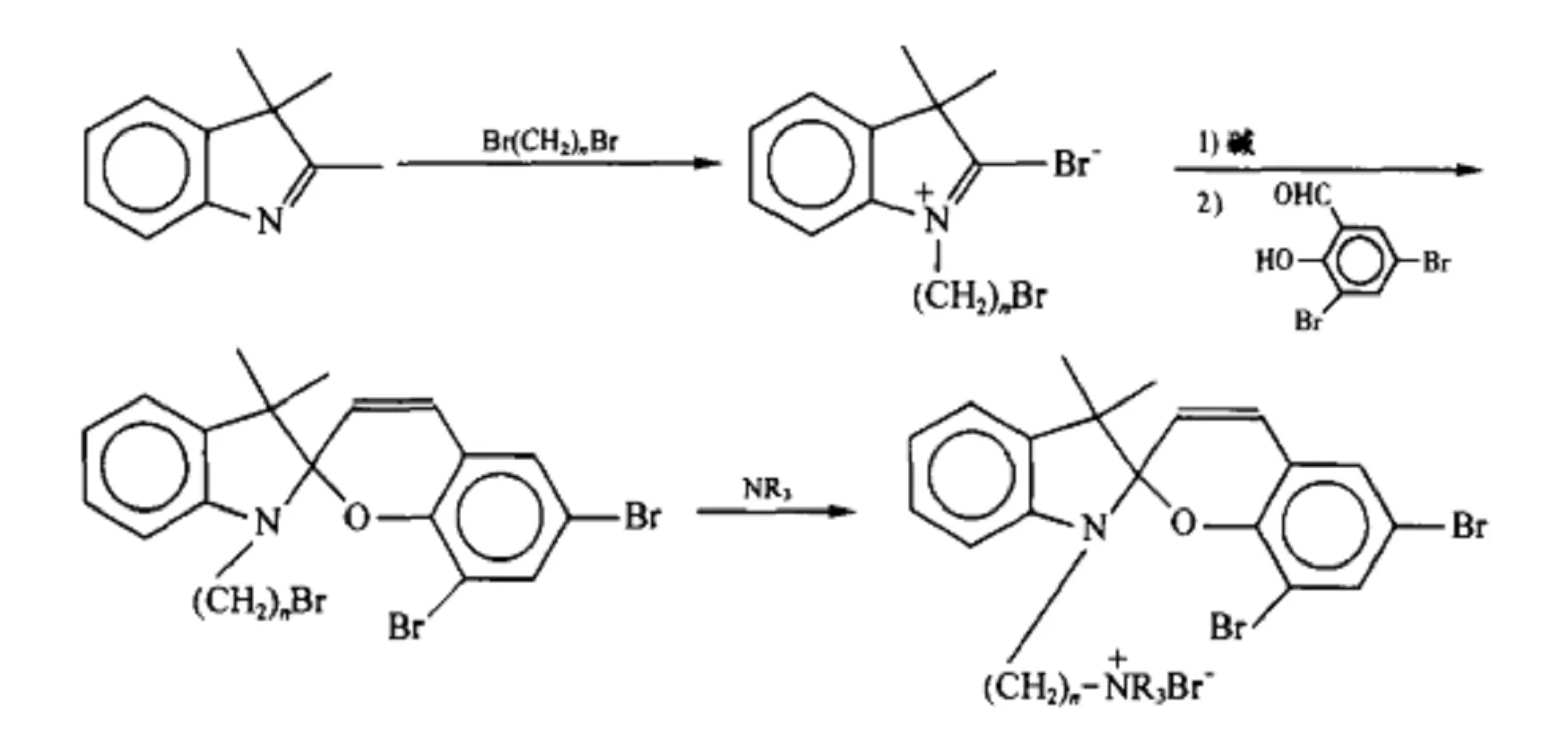
图3 螺环类光致变色中间体-吲哚啉盐中间体的合成
多米诺反应(domino reaction)是指在特定反应条件下,发生两个或两个以上键(通常为碳-碳键)形成的反应。该反应过程中,不需要额外添加试剂或催化剂,中间体也无需分离和提纯,与传统的多步合成方法相比,多米诺反应能够大大的提高反应效率和原子利用率。而严楠、熊云奎等人[8]于2014年,在低共熔溶剂氯化胆碱/草酸催化作用下,由醛、吲哚和6,10-二氧杂螺[4-5]十烷-7,9-二酮这三组分多米诺Knoevenagel-Michael反应合成了一系列新型螺环吲哚衍生物。该方法得到的产物产率较高,且条件温和,操作简单,反应时间短,对环境友好,是一种新型的值得推广的绿色合成方法。并且于2014年邹建峰和李新生[5]合成的新型衍生物中也含有吲哚型结构,但两者各有其优缺点。如图4。

图4 新型螺环吲哚衍生物的合成
同年四月魏文斌和赵祖建[9]又合成了一种新型含吲哚酮环的螺吡喃化合物,该化合物是以对取代苯胺为原料,将吡喃环引入吲哚-2-酮结构中,合成了新型化合物-5'-乙酰基-2'-氨基-1,2-二氢-6'-甲基-5-取代基-2-氧代螺[3H-吲哚-3,4'-(4H)吡喃]-3'-甲腈。该反应是水合氯醛和盐酸羟胺在硫酸钠饱和溶液中通过Sandmeyer反应制得N-(4-取代苯基)-2-肟基乙酰胺,然后制得的中间产物5-取代靛红是在浓硫酸作用下关环得到的,其再与活泼亚甲基化合物丙二腈通过克诺文格尔反应得2-(5-取代二氢吲哚-2-酮-3-亚基)丙二腈,最后与乙酰丙酮通过迈克尔加成反应合成了一系列新型的含吲哚酮环的螺环化合物。如图5。
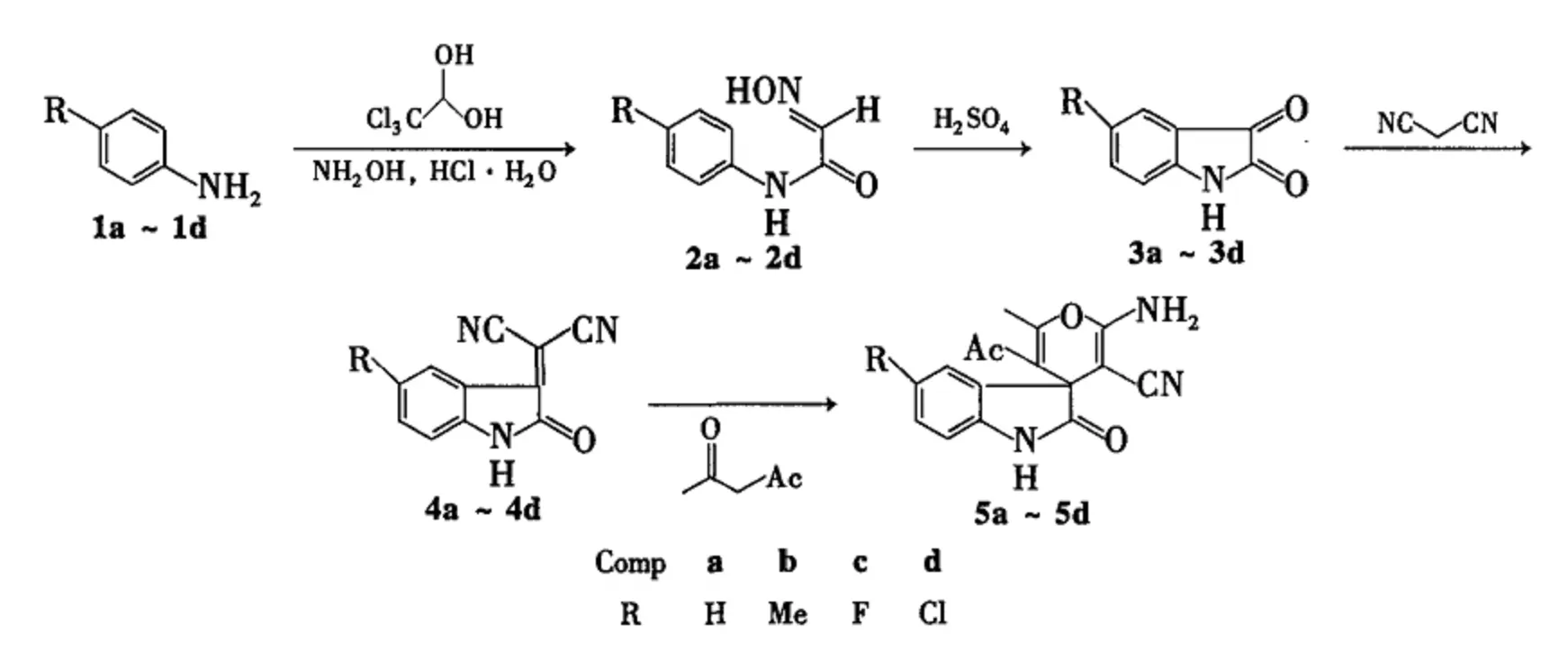
图5 含吲哚酮环的螺环化合物的合成
1.4 树状螺环化合物
树状化合物是一种新型的合成大分子材料,其特点结构是高度支化,精确的分子结构和大量的官能团,分子内存在空腔,并且分子链增长具有可控性。与线性结构的大分子化合物相比,具有良好的溶解性和较低的粘度,而且其分子尺寸通常在纳米尺度范围。可以作为多种材料使用,并在工业、农业、国防、医学等方面有重要应用前景。
一步合成法是近年来多采用的对环境友好的合成手段,利用一步法合成(一锅煮法)可以节省原料、降低了生产成本、减少了对环境的污染。例如2007年魏荣宝、李洪波和梁娅[10]三人就利用了一步合成法,以1,4-环己二醇、丙二酸二乙酯及多元醇等为原料,合成了六种二代螺环树型化合物1,2,3,4,5,6,7,8,9,10,11,12-十二氢-2,2;6,6;10,10-三[3,3-二(烷氧羰基)-1,1-环亚丁基二甲氧基]三亚苯基螺环树型化合物,其树形化合物合成是在异戊醇中完成,这样条件下产物易析出,使反应时间大大缩短。
同年9月梁娅、郭金晶、魏荣宝三人[11]又用“一锅煮法”合成了新型螺环树状化合物。
1.5 其他类型的螺环化合物
中国医药工业杂志于1993年报导的有关丁螺环酮合成中,徐燕、朱志宏等[12]利用在原来的试验方法的基础上,通过改造个别条件,如一次性加入水,在重结晶纯化时,增大异丙醇的浓度等这些条件,改进了各步反应条件和分离条件,使其合成更简单,条件更易控制,并且收率稳定。并且于2002年Li Wei等[13]、2006年施志坚、倪华文等[14]和Zeng Wulan、Meng Qinguo等[15]都是通过对已有的反应的条件进行改进,设计出了更简单有效的合成方法。如前者通过对Petersen和Testa的合成方法进行改进,在他们的基础上,Li Lei等使用亲核的Lawesson试剂攻击第一步中硫代磷酸给的氨基和将随后的P-SH加成到腈上,然后通过重排得到最终产品,即合成了新的2-(4'-甲氧基苯基)-2,4-杂-1,3,2-二氧磷啶-5,1'-螺环环己烷。此反应的优点是制备方便,适中的产率。
2009年王晓科、何锡敏等人[16]设计并合成出类似香豆素的螺环内酯化合物9,11-二甲基-2-氧杂环[5,5]-十一烷-3-酮,其是一种新型化合物。在该合成中,以艾薇醛2和吡咯烷3为原料,经缩合后得到烯胺化合物4,4与丙烯酸甲酯发生Machiel反应得到化合物5,再经选择性氢化醛成为醇化合物6,6在硫酸的催化下环合得到目标产物螺环内酯1。反应如图6。
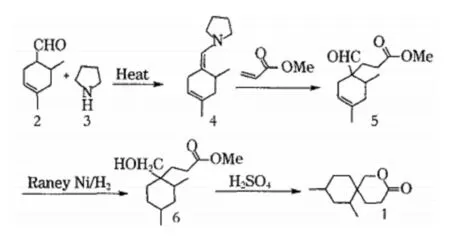
图6 螺环内酯化合物的合成
2 结束语
我们生活中的各方各面螺环化合物都得到了应用,既是可以作为生活中工具的材料,也可以作为各种药物的原料,并生产各种于我们身体有益的药物。虽然目前用于合成螺环化合物的方法已经有很多,但大多数合成方法都过于繁杂,并且产率较低。所以我们要不懈努力设计出更多方便有效,并且产率较高的合成方法为我们所用,并希望以后的合成技术能得到突破性的进展。
[1]洪 卉,黄龙江,滕大为.吲哚啉螺环化合物的生物活性及合成研究进展[J].化学试剂,2010,32(6):518-522.
[2]何晓强,解 海.阻燃剂中间体氯化螺环磷酸酯的合成改进[J].科技与开发,2007(6):16-23.
[3]马志领,赵文革,张荣珍.阻燃剂氯化螺环磷酸酯的合成及应用[J].化学世界,1996(6):309-312.
[4]冯亚青,张晓东,张卫红,等.1,3-偶极环加成反应在咋螺环化合物合成中的应用[J].应用化学,1997(14):5-9.
[5]邹建峰,李新生.不对称合成新型的吲哚螺-2,3-二氢呋喃衍生物[J].浙江大学学报(自然科学版),2014,37(2):84-92.
[6]Angew Chem.不对称Michael加成/环化反应:活性分子核心骨架启迪的多手性中心螺环氧化吲哚的合成[J].有机化学,2011(12):2189.
[7]刘振东,崔 明,李小明,等.螺环类光致变色中间体的合成[J].北京服装学院学报,2004,24(2):46-51.
[8]严 楠,熊云奎,夏剑辉,等.低共熔溶剂中新型螺环吲哚衍生物的绿色合成[J].有机化学,2015,35(2):384-389.
[9]魏文斌,赵祖建.新型含吲哚酮环的螺吡喃化合物的合成[J].合成化学,2014,22(4):513-515.
[10]魏荣宝,李洪波,梁 娅.二代螺环树形化合物1,2,3,4,5,6,7,8,9,10,11,12-十二氢-2,2;6,6;10,10-[3,3-二(烷氧羰基)-1,1-环亚丁基二甲氧基]三亚苯基的合成[J].化学学报,2007(19):2151-2154.
[11]梁 娅,郭金晶,魏荣宝.新型螺环树状化合物的合成[J].高等学校化学学报,2007(9):1681-1684.
[12]徐 燕,朱志宏,童志杰,等.丁螺环酮的合成[J].中国医药工业杂志,1993,24(2):49-51.
[13]Deng Shenglou,Liu Dongzhi,Li Wei.New synthesis and molecular structure of 2-(4'-methoxyphenyl)-2,4-dithia-1,3,2-diazaphospholidine-5,1'-spirocyclohexane[J].结构化学,2002,21(4):359-363.
[14]Shi Zhijian,Ni Huawen,Cao Weiguo,et al.Synthesis and structure elucidation of new spiro compounds with per(poly)fluoroalkyl group[J].Chinese Journal of Chemistry,2006,24:980-982.
[15]Zeng Wulan,Meng Qinguo,Guo Huanmei,et al.Synthesis and crystal structure of two novel spiro compounds containing 1,5-dioxaspiro[5.5]undecane-2,4-dione[J].结构化学,2010(5):696-699.
[16]王晓科,何锡敏,欧文华,等.新型螺环内脂的合成研究[J].上海应用技术学院学报(自然科学版),2009(12):271-274.

