南烛叶总黄酮微乳凝胶的制备
王章姐,刘自平,许 燕,王 娟
(安徽新华学院 药学院,安徽 合肥 230088)
南烛(Vaccinium bracteatum Thunb)又名乌饭树,是杜鹃花科越橘属植物,南烛叶是乌饭树的叶子,南烛叶中含有含卅一烷、无羁萜、表无羁萜醇、槲皮素、异荭草素、对-羟基桂皮酸、等多种化学成分,据《本草新编》记载,南烛叶具有益精气,强筋骨,明目,止泄之功效.鲁植雄等[1]研究发现南烛叶中总黄酮类总含量约11.64%,其中槲皮素含量达3.52%,可以用于抗衰老、抗氧化、美白、补水化妆品的原料,具有巨大的应用前景.微乳(micro emulsion,ME)水、油、乳化剂、助乳化剂按恰当的比例混匀形成的均一、澄清、热力学稳定的乳液[2-4],作为载药体应无毒、无刺激、对人体无损害,且有良好的生物相容性等.研究表明[5],微乳具有增加药物溶解度、促进吸收、提高药物稳定性、延长药物作用时间、维持恒定血药浓度等特点.凝胶具有较好的生物粘附性,将载药微乳与凝胶基质结合,制备成新剂型微乳凝胶[6],可增加药物的生物利用度及药物的稳定性,延长药物的作用时间,进一步使血药浓度更加稳定,同时克服微乳因长久水分的流失表面活性剂浓度增高,刺激性强等缺点,满足缓控释方便给药的要求[7].微乳凝胶(micro emulsion-based gels,MEGS)是将微乳与凝胶基质结合,形成透明、均一、稳定的体系[8].有着较好的生物相容性及稳定性,易清洗不污染衣物,可作为易挥发、难溶于水药物的新载体.本研究将南烛叶总黄酮制成微乳凝胶,为更好制备临床新剂型奠定基础.
1 材料与方法
1.1 材料与试剂
南竹叶总黄酮(实验室自提);芦丁对照品(中国药品生物制品检定所,批号100080-201418);聚山梨酯80(天津市光复精细化工研究所);油酸乙酯(上海源叶生物科技有限公司);聚乙二醇400(PEG 400,上海源叶生物科技有限公司);丙三醇(天津市百世化工有限公司);卡波姆940、三乙醇胺(国药集团制药有限公司).大豆油为超市购买;乙醇等其余试剂均为分析纯.
1.2 仪器
DF-101S型智能集热式恒温加热磁力搅拌器(河南省予华仪器有限公司);SHZ-D(Ⅲ)型循环水式真空泵(巩义市予华仪器有限责任公司);Autoscience AS3120超声波清洗机(奥特赛恩斯仪器有限公司);UV-2550紫外-可见分光光度仪(日本岛津公司);BT125D电子分析天平(赛多利斯科学仪器(北京)有限公司):DZF1.0型真空干燥箱(上海长源仪器设备厂);CP2115D电子天平(Satorius公司);DF-101Z型热式加热搅拌器(常州普仪器制备有限公司).
1.3 方法
1.3.1 南竹叶总黄酮溶解度的测定 取3支西林瓶,洗净干燥,备用,分别称取约2g不同油相、乳化剂和助乳化剂置于瓶中,加入过量的南烛叶总黄酮,搅拌后超声30min,以促进各相溶解,在37℃水浴中平衡48h,4000r/min离心25min,用0.45μm的微孔滤膜滤过上清液,取续滤液用甲醇稀释至适宜倍数,作为供试品溶液.分别精密吸取供试品20 μL,以上述HPLC法测定,记录峰面积,计算相应成分在不同介质中的溶解度.
1.3.2 南竹叶总黄酮微乳凝胶的制备 取南烛叶总黄酮、乳化剂、助乳化剂,精密称定,依次加入带塞锥形瓶中,于37℃水浴中溶解,混匀.再精密称定油相,加入上述锥形瓶中,混匀,在恒温磁力搅拌器下在该混合物中滴加蒸馏水,并不停搅拌使其乳化,得到南烛叶总黄酮微乳.再加入卡波姆-940,放置过夜使其自然膨胀,继续加入丙三醇,滴加三乙醇胺溶液调节pH值,得南烛叶总黄酮微乳凝胶.
1.3.3 南烛叶总黄酮微乳饱和载药量的测定 取制备好的空白微乳,加入过量的南烛叶总黄酮,于60℃水浴中搅拌,以促进南烛叶总黄酮的溶解,再在37℃水浴中平衡48h,4000r/min离心25min,用0.45μm的微孔滤膜滤过上清液,取续滤液用甲醇稀释至适宜倍数,采用HPLC测定南烛叶总黄酮含量,计算饱和载药量.
1.3.4 伪三元相图初步筛选 将已确定的乳化剂与助乳化剂按不同质量比Km值 (3∶1、2∶1、1∶1、1∶2、1∶3) 混匀后,再与油相按 1∶9、2∶8、3∶7、4∶6、5∶5、6∶4、7∶3、8∶2、9∶1 的比例混合,滴加水相中至形成澄清透明溶液或带有蓝色乳光溶液,采用origin 9.0程序绘制伪三元相图,以相图中微乳存在区域的大小来筛选助乳化剂和乳化剂.
1.3.5 正交试验设计优化处方 以卡波姆940含量(因素a)、丙三醇含量(因素b)和pH值(因素c)为考察因素,以涂抹性、油腻性、粘稠度与外观性状为评价指标,见表1、2,每个指标各占2.5分,分析综合评分.

表1 各指标评分标准
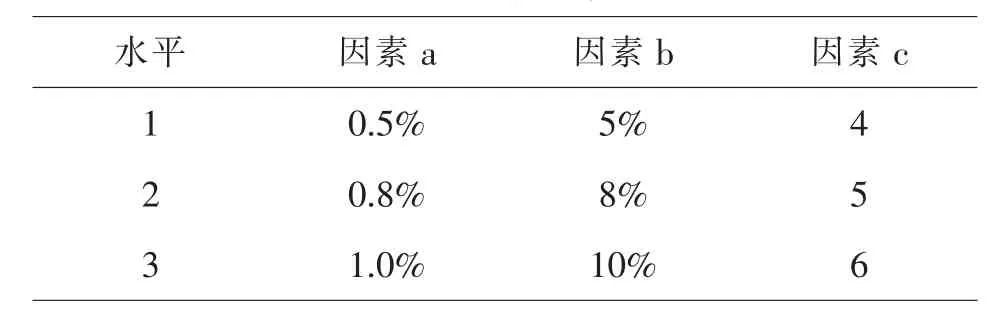
表2 因素水平表
2 结果与分析
2.1 南竹叶总黄酮在不同介质中溶解度的测定
由表2可知南竹叶总黄酮在不同油相中油酸乙酯中的溶解度明显大于大豆油,故选择油相为油酸乙酯.不同乳化剂中南竹叶总黄酮在聚山梨酯80的溶解度最大,在不同助乳化剂中的溶解度PEG 400明显大于丙三醇,故乳化剂初步确定为聚山梨酯80,助乳化剂初步确定为PEG 400.

表3 南竹叶总黄酮在不同介质中的溶解度
2.2 伪三元相图初步筛选处方
对已确定的微乳各相组分,乳化剂、助乳化剂按质量比(Km)1:3、1:2、1:1、2:1、3:1;上述比例混合均匀在与油相油酸乙酯按质量比9:1、8:2、7:3、6:4、5:5、4:6、3:7、2:8、1:9 混匀,固定乳化剂、助乳化剂和油相的总质量为1.0g.在37℃水浴磁力搅拌器下逐滴加水至澄清透明溶液或带有少许蓝色乳光的溶液的临界点各项比例,以聚山梨酯80、PEG400混合乳化剂为1个顶点,水相和油相为剩下2个顶点,用Origi8.0软件绘制伪三元相图进一步确定体系中微乳形成的区域,如图1筛选出空白微乳处方.由伪三元相图结果可知,当质量比Km值大于2:1时,随着Km值的增大微乳区缩小,Km小于2时随着Km的增大微乳区增大,Km等于2时,微乳区域最大,故选择聚山梨酯80与PEG400的质量比Km值为2.

图1 不同Km值的伪三元相图
2.3 正交试验设计优化凝胶处方
采用L9(34)因素水平表进行正交设计实验,以空白凝胶基质涂抹性、油腻性、粘稠度与外观性状为参考指标,见表.每个指标各占2.5分,分析综合评分,筛选空白凝胶的最佳处方.
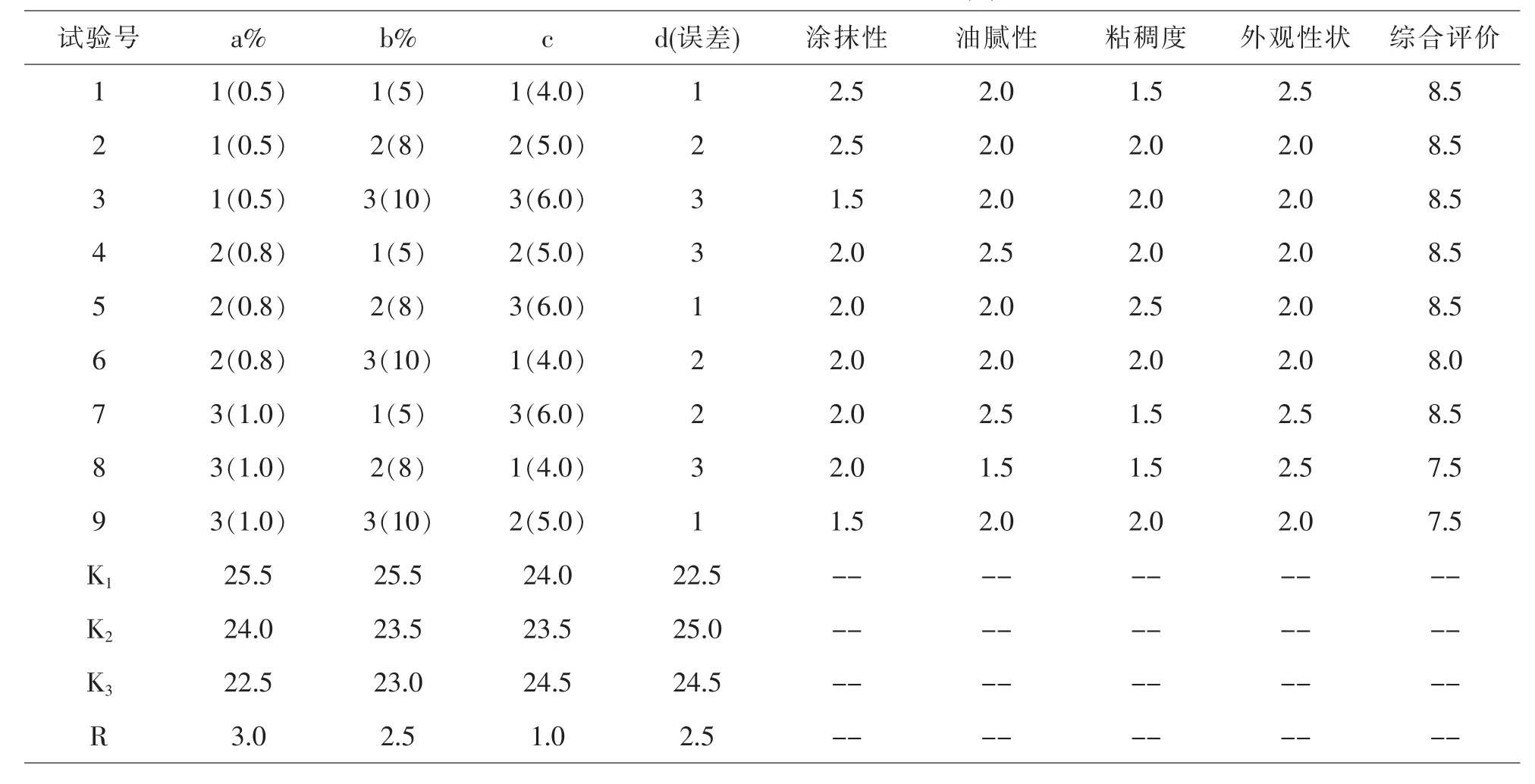
表4 凝胶处方筛选正交设计表L9(34)

表5 凝胶处方筛选方差分析
根据表4、表5,确定空白凝胶基质的最佳处方为卡波姆940用量0.5%,丙三醇用量5%,三乙醇胺溶液调节pH至6.0.
3 结语
在微乳处方筛选中,通过测定南竹叶总黄酮溶解度,可以看出在油酸乙酯中南烛叶总黄酮溶解度仍然最大;南烛叶在不同乳化剂中聚山梨酯80的溶解度较好;而在助乳化剂PEG 400中溶解度最大.
通过伪三元相图考察乳化剂、助表乳化剂在不同比例下对形成微乳区域大小影响,通过实验结果,在一定的范围内,乳化剂的用量增加,所形成的微乳区域也越大,但超出一定范围时乳化剂用量增加,微乳区域反而减小.本研究通过考察药物溶解度的大小并结合伪三元相图对微乳处方进行筛选和优化,最终确定最佳的微乳最佳处方.
本实验通过正交试验设计筛选空白凝胶基质,得到最优处方:卡波姆940用量为0.5%,丙三醇用量为5%,三乙醇胺溶液调节pH至6.0.
〔1〕鲁植雄,江水泉.超临界CO2萃取南烛叶有效成分的色谱分析 [J].南京农业大学学报,1998,22(1):101-103.
〔2〕Sable V Vera S.Formulation and evaluation of micro emulsion-based hydrogen for topical delivery[J].Int J PharmInvest,2012,2(3):140-149.
〔3〕党翔吉,魏立明,韩珊珊,等.复方栀子凝胶的处方工艺研究[J].中草药,2013,44(22):2982-2987.
〔4〕祝雨薇,蒋曙光,周建平.尹曲康唑温敏乳凝胶的研制[J].中国新药杂志,2013,22(16):1942-1947.
〔5〕姚娜,黄庆德.中药微乳凝胶剂的研究进展[J].浙江中医药大学学报,2013,37(2):217-219.
〔6〕Xian Sha,Xiao Wang.Transdermalmicro emulsion drug deliversystem forimpairing male reproductive toxicity and enhancing efficacy of Tripterygium Welford Hook [J].Fitoterapia,2012,83(4):690-698.
〔7〕谢明华.利多卡因微乳凝胶外用制剂的制备及药效学评价[J].中国现代应用药学,2015,4(6):68-70.
〔8〕赵振宇,孙浩.微乳凝胶新制剂的研究进展[J].中国医药学杂志,2014,34(5):411-413.

