内镜黏膜下挖除术治疗胃血管球瘤11例分析
黄勤 张玉 季新荣 彭金榜 郑海红 沈玲燕 叶丽萍
血管球瘤是一种由类似正常血管球变异平滑肌细胞所组成的间叶性肿瘤,多发于软组织及四肢末端,通常表现为良性肿瘤,极少数为恶性,发生在胃的血管球瘤非常罕见。肿瘤由血管球细胞、血管、平滑肌以不同比例混杂构成,具有器官样结构。目前,外科手术是治疗这类病变的主要方法,但外科手术创伤大,有一定的侵入性,并且可引起一些相关并发症。对于无症状且<3cm的血管球瘤患者,采用外科手术治疗值得进一步商榷。内镜黏膜下剥离术(endoscopic submucosal dissection,ESD)最初是用来治疗浅表性胃癌(早期胃癌)的一种内镜微创治疗方法。目前,ESD越来越多地被用来治疗胃固有肌层肿瘤。然而,ESD很少用来治疗胃血管球瘤。本文旨在评估内镜黏膜下挖除术(endoscopic submucosal excavation,ESE)治疗胃血管球瘤的有效性和安全性,现报道如下。
1 资料和方法
1.1 一般资料 2011年1月至2015年12月在本院接受ESE治疗的胃血管球瘤患者11例,其中男6例,女5例,年龄34~67岁,中位年龄47岁。纳入标准:肿瘤起源于胃内黏膜下层或固有肌层,病变≤3.5cm;无高危险超声征象(肿瘤表面破溃,回声不均匀,强回声、病变>4cm;术前血常规、凝血常规、肝肾功能、心肺功能检查等无明显异常,术前1周内未服用阿司匹林、华法林及氯吡格雷等抗凝药物。本研究经医院伦理委员会批准,所有患者均签署知情同意书。
1.2 方法
1.2.1 内镜设备及相关附件 手术均采用单通道胃镜(Q-260J,日本奥林巴斯公司)和(或)双通道内镜(GIF-2T240,日本奥林巴斯公司),透明帽(ND-201-11802,日本奥林巴斯公司)安装在内镜头端。其他附件有:透明帽(ND-201-11802,日本奥林巴斯公司),高频电切装置(ICC-200,德国爱尔博公司),注射针(NM-4L-1,日本奥林巴斯公司),hook刀(KD-620LR,日本奥林巴斯公司),圈套器(SD-230U-20,日本奥林巴斯公司),热活检钳(FD-410LR,日本奥林巴斯公司),止血钳(HX-600-135,日本奥林巴斯公司),氩等离子凝固装置,CO2气泵(日本奥林巴斯公司)。0.02%靛胭脂溶液现配用(100ml 0.9%氯化钠溶液+2ml靛胭脂+1ml肾上腺素)。
1.2.2 ESE手术 内镜术前需考虑术中中转开腹的可能,因此所有患者均在气管插管全身麻醉下完成手术治疗。具体手术步骤(图1)如下:(1)标记:应用氩离子凝固术(APC)于病变边缘行电凝标记;(2)黏膜下注射:多点黏膜下注射0.02%靛胭脂溶液(100 ml0.9%氯化钠溶液+2ml靛胭脂+1ml肾上腺素),使病变充分隆起;(3)切开:采用改良针状钩刀沿标记点切开病变外缘黏膜或十字切开病变;(4)分离:IT刀逐步分离切开的黏膜,分离过程中多次黏膜下注射,保持病灶始终隆起,完整切除病变;(5)创面处理:及时处理手术创面。应用APC或热活检钳电凝,必要时应用尼龙绳及止血钛夹闭合或缩小创面。有穿孔的病灶,尽量内镜下止血钛夹夹闭,必要时中转开腹。

图1 1例胃窦血管球瘤E S E过程(a:胃窦后壁见一直径约2.3c m×2.0 c m大小不规则扁平隆起、定标;b:超声内镜提示肿瘤累及黏膜下层;c:多点黏膜下注射充分抬举病变,钩刀行病变中央部“十”字切开;d:I T刀行黏膜下充分剥离病变;e:剥离后多枚钛夹联合尼龙绳封闭创面;f:切除标本(直径2.3c m×2.0 c m)
1.2.3 术后管理 术后常规放置胃管,禁食2~3d,埃索美拉唑注射液(瑞典阿斯利康公司)40mg,静脉注射5~7d,2次/d,随后改口服埃索美拉唑片8周,2次/d。观察有无消化道出血、穿孔症状,流质或无渣饮食5d,2周内避免粗纤维食物,避免剧烈体育活动及体力劳动。
1.2.4 病理评估 内镜下切除的标本经固定切片后,按标准HE染色行常规病理观察,并行免疫组化检查。病理诊断标准:肿瘤组织主要位于胃壁固有肌层中,光镜下见结节外被平滑肌组织,结节内血管丰富、扩张呈裂隙状,血管周围呈灶状不对称排列肿瘤细胞,形态较一致,细胞边界清楚,为圆形、椭圆形或梭形。
1.2.5 随访 术后3、6、12个月常规复查胃镜,观察创面愈合情况,随访病变有无残留或复发。以后每年行内镜检查1次。
2 结果
2.1 术前诊断 11例患者在术前均完善超声内镜及增强CT检查,超声内镜提示病变来源于固有肌层7例,黏膜下层4例,以低回声为主,2例为混合回声结构,中央部分钙化。增强CT检查均表现为软组织密度,边界清楚,密度较均匀,2例见部分钙化。10例病变增强CT扫描早期明显强化,延迟扫描持续强化,1例病变早期强化不明显。结合内镜、超声内镜及增强CT检查,术前考虑血管球瘤5例(45.5%),间质瘤3例(27.3%),异位胰腺1例(9.1%),神经内分泌肿瘤1例(9.1%),神经鞘瘤1例(9.1%)。
2.2 ESE治疗情况 病灶位于胃窦部7例,胃体部3例,胃底1例,术后病理及免疫组化证实均为血管球瘤。肿瘤直径12mm×15mm~28mm×35mm,平均18mm×26mm。
2.3 病理结果 术后病理结果(图2)示:内镜下切除的肿瘤组织主要位于胃壁固有肌层中,光镜下见结节外被平滑肌组织,结节内血管丰富。肿瘤细胞SMA均(+),10例vimentin (+),而 CD31、CD34、S-100、Dog-1、Desmin、CD117均为阴性。
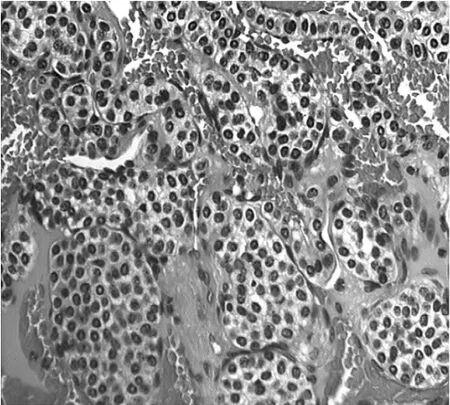
图2 患者的病理检查图片(镜下见瘤细胞增生,细胞圆形大小较一致,未见核分裂像,围绕血管生长或片状分布。H E染色,×200)
2.4 并发症 ESE完整切除病灶10例,1例病灶与肌层粘连,内镜下剥离困难,故中转腹腔镜手术。术中全层切除1例,采用尼龙绳联合止血钛夹荷包缝合,全层切除过程中伴有穿孔,表现为气腹,予以20号注射针头放气处理,术后禁食、放置胃肠减压、给予抗生素和埃索美拉唑针治疗好转,无需外科干预。治疗过程中所有病例均有少量出血,均予以热活检钳止血、APC凝固止血及钛夹成功止血,术中术后无大出血发生。
2.5 随访结果 随访3~27个月,平均18个月,未见肿瘤残留或复发,也无其他明显不适症状。
3 讨论
胃血管球瘤的病因及发病机制尚不明确,因其由血管球细胞构成,且含有正常血管球成分,部分学者认为是因血管球细胞异常增生所致。但同时免疫组化及电镜研究显示,血管球瘤细胞起源于平滑肌细胞。故也有学者认为,血管球瘤为平滑肌与血管内皮细胞间的一种过渡细胞,兼有两种细胞的特征。原发于胃的血管球瘤极为少见,发病率较低,在胃所有肿瘤中约占2.2%[1],大多数好发于胃窦,本组63.6%发生于胃窦,与文献报道相符。
胃血管球瘤临床表现不一,大部分为偶然发现,较大的肿瘤可因为消化道出血、腹部隐痛、返酸、嗳气等上消化道症状而就诊。胃血管球瘤大体表现为黏膜下肿瘤,呈结节样隆起,表面较光滑,多无包膜,但界限清楚。部分病例表面出现溃疡或浅糜烂,内镜下难以与间质瘤区分。胃血管球瘤含有丰富的血管,在平扫密度较均匀,偶尔可见钙化,在增强扫描时动脉期明显强化,延迟扫描持续强化,但强化程度降低[2]。因此内镜及CT检查对于诊断血管球瘤仍具有一定的局限性。超声内镜对于应用ESD治疗消化道隆起性病变有一定的应用价值[3]。本研究中11例病例在术前超声内镜检查提示,病变来源于固有肌层7例,黏膜下层4例,以低回声为主,部分为混合回声结构。结合内镜、超声内镜及增强CT检查,术前考虑血管球瘤5例,间质瘤3例,异位胰腺1例,神经内分泌肿瘤1例,神经鞘瘤1例,术后病理及免疫组化证实为血管球瘤,术前诊断正确率仅45.5%。较低的术前诊断率与胃血管球瘤发病率低,临床及放射医师对其诊断经验不足,部分病例缺乏特征性表现相关。有研究认为超声内镜及联合CT检查可更好地鉴别胃血管球瘤与胃间质瘤[4],但是术后病理检查及免疫组化分析仍是目前诊断胃血管球瘤的金标准[5],并可以进行肿瘤良恶性的鉴定。
在本研究之前,本院消化内科已完成了至少300例ESD术治疗上消化道黏膜下肿瘤的病例。基于前期ESD成功治疗的经验,我们采用ESE术治疗胃血管球瘤。穿孔是ESE治疗胃血管球瘤的一个主要并发症。术中全层切除1例,切除过程中伴有穿孔,表现为气腹,予20号注射针头放气处理,采用尼龙绳联合止血钛夹荷包缝合创面。术后禁食、放置胃肠减压、给予抗生素和埃索美拉唑针治疗好转。笔者处理穿孔的经验有以下几点:(1)术中使用CO2充气泵,可明显降低气胸、皮下气肿和气腹的风险;(2)严密观察气道压力,腹部触诊可以了解腹腔压力。可采用20号注射针头在胸腔或腹腔的高点穿刺放气。(3)需要有效的内科治疗,如术后胃肠减压,应用抗生素和埃索美拉唑。本组术中、术后无大出血发生,但治疗过程中所有病例均有少量出血,均予以热活检钳止血、APC凝固止血及钛夹成功止血。术中术后穿孔、出血的发生与肿瘤的部位、大小、浸润深度、手术时间、操作者的熟练程度等有关。术中始终保持视野的清晰,应用止血钛夹往往能夹闭创面,一般能避免外科手术。
本病的确诊有赖于组织病理及免疫组化分析。胃血管球瘤细胞呈圆形或椭圆形,被周围的平滑肌细胞或纤维组织分隔包围,大小一致。免疫组化显示,11例肿瘤细胞 SMA均(+),10例 vimentin(+),平滑肌标记呈阳性,不表达神经内分泌标记物,如CD31、CD34、S-100、Dog-1、Desmin、CD117 均为阴性,因此,可与胃肠道间质瘤、类癌、血管外皮细胞瘤、恶性淋巴瘤进一步鉴别。
血管球瘤绝大多数为良性,恶性血管球瘤十分少见,这也为血管球瘤内镜下完整切除提供理论依据。Kang等[6]报道过良性血管球瘤恶性变的病例。对于恶性血管球瘤的诊断国内外尚无统一标准,目前建议的诊断标准为[7]:(1)肿瘤位于深部或内脏且直径>2cm;(2)核中度或高度异型伴核分裂,>5个/50HPF;(3)出现病理性(非典型性)核分裂,表现有其他血管侵袭。上述第一条标准在胃恶性血管球瘤诊断的适用性尚存异议。Miettinen等[8]认为,直径>5cm才能作为胃血管球瘤的恶性指征。本组11例中直径>2cm有7例,核分裂像未见,术后随访10例均未出现复发、转移,1例患者移居外地未随访。对于有潜在恶性的血管球瘤,应尽早手术治疗,并且术后可辅助放疗或化疗,长期密切随访。
本研究为单中心研究,存在病例的选择性偏倚;其次,术者在内镜治疗技术方面的经验也决定ESD手术的成败,本研究所有手术均由1位有经验的内镜专家完成;且本研究样本数量有限,缺少随机对照组,随访期也相对较短。因此,有待以后进行随机对照多中心临床研究进一步评估这项技术的有效性和安全性。
[1]Kang G,Park HJ,Kim JY,et al.Glomus tumor of the stomach:a clinicopathologic analysis of 10 cases and review of the literature[J].Gut and Liver,2012,6(1):52-57.
[2]许小伍,林勇军,袁帅.胃血管球瘤CT诊断[J].安徽职业技术学院学报,2012,11(1):42-43.
[3]叶淑芳,朱晚林,叶秀津,等.超声内镜辅助下ESD治疗上消化道隆起性病变的疗效及安全性探讨[J].浙江医学,2013,35(11):1041-1044.
[4]Baek YH,ChoiSR,Lee BE,et al.Gastric glomus tumor:analysis of endosonographic characteristics and computed tomographic findings[J].Dig Endosc,2013,25(1):80-83.
[5]Vassiliou I,Tympa A,Theodosopoulos T,et al.Gastric glomus tumor:a case report[J].World J Surg Oncol,2010,8:19.
[6]Kang G,Park HJ,Kim JY.Glomus tumor of the stomach:a clinicopathologic analysis of 10 cases and review of the literature[J].Gut Liver,2012,6(1):52-57.
[7]Baek YH,Choi SR,Lee BE,et al.Gastric glomus tumor analysis of endosonographic characteristics and computed tomographic findings[J].Digestive Endoscopy,2012,24:1-3.
[8]Miettinen M,PaalE,Lasota J,etal.Gastrointestinalglomus tumors:a clinicopathologic,immunohistochemical,and molecular genetic study of 32 cases[J].Am J Surg Pathol,2002,26(3):301-311.

