一种促进神经损伤修复的药物组合物治疗22例ALS 患者1年后的疗效观察
岳茂兴 周培根 郝冬琳 李瑛 尹进南 郑琦涵 杨学峰 梅冰 孙志辉 马临庆 徐冰心 吴静 吴娟 郁婷婷 钱亿超 朱晓瓞 冯斌 徐君晨 关竹颖 岳慧 魏艳红
肌萎缩侧索硬化症(amyotrophic lateral sclerosis,ALS)是运动神经元病(motor neuron disease,MND)的一个类型,患者因大脑、脑干和脊髓中运动神经元受到侵袭、损伤[1-3],而出现进行性肌肉萎缩和无力,以致瘫痪[4],身体如同被逐渐冻住一样,故俗称“渐冻人”。到目前为止,国际医学领域暂无特效治疗方法[5]。患者症状出现后的平均寿命通常为3~5年[1,6-9]。在全球,每90 min就有1名“渐冻人”患者的生命被夺走,该疾病也被世界卫生组织列为五大绝症之一。
岳茂兴教授总结40余年来多次参加突发事故伤员紧急救治经验,和在载人航天医疗保障中针对宇航员在太空失重状态下可能发生的健康问题,如肌肉萎缩(肌肉的质量和体积减少,抗重力肌和慢肌萎缩更明显)、骨密度降低(骨质脱钙,承重骨尤为明显)、细胞免疫功能下降等,所进行的预防、治疗与研究工作体会,同时结合数十载的临床工作经验、实验研究成果,并广泛参考国内外有关资料,于2008年发明了此组合物创新疗法用以救治疑难危重症患者,挽救了一批危重病患者的生命。该疗法从2009年7月7日开始推广应用至外院,成功救治了1例在短时间内连续3次手术止血失败的严重创伤凝血病濒死患者。2010年12月22日,在1例急性脊髓炎合并阑尾炎并发T7以下完全瘫痪患者的救治中,此组合物创新疗法发挥了重要作用:患者在连续应用8.5个月后又重新站了起来,行走和功能能力也得到恢复,出院检查与长期随访并未发现患者有明显的不良反应,经磁共振成像(magnetic resonance imaging,MRI)检查证实,此组合物创新疗法的应用使得患者原本损伤的脊髓得到修复。从这一神经损伤患者的救治中获得启发后,又治疗了一些严重脑神经损伤患者,也获得比较好的效果:如应用此疗法救治了5例交通事故致严重多发伤(特重型颅脑外伤)长期深昏迷患者。其中1例在昏迷8个月后清醒,行走及部分工作能力恢复;1例患者在治疗5个月后恢复知觉和意识,能够自己站立与进食等;1例患者在治疗6个月后恢复了知觉和意识,能识人;另有2例患者在治疗9个月和11个月后逐步恢复了部分知觉和意识。临床实践证实,此组合物创新疗法确实能够使得损伤的脑和脊髓功能得到一定程度的修复。
2012年,“一种促进神经损伤修复的药物组合物及其制备方法”获得了发明专利(ZL2012 1 0272724·2),并于2015年4月28日应用于第1例重度晚期ALS患者的治疗。患者杨某在上海某医院被确诊为ALS,在外院经营养神经、口服“利鲁唑”等治疗后其症状仍进行性加重,近8个月来体重下降20.5 kg,每天需无创呼吸机持续辅助呼吸。予本组合物创新疗法治疗15 d后,口干、肉跳感、双手麻木、全身肌肉萎缩、乏力、饮水呛咳、气喘等症状明显好转,双上肢近端肌力、双下肢肌力明显增加,体重增加3.5 kg,呼吸功能明显改善,可以自由行走、浇花等,测定免疫功能(淋巴细胞亚群)明显好转。对该首例ALS患者的治疗取得了较好疗效后,团队开始逐步将本药物组合物推广应用至更多的MND(包括ALS)患者,经过医院伦理委员会研究与讨论,全体委员一致全票通过本药物组合物创新疗法的实施方案。2016年8月22日,中-瑞运动神经元病国际合作研究中心在江苏省常州市成立,当日还进行了中国-瑞典运动神经元病国际专题研讨会。2017年4月7日在常州召开了运动神经元病国际新疗法标准化治疗启动会,经过地方政府卫生和计划生育局批准,全国首个运动神经元病临床治疗中心在江苏大学附属武进医院成立。至2018年9月,已经诊治了803例MND患者,其中ALS患者184例。现在将一种用于治疗运动神经元病的药物组合物治疗22例ALS 患者1年后疗效观察报告如下。
临床资料与方法
一、一般资料
以江苏大学附属武进医院及苏州高新区人民医院2015年4月至2017年9月收治的22例ALS患者为研究对象进行前瞻性自身对照研究,其中男性10例,女性12例;年龄34~68 岁,平均年龄(51.64±9.28)岁。纳入标准:(1)经外院三级甲等医院明确诊断为确诊或拟诊ALS。(2)有完整的既往就诊资料。(3)年龄18~70岁。(4)自愿签署知情同意书。排除标准:(1)怀疑或确诊肌营养不良、重症肌无力、脊髓灰质炎后综合征、多灶性运动神经病、平山病、肯尼迪病、遗传性痉挛性截瘫、脊髓空洞症或副肿瘤综合征者。(2)脊髓及脑干肿瘤、恶性肿瘤、重症感染、严重外伤患者。(3)有严重肝脏、肾脏疾病。(4)严重腹泻或者呕吐的患者。(5)妊娠期或哺乳期妇女。(6)连续治疗时间<4个疗程或6个月(包含疗程间的休息期)。(7)任何研究者认为不适合参与研究的情况。本研究获江苏大学附属武进医院医学伦理委员会审核通过,所有患者均已签署知情同意书。
ALS患者确诊医院分布:北京协和医院4例,上海华山医院9例,北京大学第三医院3例,中国人民解放军总医院2例,其他医院4例。患者首次门诊时的病程为8~153个月,其中病程时间<12个月2例(9.09%),12~24个月9例(40.91%),>24个月11例(50.00%)。
二、方法
(一)常规对症支持治疗
纳入的患者在治疗期间均需注意呼吸、消化系统的功能。若流涎增加,可给予少量抗阻胺药;若咳痰(或痰难以咳出),可给予雾化吸入及化痰药;出现急、慢性缺氧表现(症状、体征或肺功能、动脉血气分析等辅助检查结果异常)时,尽早采用机械通气辅助呼吸;如出现焦虑、抑郁或情绪低落,给予心理调整或抗抑郁治疗等。此外,还要多翻身以防止压疮发生;进食障碍者行鼻饲或经皮内镜下胃造瘘术(percutaneous endoscopic gastrostomy,PEG)等。
(二)一种促进神经损伤修复的药物组合物治疗
所有患者在常规综合治疗基础上,将一种促进神经损伤修复的药物组合物(精氨酸1.5~5 g,异亮氨酸1.5~5 g,亮氨酸2.5~7.5 g,赖氨酸1.5~5 g,蛋氨酸0.25~1.5 g,苯丙氨酸0.25~1.5 g,苏氨酸1.5~5 g,色氨酸0.25~1.5 g,缬氨酸2.5~7.5 g,组氨酸1.5~4 g,甘氨酸1.5~4 g,丙氨酸1.5~5 g,脯氨酸1.5~4 g,天冬酰胺0.05~1.5 g,半胱氨酸0.05~1.5 g,谷氨酸1.5~5 g,丝氨酸0.25~2.5 g,酪氨酸0.05~1.5 g,L~鸟氨酸0.25~4 g,天冬氨酸0.5~2.5 g;维生素B11~2 mg,维生素B21~2 mg,维生素B310~20 mg,维生素B63~10 g;维生素C 1~3 g。药物的使用种类和剂量根据患者的具体情况进行个性化方案制定)配制在1个三升输液袋内进行静脉输注,1次/d,28 d为1个疗程,停药2周后行第2个疗程,依此类推,持续治疗时间≥4个疗程或6个月。
(三)诊断依据与标准
基于世界神经病学联盟(world federation of neurology,WFN)在1990年首次提出的El Escorial标准[10],ALS的诊断标准被修订了多次[9,11-12]。目前主要依据临床表现、体征或神经电生理检查结果所证实的侵犯范围,将诊断级别分为临床确诊、很可能和可能的ALS 3级。中华医学会神经病学分会于2012年提出了中国ALS诊断和治疗指南[8],指出ALS早期症状与多种病类似,缺乏特异的生物学确诊指标。医师常经过颈、胸、腰椎、脑部等多部位的MRI检查,与各专科医师联合诊断,先排除其他各种可能的病变,最终结合详细的病史、细致的体检和规范的神经电生理检查结果才能确诊为ALS。并根据上述证据指示的累及范围,将ALS分为临床确诊、临床拟诊和临床可能3级。
诊断标准:一般采用中华医学会神经病学会分会参照WFN意见制定的标准[8]。基本条件:(1)病情进行性发展:通过病史、体检或电生理检查,证实临床症状或体征在一个区域内进行性发展,或从一个区域发展到其他区域。(2)临床、神经电生理或病理检查证实有下运动神经元受累的证据。(3)临床体检证实有上运动神经元受累的证据。(4)排除其他疾病。根据上述特征,可作以下3个程度的分级诊断:(1)临床确诊ALS,通过临床或神经电生理检查,证实在脑干、颈段、胸段、腰骶段4个区域中至少有3个区域存在上、下运动神经元同时受累的证据。(2)临床拟诊ALS,通过临床或神经电生理检查,证实在4个区域中至少有2个区域存在上、下运动神经元同时受累的证据。(3)可能ALS,在1个区域有上下运动神经元同时受损的症状和体征,或者在2个或以上区域仅有上运动神经元受累的证据。另外,下列依据支持ALS诊断:1处或多处肌束震颤;肌电图提示神经源性损害;运动和感觉神经传导速度正常,但远端运动传导潜伏期可以延长,波幅降低;无传导阻滞[13]。
三、观察指标
(一)一般情况
统计所有患者的治疗时间、随访时间及生存、死亡情况。
(二)临床症状与体征改善
依据患者或家属自述以及医师体格检查结果,判断患者症状和体征的变化情况,记录治疗过程中和随访过程中所有患者各种症状和体征的改善情况。
(三)肌萎缩侧索硬化症改良功能评分量表(amyotrophic lateral sclerosis functional rating scale-revised,ALSFRS-R)结果
ALSFRS-R是目前最常见的自我报告式功能丢失量表,其随病程进展的下降率是患者功能减退和死亡率最重要的预测指标,评分共分为12项,满分为48分[14-17]。ALSFRS-R随时间的变化,即疾病进展率(δALSFRS-R/△FS)被证实可以预测患者的生存情况[18-19],计算公式为:疾病进展率=(48-ALSFRS-R)/病程(月)[20-21]。
(四)不良反应
记录患者在用药期间、停药休息期间以及停药随访期内的,与药物治疗有关的不良反应,并记录处置方法和预后情况。
四、统计学分析
结 果
(一)一般情况
22例ALS患者的治疗时间为6~16个月[(8.09±3.04)个月]。随访时间为0~15个月[(6.82±3.81)个月]。死亡1例,死亡原因为疾病晚期呼吸衰竭。
(二)症状及体征改善情况
本组22例肌肉萎缩好转、肌力增加3例(13.6%),舌肌萎缩、言语不清好转1例(4.5%),流涎好转2例(9.1%),吞咽功能改善1例(4.5%),四肢活动度增加2例(9.1%),1例(4.5%)不能站立和行走的患者可搀扶站立。
(三)ALSFRS-R 评分结果
22例ALS患者各阶段ALSFRS-R评分的波动范围:首次门诊时为18.0~44.0分,治疗6个月时为18.0~41.0分,末次治疗时为12.0~39.0分,末次随访6.0~38.0分。治疗6个月时的ALSFRS-R评分与治疗前比较,差异尚无统计学意义[24.50(12.3)分比27.15(14.7)分,Z=-1.183,P>0.05];随着病程的延长,末次治疗[23.50(6.0)分比27.15(14.7)分,Z=-2.557]和末次随访的评分[(23.59±7.02)分比(28.59±8.04),t=4.097]与治疗前比较均有所降低,差异有统计学意义(P均<0.05)。所有患者各阶段评分变化情况见图1~3。
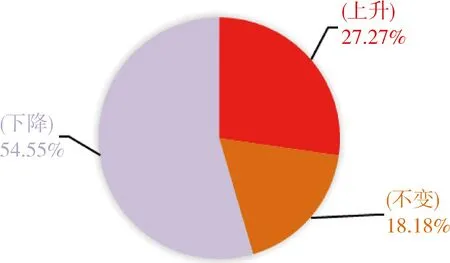
图1 22例ALS患者治疗治疗6个月前后的ALSFRS-R评分变化
注:ALS为肌萎缩侧索硬化症,ALSFRS-R为肌萎缩侧索硬化症改良功能评分量表
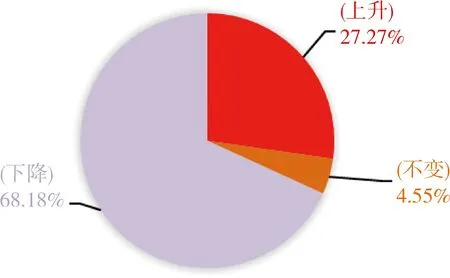
图2 22例ALS患者治疗末次治疗前后的ALSFRS-R评分变化
注:ALS为肌萎缩侧索硬化症,ALSFRS-R为肌萎缩侧索硬化症改良功能评分量表
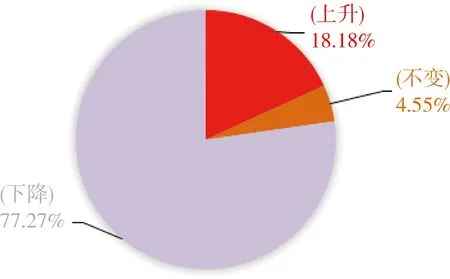
图3 22例ALS患者治疗末次随访(距首次用药后的时间≥12月)前后的ALSFRS-R评分变化
注:ALS为肌萎缩侧索硬化症,ALSFRS-R为肌萎缩侧索硬化症改良功能评分量表
(四)疾病进展率变化
对所有患者治疗和随访各阶段与治疗前的疾病进展率进行配对t检验或配对样本的Wilcoxon符号秩和检验发现,虽然患者治疗6个月和末次治疗的疾病进展率与治疗前疾病进展率差异无统计学意义[0.521(0.563)分/月比0.673(0.716)分/月,Z=-1.834,P>0.05;(0.702±0.469)分/月比(0.716±0.440)分/月,t=0.259,P>0.05],但末次随访时的疾病进展率低于治疗前的疾病进展率[(0.584±0.372)分/月比(0.716±0.440)分/月,t=2.706,P<0.05],且多数患者在治疗期间和治疗后疾病进展率均较治疗前下降。见表1。
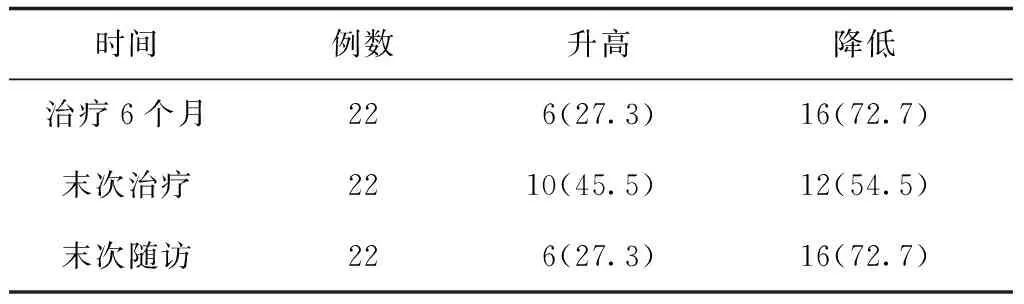
表1 22例ALS患者治疗及随访后疾病进展率变化[例,n(%)]
注:ALS为肌萎缩侧索硬化症,末次随访距首次用药的时间≥12个月
(五)不良反应
在治疗期间观察发现的不良反应包括经外周静脉注射处沿血管走行的轻微胀痛[3例(13.64%)],胃胀、恶心等胃肠道反应[2例(9.09%)],双侧脚踝以下足部麻木感[2例(9.09%)]。针对上述不适,减慢外周静脉输液速度、选择较粗大的外周静脉、选择更大型号的输液针均能改善输液胀痛,经中心静脉或输液港注射的患者未发现此类不适;对出现胃肠道反应的患者,在输液前肌肉注射10 mg甲氧氯普胺可以减轻反应;足麻木的患者中1例在停药2个月后逐步缓解消失,另1例将维生素B6用量由3 g降至2 g后,症状得到缓解。随访期间未发现严重不良反应。
讨 论
一、ALS的发病机制尚不明确,无特效治疗方法
到目前为止,ALS的发病机制还没有被探明。根据现有研究提出的假说包括有谷氨酸兴奋性毒性、线粒体损伤及功能障碍、氧化应激反应、神经胶质细胞异常、免疫炎症反应等[22-23]。约10%的患者为家族性ALS(familial amyotrophic lateral sclerosis,fAL)[24],具有家族史,而其中近2/3的患者和5%的散发性ALS(sporadic amyotrophic lateral sclerosis,sAL)患者发现了与ALS相关的致病基因[25]。所以针对可能的单一诱因进行治疗往往疗效不佳。
当前的主要治疗途径包括病因治疗、对症治疗和多种非药物的辅助治疗。目前国内外药物治疗方法包括:(1)力如太(利鲁唑片,Riluzole)[26-28]。(2)依达拉奉[29-30]。(3)神经生长因子治疗:如细胞因子的补充和调控[31-35]、内源性神经干细胞的活化与外源性神经干细胞的移植[36-39]。(4)中医中药[40]。ALS的治疗方法包括神经保护剂、抗兴奋毒性药物、神经营养因子、抗氧化和自由基清除剂、干细胞和基因治疗等。此外,ALS的综合治疗尤为重要,主要有:(1)保证充足的营养。(2)保证呼吸。(3)给予药物治疗。(4)精心护理。(5)加强心理疏导等。
二、本药物组合物疗法治疗ALS的机制探讨
笔者转换了思维方法,从整体出发,依据机体损伤在一定条件下是可以修复的理论,应用创新的药物组合物疗法获得了一些体会。笔者遵照唐代大药学家孙思邈所说的“夫为医者,必须首先洞晓病源……然后命药”[41]和黄帝内经《素问·阴阳应象大论》所云“治病必求于本”的理念,从长期的临床实践与科研工作中认识到:生命之源在于新陈代谢,疾病之因在于代谢紊乱,代谢之本在于底物、辅酶与强劲动能的支撑。基于这一新的理念所发明的创新药物组合物疗法能给患者提供“机体新陈代谢的底物、辅酶与强劲的动能”,从而促进其血液循环、酶代谢、氨基酸代谢及免疫功能逐步恢复,使受损的脑、脊髓等得到一定程度的修复,达到改善患者病情与临床症状,扼止患者危重状态进展并挽救生命的目的。
(一)多种氨基酸提供代谢底物及动能
本药物组合物中含有多种氨基酸,它们是构成生物体内蛋白质的基本单位,与生命活动有着密切关系。氨基酸在抗体内具有特殊的生理功能,是生物体内不可缺少的营养成分之一。氨基酸在人体内可通过代谢发挥下列作用:(1)合成蛋白质及核酸。(2)形成酸、激素、抗体、肌酸等含氮物质。(3)转变为碳水化合物和脂肪。(4)氧化成二氧化碳、水及尿素,并产生能量。(5)为血液系统提供新鲜的营养物质。通过调节氨基酸代谢以及血液循环,能促进受损的神经细胞再生、增强神经元存活能力。虽然在加速氨基酸代谢过程中产生了大量的氨,但是由于组合物中作为尿素循环的反应底物L-鸟氨酸的存在,可以迅速激活肝脏细胞中的尿素循环,通过该循环将氨基酸在代谢过程中产生的大量有害氨排出体外,保证了机体正常的代谢,该循环也是人体除去氨毒害作用的主要途径[42]。此外,组合物中所含的天冬氨酸是多种氨基酸及嘌呤、嘧啶碱基合成的前体,对细胞亲和力强,可作为钾、镁离子载体,向心肌输送电解质,促进细胞去极化,维持心肌收缩能力。天冬氨酸不但可以为神经营养因子的合成和运输提供能量以及原料,修复受损的神经细胞,还可以促进钾离子进入神经元的细胞内,提高其存活、增殖与分化的能力。天冬氨酸和L-鸟氨酸联合使用,还可以更大限度增加肝脏中尿素循环的活性,增强肝脏的排毒功能,迅速降低血氨,促进肝细胞自身的修复和再生,从而增强了人体自身免疫能力。
(二)多种维生素确保辅酶供应,维持氧化应激平衡,促进毒害物质排除
B族维生素是水溶性维生素,包括维生素B1、维生素B2、维生素B6、维生素B12、烟酸、泛酸、叶酸等,是推动体内代谢,把糖、脂肪、蛋白质等转化成热量时不可缺少的物质。它们具有协同作用,能够调节新陈代谢、增进免疫系统功能、促进细胞生长和分裂。其中维生素B6可能是最重要的一种。维生素B6又名吡哆素,是动物正常发育、细菌和酵母繁殖所必需的营养成分。包括吡哆醇、吡哆醛和吡哆胺3种化合物。在动物组织中,维生素B6多以吡哆醛和吡哆胺的形式存在。吡哆醇可转化为吡哆醛或吡哆胺,吡哆醛和吡哆胺、吡哆醛磷酸和吡哆胺磷酸可相互转变,但最后都以活性较强的吡哆醛磷酸和吡哆胺磷酸形式存在并参加转氨作用。人体70%~80%的维生素B6分布于肌肉组织,并在蛋白、脂质和碳水化合物的代谢中发挥着关键的作用,是氨基酸代谢与合成的重要辅酶,也是机体内许多重要酶系统的辅酶。现已知肝脏中有60多种酶代谢需要维生素B6的参与。因此,维生素B6在促进机体正常酶代谢方面起到十分重要的作用。大量损耗维生素B6者会出现氨基酸代谢紊乱。生物体内无论是神经调节还是激素调节,最终都是通过酶促反应起作用。本发明中添加的维生素B6为人体内的氨基酸代谢、神经递质γ-氨基丁酸(γ-aminobutyric acid,GABA)/谷氨酸转化提供了充足的辅酶[43-44]。基于ALS的谷氨酸兴奋性毒性和氧化应激反应病因假说,该组药物组合物可通过将脑脊液中过量的谷氨酸转化为谷氨酰胺和谷胱甘肽而起到治疗作用:(1)谷氨酰胺没有毒性,人体可以通过谷氨酰胺从脑、肌肉等组织向肝或肾转运氨,这是人体迅速解除氨中毒的一种方式。对于ALS,该方式也是迅速解除胞外过高的谷氨酸浓度对中枢神经系统产生的毒性作用,同时储藏和运输氨的重要途径。当被运至肝脏中,谷氨酰胺将氨释放出来,合成尿素后进行排泄;当被运至肾脏中,谷氨酰胺则可将释放出来的氨直接随尿排出;被运至其他组织中的谷氨酰胺还可用于合成氨基酸和嘌呤、嘧啶等含氮物质。也就是说,本药物组合物可以通过促进谷氨酰胺的合成来解除过高浓度的谷氨酸对中枢神经系统产生的明显毒性作用,并且谷氨酰胺能直接通过血脑屏障,为脑神经细胞的修复提供部分了氨基酸、嘌呤和嘧啶的合成原料。(2)谷胱甘肽的合成可以有效清除体内自由基,减轻ALS患者的症状。另外,维生素B6还是一种天然的利尿剂,而利尿就能解毒,静脉输入5 g维生素B6大约能利出尿液380 mL。吡哆醛磷酸还有一特殊的功能,那就是可以提高氨基酸和钾离子进入细胞的速率。
维生素B6在人体内的半衰期短,很快就能被排出体外。因此,一般不会对患者产生严重不良反应。本药物组合物创新疗法中的超药典剂量维生素B6的临床应用遵循了有关法律依据:维生素B6每日5~10 g已被列入GJB-FL5340国家军用标准[45]。在全军现在实行的总后勤部卫生部“战伤救治规则”中也有相关规定[46]:首剂使用维生素B61~5 g,可连续使用,1 d总量不超过10~15 g。中国目前的维生素B6口服剂量为10 mg /片,而美国已达到该剂量的50倍(500 mg /片)。由中国人民解放军第三〇六医院(总装备部总医院)研制、石家庄四药生产的2.5 g/250 mL维生素B6也已通过总后勤部批准并在临床上使用,在载人航天航天员的医疗保障中得到广泛应用。
(三)多管齐下,相辅相成,改善症状
ALS患者由于大脑、脑干和脊髓中的运动神经元细胞受到侵袭,发生了损伤和变性,以致肌肉逐渐萎缩和无力,甚至瘫痪。同时,患者的新陈代谢效率与速率降低,免疫功能、抵抗力也明显下降。基于上述理论基础,一些患者一般在应用本药物组合物疗法治疗2周左右即可出现微汗、有温暖感的表现,机体血液循环、新陈代谢的效率与速率有所提高,一部分患者的四肢活动度也会较前有所增加;治疗3个疗程后,大部分患者的病情逐步趋于稳定。但是,要使脑、脊髓等中枢神经系统中已经发生损伤、变性的神经细胞得到一定程度的修复是非常困难的。据既往的临床经验,一般至少需要长达8.5个月的持续治疗。本研究中药物组合物疗法使得22例患者中的一部分出现肌肉萎缩好转、肌力增加[3例(13.6%)],舌肌萎缩、言语不清好转[1例(4.5%)],流涎好转[2例(9.1%)],吞咽功能改善[1例(4.5%)],四肢活动度增加[2例(9.1%)]等症状的改善,甚至有1例无法站立的患者能在搀扶下站立起来。说明为ALS患者提供充足的底物、辅酶与强劲动能,从整体上改善ALS患者的新陈代谢状态,并促进体内毒害物质的排出,对其病情的延缓和改善是有帮助的。在对患者进行自开始接受治疗后长达1年的连续随访中发现,完成连续4个疗程(6个月)的规范化治疗后,不论后续用药与否,仍然对其疾病的进展起到一定的影响作用:4例(18.2%)患者的ALSFRS-R评分上升,1例(4.5%)不变,17例(77.3%)下降,其中有72.7%(16/22)的患者疾病进展率较治疗前有所降低。即使是在末次随访的ALSFRS-R评分较治疗前有所下降的患者中,仍有一部分疾病进展速率是低于治疗前的。以上的疗效分析结果证实,本创新药物组合物疗法对改善ALS患者病情与临床症状,扼止患者危重状态进展,是有一定疗效的。
总之,本药物组合物中所含多种氨基酸与丰富B族维生素,都是人体生命活动不可缺少的物质。它提供了机体代谢底物、辅酶与强劲的动能,其中鸟氨酸能够将机体产生有害的二氧化碳及氨通过鸟氨酸循环代谢排出体外,从而使得肝内酶代谢逐步恢复。维生素B6是各种氨基酸代谢的辅酶,只有较大剂量维生素B6参与,人体的生命代谢活动才能被激活。本药物组合物的巧妙搭配在人体新陈代谢中发挥着特别重要的作用。使ALS患者受损的脑、脊髓等的功能得到一定程度的修复,增强了神经元的存活能力,从而改善患者的病情与临床症状,扼止危重状态的进展。
四、一些经验和体会
截止到2018年9月,笔者团队已经诊治了803例MND患者,其中ALS患者184例,对大量临床数据的反馈总结也证实,本药物组合物疗法的确无毒、无害、无副作用,且重复性好。在对184例ALS患者的长期诊治过程中,体会并总结出了数项需要特别关注的事项:(1)预防感冒发烧。感冒发烧后,ALS患者机体的免疫功能会急剧下降,并于此后的1~2个月都难以使病情恢复至原有状态,要特别小心并加以预防。(2)防治腹泻。腹泻易至ALS患者本已衰弱的体质进一步大幅减退。(3)防治血压、血糖过度波动。遵相关专科医嘱维持高血压、糖尿病等基础疾病的稳定,有助于防止加重病情。(4)忌过度焦虑、恐惧、暴躁。波动和消极的情绪易严重影响患者生活质量,让患者吃不好、睡不好、休息不好,家属应积极引导和鼓励患者保持乐观积极的心态。(5)饮食需多样化。营养代谢支持治疗十分重要,应结合患者自身情况,尽量选择易消化、易吸收、高蛋白、富含维生素和矿物质的食物。(6)预防肺部并发症。特别注意要鼓励患者咳痰,防止发生肺炎;如出现呼吸困难,需早期使用无创呼吸机等机械通气以辅助呼吸,预防为主。(7)勿闻错误的小道消息。因各人的病情不同、病因不同、病程不同、恶化速度也不同,易出现群体性情绪低落而影响疗效,应在患者群体内宣扬传播正能量,激发患者体内潜能,使病情好转。
五、总结
被世界卫生组织列为五大绝症之一的ALS,在发病机理和特效治疗上仍有待突破。岳茂兴教授团队从整体角度思考,采用机体损伤在一定条件下是可以修复的理论,应用一种用于治神经损伤修复的药物组合物治疗ALS患者获得了一些体会。该方案经过对接受治疗者进行1年以上的疗效观察证实,的确对改善ALS患者病情有一定助益。本药物组合物疗法经临床应用证实,的确无毒、无害、无副作用、重复性好,能给ALS患者提供“机体新陈代谢的底物、辅酶与强劲的动能”,促进患者血液循环、酶代谢、氨基酸代谢及免疫功能逐步恢复,使受损的脑、脊髓等功能得到一定程度的修复,增强了神经元的存活能力,从而改善患者病情与临床症状,扼止危重状态的进展。后续团队将继续进行认真总结,进一步完善该疗法,对正在接受治疗的ALS患者增加导药与改善神经功能缺失的药物,在综合治疗方面巧妙搭配,以期对ALS患者改善病情有更大的帮助。
志谢:本项目得到了王正国、陈冀胜、顾玉东、钟世镇、盛志勇五位院士的支持和帮助,得到陈亦江、梁华平、黄琴梅、黄晞、杨晓兰、楚鹰、刘希华、郝瑞生、黄亚博、陈宁、王立祥、邱泽武、刘青云、陈强、付研、周仁平、黄彤舸、童飞、廖联明、刘保池等的指导和帮助,在此一并致谢

