温度对水热法合成二硫化钼结构的影响
孙 娴,常芳娥,吴新明,坚佳莹,王 霞
(西安工业大学 材料与化工学院,西安 710021)
二硫化钼(MoS2)是具有六方晶系的类似于三明治状的层状结构的过渡金属硫化物,层与层之间通过弱的范德华力相结合[1].层状结构决定了其良好的润滑性能,二硫化钼以摩擦因数低,抗压强度高和稳定性好等优点被用作重要的固体材料润滑剂[2].此外,二硫化钼还被应用于加氢脱硫催化剂[3]、电极材料[4-6]、超导材料以及无水锂电池中,尤其在航空航天领域有非常大的发展潜力.因此,二硫化钼的制备方法与性能研究越来越受到人们的重视.
迄今为止,国内已有很多二硫化钼的制备方法,常用的制备方法有气相法、液相法和固相法.气相法[7]主要包含化学气相沉积法[8-9]、模版法[10]和磁控溅射法等;液相法[11]主要有化学沉淀法[12]、溶剂热反应[13]、溶胶-凝胶法[14]和微乳液法[15]等;固相法[16]主要包含固相分解法、机械剥离法和高温硫化法等.文献[17]采用溶剂热法,以自制2-十一烷基-1 -乙基硫脲基咪唑啉作为分散剂,以钼酸钠、硫脲和水合肼为原料,乙醇为溶剂合成了球形二硫化钼;文献[18]以钼酸钠为钼源,将不同的硫源(硫脲、硫代乙酰胺和硫化钠)采用水热法合成了绒毛状和囊泡状的二硫化钼,通过在氩气中800 ℃煅烧得到富勒烯状中空二硫化钼纳米粒子.在上述的制备方法中,一般的溶剂热反应体系需要的温度比较低,反应条件相对温和,反应的密闭性很好,不需要通惰性气体保护,但此类方法得到的产品品相相对较差,且溶剂易挥发,环境友好性差.若采用高温反应,将温度提高到300 ℃甚至更高,或者延长反应时间,只能得到无定型的二硫化钼,且反应能耗较大.因此,本研究改善了水热法制备二硫化钼的方案,较以往的合成二硫化钼的水热法,具有时间短,温度更低,且不需要高温退火处理的优点.且用水作为溶剂,避免了以往反应中使用一些有机溶剂的污染,为二硫化钼的合成提供了更为优良的途径.
本文以仲钼酸铵和硫脲为水热合成法的原料,在不同反应温度下(120 ℃、160 ℃、200 ℃、230 ℃和260 ℃)分别反应合成了二硫化钼材料,并对生成的二硫化钼进行了测试与表征,结果表明,反应温度对于二硫化钼的产量,晶化程度及微观形貌有着显著的影响;反应温度为230 ℃时,MoS2纯度和结晶化程度均比较高,微观片层结构明显,平整有序.
1 实验材料及方法
1.1 实验材料及仪器
本实验使用的原料为天津市大茂化学试剂厂的仲钼酸铵((NH4)6Mo7O24·4H2O),分析纯;天津市致远化学试剂有限公司的硫脲(CH4N2S),分析纯;西安市长安区化学试剂厂的浓盐酸(HCl),分析纯;天津市大茂化学试剂厂的无水乙醇(C2H5OH)和自制的去离子水,分析纯.
利用天津天宇实业有限公司的干燥箱(型号:XMTD-1000型)进行高温反应和产物干燥;采用电子天平(型号:FA2204)对产物质量进行称量;使用日本岛津公司的X-射线衍射仪(X-Ray Diffraction,XRD)(型号:UV-2550),美国赛默飞世尔科技公司的X射线光电子能谱仪(X-Ray Photoelectron Spectroscopy,XPS)(型号:Escalab 250XI型)和北京瑞利公司的傅里叶-红外光谱仪(Fourier Transform Infrared Spectrometer,FTIR)(型号:WQF-31)对材料结构进行分析;使用日本电子株式会社的扫描电子显微镜(Scanning Electron Microscope,SEM)(型号:JSM-6360LV)对材料微观形貌进行表征,采用热失重分析仪(Thermo Gravimetric Analyzer,TGA)对材料热稳定性进行测试.
1.2 MoS2的合成
利用水热法合成MoS2将0.494 4 g (NH4)6Mo7O24·4H2O (0.4 mmol)与0.479 6 g CH4N2S (6.3 mmol)分别装入两个干燥的烧杯中,然后分别加入30 mL离子水中,利用磁力搅拌机搅拌30 min至完全溶解;将仲钼酸铵溶液与硫脲溶液混合,继续搅拌10 min,使其充分混合;加入浓HCl调节pH至2;迅速将溶液转入聚四氟乙烯反应内衬中,然后密闭,在不同的设定温度下(120 ℃、160 ℃、200 ℃、230 ℃和260 ℃)加热24 h,反应完成后自然冷却至室温后,取出反应釜,将获得的溶液用去离子水和酒精分别洗涤三次,去除掉多余的溶液和杂质,最后放置于真空干燥箱中60 ℃以下干燥15 h,最终得到粉末状固体产物.反应方程式为:4(NH4)6Mo7O24·4H2O+63CH4N2S+42H2O→150NH3↑+63CO2↑+7H2SO4+28 MoS2.
2 结果与分析
2.1 产物的质量
图1为不同温度制备的MoS2的产量图.温度从低到高,当温度为120 ℃时,产物的质量m仅为0.052 7 g,只能看到极少的黑色粉末;当温度为160 ℃时,产量有所提高,增加至0.199 8 g;升高温度至200 ℃时,得到0.340 3 g的MoS2,与前两个温度相比,有较多的增长,但仍然与方程式计算所得的理论值0.448 0 g有较大差距;当温度达到230 ℃,产量为0.422 5 g,接近理论值,继续升高温度至260 ℃,生成的MoS2减少至0.410 4 g.温度较低时,不利于反应的进行;升高温度,反应逐渐加剧,生成大量的气体,反应釜内压强越来越高,当温度达到230 ℃时,反应在正方向上达到了极限,容器内很高的压强使得反应开始向逆方向进行,导致在温度为260 ℃时,产量有所降低.因此,在230 ℃时MoS2的产量达到最高.
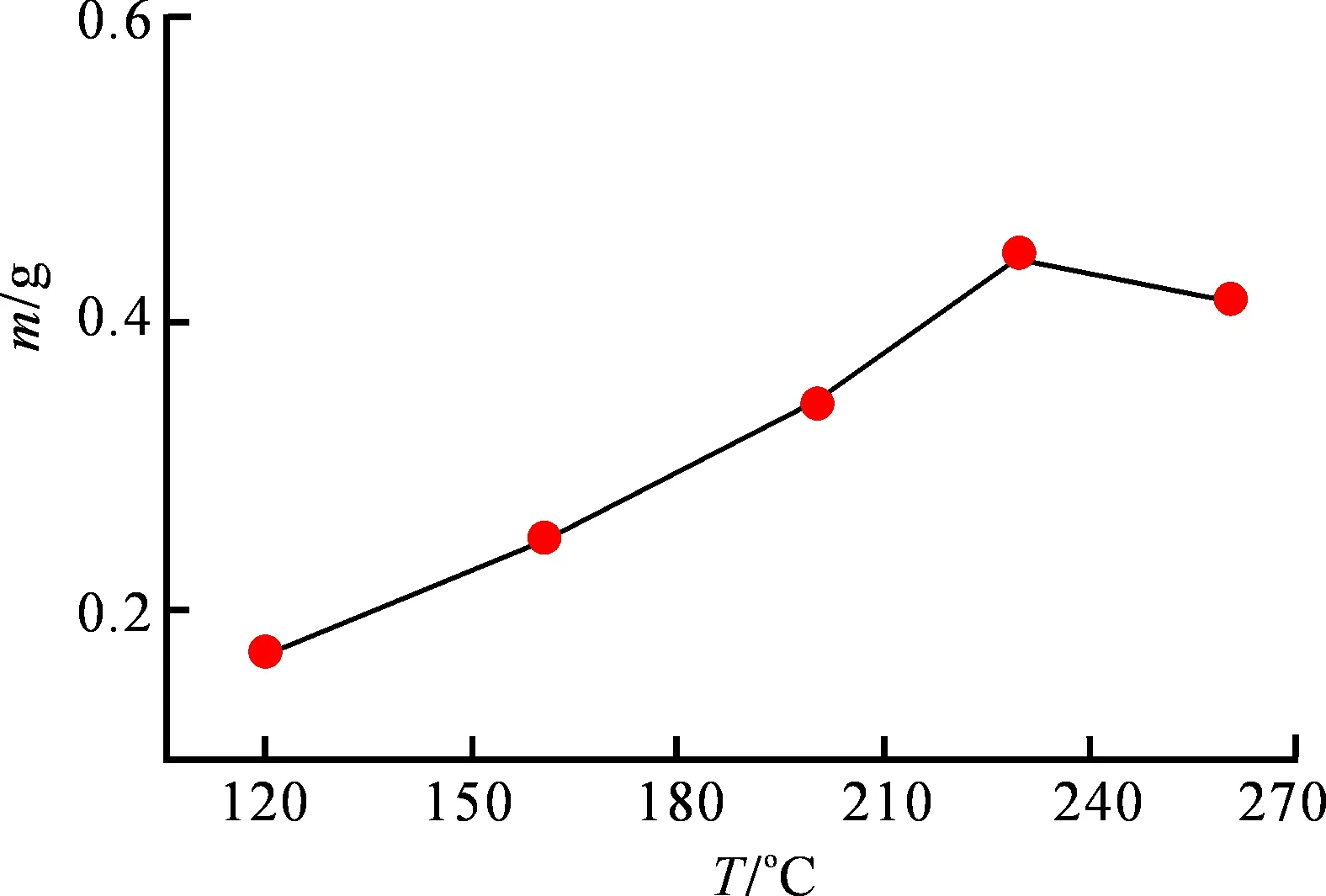
图1 不同温度制备MOS2的质量
2.2 X射线衍射谱分析
图2为不同温度制备的MoS2的XRD图,从图2可以看到,在120 ℃时,衍射峰基本无特征峰出现,整个谱图平缓无起伏,说明此温度生成的产物很少且结晶化程度很低;在160 ℃时,只有微弱的起伏出现,强度非常小,宽度无边界;在200 ℃时,衍射峰的宽度依然比较模糊,强度也很小,但特征峰的雏形已经基本显示出来,表明在此温度下有产物生成,但所得到的产物结晶度较低;当温度升高至230 ℃时,衍射峰变得清晰,四个特征峰均明显地显现出来,在2θ为14.1°,33.9°,39.5°和59.1°处有特征峰出现,经过与标准卡片(JCPDS37-1492)比对,特征峰归属于MoS2的(002)、(101)、(103)和(110)晶面,且特征峰很尖锐,说明产物结晶度很好;温度升高至260 ℃时,特征峰的强度变小,峰型变得不是很尖锐,说明此温度生成的MoS2结晶化程度有所降低.因此,230 ℃有利于MoS2的生成与结晶.
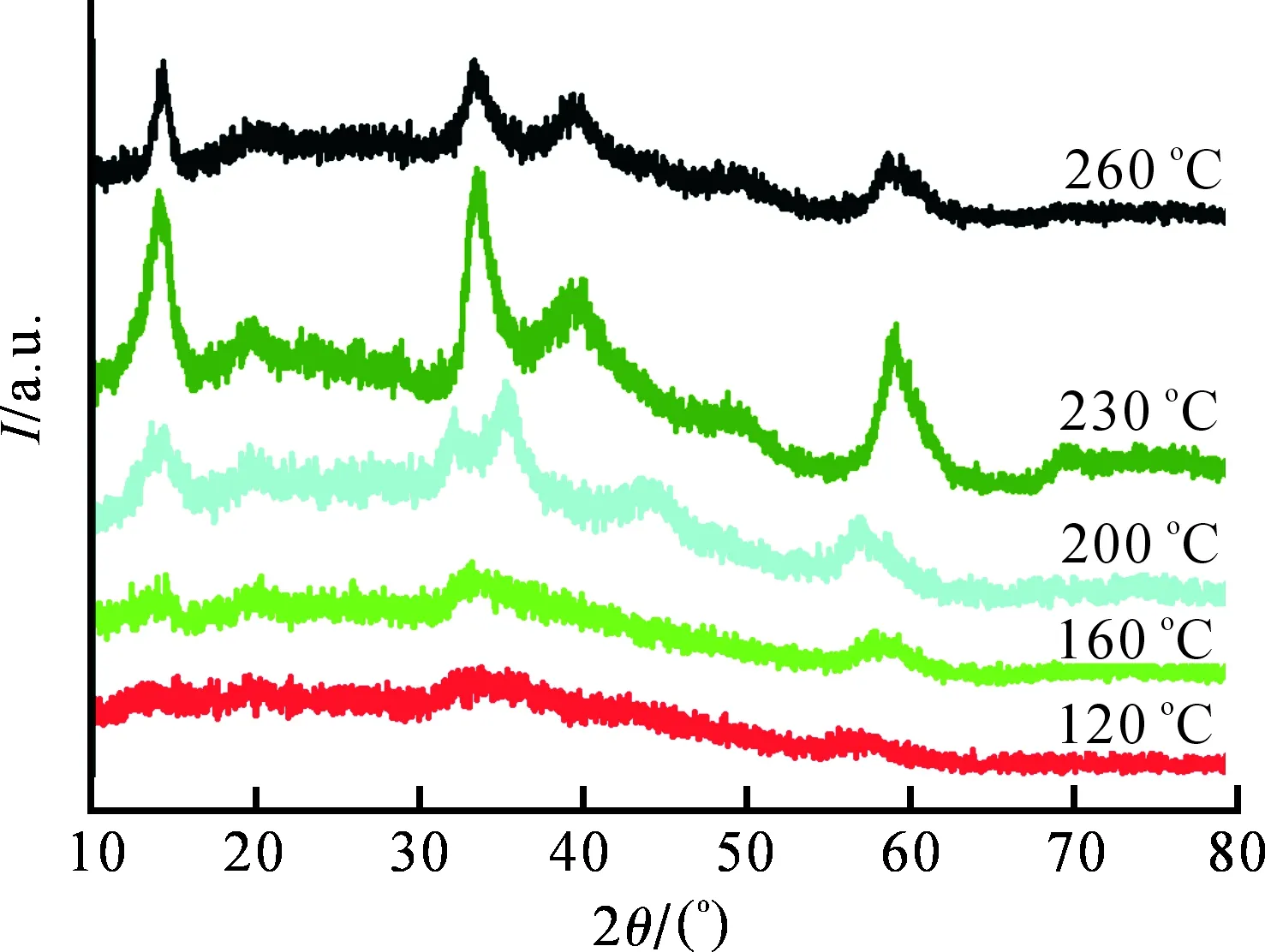
图2 不同温度制备MoS2的XRD图
2.3 傅立叶-红外光谱分析
图3为不同温度制备MoS2的FTIR图,从图3可以看出,在120 ℃时,曲线平缓,无明显峰出现;在160 ℃时,在750 cm-1、1 400 cm-1和3 500 cm-1附近有比较宽的凸起,表现出微弱的峰;在200 ℃、230 ℃和260 ℃时,峰的位置和强度基本一致,在708 cm-1和3 425 cm-1处出现的宽而高的峰是由于-OH的伸缩振动,表明样品中含有少量水份;在1 402 cm-1处出现的峰对应于C-O的伸缩振动,是由于反应残留的原料而引起.
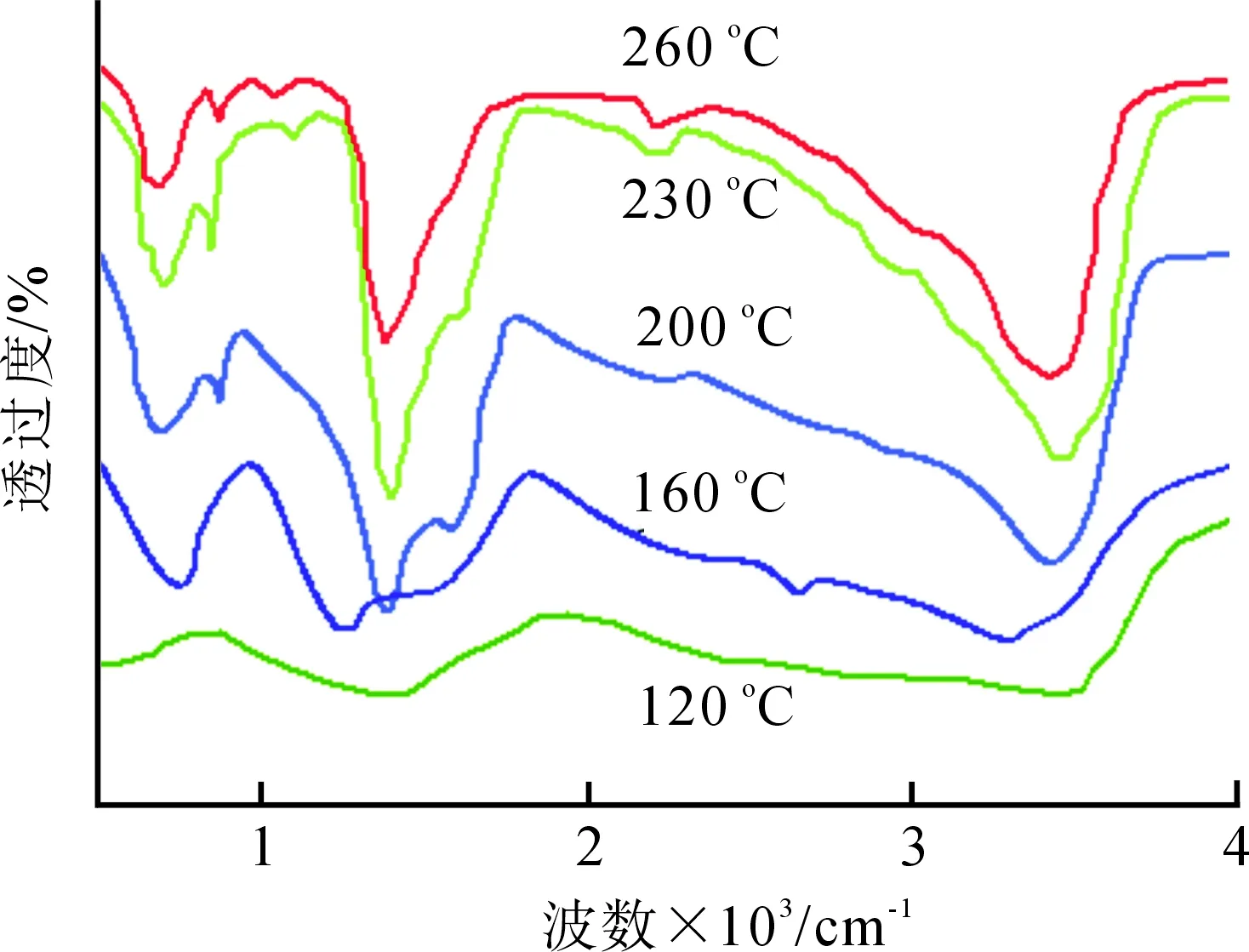
图3 不同温度制备MoS2的FTIR图
2.4 热失重分析
图4为不同温度制备MoS2的TGA曲线.由图4可以看出,反应温度由120 ℃升高至230 ℃,MoS2的分解温度依次升高,分别为98 ℃、167 ℃、193 ℃和223 ℃,温度较低时,产物中含有的未发生反应的原料较多,在加热下最先开始分解,反应温度升高,参与反应的原料逐渐变多,直至230 ℃时,最大程度的反应生成了MoS2,分解温度随着产物中MoS2含量的增加而升高;当温度达到260 ℃时,分解温度降低为209 ℃,这是由于少量原料的存在使得产物纯度降低而导致.反应温度由120 ℃升高至230 ℃,MoS2热失重后的剩余率依次升高,分别为20%,23%,24%和30%,当反应温度达到260 ℃时,剩余率降低至28%,说明MoS2纯度越高,热稳定性越好.综合所述,在230 ℃时,产物中MoS2的纯度高,最不容易分解,热稳定性好.

图4 不同温度制备MoS2的TGA图
2.5 扫描电镜分析
图5为不同温度制备的MoS2的SEM图.

图5不同温度制备的MoS2的SEM图
Fig.5 SEM micrographs of MoS2at different temperatures
由图5可看出,在120 ℃(图5(a)和图5(b))时,还没有完整的二硫化钼产生,有较多的微小颗粒,表面凹凸不平,无法观察到细微结构;在160 ℃(图5(c)和图5(d))时,表面虽然有一些类似于二硫化钼的小球体,但是很少有规则的形貌;在200 ℃(图5(e)和图5(f))时,有许多的二硫化钼晶体产生,但颗粒聚集很严重,粒径大小差异大,可观察到小的片层但不明显;当温度为230 ℃(图5(g)和图5(h))时,可观察到尺寸约为100~200 nm的片层结构的MoS2,形貌规整,表面光滑,且层状结构很清晰;当260 ℃(图5(i)和图5(j))时,层状MoS2的表面无明显变化,尺寸有所变小,片层边界变的模糊.通过以上微观形貌分析可以发现,在230 ℃反应温度时,最适于MoS2片层结构的生成.
2.6 X射线光电子能谱分析
以上分析得出反应温度为230 ℃时所得到的MoS2在产量、纯度、结晶状况、微观形貌和热稳定性等方面均具有比较明显的优势,为了进一步证实这一结果,本文对230 ℃制备的MoS2进行了XPS测试.图6即为230 ℃制备的MoS2中的Mo3d、S2p的XPS谱图.由图6(a)可以看出,产物在结合能为160 eV和230 eV附近出现峰,分别代表了S和Mo,可以确定产物含有Mo和S元素;其中含有的微量杂质导致在其他区域出现了少数峰,如在410 eV和530 eV处出现的峰分别代表了H和O元素,是由于产物中含有的水份所引起.由图6(b)可以看出,Mo3d5/2和Mo3d3/2的结合能分别为229.3 eV和232.3 eV,图6(c)显示S2p的结合能为162.1 eV,峰值与MoS2标准值一致.230 ℃时的MoS2的特征峰明显,峰型尖锐,峰值高,说明温度对于MoS2的生成有较大的影响,且230 ℃是采用该方法合成MoS2比较适合的温度.
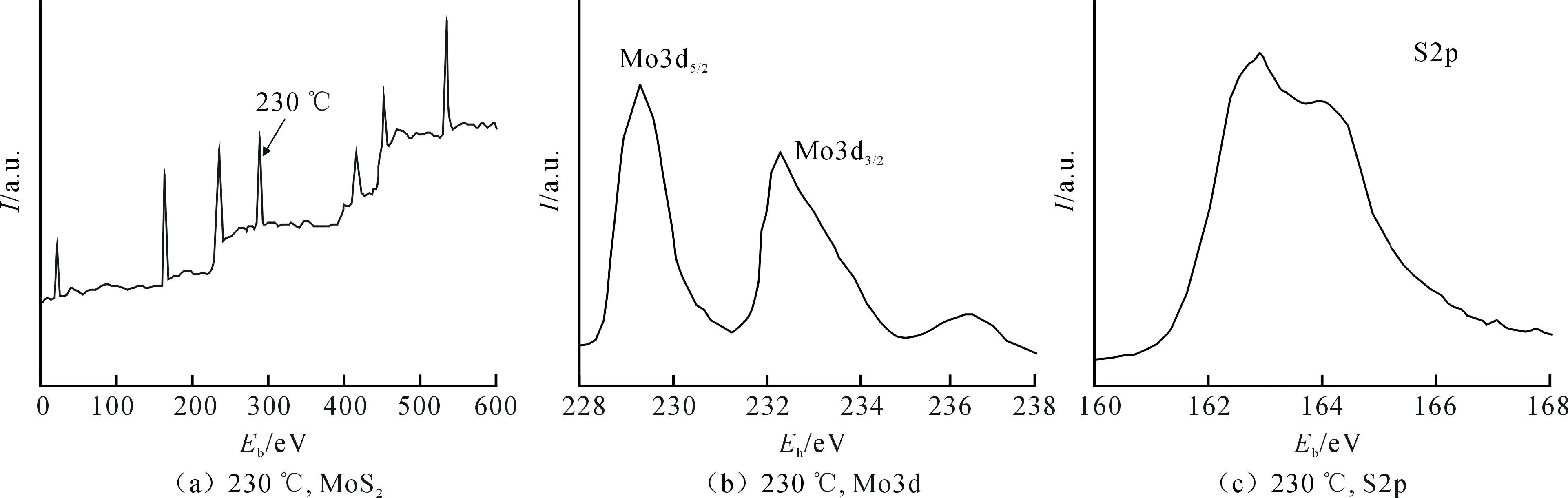
图6 230 ℃制备的MoS2,Mo3d和S2p的XPS图Fig.6 XPS patterns of MoS2,Mo3d and S2p at 230 ℃
3 结 论
1) 原料为仲钼酸铵和硫脲,方法为水热合成法,实验条件易实现,成本低,无副产物生成,在较短时间内可以生成较多高纯度的二硫化钼;
2) 在120 ℃和160 ℃时,只有少量的二硫化钼生成,且微观形貌极差,在200 ℃时,反应虽然可以生成较多的二硫化钼,但聚集严重,形貌不规整,尺寸大小不均匀,结晶状况差;在230 ℃时,生成的二硫化钼表现出很好的结晶性,微观形貌规整,片状结构清晰,表面光滑且分布均匀;在260 ℃时,生成的二硫化钼尺寸有所变小.因此,反应温度对于二硫化钼的生长,结晶化程度和粒径,以及微观形貌有着显著的影响.
3) 在本实验中生成的二硫化钼产量与理论值有一定的差异,在后期的实验中,尝试去改变反应中水的用量来促进反应进一步向正方向进行,使得二硫化钼的产量向理论值靠近.

