FGF4在牛早期胚胎发育过程中的表达
刘瑞琪,王玮玮,屈鹏祥,马晓楠,王勇胜,卿素珠
(西北农林科技大学动物医学院,陕西杨凌 712100)
成纤维生长因子(fibroblast growth factor,FGF)家族,又称为肝素亲和生长因子(heparin binding growth factor,HBGF),是一类能促进成纤维细胞生长的多肽类活性物质,约有23种,大多数与肝素结合发挥作用[1]。 FGF对于细胞生长、分化是重要的调控因子;可维持早期胚胎发育和器官形成的祖细胞,并且调节它们的生长、分化,构成特定的组织;高度限制在特殊细胞亚型的特殊发育阶段;可促进细胞有丝分裂、趋化与血管生成、促进中胚层和神经外胚层细胞的存活与生长等[2]。
成纤维生长因子4是属于FGF4亚型因子,它可分泌带有切割的N-端信号肽的蛋白,通过旁分泌分泌到细胞外,结合和激活FGF受体(fibroblast growth factor receptors,FGFRs)引起生物反应。研究表明,FGF4在小鼠早期胚胎发育过程中发挥重要作用。早在1994年,Rappolee等研究发现FGF4 mRNA是母源型转录因子[3]。近年的研究表明,在小鼠早期胚胎发育过程中,FGF4特异性的分布于内细胞团中,调控内细胞团分化为外胚层和原始内胚层,决定外胚层和原始内胚层的分布比例[4],并且调控着外胚层和胚外外胚层交流的诱导信号[5]。随着研究的进一步深入,发现FGF4突变的小鼠胚胎在植入前死亡,可能是因为FGF4的异常表达干扰了早期胚胎发育过程中内细胞团的生长[6]。此外,有研究表明,敲除FGF4基因的小鼠也将导致胚胎植入后流产[7],分析认为FGF4的异常表达影响了小鼠胎盘的发育及功能[8]。以上研究结果表明,FGF4是小鼠早期胚胎发育过程中一个重要因子,异常表达会影响早期胚胎的发育。目前,有关FGF4在牛早期胚胎发育过程中的分布及功能意义尚未见报道,本研究通过实时荧光定量PCR和免疫荧光染色技术,对FGF4在牛早期胚胎发育各个阶段的表达和定位规律进行研究,为探讨其在牛早期胚胎发育过程中可能的作用提供依据。
1 材料与方法
1.1 材料
1.1.1 生物材料 试验所用牛卵巢,采自西安市某屠宰场;冷冻精子,购自上海光明荷斯坦牧业有限公司。
1.1.2 主要试剂 RNA提取试剂盒Cells-to-signal Kit,Invitrogen公司产品;反转录试剂盒cDNA synthesis kit,TaKaRa公司产品;荧光定量试剂盒SYBR Premix ExTaq,Promega公司产品;兔源Anti-FGF4多克隆抗体(ab106355),Abcam公司产品;Alexa Fluor 488标记山羊抗兔IgG二抗、免疫染色固定液、封闭液一抗、二抗稀释液和DAPI等,碧云天公司产品。采卵液、卵母细胞成熟液、精子获能受精液、胚胎体外培养液,按照文献配制[9]。
1.2 方法
1.2.1 卵母细胞的收集 采集的牛卵巢存放于含有100 mg/L链霉素、20 U/L青霉素的37℃生理盐水的恒温瓶中,4 h~6 h内送回实验室。生理盐水洗涤3次后,去除卵巢表面的附属组织,用12号针头注射器采用抽吸法抽吸卵巢表面的卵泡,将抽吸出的卵泡液置于直径60 mm平皿中,体视显微镜下收集卵丘-卵母细胞复合体(cumulus oocyte complexes,COCs),在采卵液中洗涤3次,选取卵丘细胞包裹较好且胞质均匀的COCs放入卵母细胞成熟液中培养,培养条件为38.5℃、体积分数为5%的CO2。
1.2.2 体外受精胚胎的收集 COCs在培养22 h~24 h后,利用移液枪吹吸数次,使颗粒细胞呈松散状,挑选带有第一极体的成熟卵母细胞在精子获能受精液中洗涤3次,收取10个MⅡ期(Metaphase Ⅱ)卵母细胞备用,然后将剩余卵母细胞放至精子获能受精液的微滴中(用矿物油覆盖)进行后续试验。提前将6 mL的精子获能受精液置于15 mL的离心管中,倾斜放置于38.5℃、体积分数为5%的CO2培养箱平衡8 h以上。将冷冻精子在38℃水浴中解冻,用玻璃吸管将其缓缓注入平衡好的精子获能受精液的离心管底部,之后45°倾斜离心管,于38.5℃、体积分数为5%的CO2培养箱静置45 min,使得精子能够自由上浮,吸取上清液部分,置于新的15 mL离心管中1 000 r/min离心10 min,弃上清,保留其底部200 μL的液体轻轻混匀,移入含有成熟卵母细胞的微滴中,在38.5℃、体积分数为5%的CO2条件下培养10 h~14 h。将受精的卵母细胞用10 g/L透明质酸酶完全清除颗粒细胞层后,移至胚胎体外培养液中洗涤3次,而后移到预先平衡4 h~6 h的胚胎体外培养液的微滴中,每个微滴放置约50个受精卵,在38.5℃、体积分数为5%的CO2中培养。在24、48、72、120、168 h分别收取2-细胞、4-细胞、8-细胞、桑椹胚和囊胚期的胚胎。
1.2.3 总RNA提取及cDNA合成 分别收取各时期的早期胚胎10个,按照RNA提取试剂盒Cells-to-signal Kit说明书提取胚胎总RNA,取不同时期胚胎的RNA 2 μg ,按照反转录试剂盒cDNA synthesis kit说明书反转录为cDNA,置-20℃保存。
1.2.4 实时荧光定量PCR 根据GenBank中公布的牛cDNA序列,利用Primer 5.0设计特异性引物(表1),由上海生工生物工程技术服务有限公司合成。
以各时期的胚胎cDNA为模板进行实时荧光定量PCR,反应体系:上、下游引物(0.2 mmol/L)各0.4μL,模板cDNA 2μL,SYBR○RPremix ExTaqTM Ⅱ 10μL,Passive ROX Reference Dye Ⅱ 0.4 μL, ddH2O 6.8μL,总反应体系为20μL。每个样品重复3次,使用Step One real-time PCR system (Step One and Step One Plus;ABI)进行RT-PCR,反应程序:95℃ 30 s;95℃ 5 s,60℃ 30 s,共40个循环。以GAPDH为内参基因,通过2-△△Ct法计算FGF4的相对表达量。
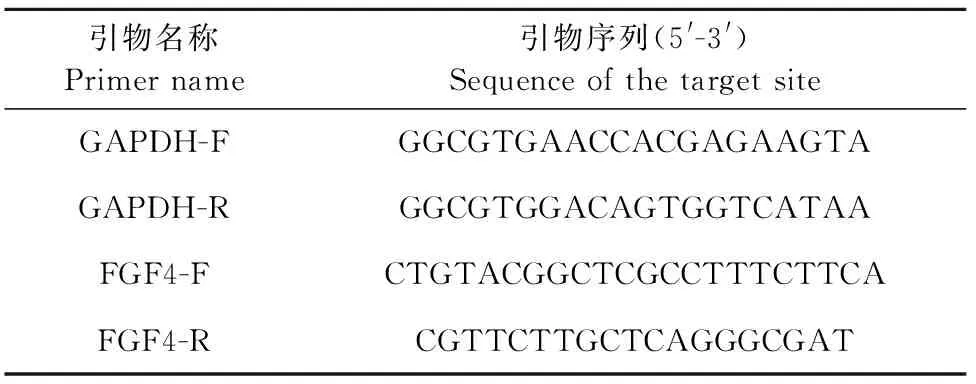
表1 试验所用引物序列
1.2.5 免疫荧光染色 各时期胚胎经免疫染色固定液固定2 h,用PBS-PVA洗涤5 min×3。 3 mL/L Triton X-100室温透化30 min,PBS-PVA洗涤5 min×3。封闭液4℃过夜,PBS-PVA洗涤5 min×3。加入FGF4一抗(工作浓度1∶200),4℃过夜孵育,PBS-PVA洗涤5 min×3。加入Alexa Fluor 488标记山羊抗兔IgG二抗(工作浓度1∶1 000),避光室温孵育2 h~4 h,PBS-PVA洗涤5 min×3,DAPI 染5 min,PBS-PVA洗5 min×3;抗荧光淬灭封片剂封片,荧光显微镜下观察并照相。
1.2.6 数据处理及分析 所有试验数据均重复3次,所得数据通过SPSS 19.0软件进行统计学分析,P<0.05为差异显著,P<0.01为差异极显著。
2 结果
2.1 FGF4 mRNA在牛早期胚胎发育过程中的表达
不同时期牛早期胚胎中FGF4 mRNA的表达情况见图1。由图1可知,FGF4 mRNA在牛MⅡ期卵母细胞及早期胚胎的各阶段均有表达,相比于MⅡ期卵母细胞,FGF4 mRNA的表达量在2-细胞胚显著下降,随后持续增加,但在4-细胞胚时FGF4 mRNA的表达量仍低于MⅡ期卵母细胞,8-细胞胚时FGF4 mRNA的表达量已显著高于MⅡ期卵母细胞,至桑椹胚期FGF4 mRNA的表达量达到峰值,而后在囊胚期表达量显著下降、但仍高于8-细胞期及之前各时期胚胎中的表达量。
2.2 FGF4在牛早期胚胎中的分布规律
FGF4阳性反应呈绿色荧光,细胞核呈蓝色荧光。不同阶段牛早期胚胎FGF4的分布情况见图2。由图2可知,FGF4蛋白在牛MⅡ期卵母细胞及各时期的早期胚胎中均有表达,但在不同时期胚胎的定位及反应强度有所不同。在MⅡ期卵母细胞、2-细胞胚及4-细胞胚,FGF4在卵母细胞及卵裂球的细胞质和细胞核中均有表达。而在8-细胞胚及桑椹胚,FGF4主要定位于卵裂球的胞质,而细胞核中未见阳性反应。至囊胚阶段,FGF4在内细胞团及滋养层细胞中均有表达,尤以内细胞团的反应更强,且主要定位于细胞质。

MⅡ.MⅡ卵母细胞;2-cell.2-细胞胚;4-cell.4-细胞胚;8-cell.8-细胞胚;M.桑椹胚;B.囊胚
MⅡ.MⅡoocytes,2-cell.2-cell stage;4-cell.4-cell stage;8-cell.8-cell stage;M.Morula;B.Blastocyst
图1 FGF4 mRNA在牛早期胚胎中的相对表达量
Fig.1 Relative expressional amount of FGF4 mRNA in bovine early stage embryos
3 讨论
Rappolee D A等[3]发现在小鼠胚胎中FGF4从MⅡ期卵母细胞至囊胚阶段均有表达,其在2-细胞期表达量有所下降,在囊胚期高度表达,认为FGF4是一种母源性转录因子。在哺乳动物中,精子染色质与卵母细胞染色质融合,形成合子基因组,合子型基因激活并转录,最终获得发育的全能性[10]。而在合子型基因激活前,细胞分裂受母源性转录因子调控,受精卵中储存着大量的母源mRNA、蛋白质、细胞器,这些物质合成更多的细胞因子,支持并指导早期胚胎的发育。在此过程中母源物质逐步消耗,直到合子型基因被激活,合子型基因的适时表达并完全取代母源基因,以实现胚胎发育由母源型调控向合子型调控的过渡。而缺少这一过程的动物胚胎无法进一步发育,胚胎发育受到阻滞,这表明母源型调控向合子型调控的转变对胚胎发育至关重要。值得注意的是,研究表明大部分母源因子,在合子型基因转录激活后仍表达,而且缺失这些母源因子对胚胎是致死性的[11]。然而,不同物种由母源性转录因子调控向合子型基因调控过渡的时期不同,小鼠的合子激活期为2-细胞胚胎晚期[12-13],牛的合子激活期为4-细胞胚晚期或8-细胞时期[14],这使得一些基因在小鼠和牛胚胎中的表达有所不同,并且同一个基因在合子激活前后表达亦有所不同。本研究通过qRT-PCR检测FGF4在牛早期胚胎中的表达规律,结果显示FGF4在牛的MⅡ期卵母细胞及各阶段的早期胚胎均有表达,与MⅡ期卵母细胞相比,2-细胞胚FGF4 mRNA表达量显著下降,随后持续增加,直至8-细胞期表达量显著高于MⅡ期卵母细胞,至桑椹胚阶段FGF4的表达量最高。这种表达规律可能是因为合子型基因激活前,母源因子FGF4维持了这段时期的细胞分裂,消耗其表达。但随着合子型基因的激活,FGF4的表达也得到了提高。

图2 FGF4在不同时期牛早期胚胎的分布
胚胎中细胞的分布决定细胞命运和极性[15],母源因子在胚胎极性形成时发挥重要作用,8-细胞期获得极性是决定细胞命运的关键时期[16]。本研究结果表明FGF4在MⅡ期卵母细胞及8-细胞期前的各阶段早期胚胎的细胞质和细胞核中均有表达,而在8-细胞期及之后的桑椹胚和囊胚期FGF4只在细胞质中表达,这可能是因为FGF4在胚胎发育中与胚胎发育极性相关,然而FGF4在牛胚胎中迁移具体的机制仍需进一步研究。在小鼠囊胚中,FGF4特异性表达在内细胞团中,是形成功能性内细胞团所必须的[3,17],通过影响种系特异性基因的分布,调控内细胞团分化原始内胚层的过程[18]。而本研究结果表明,牛囊胚中FGF4在内细胞团和滋养层中均有表达,并在内细胞团中表达水平较高,这与Takashi F及Manabu O的研究结果一致[19-20]。这可能是因为FGF4是一种分泌型蛋白,内细胞团能够分泌FGF4并通过旁分泌方式作用于滋养层细胞,其断裂的N端信号多肽通过结合并激活FGFRs作为细胞外蛋白介导生物反应,可与细胞溶质接头蛋白和RAS-MAPK、PI3K-AKT、PLCγ和STAT胞内信号旁路相互作用,从而进一步影响滋养层的增殖。另有研究表明,在胚胎附植后FGF4将调控功能性内细胞团的形成,并影响滋养层部分发育为胎盘组织的过程[7,21-22]。
本研究从mRNA和蛋白水平观察了FGF4在牛MⅡ卵母细胞及各阶段早期胚胎的表达模式,首次确定了FGF4在牛早期胚胎发育过程中的时空表达规律,为进一步研究FGF4基因在牛早期胚胎发育过程中的调控机制提供了依据。
[1] Ornitz D M, Itoh N. The fibroblast growth factor signaling pathway[J].Wiley Interdiscip Rev Dev Biol,2015,4(3):215-266.
[2] 邹 敏,江一平.Fgf4信号通路在早期胚胎发育过程中的作用[J].中外健康文摘,2012,15(9):17-18.
[3] Rappolee D A,Basilico C,Pate Y,et al.Expression and function of FGF-4 in peri-implantation development in mouse embryos[J].Development,1994,120:2259-2269.
[4] Krawchuk D,Yamanaka N H,Anani S,et al.FGF4 is a limiting factor controlling the proportions of primitive endoderm and epiblast in the ICM of the mouse blastocyst[J].Dev Biol,2013,384(1):65-71.
[5] Dailey L,Ambrosetti D,Mansukhani A,et al.Mechanisms underlying differential responses to FGF signaling[J].Cytokine Growth Factor Rev,2005,16(2):233-247.
[6] Feldman B,Poueymirou W,Papaioannou V E,et al.Requirement of FGF-4 for post-implantation mouse development[J].Science,1995,267:246-249.
[7] Goldin S N,Papaioannou V E.Paracrine action of FGF4 during peri-implantation development maintains trophectoderm and primitive endoderm [J].Genesis,2003,36(1):40-47.
[8] Rossant J,Cross J C.Placental development:Lessons from mouse mutants[J].Nat Rev Genet,2001,2(7):538-548.
[9] 李文哲.MicroRNA-145和microRNA-483对牛核移植胚胎早期发育的影响[D].陕西杨凌:西北农林科技大学,2016.
[10] Li E.Chromatin modification and epigenetic reprogramming in mammalian development[J].Nat Rev Genet,2002,3(9):662-673.
[11] 胥鹏飞,孟安明.斑马鱼母源因子在胚胎发育中的作用[J].中国科学:生命科学,2014(10):954-964.
[12] Christine B,Ecric N,Pascale D.Endogenous transcription occurs at the 1-cell stagein the mouseembryos[J].Exp Cell Res,1995,218(1):57-62.
[13] Schultz R M.Regulation of zygotic gene activation in the mouse[J].Bioessays,1993,15(8):531-538.
[14] Memili E,First N L.Zygotic and embryonic gene expression in cow: a review of timing and mechanisms of early gene expression as compared with other species[J].Zygote,2000,8(1):87-96.
[15] Johnson M H,Ziomek C A.The foundation of two distinct cell lineages within the mouse morula[J].Cell,1981,24(1):71-80.
[16] Hirate Y,Hirahara S,Inoue K,et al.Polarity-dependent distribution of angiomotin localizes hippo signaling in preimplantation embryos[J].Curr Biol,2013,23(13):1181-1194.
[17] Niswander L,Martin G R.Fgf-4 expression during gastrulation, myogenesis, limb and tooth development in the mouse[J].Development,1992,114(3):755-768.
[18] Kang M,Piliszek A,Artus J,et al.FGF4 is required for lineage restriction and salt-and-pepperdistribution of primitive endoderm factors but not theirinitial expression in the mouse[J].Development,2013,140(2):267-279.
[19] Fujii T,Moriyasu S,Hirayama H,et al.Aberrant expression patterns of genes involved in segregation of inner cell mass and trophectoderm lineages in bovine embryos derived from somatic cell nuclear transfer[J].Cell Reprogram,2010,12(5):617-625.
[20] Ozawa M,Sakatani M,Yao J Q,et al.Global gene expression of the inner cell mass and trophectoderm of the bovine blastocyst Fibroblast growth factor 4-induced migration of porcine trophectoderm cells is mediated via the AKT cell signaling pathway[J].BMC Dev Biol,2012,12(33):1-13.
[21] Magaia G V,Rodríguez A,Zhang H,et al.Paracrine effects of embryo-derived FGF4 and BMP4 during pig trophoblast elongation[J].Dev Biol,2014,387:15-27.
[22] Tanaka S,Kunath T,Hadjantonakis A,et al.Promotion of trophoblast stem cell proliferation by FGF4[J].Science,1998,12(282):2072-2075.

