标准通道经皮肾镜碎石术中肾盂内压的改变及对肾小球滤过率的影响*
(承德医学院附属医院 泌尿外科,河北 承德 067000)
经皮肾镜碎石术(percutaneous nephrolithotomy,PCNL)已经成为肾脏铸型结石及多发、复杂肾结石的常规治疗手段。无论是14F~18F的微创经皮肾镜碎石术(minimally invasive percutaneous nephrolithotomy,mPCNL),抑或24F~30F的标准通道PCNL,皮肾通道建立时除能引发肾实质撕裂出血外,高流量生理盐水灌注使肾盂内压增高可导致灌注液返流、细菌和内毒素吸收而继发感染、脓毒血症等。生理状况下人的肾盂内压力约7.35 mmHg[1]。肾脏的生理状态及自然的病理过程中,肾盂内压很少超过67.50 mmHg。尽管mPCNL通道直径变小,创伤减轻,输血率稍低于PCNL(1.4%和10.4%)[2],但手术视野小、操作空间窄、手术费时,对于铸型或复杂多发结石,带来了更多的残石及肾盂灌注压相对较高等问题,术中肾盂内压甚至高达200.00 mmHg[3-4]。标准PCNL通道直径变大,一期结石清除率为86.4%,二期可达97.3%[5],但该操作对术中肾盂内压的影响以及对肾脏早期功能的损伤情况,文献报道极少,标准通道PCNL及mPCNL孰优孰劣尚无定论。笔者对标准通道PCNL术中肾盂内压的变化进行了动态监测,并以99mTc-DTPA核素肾动态显像精确评估标准通道PCNL创伤对手术后早期肾脏功能的影响。
1 资料与方法
1.1 一般资料
2013年1月-2014年8月162例肾结石患者被选入研究组在我院接受了标准通道PCNL术,其中6例患者因其他脏器手术而终止PCNL退出研究,重度肾积水5例,因患肾肾小球滤过率(glomerular filtration rate,GFR)<10 ml/min均行肾切除术而未入组。本组男81例,女75例,年龄27~72岁,平均(48.04± 10.39)岁。根据B超有无肾积水及程度分为[6]:正常无积水组56例、轻度积水组62例、中度积水组38例。术前均行血尿常规、凝血功能、血生化、心电图、泌尿系B超、腹平片(kidney ureter bladder,KUB)、静脉尿路造影(intravenous urogram,IVU)及64层螺旋CT泌尿系统三维重建等检查。
1.2 手术适应证
肾结石直径>2.0 cm或体外冲击波碎石术(extracorporeal shock wave lithotripsy,ESWL)治疗失败的直径>1.5 cm的肾结石及上段输尿管结石为手术适应证。经腹部X线片测量结石最大纵径0.6~5.0 cm,平均(2.13±0.94)cm。最大横径0.5~3.0 cm,平均(1.51±0.61)cm。
1.3 排除标准
未纠正的凝血功能障碍、肾脏畸形(马蹄肾、重复肾、先天性肾脏旋转不良等)、脊柱畸形、合并严重感染未能有效控制者、严重心肺功能不全及病态肥胖患者被排除。由于肾盂内压受多种因素影响,故全部手术固定由一位主任医师操作。由于出血量过多易导致失血性休克,进而影响肾功能,故对术中术后出血≥400 ml或输血者排除在外。研究方案被医院伦理道德法制机构审查并批准。患者被告知研究内容,取得同意后予以签字。
1.4 手术操作及肾盂内压监测
患者全麻后取膀胱截石位,会阴部碘伏消毒铺无菌单。经膀胱镜向患侧输尿管逆行置入6F输尿管导管至肾盂内,同时留置18F气囊导尿管固定。留置的输尿管导管通过美国Medex压力传感器模块,密闭连接多参数监护仪(荷兰Philips MP30型)血压测量通道,压力传感器固定在肾盂平面,测压系统调零。术中实时监测记录肾盂内压变化。患者改俯卧位,腹部垫枕使腰背部成一平面。手术区常规碘伏消毒铺巾并贴无菌塑料薄膜。B超定位、引导下,17.5G穿刺针于第11肋间或第12肋下,腋后线与肩胛下线之间,选取后组肾盏穿刺,见尿液溢出,置入导丝,退出穿刺针。切开皮肤约8 mm,沿导丝以筋膜扩张器(德国UroVision)自10F、12F、14F至16F顺序扩张,置入Peel-Away鞘,再以18F、21F套叠式金属扩张器逐步扩张,推入24F金属镜鞘至肾集合系统内,建立标准通道,引入20.8F肾镜(德国Wolf)。以生理盐水作为灌流液,液压灌注泵加压灌注,灌注流量平均300 ml/min。采用瑞士EMS第三代气压弹道超声碎石清石系统碎石,气压弹道输出脉冲频率设定为8~12 Hz,超声能量输出设定在70.0%~80.0%,占空比70.0%。术后常规顺行留置6F双J管内引流,PCNL通道放置14F肾造瘘管引流。术后5 d夹闭造瘘管,复查KUB和B超,如残留结石直径≤0.5 cm,则拔除肾造瘘管,无漏尿1或2 d后拔除尿管,药物等排石治疗。如残石直径≥1.2 cm,1周后行二期取石;0.6~1.2 cm者行ESWL治疗。术后4周门诊复查拔除双J管。
1.5 核素肾动态显像检查
患者PCNL术前及术后1周接受核素肾动态显像检查。受试者检查前30 min饮水300 ml。患者取仰卧位,SPECT(美国GE公司InfiniaVC Hawkeye,配低能高分辨准直器)探头表面朝上置于检查床下,探头视野包括双肾区及腹主动脉。于肘静脉“弹丸”式注射99mTc-DTPA(北京原子高科股份有限公司,放化纯95%)8~12mCi后即刻行动态图像采集,先以1帧/2 s采集60 s,继以1帧/min采集20 min,共连续采集21 min,采集矩阵128×128,放大倍数1.0。注射显像剂前及采集结束后分别测量注射器内放射性计数。图像处理由仪器自带软件“Renal analysis”按计算机专用程序对左右肾及本底区勾画感兴趣区(region of interest,ROI),获得双肾动脉血流灌注曲线、功能相的肾图曲线,计算双肾GFR。
1.6 统计学方法
采用SPSS 19.0软件(Chicago,IL)处理数据。计量资料以均数±标准差(±s)表示,PCNL术前与术后GFR变化采用配对t检验,组间为方差分析。PCNL术前与术中肾盂内压变化采用独立样本t检验,术前与术后GFR变化和术中肾盂内压、手术时间、碎石时间、失血量参数间的相关性采用Pearson相关分析。以P<0.05为差异有统计学意义。
2 结果
2.1 PCNL碎石前、碎石中肾盂内压的变化
手术时间83~113 min,手术一期结石清除率75.0%。无术中、术后出血需输血者,无胸膜、腹腔器官损伤等严重并发症发生。正常组和轻度积水组碎石前、碎石中肾盂内压的变化差异无统计学意义(P>0.05)。中度积水组碎石中肾盂内压高于碎石前,差异有统计学意义(P<0.05)。碎石前3组间肾盂内压比较差异无统计学意义(P>0.05)。碎石中正常组与轻度积水组肾盂内压比较差异无统计学意义(P>0.05),中度积水组碎石中肾盂内压高于正常组和轻度积水组,差异有统计学意义(P<0.05)。术中可见肾盂内压瞬间升高,最高达67.00 mmHg,持续时间短暂,多发生于探针触碰导管或肾盂壁时。但各组平均肾盂内压,无论PCNL碎石前、碎石中,均<30.00 mmHg。见表1。
2.2 PCNL前后核素肾动态显像GFR比较
核素肾动态显像测定的PCNL围手术期GFR变化比较如表2所示。各组PCNL术前与PCNL术后GFR变化差异无统计学意义(P>0.05)。
表1 各组PCNL术前术中肾盂内压变化比较 (mmHg,±s)Table 1 Comparison of renal pelvic pressure during preoperative and intraoperative PCNL in different groups (mmHg,±s)
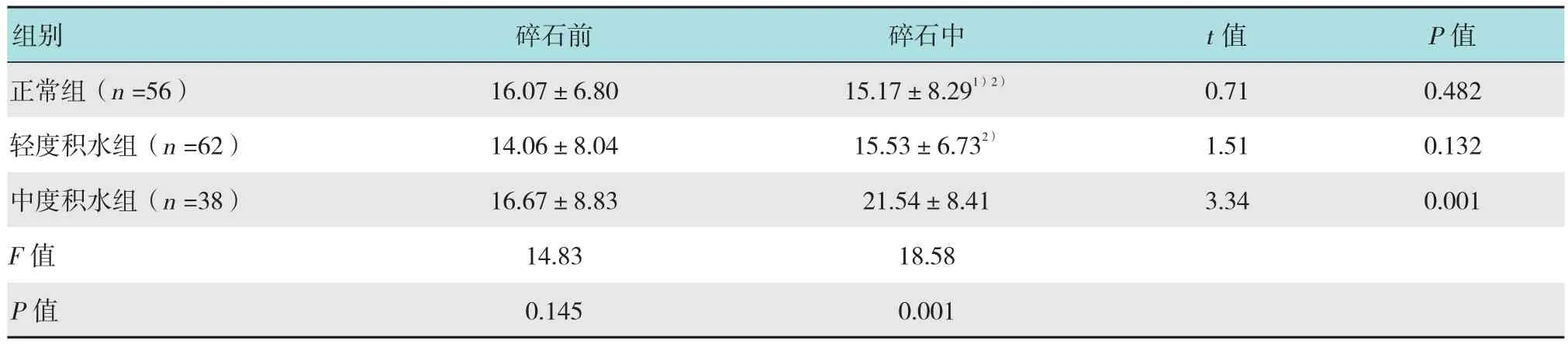
表1 各组PCNL术前术中肾盂内压变化比较 (mmHg,±s)Table 1 Comparison of renal pelvic pressure during preoperative and intraoperative PCNL in different groups (mmHg,±s)
注:1)与轻度积水组比较,P >0.05;2)与中度积水组比较,P <0.05
组别 碎石前 碎石中 t值 P值正常组(n =56) 16.07±6.80 15.17±8.291)2) 0.71 0.482轻度积水组(n =62) 14.06±8.04 15.53±6.732) 1.51 0.132中度积水组(n =38) 16.67±8.83 21.54±8.41 3.34 0.001 F值 14.83 18.58 P值 0.145 0.001
表2 PCNL前后核素肾动态显像GFR比较 (ml/min,±s)Table 2 Comparison of glomerular filtration rate during preoperative and postoperative PCNL in different groups (ml/min,±s)

表2 PCNL前后核素肾动态显像GFR比较 (ml/min,±s)Table 2 Comparison of glomerular filtration rate during preoperative and postoperative PCNL in different groups (ml/min,±s)
注:术前组间:1)与轻度积水组比较,P >0.05;2)与中度积水组比较,P <0.05;术后组间:3)与轻度积水组比较,P >0.05;4)与中度积水组比较,P <0.05
组别 PCNL术前 PCNL术后 t值 P值正常组(n =56) 43.98±11.901)2) 42.90±13.053)4) 0.79 0.465轻度积水组(n =62) 45.82±12.342) 43.97±12.294) 1.08 0.296中度积水组(n =38) 32.02±13.54 31.85±15.52 0.07 0.943 F值 4.33 3.65 P值 0.022 0.041
3 讨论
标准通道PCNL在处理复杂、多发、感染性结石及铸型结石上已充分显现高效、微创的特点。为保持术中视野清晰,需要灌注泵持续进行肾盂内生理盐水灌流。体外研究表明,高压灌注可提升肾盂内压力,引发肾盂静脉及淋巴管返流,导致发热、感染和脓毒血症等,严重者可危及患者生命。尽管肾盂内压受多重因素影响,但在结石大小相对固定、手术操作医师固定、手术流程稳定的情况下,肾积水状况及穿刺通道大小,更易影响肾盂内压。标准通道PCNL在临床上已得以普遍应用,尽管24F的标准操作通道较mPCNL增大,EMS超声弹道碎石清石系统也兼具负压吸引功效,但不同程度的积水肾在标准通道碎石中肾盂内压的变化情况,文献报道极少,而标准通道PCNL导致的微创伤对肾功能,尤其对伴有肾积水、肾功能不全的患肾功能的影响尚需深入研究。
HOLST等[1]报道生理状况下的肾盂内压力约7.35 mmHg(0.98 kPa)。体外研究表明,35.00 mmHg以上的肾盂压力会引起持续的肾盂静脉及淋巴管逆流,在存在感染时,15.00~18.00 mmHg的压力即可造成逆流[7]。14~18F通道的mPCNL在处理大结石时会延长手术时间,并发症发生率会相应增加。mPCNL由于通道狭小,碎石中的灌注冲洗更容易引起肾盂内压增高,导致反流及术后发热,压力最高可达生理状况下肾盂内压力的数十倍[8-9]。标准通道下PCNL的肾盂压力变化,文献鲜有报道。在肾结石合并积水情况下,标准通道PCNL对肾盂内压的影响尚不明确。本研究显示,当常规灌注流速平均300 ml/ min时,无积水正常组和轻度积水组碎石前、碎石中肾盂内压的变化差异无统计学意义(P>0.05)。中度积水组碎石中肾盂内压高于碎石前,差异有统计学意义(P <0.05)。碎石前无论是否合并肾积水及积水程度,各组肾盂内压差异无统计学意义(P >0.05)。碎石中,无积水正常组与轻度积水组肾盂内压比较差异无统计学意义,中度积水组碎石中肾盂内压高于正常组和轻度积水组(P <0.05)。结果提示,合并肾积水越重,碎石中肾盂内压越易升高。分析原因,积水加重后,集合系统容量变大,标准通道PCNL灌注的液体瞬间潴留量过多,不能迅速自管鞘流出,导致肾盂内压升高。肾盂内压高于肾实质返流极限值30.00 mmHg为肾盂内高压。尽管本实验各组平均肾盂内压无论PCNL碎石前、碎石中均<30.00 mmHg,但碎石中瞬间肾盂压可达67.00 mmHg,可能与探针过于挤压结石、黏膜组织或测压导管有关。肾盂压力增高时易致解剖最薄弱处肾盏穹隆部发生破裂,冲洗液经破裂处外渗至肾周或冲洗液进入肾间质,使肾内压升高并损伤肾小管。冲洗液还可通过管壁沿疏松的结缔组织渗出至肾周。因此,相对于mPCNL,虽然标准通道工作内径增大,灌注相对低压,结合超声气压弹道碎石清石系统(EMS)的使用,碎石排石效率更高,但对于积水明显的肾结石,也应注意灌注液的速度及排出通畅情况,尤其是感染性结石,更应避免因返流的发生而导致感染扩散、加重等。
随着24F的标准通道增大,是否意味着比14F~18F的mPCNL会造成更大的肾损伤,导致更多肾单位丧失而影响肾功能呢?HOLMAN等[10]报道8.0%~11.0%的患者PCNL术后血肌酐显著性升高,而DAWABA等[11]在PCNL术后2周检测患者肾功能,却发现其与术前相比差异无统计学意义。这些文献中肾功能评估指标多为反映总肾功能的血肌酐、肌酐清除率、尿β2MG等。GFR代表单位时间内肾脏生成的滤液量,可直接反映肾脏的过滤功能,而99mTc-DTPA是一种几乎全部被肾小球滤过而不被肾小管吸收和分泌的放射性物质,测定其清除率能精确反映GFR,被公认为是评价肾功能的金指标[12]。笔者采用99mTc-DTPA核素肾动态显像评估了标准通道PCNL创伤对手术后早期肾脏功能的影响,发现各组PCNL术前与PCNL术后1周时GFR变化差异无统计学意义(P>0.05)。活体猪动物模型病理实验研究观察到,当肾盂内灌流压达到26.66 kPa(约200.00 mmHg),透射电镜下可见肾近曲小管上皮细胞细胞器扩张,胞质内空泡形成,微绒毛紊乱、脱落等细胞受损表现[13],而本研究各实验组的平均肾盂内压,无论PCNL碎石前、碎石中均<30.00 mmHg,患者可很好地耐受PCNL手术所带来的影响。对猪进行16F、32F的经皮肾穿刺造瘘术,肾造瘘管于1周后拔除并尸检动物标本,实验研究显示16F和32F的肾造瘘道所致的瘢痕体积以及其所占整个肾皮质体积的百分率,两者比较差异无统计学意义,表明通道直径虽然增大,但并未增加肾皮质的损伤[14]。一些学者认为,mPCNL因手术视野小、操作空间窄、手术费时,术中肾盂内压明显较高,对于铸型或复杂多发结石,mPCNL只能作为标准PCNL的扩展而不能取代[15-16]。当然,标准通道PCNL不增加肾功能损伤的重要因素之一,还应保证术中术后较少的出血量等。
本研究结果显示,标准通道PCNL手术对无积水肾或轻度积水肾的肾盂内压无明显影响,对中度以上的肾积水,碎石手术中应注意灌注液的速度及排出通畅情况,避免因肾盂内压增高发生返流而导致感染。标准通道建立所造成的物理损伤并未对手术肾的功能产生显著影响。由于本组研究的病例数较少,仍需后续多中心、大样本的病例进行深入研究探讨。
[1]HOLST U, DISSING T, RAWASHDEH Y F, et al. Norepinephrine inhibits the pelvic pressure increase in response to flow perfusion[J]. J Urol, 2003, 170(1):268-271.
[2]CHENG F, YU W, ZHANG X, et al. Minimally invasive tract in percutaneous nephrolithotomy for renal stones[J]. J Endourol, 2010, 24(10):1579-1582.
[3]REHMAN J, MONGA M, LANDMAN J, et al. Characterization of intrapelvic pressure during ureteropyeloscopy with ureteral access sheaths[J]. Urol, 2003, 61(4):713-718.
[4]GUOHUA Z, WEN Z, XUN L, et al. The in fl uence of minimally invasive percutaneous nephr olithotomy on renal pelvic pressure in vivo[J]. Surg Laparosc Endosc Percutan Tech, 2007, 17(4):307-310.
[5]SUKUMAR S, NAIR B, GINIL K P, et al. Supracostal access for percutaneous nephrolithotomy:less morbid, more effective[J]. Int Urol Nephrol, 2008, 40(2):263-267.
[6]王新房. 临床技术操作规范-超声医学分册[M]//中华医学会.临床技术操作规范. 北京:人民军医出版社, 2007:128.
[6]WANG X F. Clinical technical operation speci fi cation-Ultrasound medical branch[M]// Chinese Medical Association. Clinical technology operation. Beijing:People’s Military Medical Publishing House, 2007:128. Chinese
[7]LOW R K. Nephroscopy sheath characteristics and intrarenal pelvic pressure:human kidney model[J]. J Endourol, 1999, 13(3):205-208.
[8]曾国华, 钟文, 李逊, 等. 微创经皮肾穿刺取石术中肾盂内压变化的临床研究[J]. 中华泌尿外科杂志, 2007, 28(2):101-103.
[8]ZENG G H, ZHONG W, LI X, et al. The variation of renal pelvic pressure during minimally invasive percutaneous nephrolithotomy[J]. Chin J Urol, 2007, 28(2):101-103. Chinese
[9]REHMAN J, MONGA M, LANDMAN J, et al. Characterization of intrapelvic pressure during ureteropyeloscopy with ureteral access sheaths[J]. Urology,2003, 61(4):713-718.
[10]HOLMAN E, KHAN A M, PÁSZTOR I, et al. Simultaneous bilateral compared with unilateral percutaneous nephrolithotomy[J]. BJU Int, 2002, 89(4):334-338.
[11]DAWABA M S, SHOKEIR A A, HAFEZ A, et al. Percutaneous nephrolithotomy in children:early and late anatomical and functional results[J]. J Urol, 2004, 172(3):1078-1081.
[12]CARLSEN O. The gamma camera as an absolute measurement device:determination of glomerular filtration rate in99mTc-DTPA renography using a dual head gamma camera[J]. Nucl Med Commun, 2004, 25(10):1021-1029.
[13]吴荣佩, 李晓飞, 郭颖, 等. 肾盂内高压灌流对肾单位结构影响的实验研究[J]. 中华泌尿外科杂志, 2006, 27(3):162-165.
[13]WU R P, LI X F, GUO Y, et al. Experimental study of nephron injury caused by high pressure intrapelvic perfusion and its clinical significance[J]. Chin J Urol, 2006, 27(3):162-165. Chinese
[14]曾国华, 李逊, 何朝辉, 等. 微创经皮肾取石术和传统经皮肾镜取石术对肾皮质损伤的比较[J].中华实验外科杂志, 2004, 21(12):1551-1552.
[14]ZENG G H, LI X, HE Z H, et al. Comparision of renal parenchymal injury after mini and standard percutaneous nephrolithotomy[J]. Chin J Exp Surg, 2004, 21(12):1551-1552. Chinese
[15]TEPELER A, AKMAN T, SILAY M S, et al. Comparison of intrarenal pelvic pressure during micro-percutaneous nephrolithotomy and conventional percutaneous nephrolithotomy[J]. Urolithiasis, 2014, 42(3):275-279.
[16]LAHME S, ZIMMERMANNS V, HOCHMUTH A, et al. Minimally invasive PCNL (mini-perc). alternative treatment modality or replacement of conventional PCNL[J]. Urologe A, 2008, 47(5):563-568.

