不同剂量布托啡诺经鼻给药超前镇痛对老年患者苏醒期术后寒战发病率的影响
杨林,孙德峰,何颖,张宇,韩俊,刘若传
(大连医科大学附属第一医院 1.神经电生理科,2.麻醉科,辽宁 大连 116011)
术后寒战(postoperative shivering)是麻醉苏醒期常见的并发症,其发生率从5%~60%不等,会使机体代谢增加、耗氧量增加,二氧化碳产生增多,严重者可能导致低氧血症和乳酸中毒[1-3]。这对于合并有高血压和冠状动脉粥样硬化性心脏病(简称冠心病)老年患者来说,无异于雪上加霜。目前预防和治疗术后寒战反应如哌替啶、曲马多等阿片类药物,因呼吸抑制、镇静过度以及恶心呕吐等不良反应而限制了其应用[4-6],阿片受体激动-拮抗剂布托啡诺(Butorphanol)是吗啡喃的衍生物,在镇痛的同时具有良好的镇静作用,其通过激动κ受体而产生镇痛作用,通过部分拮抗μ受体而降低恶心、呕吐等术后不良反应的发生,几乎无呼吸抑制作用,镇痛强度是吗啡的4~8倍,被越来越广泛地应用于临床麻醉或术后镇痛[7-8]。文献报道布托啡诺经鼻腔给药起效快、达峰时间20 m in,绝对生物利用度高[9]。本课题组前期研究表明,布托啡诺经鼻给药超前镇痛优于静脉给药和芬太尼经鼻给药途径[10],但其不同剂量经鼻给药超前镇痛对苏醒期术后寒战的影响尚不清楚。本研究拟观察不同剂量布托啡诺经鼻给药超前镇痛对行胃、结肠癌根治术的老年患者术后寒战发病率的影响,以期探寻能使术后寒战发病率低且副作用小的经鼻给药途径的最佳用药剂量。
1 资料与方法
1.1 一般资料
选择2014年1月1日-2016年9月30日在大连医科大学附属第一医院住院的全身麻醉下行胃、结肠癌根治术的老年患者360例,其中,男性172例,女性188例,年龄65~81岁,体重67~89 kg,美国麻醉医师协会(the American Society of Anesthesiologists,ASA)分级Ⅱ或Ⅲ级,无吸毒史,无神经肌肉疾病史,近期未服用抗凝、镇静剂、抗抑郁及镇痛药,肝肾功能正常。采用随机数字表法,将其随机分为5组(n=72):布托啡诺0.005 mg/kg组(B1组)、布托啡诺0.010 mg/kg组(B2组)、布托啡诺0.020 mg/kg组(B3组)及布托啡诺0.030 mg/kg组(B4组)及对照组(C组)。本研究已获该院医学伦理委员会批准,并与患者或其家属签署知情同意书。
1.2 麻醉方法
术前常规禁食6 h、禁水2 h,均未术前用药。麻醉方法选用气管内插管全凭静脉麻醉。B1、B2、B3及B4组分别于麻醉诱导前10 min按照各自剂量经鼻给予布托啡诺(商品名:诺扬,1 ml︰1 mg,江苏恒瑞医药股份有限公司,批号13061534,均由生理盐水补至3.5 ml);C组以等容量生理盐水替代。所有患者均予以静脉注射咪达唑仑0.05 mg/kg、舒芬太尼0.2μg/ kg、丙泊酚1 mg/kg、罗库溴铵0.3 mg/kg快速麻醉诱导,采用可视喉镜明视下插管,气管内插管完成后接麻醉机行机械通气,呼吸频率8~12次/min,吸呼比1︰2,潮气量8~10 ml/kg,分钟通气量100~120 ml/kg,氧浓度60%~70%,术中调节潮气量以维持呼气末二氧化碳分压35~45 mm Hg(1 mmHg=0.133 kPa)左右。予以静脉输注舒芬太尼0.2μg/(kg·h)、顺式阿曲库铵 0.15 ~ 0.30 mg/(kg·h)及丙泊酚2~3 mg/(kg·h)维持麻醉。术中先以0.5~1.0 ml/(kg·min)的速率静脉输注6%羟乙基淀粉130/0.4和乳酸钠林格氏液20~40 min,然后以0.25 ml/(kg·min)的速率维持,晶胶比3︰1,同时予以持续静脉输注甲氧明1.5~4.0μg/(kg·min)或乌拉地尔符合艾司洛尔维持平均动脉压(mean arterial pressure,MAP)波动幅度不超过基础值的20%,并及时调整丙泊酚的输注速度使脑电双拼指数(bispectral index,BIS)值控制在50~60左右,手术结束前15 min停止输注丙泊酚。待气管导管拔除、MAP稳定后停止输注血管活性药物。术毕立即将患者转至麻醉后监测治疗室(PACU),待改良Aldrete苏醒评分>12分,任何一项不低于1分后,送回病房。手术室环境温度为22~24℃,手术后恢复室环境温度为24~25℃,均未实施液体及保温毯加温。
1.3 经鼻给药方法
让患者仰卧于床上,头尽可能后仰,使鼻腔低于口咽部,鼻孔朝上,用简易滴鼻器(2 ml注射器顶端连接带有接头的硬膜外导管,在距接头2 cm处截断)滴注布托啡诺稀释液,滴药时可将药液顺着鼻孔一侧缓慢流下,让鼻腔侧壁起缓冲作用,以免药液直接入咽部而影响药物吸收;双侧鼻腔轮流滴注并在滴药后轻按两侧鼻翼2~3次,使药液布满鼻腔,保持原体位1 min,使药液充分吸收后嘱患者转为诊疗位[11]。
1.4 改良Aldrete麻醉苏醒评分标准[12]
①清醒程度:完全清醒2分,嗜睡但可唤醒1分,无反应0分;②活动能力:自主或遵医嘱活动四肢和抬头2分,自主或遵医嘱活动二肢和有限抬头1分,不能活动肢体或抬头0分;③血流动力学稳定程度:血压为麻醉前水平±20%以内者2分,血压为麻醉前水平±20%~49%以内者1分,血压为麻醉前水平±50%者0分;④氧合状态:呼吸空气血氧饱和度(简称SpO2)≥92%者2分,SpO2≥90%者1分,SpO2<90%者0分;⑤术后疼痛评估:无疼痛2分,中等疼痛可用口服药物处理1分,剧烈疼痛需注射药物0分;⑥呼吸稳定与否:能够深呼吸以及自主咳嗽2分,呼吸困难或受限,可能用口、鼻咽通气道者1分,呼吸暂停或微弱呼吸,需呼吸器治疗或辅助呼吸者0分;⑦术后恶心呕吐症状:能够饮用液体2分,恶心但未吐者1分,恶心呕吐者0分。
1.5 观察指标
入室后采用迈瑞(Beneview T8)常规监测心电图(ECG)、血压(BP)、心率(HR)、SpO2、中心体温(鼻咽温度),行桡动脉及颈内静脉穿刺置管,用于监测有创动脉压及中心静脉压(central venous pressure,CVP)。使用HXD-1型脑电多功能监测仪监测BIS。统计手术时间、麻醉苏醒时间(停药到呼之睁眼的时间)、拔管时间(停止麻醉用药到拔除气管导管时间)、在PACU内停留时间、术中舒芬太尼和丙泊酚的用量及苏醒期恶心呕吐、喉痉挛、呼吸抑制等不良反应的发病率,并进行术后寒战评级及拔管后5 min口述镇痛评分。
1.6 寒战强度分级
寒战强度分级[13]:0级,无寒战;Ⅰ级,竖毛或(和)外周血管收缩或(和)外周青紫,但无肌颤;Ⅱ级,仅1组肌群肌颤;Ⅲ级,超过1组肌群肌颤;Ⅳ级,全身肌颤。Ⅲ、Ⅳ级持续3 min仍不消失判定为寒战。
1.7 口述镇痛评分标准
口述镇痛评分标准[14]:0分:无痛;1分:轻微疼痛;2分:中等疼痛;3分:剧烈疼痛。
1.8 统计学方法
采用SPSS 22.0统计学软件进行数据分析,计量资料以均数±标准差(±s)表示,组间比较采用单因素方差分析,运用SNK-q检测法进行各组间的两两比较,计数资料组间比较采用χ2检验,运用分割法进行各组间的两两比较。P<0.05为差异有统计学意义。
2 结果
2.1 5组患者一般情况和手术情况各指标的比较
5组患者年龄、体重、ASA分级、高血压和冠心病的病例及合并肺部疾患的病例数等一般情况及丙泊酚用量等比较差异无统计学意义(P>0.05),与B1及C组比较,B2、B3及B4组舒芬太尼用量明显减少(P<0.05)(见表1)。与B1、B4及C组比较,B2及B3组的麻醉苏醒时间、拔管时间、在PACU内停留时间明显缩短(P<0.05),而手术时间5组差异无统计学意义(P>0.05)(见表2)。与B1及C组比较,B2、B3及B4组的苏醒期恶心呕吐、呼吸抑制及喉痉挛的发病率及拔管5 min口述镇痛评分差异有统计学意义(P<0.05)(见表 3)。B2、B3 及 B4 组的寒战评级Ⅲ级和Ⅳ级的例数及寒战发病率低于B1及C组(P<0.05)(见表 4)。
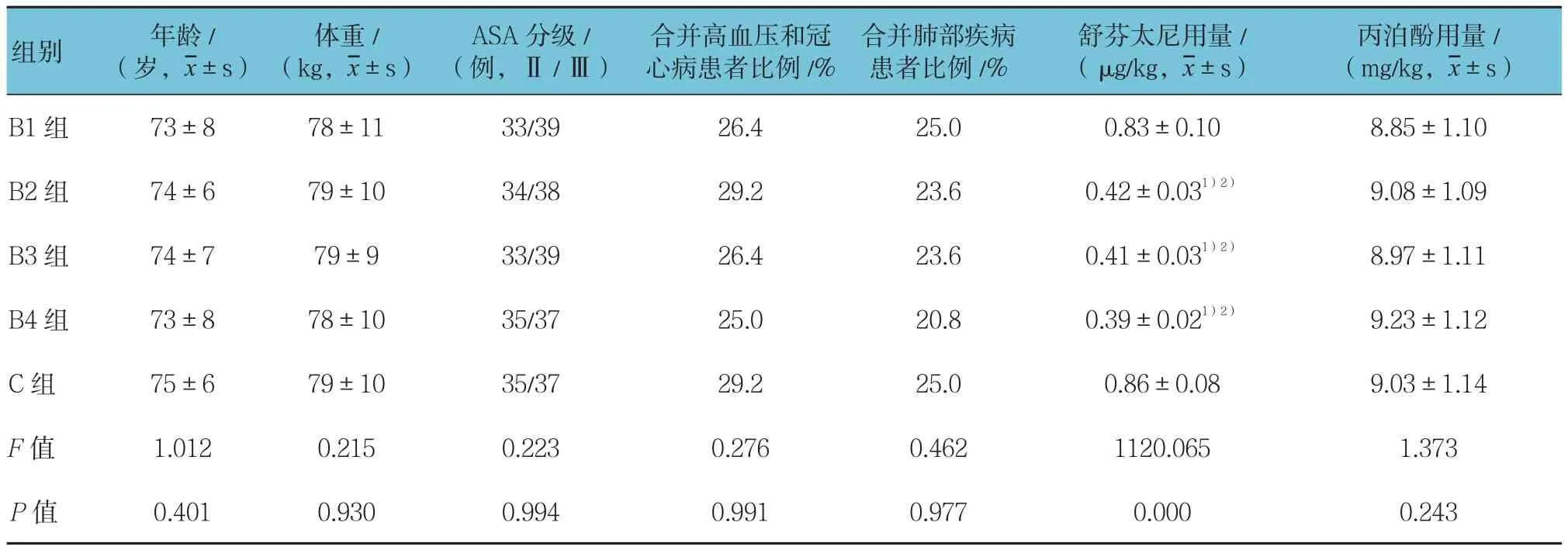
表1 5组患者一般情况和手术情况各指标的比较 (n =72)
表2 5组患者在手术、苏醒、拔管及在PACU内停留时间的比较 (n =72,min,±s)
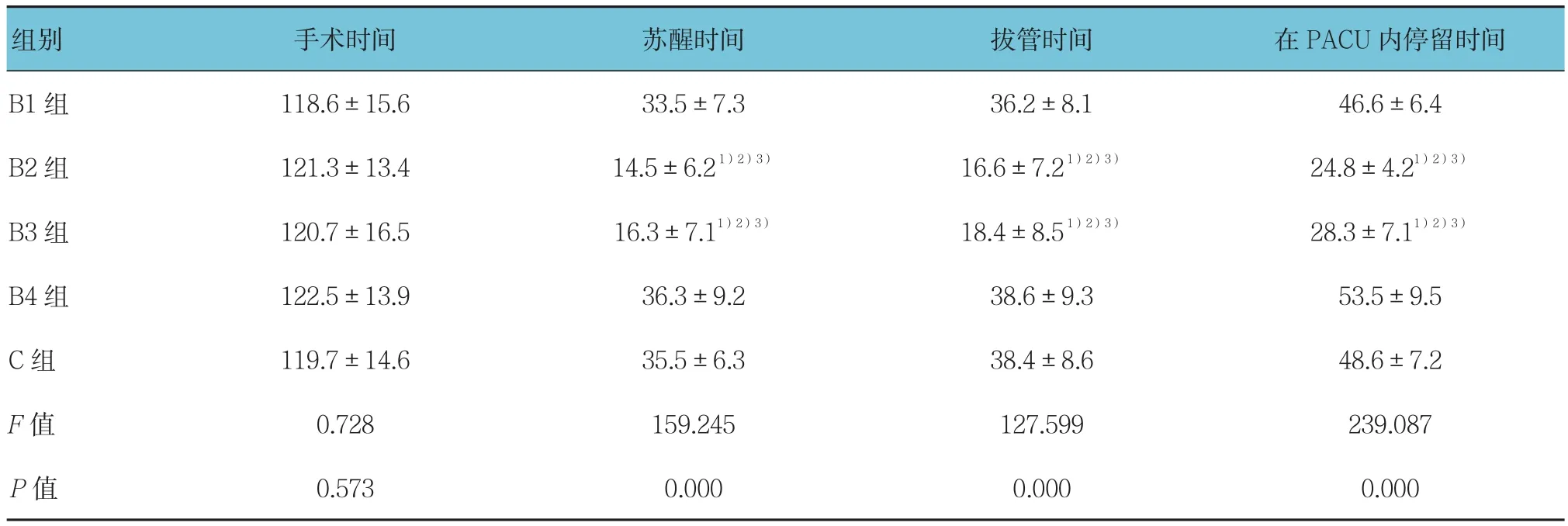
表2 5组患者在手术、苏醒、拔管及在PACU内停留时间的比较 (n =72,min,±s)
注:1)与 B1组比较,P <0.05;2)与 C 组比较,P <0.05;3)与 B4组比较,P <0.05
组别 手术时间 苏醒时间 拔管时间 在PACU内停留时间B1 组 118.6±15.6 33.5±7.3 36.2±8.1 46.6±6.4 B2 组 121.3±13.4 14.5±6.2 1)2)3) 16.6±7.2 1)2)3) 24.8±4.21)2)3)B3 组 120.7±16.5 16.3±7.11)2)3) 18.4±8.5 1)2)3) 28.3±7.11)2)3)B4 组 122.5±13.9 36.3±9.2 38.6±9.3 53.5±9.5 C 组 119.7±14.6 35.5±6.3 38.4±8.6 48.6±7.2 F值 0.728 159.245 127.599 239.087 P值 0.573 0.000 0.000 0.000
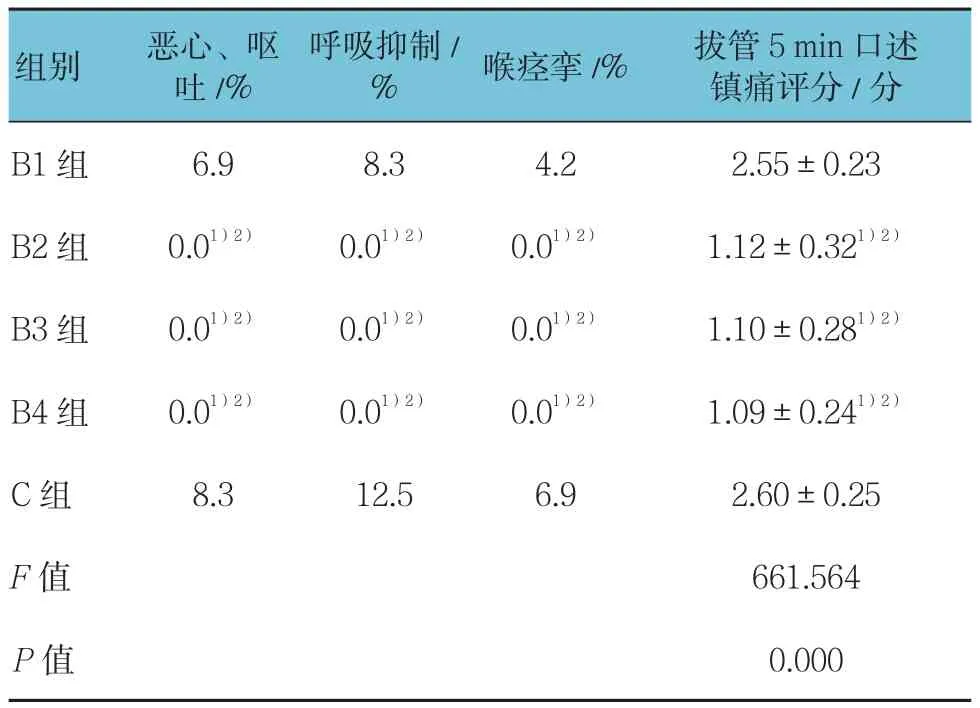
表3 五组患者麻醉苏醒期不良反应发病率的比较 (n =72)
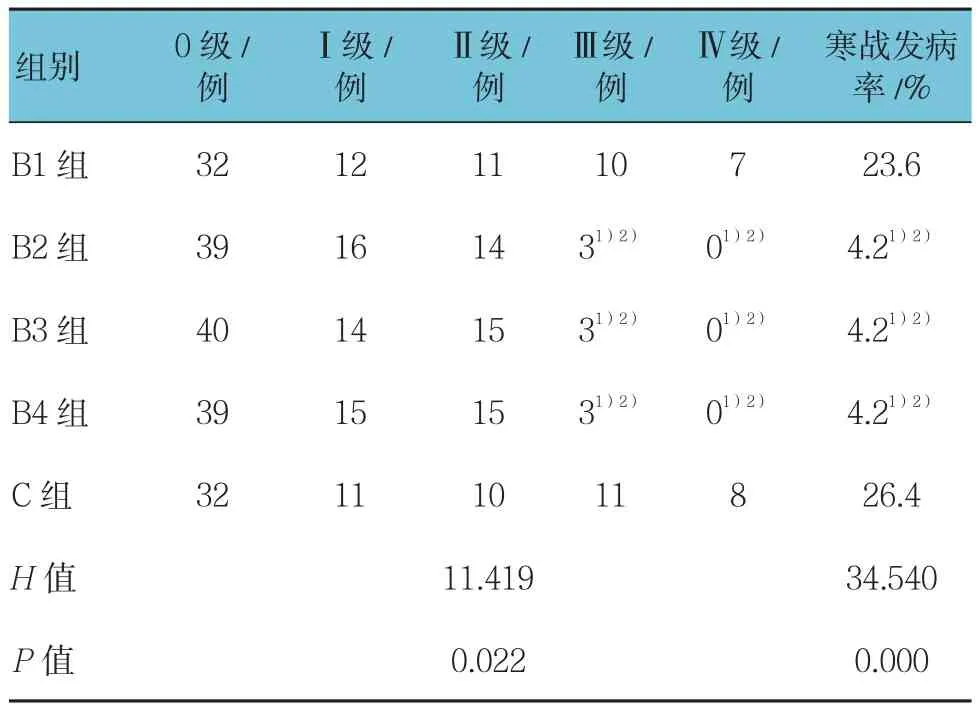
表4 5组患者术后寒战发生情况比较 (n =72)
3 讨论
人类的体温包括表层体温和深层体温(中心体温),中心体温一般维持在1个极其狭窄的阈值范围内(>0.40℃),期间无体温调节反应。但当体温高于或低于该阈值范围时,人体开始体温调节反应,即寒冷时血管收缩、寒战;受热时血管舒张、出汗。寒战是机体的正常生理反应,而对于麻醉手术后的患者,寒战是一种应激反应,其会对患者的生理、心理造成不良影响。术中由于麻醉药物影响人体新陈代谢产热减少、暴露的体表与寒冷外周环境的热交换、静脉通路开放导致外周-核心体温的再分布及腹腔较凉液体冲洗等原因可使机体体温下降。低体温会使药物代谢率降低、苏醒延迟,易发生低血压、心律失常、心肌缺血及呼吸性酸中毒。全身麻醉期间因患者意识丧失,不存在行为性体温调节反应,且由于所有的全身麻醉药都可明显抑制正常的自主体温调节机制[15-16],使发汗阈值轻度升高、寒战阈值明显降低,因此全身麻醉期间尤其在使用肌肉松弛药时不会出现寒战反应,无法使体温得以恢复。而全身麻醉患者麻醉苏醒期发生寒战,可能是体温调节中枢功能恢复后对于核心体温下降的反应及术后疼痛引起。中心体温降低是大多数麻醉后寒战发生的最主要原因[13]。
既往研究结果表明,疼痛产生的过程中,神经系统具有某种“可塑性”,在疼痛发生之前予以镇痛药,可影响神经系统的这种“可塑性”,可能产生较完全性传导阻滞,从而减少或消除伤害引起的疼痛,达到镇痛的目的[17-18]。经鼻给药方式因药物生物利用率较高而被广泛应用于临床[9],本课题组前期研究表明,布托啡诺经鼻给药超前镇痛可有效地抑制阻塞性睡眠呼吸暂停低通气综合征(OSAHS)老年患者改良悬雍垂成形术(H-UPPP)术后疼痛,且可减少术后镇痛药用量及术后认知功能障碍(POCD)的发病率,其优于静脉给药和芬太尼经鼻给药途径[10]。
本研究中,B2、B3及B4组的恶心呕吐、呼吸抑制及喉痉挛的发病率显著低于B1及C组,其可能与术中舒芬太尼用量较少有关,而布托啡诺0.01~0.02 mg/kg经鼻给药超前镇痛苏醒期术后寒战发病率及寒战评级III级、IV级例数低的原因,可能与拔管5 min口述镇痛评分较低以及布托啡诺拥有的较佳的镇静效应有关。由于布托啡诺主要激动κ受体,在产生较好镇痛的同时兼具有良好的镇静作用,既可使患者苏醒期免于疼痛等不良刺激,又可能因其较好的镇静作用,使寒战阈值降低,从而有效地降低苏醒期术后寒战的发病率。当然,术中控制合适室温,减少热量的散失,防止体热的再分布,附以液体加温及应用加温毯,尽可能维持术中体温平衡,才是降低术后寒战发病率的根本。至于B2及B3组的麻醉苏醒时间、拔管时间、在PACU内停留时间明显短于B1、B4及对照组,可能与舒芬太尼及布托啡诺用量较少有关,同时也暗示B4组尽管术后寒战发病率较低,但由于其麻醉苏醒时间、拔管时间、在PACU内停留时间明显长于B2及B3两组,说明布托啡诺0.03 mg/kg这个剂量经鼻给药可能因镇静作用过强而不利于老年人麻醉后恢复。
综上所述,布托啡诺0.01~0.02 mg/kg经鼻给药超前镇痛可较显著地降低老年患者苏醒期术后寒战的发病率,且术后恶心、呕吐等其他并发症明显减少,无苏醒延迟,值得在临床推广。
[1]ALFONSI P. Postanaesthetic shivering epidemiology,pathophysiology and approaches to prevention and management[J].Drugs, 2001, 61(15): 2193-2205.
[2]BUGGY D J, CROSSLEY A W. Thermoregulation, mild perioperative hypothermia and postoperative shivering[J]. Br J Anaesth, 2000, 84(5): 615-628.
[3]DAL D, KOSE A, HONCA M, et al. Efficacy of prophylactic ketamine in preventing postoperative shivering[J]. Br J Anaesth,2005, 95(2): 189-192.
[4]TSAI Y C, CHU K S. A comparison of tramadol, amitriptyline, and meperidine for postepidural anesthetic shivering in parturients[J].Anesth Analg, 2001, 93(5): 1288-1292.
[5]SAGIR O, GULHAS N, TOPRAK H, et al. Control of shivering during regional anaesthesia: prophylactic ketamine and granisetron[J]. Acta Anaesthesiol Scand, 2007, 51(1): 44-49.
[6]HORN E P, STANDL T, SESSLER D, et al. Physostigmine prevents postanesthetic shivering as does meperidine or clonidine[J].Anesthesiology, 1998, 88(1): 108-113.
[7]LI X, XIAO Q, LI W. Comparison of the effects of dezocine,fentanyl, and placebo on emergence agitation after sevoflurane anesthesia in children[J]. Int J Clin Pharmacol Ther, 2015, 53(3):241-246.
[8]DU B X, SONG Z M, WANG K, et al. Butorphanol prevents morphine-induced pruritus without increasing pain and other side eff ects: a systematic review of randomized controlled trials[J]. Can J Anaesth, 2013, 60(9): 907-917.
[9]DAVIS G A, RUDY A, ARCHER S M, et al. Bioavailability of intranasal butorphanol administered from a single-dose aprayer[J].J Health Syst Pharm, 2005, 62(1): 48-53.
[10]YANG L, SUN D F, WU Y, et al. Intranasal administration of butorphanol benefits old patients undergoing H-uvulopalatopharyngoplasty: a randomized trial, BMC Anesthesiology, 2015,15: 20.
[11]刘冬冬, 王树波, 张瑞芹, 等. 芬太尼与舒芬太尼鼻腔给药用于无痛肠镜的效果比较[J]. 临床麻醉学杂志, 2011, 27(2):163-166.
[12]ALDRETE J A, KROULIK D. The Post-Anesthesia Recovery Score Revisited[J]. J Clin Anesth, 1995, 7(1): 89-91.
[13]CROSSLEY A W, MAHAJAN R P. The intensity of postoperative shivering is unrelated to axillary temperature[J]. Anaesthesia,1994, 49(3): 205-207.
[14]GUIGNARD B, BOSSAND A E, COSTE C, et al. Acute opioid tolerance:intraoperative remifentanil increases postoperative pain and morphine requirement[J]. Anesthesiology, 2000, 93(2): 409-417.
[15]XIONG J, KURZ A, SESSLER D I, et al. Isoflurane produces marked and nonlinear decreases in the vasoconstriction and shivering thresholds[J]. Anesthesiology, 1996, 85(2): 240-245.
[16]MATSUKAWA T, KURZ A, SESSLER D I, et al. Propofol linearly reduces the vasoconstriction and shivering thresholds[J].Anesthesiology, 1995, 82(5): 1169-1180.
[17]GOTTSCHALK A, SMITH D S. New concepts in acute pain therapy: preemptive analgesia[J]. Am Fam Physician, 2001,63(10): 1979-1984.
[18]KISSIN I. Preemptive analgesia[J]. Anesthesiology, 2000, 93(4):1138-1143.

