安徽省食管癌分级诊疗指南
(2016版)
一、我国及我省食管癌的现状
食管癌是世界上第九大肿瘤,全世界每年约有40万人死于食管癌。从世界范围来看,亚洲、东南非洲、法国北部和南美洲为食管癌高发区。作为亚洲的人口大国,我国是食管癌的高发国家,又是食管癌死亡率最高的国家,其发病率在国内所有恶性肿瘤中居第5位,而死亡率居第4位。在欧美发达国家,食管癌以腺癌为主。在我国,食管癌中95%以上是鳞状细胞癌,少数为起源于食管腺体或异位胃粘膜的腺癌,偶见有腺鳞癌或腺棘癌。食管癌的发病在我国呈现明显的地区差异,一定区域内的绝对高发与周边地区的相对低发形成鲜明对照,构成我国食管癌最典型的流行病学特征。根据国家防癌办第三次肿瘤普查资料,食管癌的高发省份为河北、河南、福建和重庆,其次为新疆、江苏、山西、甘肃和安徽。我省为食管癌高发省份,近年来食管癌发病率逐年上升,尤其是皖北、皖东和大别山区。全省各地医疗卫生条件差异很大,医院医疗仪器、设备及医疗技术水平参差不齐,由此造成食管癌诊治过程中的诊断标准把握不一,治疗方法不规范的情况时有发生。
二、食管癌病因、定义及分类
(一)食管癌病因
食管癌的确切病因目前尚不清楚。食管癌的发生与该地区的生活条件、饮食习惯、存在强致癌物、缺乏一些抗癌因素及有遗传易感性等有关。
(1)亚硝胺类化合物和真菌毒素
①亚硝胺是被公认的化学致癌物,其前体包括硝酸盐、亚硝酸盐、二级或三级胺等,在高发区的粮食和饮水中,其含量显著增高,且与当地食管癌和食管上皮重度增生的患病率呈正相关。国内已成功用甲苄亚硝胺诱发大鼠的食管癌,并证实亚硝胺能诱发人食管鳞状上皮癌。
②真菌毒素的致癌作用各种霉变食物能产生致癌物质。镰刀菌、白地霉菌、黄曲霉菌和黑曲霉菌等真菌不但能还原硝酸盐为亚硝酸盐,并能增加二级胺的含量,促进亚硝胺的合成。霉菌与亚硝胺协同致癌。
(2)饮食刺激与食管慢性刺激
一般认为食物粗糙、进食过烫,咀嚼槟榔或烟丝等习惯,造成对食管黏膜的慢性理化刺激,可致局限性或弥漫性上皮增生,形成食管癌的癌前病变。慢性食管疾病如腐蚀性食管灼伤和狭窄、胃食管反流病、贲门失弛缓症或食管憩室等患者食管癌发生率增高,可能是由于食管内容物滞留而致慢性刺激所致。
(3)营养因素
饮食缺乏动物蛋白、新鲜蔬菜和水果,摄入的维生素A、B2和C缺乏,是食管癌的危险因素。流行病学调查表明,食物、饮水和土壤内的元素钼、硼、锌、镁和铁含量较低,可能与食管癌的发生间接相关。
(4)遗传因素
食管癌的发病常表现家族性聚集现象。在我国高发地区,本病有阳性家族史者达25%~50%,其中父系最高,母系次之,旁系最低。食管癌高发家族的外周血淋巴细胞染色体畸变率较高,可能是决定高发区食管癌易感性的遗传因素。调查还发现林县高发区居民迁至他县后,食管癌发病率与死亡率仍保持较高水平。这些现象说明遗传与食管癌有一定的关系。
(5)癌基因
环境和遗传等多因素引起食管癌的发生,其涉及的分子生物学基础,目前认为是癌基因激活或抑癌基因失活的基因变化所致,研究已证实的有Rb、P53等抑癌基因失活,以及环境等多因素使原癌基因H—ras、C-myc和hsl-1等激活有关。
(6)人乳头状病毒
一些研究发现食管上皮增生与乳头状病毒感染有关,食管上皮增生则与食管癌有一定关系。但两者确切的关系有待进一步研究。
(二)食管癌定义
(1)食管癌
从下咽到食管胃结合部之间食管上皮来源的癌。
①食管鳞状细胞癌
食管鳞状细胞分化的恶性上皮性肿瘤。
②食管腺癌
主要起源于食管下1/3的Barrett粘膜的腺管状分化的恶性上皮性肿瘤,偶尔起源于上段食管的异位胃粘膜,或粘膜和粘膜下腺体。
(2)早期食管癌
指局限于食管粘膜和粘膜下层的肿瘤,不伴淋巴结转移,包括原位癌、粘膜内癌和粘膜下癌。
(3)Barrett食管
指食管下段的复层鳞状上皮被单层柱状上皮所代替。
(4)食管的癌前疾病和癌前病变
癌前疾病包括慢性食管炎、Barrett食管、食管白斑症、食管憩室、贲门失弛缓症、食管息肉、食管溃疡、食管黏膜损伤、返流性食管炎和食管良性狭窄等。
癌前病变指鳞状上皮不典型增生,包括轻度、中度和重度不典型增生。
(三)食管癌分类
(1)食管的分段(AJCC/UICC,2009第7版)
①颈段食管,上自下咽,下达胸廓入口即胸骨上切迹水平。周围毗邻气管、颈血管鞘和颈椎。内镜下测量距上切牙15~20 cm。
②胸上段食管,上起胸廓入口,下至奇静脉弓下缘水平。其前面被气管、主动脉弓及分支和头臂静脉包围,后面为胸椎。内镜下测量距上切牙20~25 cm。
③胸中段食管,上起奇静脉弓下缘,下至下肺静脉水平。其前方是两个肺门之间结构,左邻胸降主动脉,右侧游离直接与胸膜相贴,后方为胸椎。内镜下测量距上切牙25~30 cm。
④胸下段食管,上起自下肺静脉水平,下至胃。其前邻心包,后邻脊椎,左为胸降主动脉,右为胸膜。内镜下测量距上切牙30~40 cm。
(2)食管癌的分类
①食管癌的大体分型
早期食管癌:包括隐伏型、糜烂型、斑块型和乳头型。
中晚期食管癌:包括髓质型、蕈伞型、溃疡型、缩窄型和腔内型。
②WHO食管癌组织学分类(见附录1)
三、食管癌的筛查、诊断与评估
(一)食管癌的筛查
(1)筛查对象
根据我国国情、食管癌危险因素及流行病学特征,符合下列①和②~⑥中任一项者应列为食管癌高危人群,建议作为筛查对象:①年龄>40岁;②来自于食管癌高发区;③有上消化道症状;④有食管癌家族史;⑤患有食管癌前疾病或癌前病变;⑥具有其他食管癌高危因素(吸烟、重度饮酒、头颈部或呼吸道鳞癌)。
(2)筛查方法
内镜和活检病理检查是目前诊断食管癌的金标准。内镜下食管黏膜碘染色加指示性活检的组合操作技术,已成为我国现阶段最实用有效的筛查方法。食管造影检查具有方便快捷、经济实惠及痛苦小等优点,也可作为初步体检和筛查的方法之一。既往使用的食管拉网细胞学检查等筛查方法因诊断效能及接受度等问题,已基本被淘汰,不作推荐。早期食管癌内镜筛查流程见图1

图1 早期食管癌筛查及内镜精查流程图
SM1:肿瘤累及黏膜下层上1/3
SM2:肿瘤累及黏膜下层中1/3
(二)食管癌的诊断
(1)诊断依据
①高危因素
食管癌高发区,年龄在45岁以上,有肿瘤家族史或者有食管癌的癌前疾病或癌前病变者是食管癌的高危人群。
②症状
1.吞咽食物时有梗噎感、异物感、胸骨后疼痛,或明显的吞咽困难,或长期有反酸、嗳气、吐粘液等,考虑有食管癌的可能,应进一步检查。
2.吞咽食物时有梗噎感、异物感、胸骨后疼痛一般是早期食管癌的症状,而出现明显的进行性吞咽困难一般提示食管病变为进展期。
3.临床诊断为食管癌的病人出现胸痛、背痛、咳嗽、呼吸困难、发热、贫血、声音嘶哑、饮水呛咳、呕血等,应考虑有食管癌外侵周围器官的可能。
③体征
1.大多数食管癌病人无明显相关阳性体征。
2.临床诊断为食管癌的病人近期出现头痛、恶心或其他神经系统症状和体征,骨痛、肝肿大、皮下结节、颈部淋巴结肿大等提示远处转移的可能。
④辅助检查
1.影像学检查:
a.食管造影检查:食管、胃钡餐造影X线透视或摄片是诊断食管癌和胃食管交界部肿瘤最常用的方法,病变部位的黏膜改变是观察的重点,可以确定癌灶的部位和长度。
b.CT检查:颈、胸、腹部增强CT应作为食管癌术前的常规检查,主要用于食管癌临床分期、可切除性评价、手术径路的选择和术后随访。
c.超声检查:可用于发现腹部重要器官及腹腔淋巴结有无转移,也用于颈深部淋巴结的检查。
d.MRI:可在冠状面和矢状面成像,可为放疗定位提供信息,可用于明确肿瘤和气管隆突、左肺动脉及降主动脉的关系。
e.PET-CT:在评价食管癌远处转移、外侵范围及程度、发现早期食管癌和评估放化疗的效果方面优于普通CT。
2.实验室检查:血常规、肝功能、肾功能、血糖、电解质以及肿瘤标记物:TPA(组织多肽抗原)、CEA(癌胚抗原)、cyfra21-1(细胞角质素片段19)、SCC(鳞癌相关抗原)等。
3.肺功能,心电图,心功能等检查。
4.组织学或细胞学检查:
a.食管镜活组织学检查或食管脱落细胞学检查:食管镜检查是食管癌诊断中常规且必不可少的。对于食管脱落细胞学检查阳性,影像学检查无明显阳性发现者必须行食管镜检查。
b.食管内镜超声(EUS):是评价食管癌临床分期最重要的检查手段,判断食管癌的浸润层次、向外扩展深度以及有无纵膈淋巴结或腹腔脏器转移等,对指导外科行根治性切除可能性有帮助,对T和N分期的准确性优于CT检查。另外可行定位穿刺组织学检查,对复杂、疑难、常规检查手段难以诊断的患者更具有优势。
c.色素内镜:主要用于高发区高危人群是食管癌的筛查,可进一步提高食管癌的阳性检出率,有碘染色法、亚甲蓝染色法。
d.支气管镜检查:对于癌变位于隆突以上的食管癌拟手术病例,应行支气管镜检查以明确气管、支气管有无受侵。
e.锁骨上淋巴结活检:如锁骨上或颈部淋巴结肿大,可行穿刺或切取活检,以确定有无转移。
f.胸腔镜、腹腔镜和纵膈镜检查:是评估食管癌分期的有效方法,与无创伤性检查比较,可以更加准确的判断食管癌局部侵犯、淋巴结以及远处转移情况,另外还可以用来判断进展型食管癌患者新辅助治疗的效果。
2.诊断
(1)临床诊断
①吞咽食物时有梗噎感、异物感、胸骨后疼痛或出现明显的吞咽困难,食管造影:早期可见食管粘膜皱襞紊乱、粗糙、或有中断现象;小的充盈缺损;局限性管壁僵硬或钡剂滞留;小龛影等表现。中晚期则有管腔不规则改变伴充盈缺损,黏膜皱襞消失、中断、排列紊乱与破坏;食管壁僵硬、管腔狭窄;溃疡龛影;病变食管周围软组织块影;巨大充盈缺损和管腔增宽;病变段以上食管扩张。
②吞咽食物时有梗噎感、异物感、胸骨后疼痛或出现明显的吞咽困难,胸部CT检查发现食管管壁的环形增厚或不规则增厚。
临床诊断:根据高危人群、临床症状、临床体征、影像学检查以及内镜检查,拟诊食管癌病例需经病理学检查确诊。
(2)病理诊断
经细胞学或组织病理学检查明确者可诊断为食管癌。
①食管镜检查刷片细胞学或活检阳性,早期病变多限于黏膜(原位癌),表现为:局限性黏膜糜烂;黏膜粗糙呈小颗粒感;边界不清的局部黏膜充血;小结节、小斑块或小溃疡。中、晚期则表现为:结节状或菜花状肿物,黏膜充血水肿、糜烂或苍白僵硬,触之易出血,见溃疡,部分有不同程度的管腔狭窄。
②食管癌的发展过程中,形态学有明显的改变,根据原发肿瘤大体标本的外观形态,可分为早期和中晚期两大类:
早期食管癌分为四型:隐伏型(充血型)、糜烂型、斑块型和乳头型。其中以斑块型为最多见,癌细胞分化较好,糜烂型次之,癌细胞分化较差。隐伏型是食管癌最早期的表现,多为原位癌。乳头型病变较晚,但癌细胞分化一般较好。
中晚期分为四型:
a.髓质型:管壁明显增厚并向腔内外扩展,使癌瘤的上下端边缘呈坡状隆起,切面呈灰白色均匀致密的实体肿块。
b.蕈伞型:瘤体呈卵圆形扁平肿块状,向腔内呈蘑菇样突起。隆起的边缘与其周围的黏膜境界清楚,瘤体表面多有浅表溃疡,其底部凹凸不平。
c.溃疡型:瘤体的黏膜面呈深陷而边缘清楚的溃疡。溃疡的大小和外形不一,深入基层,阻塞程度较轻。
d.缩窄型:瘤体形成明显的环形狭窄,累及食管全部周径。
③临床诊断为食管癌,食管外病变(锁骨上淋巴结、皮肤及其他部位结节)经活检或细胞学检查明确诊断者。
(3)鉴别诊断
早期无吞咽困难时,应与食管炎、食管憩室及食管静脉曲张等疾病相鉴别;中晚期有吞咽困难时,应与食管良性肿瘤、贲门失迟缓症和食管良性狭窄等疾病相鉴别。
①食管良性狭窄:食管化学性烧伤或返流性食管炎引起的瘢痕狭窄。前者以儿童及年轻人较多,一般由误服强酸或强碱的历史,后者病变一般位于食管下段,常伴有食管裂孔疝或先天性短食管。鉴别主要靠食管造影、食管镜及活检。
②贲门痉挛:主要症状为间歇性吞咽困难,病程长,间歇性发作,病人平均年龄较轻,食管造影和食管镜检查有典型的改变。
③食管憩室:食管中段的憩室常有吞咽障碍、胸骨后疼痛等症状,而吞咽困难较少。食管憩室有发生癌变的机会,因此在诊断食管憩室的时候应避免漏诊。
④食管结核:少见,可有吞咽困难,影像学表现为食管粘膜破坏,鉴别主要靠食管镜及活检。
⑤食管其他肿瘤:以平滑肌瘤常见,一般症状较轻,X线检查表现为“涂抹征”,进一步鉴别主要依靠胸部CT及食管镜检查,一般不取活检。食管其他恶性肿瘤如食管肉瘤,临床表现不易与食管癌鉴别,鉴别诊断依靠X线检查和食管镜检查。
⑥其他:如功能性吞咽困难,重症肌无力,食管功能性痉挛以及食管外压迫,均须根据患者病史、症状、体征以及X线检查和食管镜检查来鉴别。
(三)食管癌的评估
食管癌的术前评估
(1)临床TNM分期
是指在术前通过有创或无创的方法获取所有相关的临床信息进行的分期。术前分期主要是确定病变范围、有无远处脏器转移、有淋巴结受累及周围组织局部侵犯,准确的术前分期将有助于选择合理的治疗方案。而要准确了解与肿瘤分期相关的临床信息就必须借助于CT、MRI、食管内镜超声(EUS)和正电子发射断层(PET)等非侵入性影像学手段以及支气管镜、胸腔镜、纵膈镜和腹腔镜等微创侵入性手段进行准确的临床TNM分期。
(2)术前风险评估
①心血管疾病风险评估
心功能的评价手段有主观症状、体征、静态心电图、平板运动心电图、超声心动图,放射性核素心室造影等。风险评估应从患者既往病史开始,关注有无冠心病、高血压、心脏手术史,从而全面对其心功能进行评估。
②呼吸道疾病风险评估
肺功能的评价手段包括静态和动态两种手段。静态的检查手段包括屏气实验、肺通气功能和弥散功能、血气分析等检查。动态的手段包括简单爬楼梯实验、运动心肺功能检测等。风险评估也要从患者既往有无慢性呼吸道疾病史(如哮喘、慢性支气管炎、肺气肿、肺心病、肺结核、胸膜炎等),有无胸部外伤手术史,有无放化疗史等。结合静态和动态检查结果对肺功能进行评估。
③肝肾功能的评估
通过免疫过筛、肝功能全项、肾功能全项进行检查。结合检查结果,必要时可请相关专业医师会诊参与评估,以确定能否手术以及手术的风险。
④营养状况的评估
通过对患者的生化常规检查,以及对患者体重的测量和入院体检,评估患者的营养状况,判断能否耐受手术,必要时需术前予以营养支持治疗后再行手术治疗,以利于围手术期快速康复,减少术后并发症的发生。
四、食管癌的治疗
(一)治疗原则
临床上应采取手术为主的综合治疗原则,结合放疗、化疗、中医中药治疗和对症治疗。根据病人的机体状况,肿瘤的病理类型、侵犯范围(病期)和发展趋向,有计划地、合理地应用现有的治疗手段,充分征求患者及其家属的意见,遴选合理的诊治方案,精确诊断,精准治疗,以期最大幅度地根治、控制肿瘤和提高治愈率,改善病人的生活质量。对拟行放、化疗的病人,应做Karnofsky或ECOG评分(附录2)。
(二)手术治疗原则
(1)手术适应证
包括:①病变未侵及重要器官(T0~4a),淋巴结无转移或转移不多(N0~2)。身体其他器官无转移者(M0)。即2009第7版UICC食管癌分期(附录3)中的0、Ⅰ、Ⅱ及Ⅲ期(除T4b和N3的患者);②术前新辅助化疗后、术前放疗后,身体条件较好,可耐受开胸手术;③放射治疗未控制或复发病例,无局部明显外侵或远处转移征象;④少数虽高龄(>80岁)但身体强健无伴随其他疾病,而且重要脏器储备功能良好也可慎重考虑手术治疗;⑤无严重心脑肝肺肾等重要器官功能障碍,无严重伴随疾病,身体状况可耐受开胸手术。
(2)手术禁忌证
包括:①一般情况和营养状况很差,严重恶病质;②病变严重外侵(T4b),多野(两野以上)和多个淋巴结转移(N3),全身其他器官转移(M1),即2009版UICC食管癌分期中的Ⅲc~Ⅳ期(T4b或N3或M1);③心肺肝脑肾重要脏器有严重功能不全者。
(3)手术方法的选择
应根据肿瘤的位置、淋巴转移的规律选择合适的手术方法;根治性手术切除范围应包括有肿瘤的食管,切除食管的长度至少距肿瘤上下缘各5 cm,根治性切除还包括两侧纵隔胸膜,心包、食管周围和椎前筋膜之间的所有淋巴结、脂肪血管组织以及整个纵隔和腹部淋巴结(二野)。有时需清扫中下颈部淋巴结(三野)。
①胸下段食管癌:有三种手术方法:①Sweet手术,即通过一切口手术(左胸切口或胸腹联合切口),胃-食管左胸弓上或弓下吻合。②Ivor-Lewis手术,即经右胸和腹部双切口手术,胃-食管右胸顶吻合。该手术优点是可彻底清扫腹腔胃周淋巴结及全纵隔淋巴结,同时能切除足够长食管。③McKeown手术,即颈、胸、腹三切口手术,胃-食管颈部吻合。该手术的优点是可以做到真正意义上的三野淋巴结清扫。
②胸中段食管癌:Sweet、Lewis、McKeown三种手术均可采用,为保证足够的食管上切缘,McKeown手术可能更好。
③胸上段食管癌:首选McKeown手术合并颈淋巴结清扫(三野清扫);对病变位置较高接近胸廓入口的T1N0病人可采用不开胸食管拔脱术。
④替代食管的胃、空肠、结肠上提径路:包括食管床、胸内、胸骨后隧道及胸前皮下隧道。其中以食管床的距离最短,胸内次之,均为常用途径。胸骨后隧道稍远,胸前皮下隧道距离最远。行胸内吻合时,常用途径为食管床和胸内途径。肿瘤有残留或术后需行食管床放疗者应经胸骨后径路。
⑤食管癌胸腔镜微创手术适应症(食管癌规范化诊治指南,第2版):一般认为适用于:1.能在传统开放食管切除术(OE)下切除的早中期食管癌患者大多数都能进行微创食管切除术(MIE);2.中晚期食管癌经过术前化疗或放疗后,如病变降期,也可进行微创食管切除术(MIE);3.特殊的情况:患者全身状况较差,不能耐受开放食管切除术(OE)者,晚期食管癌的姑息性手术等。目前临床上食管癌微创手术方法主要包括胸腹腔镜联合食管癌切除术(包括胸内吻合的Ivor-Lewis手术、颈部吻合的McKeown手术)和纵膈镜腹腔镜联合食管癌切除术等。
(4)手术彻底性的表达:
R0:肿瘤切除彻底,区域淋巴结及原发肿瘤均无肉眼和镜下残留。
R1:区域淋巴结及原发肿瘤镜下残留。
R2:区域淋巴结及原发肿瘤肉眼残留。
(三)化学治疗
食管癌化疗分为新辅助化疗(术前)、辅助化疗(术后)、同步放化疗、姑息性化疗。
(1)治疗原则
①必须掌握临床适应证。
②必须强调治疗方案的规范化和个体化。
(2)治疗方案的选择(食管癌化学治疗临床路径2012版)
①新辅助化疗:适用于T3N1-3M0和部分T4N0-3M0(侵及心包、膈肌和胸膜)食管癌患者。
②术后辅助化疗:适用于ⅡB期、Ⅲ期食管腺癌患者,及所有术后切缘阳性或肿瘤残留的食管癌患者。
③同步放化疗:结合放疗治疗无法手术的Ⅱ、Ⅲ期食管癌患者。
④姑息性化疗:适用于Ⅳ期食管癌患者或治疗后复发患者。
⑤食管腺癌的化疗方案,可参考胃癌的化疗。
(3)治疗效果
化学治疗的疗效评价参照WHO实体瘤疗效评价标准或RECIST疗效评价标准(见附录4)。
(4)常用方案
对于食管鳞癌:
DDP+5-Fu(顺铂加氟尿嘧啶)是最常用的化疗方案,其他可选择的有:
DDP+TXT(顺铂加多西紫杉醇)
DDP+PTX(顺铂加紫杉醇)
Oxaliplatin+5-Fu(奥沙利铂加氟尿嘧啶)
对于食管腺癌,常用的方案是:
ECF方案(表阿霉素加顺铂加氟尿嘧啶)
注:铂类可选择顺铂、奥沙利铂、奈达铂等。
(四)放射治疗
食管癌放疗包括根治性放疗、同步放化疗、姑息性放疗、术前和术后放疗等。
(1)治疗原则
①应在外科、放疗科、肿瘤内科共同研究和/或讨论后决定食管癌患者的治疗方案。
②除急诊情况外,应在治疗前完成必要的辅助检查和全面的治疗计划。
③对于可能治愈的患者,治疗休息期间也应予以细心的监测和积极的支持治疗。
④术后放疗设计应参考患者手术病理报告和手术记录。
⑤同步放化疗时剂量为50~50.4 Gy(1.8~2 Gy/d)。单纯放疗国内习惯使用剂量为60~70 Gy/6~7周。
(2)治疗方案的选择(食管癌放射治疗临床路径2012版)
①对于不适合外科手术或拒绝手术的病例,根据患者的身体条件,可以选择放化同步治疗或单纯放疗±化疗。
②颈部食管癌,T1b分期及以上,可选放化综合治疗。
③对于T2期以上可手术的食管癌,可选择术前放化同步治疗。
④T3期以上或淋巴结阳性的,可选择术后放疗、化疗。
⑤对于切缘阳性的病例,应接受术后放疗。
⑥IV期病例,可考虑局部姑息性放疗。
(3)治疗效果
放射治疗的疗效评价参照WHO实体瘤疗效评价标准或RECIST疗效评价标准(见附录4)。
(4)防护
采用常规的放疗技术,应注意对肺、肾、肺、心脏和脊髓的保护,以避免对它们的严重放射性损伤。急性放射性肺损伤及急性食管炎参照RTOG分级标准(见附录5)。
(5)三维适形放疗技术(3DCRT)是目前较先进的放疗技术。如条件允许可用于食管癌患者,并用CT机来进行放疗计划的设计、确认和实施。
(五)食管癌的对症支持治疗
对于晚期食管癌患者,支持治疗的目的是减轻痛苦,提高患者的生活质量,尽可能延长其生存期。
(1)晚期食管癌的营养支持
①对于预计生存期超过3个月且存在营养不良或营养风险(主要是预计口服摄入小于预计能量消耗的60%,且长于10天者,或预计不能进食时间长于7天者,或已发生体重下降者)的晚期食管癌患者,应给予营养支持,目的是通过纠正或改善机体的营养状况和免疫功能,提供对肿瘤进行综合治疗的机会,减少各种不良反应和并发症。具体营养支持治疗的方法可以采用肠内营养(PN)或(和)肠外营养(EN)。
②对于预计生存期不超过3个月的终末期食管癌患者,营养支持虽然有可能延长生存期,但是同时也有延长痛苦的风险,为避免延长患者的濒死过程,尊重患者的生活和自主权力,公平合理的应用有限的医疗资源,医师需要同时考虑临床指征和社会伦理学因素,充分与家属商量,寻求伦理委员会的指导吗,合理掌握营养支持指征。
(2)吞咽困难的治疗
吞咽困难是晚期食管癌患者最长见的症状,主要是因为瘤体的机械性阻碍,有时也可能与食管正常蠕动减低的功能性因素有关。治疗方法主要是梗阻部位的再疏通和管饲通道的建立。具体方法有:①对于至少能进食半流食的食管癌中度梗阻患者,可考虑内镜下行食管扩张,但该方法疗效持续短暂且有穿孔的风险;②对于只能进食全流食的重度梗阻患者,可选择置入食管内支架;③对于完全进食梗阻的患者,可以选择内镜下置入鼻胃营养管或鼻肠营养管,必要时可行空肠造瘘术;④合并食管气管瘘和纵膈瘘的患者,可考虑带膜支架的置入,但对于感染严重者需谨慎使用。
(3)食管癌的镇痛治疗
晚期食管癌患者疼痛的主要原因有肿瘤直接压迫刺激神经、肿瘤对痛觉敏感组织的刺激、肿瘤分泌化学致痛因子、肿瘤伴随炎症因素致痛、治疗后诱导的外周神经病变疼痛、较少见的骨转移以及心理因素致痛等。
疼痛治疗一般采用药物治疗和非药物手段,后者包括手术、放化疗、神经阻滞、认知心理治疗、中医等。
五、食管癌的预防
(一)病因学预防
少吃或者不吃富含亚硝胺类的食物。亚硝胺主要存在于腌制和霉变的食物中,尽量不吃或者少吃腌制食品。
改善膳食结构。在日常生活中,对食物的多样性要进行必要的搭配,注意微量元素的摄入,特别注意对维生素A、B的摄取量,多吃新鲜蔬菜、水果及肉类。
对于遗传因素,有家族史者可以通过定期体检,以期早发现、早治疗,提高患者的生活质量和生存时间。
改变不良生活习惯,做到不吸烟,不饮酒,减少被动吸烟的机会。不吃过热和过烫的食物。
(二)发病学预防
(1)积极治疗食管上皮增生,处理癌前病变,对于食管炎、食管息肉及食管憩室及时诊疗。
(2)大力开展防癌宣传教育,普及抗癌知识,在高发区人群中做普查、筛检等。
六、食管癌的分级诊疗服务目标、流程、双向转诊标准与各级医院的服务对象
(一)目标
充分发挥团队服务作用,切合我省食管癌的发病情况,在食管癌的诊治方面引入准入制度,规定不同级别的医院在诊断治疗方面必须具备基本的标准,使我省食管癌的患者能够得到合理、有效、规范化的诊治,降低手术并发症及围手术期死亡率,并进一步提高食管癌患者的远期生存期和生活质量。
(二)分级诊疗服务流程(见图2)
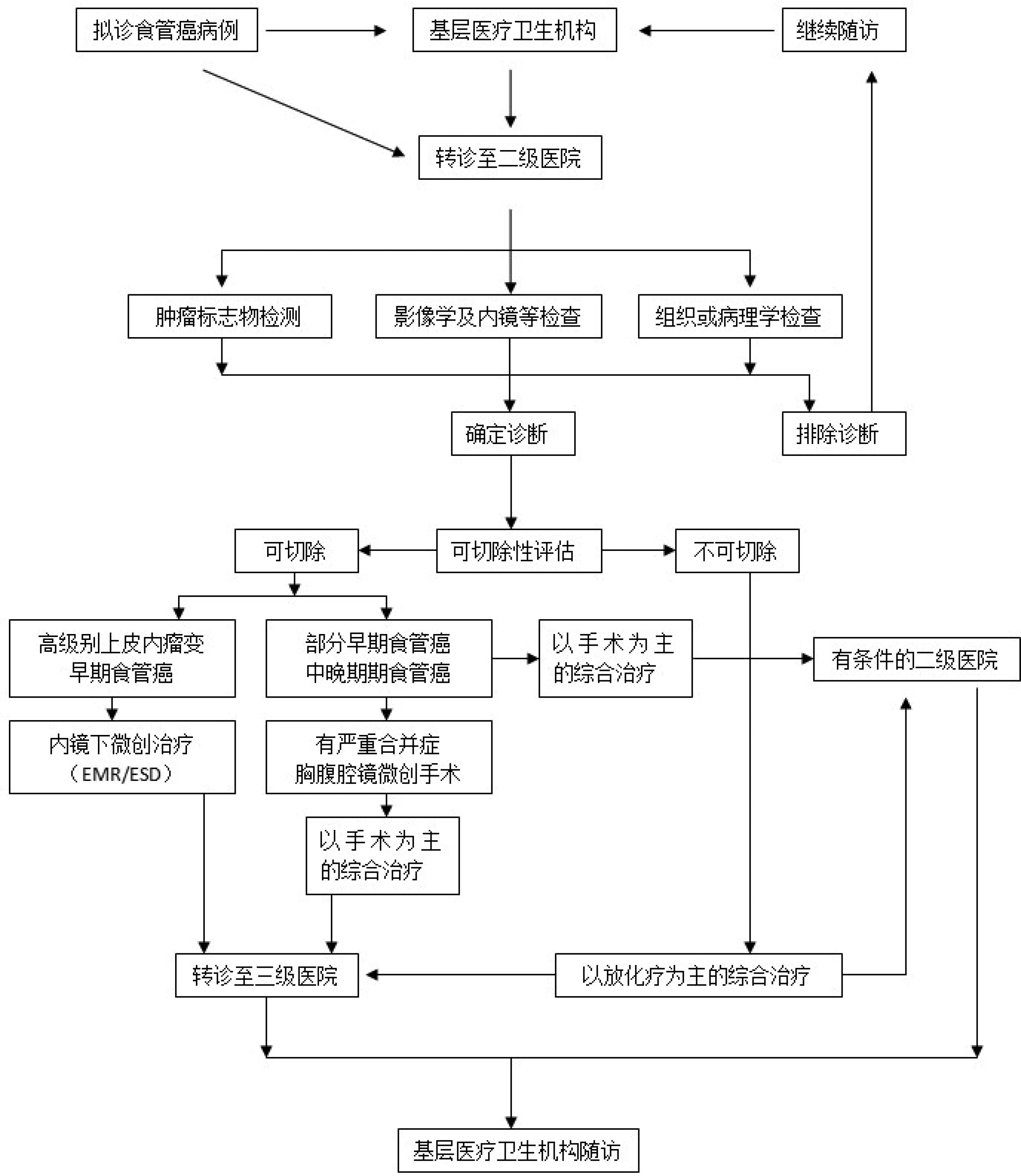
图2 分级诊疗服务流程图
(三)双向转诊标准
(1)基层医疗机构向县级或城市二级以上医院转诊的指征
①初诊怀疑为食管癌但不能确诊者。
②初诊为食管癌前疾病或癌前期病变者。
③高危人群筛查后有食管癌可能,不具备诊断条件者。
④食管癌术后康复出院,再次出现并发症者。
⑤食管癌经放化疗为主的综合治疗,出院后出现严重副反应需继续治疗者。
(2)县级或城市二级医院向城市三级医院转诊指征
①不具备胸外科手术条件的县级或城市二级医院接诊到确诊或疑诊食管癌的患者。
②初诊为食管癌前疾病或癌前期病变,不能明确或不能有效治疗者。
③食管癌病变范围较大,有外侵,手术难度较大,手术风险较高的患者
④伴有合并症(如高血压、冠心病、糖尿病、肝肾功能不全、心肺功能不全等)较多的高危人群。
⑤不具备胸腹腔镜资质的县级或城市二级医院,患者要求或具备微创手术条件可以行微创手术的。
⑥高级别上皮内瘤变或早期食管癌可以行内镜下微创治疗(EMR/ESD),县级或城市二级医院不具备相关条件的。
⑦患者或家属要求转至上级医院,同时县级或城市二级医院认为有此必要的。
⑧不具备放化疗条件的县级或城市二级医院接诊到确诊食管癌的患者。
(3)城市三级医院向县级或城市二级及以下医院转诊的指征
①食管癌术后患者,病情稳定,仅需康复医疗或定期复诊的。
②食管癌术后出现并发症,处理后病情稳定,已无需继续住院,但需长期管理的。
③食管癌经放化疗后,病情稳定,仅需康复医疗或定期复诊的。
④食管癌手术或放化疗后,还需继续辅助治疗或继续完成化疗疗程者。
⑤患者或家属要求转至下级医院的。
(四)各级医院的服务对象
(1)基层医疗机构服务对象:
①基层首诊工作,初步筛选怀疑食管癌的患者、依据自身条件予以初步检查。
②食管癌治疗后,需要消化道功能恢复和全身心肺功能恢复的辅助治疗及疗效观察。
③食管癌治疗(包括手术及放化疗)后病情稳定的患者的延续服务(康复、护理、理疗、随访等服务),建立健康档案。
④具有食管癌高危因素人群的肿瘤预防、健康教育及科普宣传。
(2)县级或城市二级医院服务对象:
①对基层医疗机构转来的疑似食管癌患者进一步明确诊断。
②对于确诊食管癌的患者依据患者的病情,结合医院自身条件,予以手术治疗或化疗。
③有条件医院可以行放射治疗。
④承接上级医院下转的病情稳定的患者的延续服务(化疗、康复、护理、理疗和随访等服务)。
⑤有腔镜手术条件和技术者可以逐步开展微创腔镜手术。
(3)城市三级医院服务对象:
①诊治下级医院转来的合并症多、病情复杂的食管癌患者。
②承接下级医院无法处理的危重症食管癌患者。
③开展下级医院不具备条件的食管癌腔镜微创手术治疗。
④承接下级医院诊治(包括手术、放化疗等)后有严重并发症的患者。
⑤患者或其家属要求在三级医院就诊行食管癌治疗。
⑥负责辖区内医疗质量控制和食管癌的综合诊治水平的提升,定期举办省、市级食管癌诊疗培训班,不断完善各级医院对于食管癌的诊疗规范。
七、食管癌的健康管理服务规范
食管癌的健康管理的实质就是肿瘤的预防、治疗及康复相结合。要求:
①不同级别的医院相互协作、共同进行管理。作为各级医疗机构,首先要对人民群众开展健康教育、普及食管癌的防治知识。
②各级医疗机构依据自身条件,结合患者的病情,采取最合理有效的诊疗方法来保证食管癌的治疗质量,提高治疗效果。
③各级医院应当规定准入制度,规定不同级别的医院在诊断治疗方面必须具备的基本标准,从而提高食管癌患者的远期生存率和生活质量。
④建立健全健康档案,提供多方位的诊治、康复、护理、随访及临终关怀等服务。
八、致谢
蚌埠医学院第一附属医院 唐 震 教授
安徽医科大学第一附属医院 张仁泉 教授
安徽省立医院 徐美青 教授
皖南医学院附属弋矶山医院 丁伯应 教授
蚌埠市第三人民医院 李洪林 主任
阜阳市人民医院 孙仲涛 主任
界首市人民医院 黄 琨 主任
固镇县人民医院 张金国 主任
阜南县人民医院 李汉城 主任
五河县人民医院 蒋胜战 主任
附件目录
附录1 WHO食管癌组织学分类(2000)
上皮性肿瘤 Epithelial tumours
鳞状细胞乳头状瘤 Squamous cell papilloma
上皮内瘤变 Intraepithelial neoplasia
鳞状上皮 Squamous
腺上皮(腺瘤) Glandular(adenoma)
癌 Carcinoma
鳞状细胞癌 Squamous cell carcinoma
疣状(鳞状细胞)癌 Verrucous (squamous)carconoma
基底鳞状细胞癌 Basaloid squamous cell carcinoma
梭形细胞(鳞状细胞)癌 Spindle cell (squamous)carconoma
腺癌 Adenocarcinoma
腺鳞癌 Adenosquamous carcinoma
粘液表皮样癌 Mucoepidermoid carcinoma
腺样囊性癌 Adenoid cystic carcinoma
小细胞癌 Small cell carcinoma
未分化癌 Undifferentiated carcinoma
其他 Others
类癌 Carcinoid tumor
非上皮性肿瘤腺癌Non-epithelial tumors
平滑肌瘤 Leiomyoma
脂肪瘤 Lipoma
颗粒细胞瘤 Granular cell tumor
胃肠间质瘤 Gastrointestinal stromal tumor
良性 Benign
不确定,恶性倾向 Uncertain malignant potential
恶性 Malignant
平滑肌肉瘤 Leiomyosarcoma
横纹肌肉瘤 Rhabdomyosarcoma
Kaposi肉瘤 Kaposi sarcoma
恶性黑色素瘤 Malignant melanoma
其他 Others
附录2患者状况评分
Karnofsky评分(KPS,百分法)
评分见表1:

表1 Karnofsky评分
Zubrod-ECOG-WHO评分(ZPS,5分法)
评分见表2:

表2 Zubrod-ECOG-WHO评分
附录3第7版食管癌TNM定义
1、原发肿瘤(Primary Tumor,T)
Tx:原发肿瘤不能确定;
T0:无原发肿瘤证据;
Tis:重度不典型增生;
T1:肿瘤侵犯粘膜固有层、粘膜肌层、或粘膜下层;
T1a:肿瘤侵犯粘膜固有层或粘膜肌层;
T1b:肿瘤侵犯粘膜下层;
T2:肿瘤侵犯食管肌层;
T3:肿瘤侵犯食管纤维膜;
T4:肿瘤侵犯食管周围结构;
T4a:肿瘤侵犯胸膜、心包或膈肌(可手术切除);
T4b:肿瘤侵犯其他邻近结构如主动脉、椎体、气管等(不能手术切除)。
2、区域淋巴结(Regional Lymph Nodes,N)
Nx:区域淋巴结转移不能确定;
N0:无区域淋巴结转移;
N1:1~2枚区域淋巴结转移;
N2:3~6枚区域淋巴结转移;
N3:≥7枚区域淋巴结转移。
注:必须将转移淋巴结数目与清扫淋巴结总数一并记录
3、远处转移(Distant Metastasis,M)
M0:无远方转移;
M1:有远方转移。
4、肿瘤分化程度(Histologic Grade,G)
Gx:分化程度不能确定——按G1分期;
G1:高分化癌;
G2:中分化癌;
G3:低分化癌;
G4:未分化癌——按G3分期。
1.鳞状细胞癌(包括其他非腺癌类型)
注:*为肿瘤部位按肿瘤上缘在食管的位置界定,X指未记载肿瘤部位。
2.腺癌
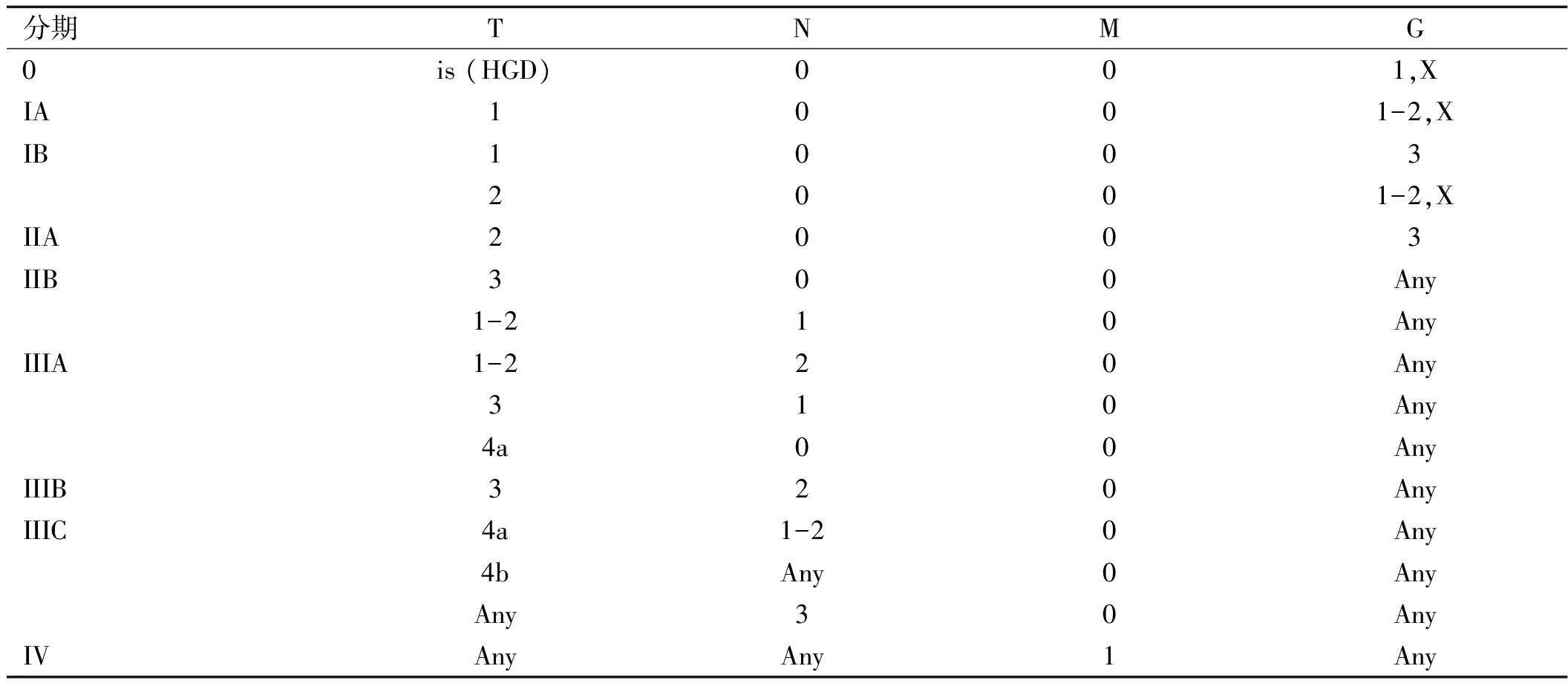
分期TNMG0is(HGD)001,XIA1001-2,XIB10032001-2,XIIA2003IIB300Any1-210AnyIIIA1-220Any310Any4a00AnyIIIB320AnyIIIC4a1-20Any4bAny0AnyAny30AnyIVAnyAny1Any
3.食管癌的区域淋巴结名称与编码

编码名称部位描述1锁骨上淋巴结位于胸骨上切迹与锁骨上2R右上气管旁淋巴结位于气管与无名动脉根部交角与肺尖之间2L左上气管旁淋巴结位于主动脉弓顶与肺尖之间3P后纵隔淋巴结位于气管分叉之上,也称上段食管旁淋巴结4R右下气管旁淋巴结位于气管与无名动脉根部交角与奇静脉头端之间4L左下气管旁淋巴结位于主动脉弓顶与隆突之间5主肺动脉窗淋巴结位于主动脉弓下、主动脉旁及动脉导管侧面6前纵隔淋巴结位于升主动脉和无名动脉前方7隆突下淋巴结位于气管分叉的根部8M中段食管旁淋巴结位于气管隆突至下肺静脉根部之间8L下段食管旁淋巴结位于下肺静脉根部与食管胃交界之间9下肺韧带淋巴结位于下肺韧带内10R右气管支气管淋巴结位于奇静脉头端与右上叶支气管起始部之间10L左气管支气管淋巴结位于隆突与左上叶支气管起始部之间15膈肌淋巴结位于膈肌膨隆面与膈脚之间(膈上)16贲门周围淋巴结位于胃食管交界周围的淋巴结(膈下)17胃左淋巴结位于胃左动脉走行区18肝总淋巴结位于肝总动脉走行区19脾淋巴结位于脾动脉走行区20腹腔淋巴结位于腹腔动脉周围
注:11-肺叶间淋巴结,12-肺叶淋巴结;13-肺段淋巴结;14-肺次段淋巴结不属于食管癌引流淋巴结,本表未列出。
附录4放射治疗及化学诊疗疗效判定标准
(1)WHO实体瘤疗效评价标准(1981)
完全缓解(CR):肿瘤完全消失超过1个月。
部分缓解(PR):肿瘤最大直径及最大垂直直径的乘积缩小达50%,其他病变无增大,持续超过1个月。
病变稳定(SD):病变两径乘积缩小不超过50%,增大不超过25%,持续超过1个月。
病变进展(PD):病变两径乘积增大超过25%。
(2)RECIST疗效评价标准(2000)
①靶病灶的评价
完全缓解(CR):所有靶病灶消失。
部分缓解(PR):靶病灶最长径之和与基线状态比较,至少减少30%。
病变进展(PD):靶病灶最长径之和与治疗开始之后所记录到的最小的靶病灶最长径之和比较,增加20%,或者出现一个或多个新病灶。
病变稳定(SD):介于部分缓解和疾病进展之间。
②非靶病灶的评价
完全缓解(CR):所有非靶病灶消失和肿瘤标志物恢复正常。
未完全缓解/稳定(IR/SD):存在一个或多个非靶病灶和/或肿瘤标志物持续高于正常值。
病变进展(PD):出现一个或多个新病灶和/或已有的非靶病灶明确进展。
最佳总疗效的评价
最佳总疗效的评价是指从治疗开始到疾病进展或复发之间所测量到的最小值。通常,患者最好疗效的分类由病灶测量和确认组成。
附录5急性放射性损伤和急性食管炎分级标准
(1)急性放射性肺损伤RTOG分级标准
0级:无变化。
1级:轻度干咳或劳累时呼吸困难。
2级:持续咳嗽需麻醉性止咳药/稍活动即呼吸困难,但休息时无呼吸困难。
3级:重度咳嗽,对麻醉性止咳药无效,或休息时呼吸困难/临床或影像有急性放射性肺炎的证据/间断吸氧或可能需类固醇治疗。
4级:严重呼吸功能不全/持续吸氧或辅助通气治疗。
5级:致命性。
(2)急性食管炎诊断RTOG标准
0级:无变化。
1级:轻度吞咽困难,需要表面麻醉或止痛剂或软食。
2级:中度吞咽困难,需要麻醉剂或流食。
3级:重度吞咽困难,或脱水,或体重减轻15%需要管饲饮食。
4级:完全梗阻、溃疡或穿孔。
5级:致命性。

