光催化材料对微生物燃料电池的影响
李维国,张丹丹, 2,贾玉红, 2,尤 宏, 2
(1.哈尔滨工业大学(威海)海洋科学与技术学院,山东 威海 264209;2.城市水资源与水环境国家重点实验室(哈尔滨工业大学), 哈尔滨 150090)
微生物燃料电池(Microbial fuel cell,MFC)能利用细菌作为催化剂氧化有机物,传递电子到电极,产生电能,被认为是污水处理最具前景的处理方式之一[1-2].传统的微生物燃料电池由阳极室和阴极室以及分隔它们的质子交换膜(Proton exchange membrane,PEM)组成,两电极室使用的电极材料一般为碳材料.阴极作为实现高功率输出的主要限制因素[3],通常表面有催化剂负载[4],如铂(Pt)等,但贵金属的极高成本限制了其在MFC中的大规模应用.电极是系统重要的组成部分,不同的电极材料,物理和化学特性不同(如表面积、导电性、化学稳定性等),相应地,微生物附着性、电子传递速率、电极电阻、电极表面反应速率也会不同[5].为提高MFC的输出功率,开发经济高效的电极材料成为研究热点.
近几年,关于半导体光催化和光电化学过程的研究越来越多[6],光催化燃料电池(Photocatalytic fuel cell,PFC)利用半导体作为光电极,利用其光催化形成的氧化还原体系降解有机物并产电.光能的输入使高活性自由基与有机物或O2等进行直接快速地反应,能够提高燃料电池产电效率.Jing Bai等[7]总结了适合作为光电极的半导体材料,包括对紫外光响应的光电阳极,如纳米TiO2,纳米管阵列形式的TiO2/Ti等;对可见光响应的光电阳极,如WO3/W,BiOBr/Ti,CdS/TiO2等;以及对可见光响应的光电阴极,如Cu2O纳米线、Cu2O/Cu等.半导体特殊的电子带结构使其具有光催化效应,光激发下电子能够从价带跃迁到导带,形成光生电子(e-)-空穴(h+)对.空穴具有强氧化性,电子具有强还原性,可形成氧化还原体系.作为光电阳极,光生空穴会氧化其表面的有机物,光生电子通过外电路传递到阴极,如图1(A)所示;作为光电阴极,光生空穴会与来自阳极的电子结合,光生电子会还原其表面的氧化性物质,如H+、O2、特定污染物等,如图1(B)所示.同时,该光电化学反应能够降低光生电子-空穴复合的几率,提高氧化或还原性能.
Yue Du等[8]利用光电阳极-生物阴极组成光电化学电池,以对紫外光响应的纳米管阵列TiO2/Ti为光电阳极,在阳极室内降解甲基橙;阴极室内,生物阴极利用其表面附着的具有电化学活性的微生物摄取来自阳极的电子,O2的还原和氨氮的硝化同步发生.装置最大输出功率为211.32 mW/m2,与对比实验中光电阳极-负载50 mg Pt/C的碳刷阴极装置的性能相当,证实光电极与生物电极组合装置的高性价比.Sajid Ali Ansari等[9]研究的PtOx@M-TiO2(x=0,1,2)纳米复合材料,通过对TiO2改性,提高了对可见光吸收效率.将改性电极作为光电阴极,组成生物阳极-光电阴极光催化微生物燃料电池,能够产生4.34 mW/m2的功率密度,相比碳纸作为阴极产生2.09 mW/m2的功率密度,明显提高MFC输出功率.
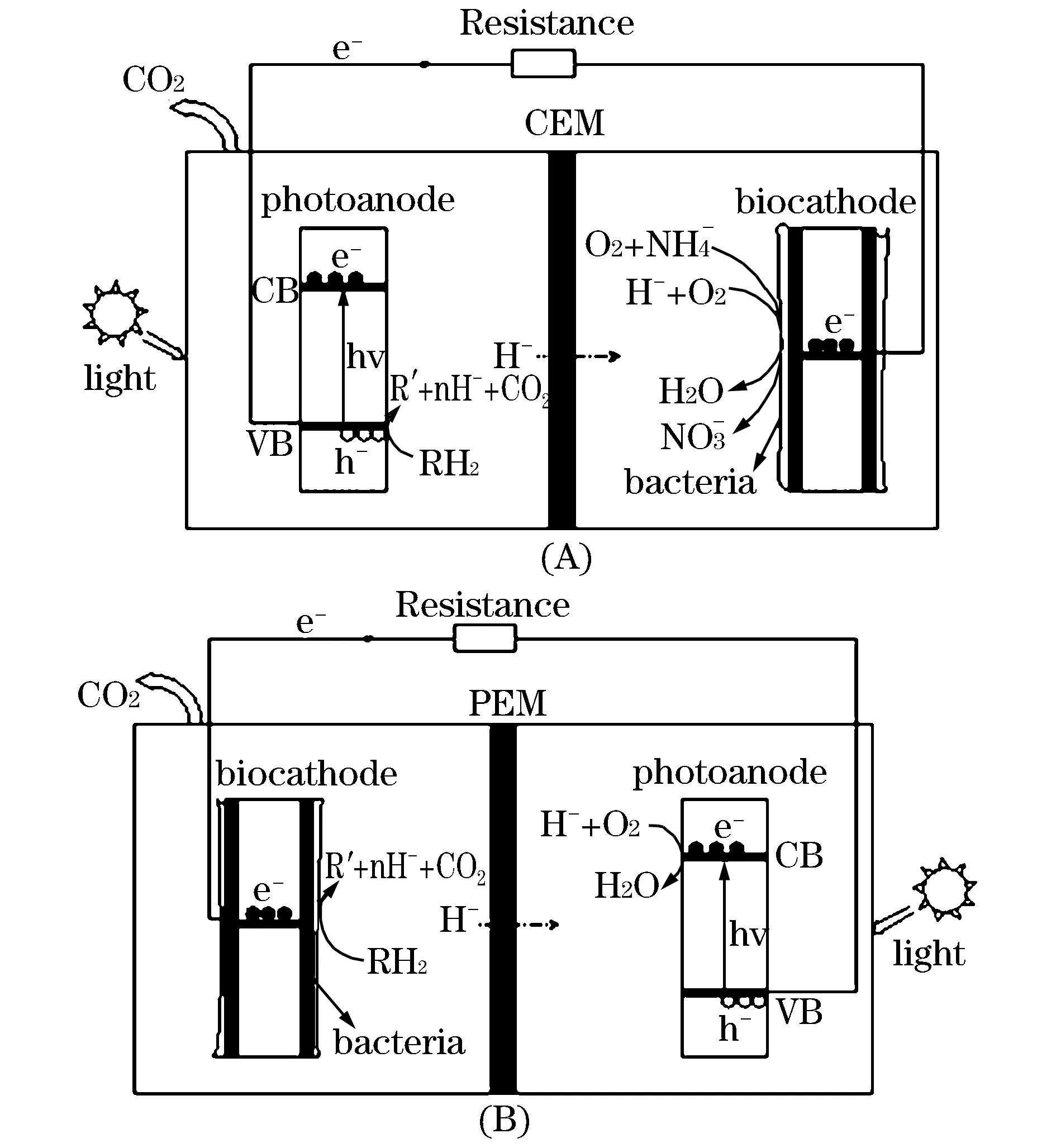
图1 光电极工作机制
1 光催化微生物燃料电池的工作原理
光催化微生物燃料电池能耦合光能与微生物代谢反应来产电,工作原理如图1(A)所示.生物阳极-光电阴极光催化微生物燃料电池装置可由两个相同尺寸的圆柱组成,分别作为阳极室和阴极室;在阳极室上方开一个小孔,便于气体逸出,注入和提取水样等操作;在阴极室中,侧面安装可操控的石英窗,能够进行光照射;两个腔室由一个质子交换膜分隔,在阳极室,生物阳极释放质子和电子.质子可通过电解质透过膜被输送到阴极,而电子可以通过外部电路传递到阴极.阴极室内,光照射下,阴极表面产生光生电子和光生空穴,产生的空穴极易与阳极传输过来的电子结合;阴极表面激发产生的剩余电子与阴极室内的O2以及与阳极扩散过来的H+发生还原反应.此时,光催化微生物燃料电池构成一个完整的回路,能够在降解有机物的同时,耦合光能产电.
2 光催化微生物燃料电池的构建与产电性能
在光催化微生物燃料电池研究中,生物电极的功能不仅是导体,也是细菌的载体[10].光电极作为与生物电极协同作用的一方,光催化效果要明显,同时对太阳光的利用率要高.因而,作为光电极的光催化材料,需要对可见光有良好的响应.随着太阳光光催化[11]和光反应器[12]的不断发展,特别是使用纳米技术合成和制造的新光催化剂,可以极大地提高特定材质的光催化效率[13].
Lu等[14]以金红石包覆的石墨为光电阴极与生物阳极构建了一个光催化型的双室微生物燃料电池.两室由阳离子交换膜(Cation exchange membrane,CEM)分隔,在阴极室中使用1mol/L KCl做电解质,利用天然金红石的可见光响应,在其表面还原氧气.该研究采用石墨板作为阳极,阳极室内接种厌氧污泥,将装置在光照和无光状态下的产电性能进行对比,观察该类型的微生物燃料电池的光响应效果.待装置在无光下系统产电稳定,由无光条件切换到模拟自然光条件下,装置的输出电压在大约50 min内从337 mV提高到384 mV;继续稳定照射50 min后,输出电压达到稳定,此后关掉光源,装置的电压迅速下降,在大约50 min内电压重新降低到340 mV左右.对装置的功率密度进行测量,发现在光照和无光条件下获得的最大功率密度分别为12.03和7.64 W/m3.上述结果证明了该装置具有良好的光响应,光照能够提高电池的产电性能.
Zhe Sun等[15]使用纳米线阵列的CuO作为光电阴极,接种厌氧污泥的碳纤维刷作为生物阳极,构建双室H型光催化微生物燃料电池.阳极室和阴极室由CEM分隔,阴极室使用0.5mol/L Na2SO4溶液作为电解质,并进行曝气以保持溶解氧充足.在黑暗和模拟自然光条件下探究其电池性能,得到光照条件下功率密度为46.44 mW/m2,相比黑暗条件下的36.99 mW/m2增加了126%;开路电压光照条件下为466 mV,相对黑暗条件下的412 mV增加了113%.极化曲线结果显示,装置光照时内阻为333 Ω,相比无光条件下的354 Ω降低了6%;电化学阻抗谱(Electrochemical impendance spectroscopy,EIS)结果表明,光电阴极CuO的溶液电阻和电子转移电阻在黑暗条件下分别为179.9 Ω和7.92 Ω,光照条件下分别降到138.6 Ω和2.04 Ω,光照条件下阴极内阻的减少提高了电池的性能.
Fang Qian等[7]使用对可见光响应的纳米线阵列形式的p型Cu2O作为光电阴极,接种产电菌(Shewanella oneidensis MR-1)的碳布作为生物阳极,组成太阳能驱动的光催化微生物燃料电池.由CEM分隔阳极室和阴极室,阴极室使用0.1mol/L磷酸钾缓冲溶液作为电解质,阳极室采用胰蛋白酶大豆肉汤(TSB)作为产电菌的底物.在有光和无光条件下对装置进行测试,光照强度100 mW/cm2时,光电阴极瞬时光电压达到0.25 V(相对Ag/AgCl电极,下同);生物阳极在有光与无光条件下维持-0.3 V的稳定电压,证明了Cu2O光电阴极具有光响应效果.为了验证装置的产电性能,以及生物阳极与光电阴极的协同效应,在零偏压和光照强度20 mW/cm2条件下,做了一系列对照实验.当装置采用Pt阳极-光电阴极时,能够产生0.6 μA的微弱光电流;采用生物阳极-Pt阴极时,表现出20 μA的本底电流,无光电流产生;而生物阳极-光电阴极组成的光催化微生物燃料电池产生200 μA(50 μA/cm2)的大量电流,成功证明生物阳极和光电阴极的协同作用.在有持续底物供给的情况下,装置能产生持续的电流.
不同的MFC系统中,电子转移过程涉及复杂的机制,直接导致电池性能的不同[16].在微生物然燃料电池中,阴极表面电子受体主要取决于阴极室内电解液组成以及阴极表面的氧化还原电势,氧气由于其丰富的可持续性和环境清洁,是阴极良好的电子受体.如果质子充当阴极表面的电子受体,这个类型的MFC被称为微生物电解池(Microbial electrolysis cell,MEC),可同时满足污水处理和对清洁能源的需求[17].微生物电解池具有产氢的优势,但体系产氢的壁垒需要外部偏压的输入,增加了体系的复杂性和成本.光催化微生物电解池利用光能代替输入的电能,增加总能量的回收率. YanRong He等[18]利用TiO2光电阴极与生物阳极协同作用,组成光催化微生物电解池,紫外光照射下得到3.5 μmol/h的平均产氢速率.
Qingyun Chen等[19]使用纳米棒阵列形式的TiO2作为光电阴极,碳纤维刷接种厌氧污泥作为生物阳极.由PEM分隔阳极室和阴极室,阴极室使用0.2 mol/L Na2SO4作为电解质,组成光催化微生物电解池.在模拟自然光和无光条件下测试电池性能.装置无外部偏压,外接负载10 000 Ω时,光照条件下所产生的电流密度为50~55 mA/m2,而无光条件下的空白电流密度仅为20~25 mA/m2,上述结果证实光照射下TiO2光电阴极与生物阳极能够协同提高装置的产电效率.测试得到光照条件下该电池内阻大约是10 000 Ω,此时输出功率密度为6.0 mW/m2.当外阻从100 000 Ω降到1 000 Ω,电流密度从15 mA/m2很快升到95 mA/m2,外阻为1 000 Ω时,产氢速率大约为4.4 μL/h.而当外电阻继续降低,电流密度仅轻微上升至105 mA/m2,表明此时电流的增加受限于内阻.此装置比传统的微生物燃料电池和其他电化学电池内阻大[20],原因如下:电荷转移到光电阴极过程产生的内阻;阴极上负载的半导体薄膜产生的内阻;离子通过质子交换膜的运输过程产生的内阻等.为了减小内阻,可增大光照强度或增大光电阴极光照面积,也可在光电阴极上使用较薄的光催化剂层[21].
Dawei Liang等[22]通过在Cu2O表面旋转涂覆适宜厚度的NiOx层制造Cu2O/NiOx复合光电阴极,与生物阳极协同组成光催化微生物电解池,装置由PEM分隔的两室组成.Cu2O/NiOx光电阴极能更有效地利用光激发的电子,同时提高Cu2O光电阴极的化学稳定性.可见光下对装置进行光电性能考察,相较同样情况下装置以空白Cu2O作为光电阴极,电流-时间衰减曲线结果证实Cu2O/NiOx电极产生285.9 μA/cm2的电流密度,比空白的Cu2O电极高4.7倍.光照射4 h后,空白Cu2O光电阴极电流减少56.2%,复合Cu2O/NiOx光电阴极只有的23.8%的电流减少,表明复合Cu2O/NiOx光电阴极大大改善了电极的稳定性.该研究还考察了外加偏压对氢气产生的影响,装置外加0.2 V偏压,在连续光照射下H2的产率为5.09 μL·h-1cm-2,无光条件下没有检测到氢气,说明装置具有光催化效果;在0.4 V的外加偏压下,有光和无光条件下装置产氢速率分别为4.89 μL·h-1cm-2、4.55 μL·h-1cm-2,说明装置外加高偏压下,电化学催化是产氢的主要控制因素.
微生物燃料电池的输出功率P=E2/R,电池的输出功率主要由电势和内阻两个主要因素决定的[22].光照条件下,光催化微生物燃料电池通过光电极与生物电极的协同效应能提高输出电压,从而提高功率密度.微生物燃料电池的内阻主要包括电解液的阻值、微生物在阳极表面反应的活性内阻、阳极内阻、阴极表面反应的活性内阻、阴极内阻等[14].光激发下,光电极产生的光生电子和空穴使表面反应速率增加,提高了电子转移速率从而降低了阴极内阻[15].光催化微生物燃料电池可通过提高输出电压和降低电极内阻两个方面提高输出功率.
3 光催化微生物燃料电池污染物去除
目前,光催化微生物燃料电池产能情况更受到关注,如产电性能、清洁能源H2的产生速率等,用来去除污染物的例子还不多.Yan Li等[23]研究的光催化微生物燃料电池,探究了金红石包覆的石墨光电阴极对含Cr6+污染物的去除情况.光照下,初始质量浓度26 mg/L的Cr6+经22 h后还原了88%,相比无光条件下还原率提高了23%.Hongrui Ding等[24]利用类似的装置在阴极室内降解甲基橙.结果发现,闭合电路+金红石包覆石墨阴极+光照、闭合电路+石墨阴极+光照、闭合电路+金红石包覆石墨阴极+无光、闭合电路+石墨阴极+无光、开放电路+金红石包覆阴极+光照条件下,装置对MO的脱色率依次降低,分别为72%、61%、45%、45%、17.8%.结果表明在闭合电路、光照和金红石包覆的必要条件下装置具有明显的光催化效应.实验中还发现,装置的产电率与阴极室污染物的去除存在正相关的关系,产电率的提高有利于污染物的去除.Yue Du等[8]利用光电阳极-生物阴极组成的光电化学电池,探究阳极室内降解甲基橙的情况,并与配置了相同光电阳极,阴极为负载不同量催化剂(Pt/C)的碳刷装置相比较.光照条件下,开放电路+Pt/C(0 mg)碳刷阴极、闭合电路+Pt/C(0 mg)碳刷阴极、闭合电路+Pt/C(35 mg)碳刷阴极、闭合电路+Pt/C(50 mg) 碳刷阴极、闭合电路+Pt/C(75 mg) 碳刷阴极、闭合电路+生物阴极,甲基橙的降解速率常数k分别为0.0009 、0.0025、0.0070、0.0012 、0.0160、0.0012 min-1.结果显示,开放电路甲基橙降解速率明显低于闭合电路,闭合电路+生物阴极甲基橙降解速率与闭合电路+Pt/C(50 mg) 碳刷阴极降解速率相当,证明了光电阳极与生物阴极能产生协同作用.
4 结 语
光催化微生物燃料电池利用光电极和生物电极的协同作用,既能同步利用太阳能又提高了微生物燃料电池的产能效率,可应用于能源生产和污染物去除,具有很好的发展前景.目前光催化微生物燃料电池构型比较简单,一般为双室H型;阳极材料普遍采用石墨棒,石墨纤维刷,碳布,碳纸,碳毡,和网状玻璃碳(RVC)等;光电阴极的研究集中于金属氧化物半导体光催化材料,包括在碳材料或导电玻璃上负载光催化剂或直接金属基板上生成光催化剂等.
为了提高光催化型微生物燃料电池的产电性能和污染物去除效果,阳极室作为微生物生长的环境,从构型到阳极材料及介质组成都需要优化.目前有针对阳极材料预处理的研究以提高微生物在电极表面的富集和产电性能;装置的构型应尽可能减少反应器的内阻,增大功率输出.为推进光催化MFC技术的实际应用,关键是要建立低成本和稳定的装置.光电极应是易制且低成本的半导体材料,同时应具有良好的带隙,以提高太阳光利用效率,制备的电极必须是可伸缩的.此外,光电极在溶液中要化学稳定.
光催化微生物燃料电池的应用推广依托微生物电化学、半导体光催化材料、微生物燃料电池构型等技术的发展,对各方面进行深入研究,有利于实现可再生能源(生物能、光能等)处理环境污染问题.
[1] LOGAN B E, HAMELERS B, ROZENDAL R A,etal. Microbial fuel cells: methodology and technology [J]. Environmental Science & Technology, 2006, 40(17): 5181-5192.
[2] WANG X, CHENG S, FENG Y J,etal. Use of carbon mesh anodes and the effect of different pretreatment methods on power production in microbial fuel cells [J]. Environmental Science & Technology, 2009, 43(17): 6870-6874.
[3] PARK D H, ZEIKUS J G. Improved fuel cell and electrode designs for producing electricity from microbial degradation [J]. Biotechnology and Bioengineering, 2003, 81(3): 348-355.
[4] PARK H I, MUSHTAQ U, PERELLO D,etal. Effective and low-cost platinum electrodes for microbial fuel cells deposited by electron beam evaporation [J]. Energy & Fuels, 2007, 21: 2984-2990.
[5] ZHOU M H, CHI M L, LUO J M,etal. An overview of electrode materials in microbial fuel cells [J]. Journal of Power Sources, 2011, 196(10): 4427-4435.
[6] TIAN J J, CAO G Z. Design, fabrication and modification of metal oxide semiconductor for improving conversion efficiency of excitonic solar cells [J]. Coordination Chemistry Reviews, 2016.
[7] BAI J, WANG R, LI Y P,etal. A solar light driven dual photoelectrode photocatalytic fuel cell (PFC) for simultaneous wastewater treatment and electricity generation [J]. Journal of Hazardous Materials, 2016, 311: 51-62.
[8] DU Y, FENG Y J, QU Y P,etal. Electricity generation and pollutant degradation using a novel biocathode coupled photoelectrochemical cell [J]. Environmental Science & Technology, 2014, 48(13): 7634-7641.
[9] ALI A S, MANSOOB K M, OMAISH A M,etal. Improved electrode performance in microbial fuel cells and the enhanced visible light-induced photoelectrochemical behaviour of PtOx@M-TiO2 nanocomposites [J]. Ceramics International, 2015, 41(7): 9131-9139.
[10] WEI J C, LIANG P, HUANG X. Recent progress in electrodes for microbial fuel cells[J]. Biotechnology and Bioengineering, 2011, 102(20): 9335-9344.
[11] ZOU Z G, YE J H, SAYAMA K,etal. Direct splitting of water under visible light irradiation with an oxide semiconductor photocatalyst[J]. Nature, 2001, 414(6864): 625-627.
[12] MALATO R S, BLANCO G J, MALDONADO R M I,etal. Engineering of solar photocatalytic collectors [J]. Solar Energy, 2004, 77(5): 513-524.
[13] SPASIANO D, MAROTTA R, MALATO S,etal. Solar photocatalysis: materials, reactors, some commercial, and pre-industrialized applications. A comprehensive approach [J]. Applied Catalysis B: Environmental, 2015, 170/171: 90-123.
[14] LU A H, LI Y, JIN S,etal. Microbial fuel cell equipped with a photocatalytic rutile-coated cathode[J]. Energy & Fuels, 2010, 24(2): 1184-1190.
[15] SUN Z, CAO R X, HUANG M H,etal. Effect of light irradiation on the photoelectricity performance of microbial fuel cell with a copper oxide nanowire photocathode [J]. Journal of Photochemistry and Photobiology A: Chemistry, 2015, 300: 38-43.
[16] QIAN F, WANG G M, LI Y. Solar-driven microbial photoelectrochemical cells with a nanowire photocathode [J]. Nano Letters, 2010, 10(11): 4686-4691.
[17] WANG H Y, QIAN F, LI Y. Solar-assisted microbial fuel cells for bioelectricity and chemical fuel generation [J]. Nano Energy, 2014, 8: 264-273.
[18] HE Y R, YAN F F, YU H Q,etal. Hydrogen production in a light-driven photoelectrochemical cell [J]. Applied Energy, 2014, 113: 164-168.
[19] CHEN Q Y, LIU J S, LIU Y,etal. Hydrogen production on TiO2 nanorod arrays cathode coupling with bio-anode with additional electricity generation [J]. Journal of Power Sources, 2013, 238: 345-349.
[20] FAN Y Z, SHARBROUGH E, LIU H. Quantification of the internal resistance distribution of microbial fuel cells [J]. Environmental Science & Technology, 2008, 42: 8101-8107.
[21] WANG Y H, WANG B S, LIU Y P,etal. Electricity and hydrogen co-production from a bio-electrochemical cell with acetate substrate[J]. International Journal of Hydrogen Energy, 2013, 38(16): 6600-6606.
[22] 孙 哲, 黄满红, 陈 亮, 等. 光催化型微生物燃料电池研究进展[J]. 工业水处理, 2014, 34(3): 11-14.
[23] LI Y, LU A H, DING H R,etal. Cr(VI) reduction at rutile-catalyzed cathode in microbial fuel cells[J]. Electrochemistry Communications, 2009, 11(7): 1496-1499.
[24] DING H R, LI Y, LU A H,etal. Photocatalytically improved azo dye reduction in a microbial fuel cell with rutile-cathode[J]. Bioresource Technology, 2010, 101(10): 3500-3505.

