毛细管电泳-电化学发光法测定金钗石斛中石斛碱的含量
邓光辉,罗珍连
(广西民族大学 化学化工学院 广西林产化学与工程重点实验室,南宁530006)
金钗石斛(Dendrobium nobile Lindl)为兰科属多年附生草本植物,其入药始载于《神农本草经》,享有“仙草”之美誉,是名贵中药材石斛的来源之一[1]。金钗石斛的主要有效成分有生物碱类化合物、酚类化合物、多糖等[2],其中,生物碱类成分是最早从石斛属植物中分离得到的物质[3]。石斛碱为金钗石斛的特征性成分,具有止痛、解热、降低心率和血压、减慢呼吸、解巴比妥毒等作用[4-5],有较高的研究开发价值。2010年版《中国药典》以石斛碱含量作为金钗石斛的质量控制指标[6]。
石斛碱的测定方法有气相色谱法[7-8]和高效液相色谱法[9-10]。与高效液相色谱法相比,毛细管电泳-电化学发光法(CE-ECL)是一种高效快速、样品消耗少、成本低的分离检测技术[11-12]。CE-ECL已经成功应用于生物碱研究[13-17],但尚未见到 CEECL测定金钗石斛碱的报道。本工作对金钗石斛中具有药理活性成分的石斛碱进行提取,采用CEECL测定其含量。
1 试验部分
1.1 仪器与试剂
MPI-A型毛细管电泳电化学发光检测系统,配未涂层石英毛细管(50μm×55cm)、直径500μm铂工作电极、Ag/AgCl参比电极和铂辅助电极;PHS-3E型酸度计;KQ-100DB型数控超声波清洗器;1810-B型自动双蒸馏器。
Ru(bpy)32+溶液:5mmol·L-1,称取适量三联吡啶氯化钌六水合物,用水溶解配制成20mmol·L-1溶液,再用70mmol·L-1磷酸盐缓冲溶液(PBS,pH 8.10)稀释配制成5mmol·L-1。
标准储备溶液:500mg·L-1,称取石斛碱对照品5.0mg置于10mL容量瓶中,用甲醇溶解并定容,摇匀,使用时用pH 8.10PBS进行稀释。
石斛碱标准品纯度99%,三联吡啶氯化钌六水合物、甲醇、乙醇为分析纯,试验用水为二次蒸馏水,其他试剂均为分析纯。
1.2 试验方法
称取金钗石斛粉末1.000 0g置于100mL锥形瓶中,加入乙醇50mL,称定质量,超声提取30min,冷却,再称定质量,用无水乙醇补足失重,滤液经0.45μm乙酸纤维膜过滤备用。
依次 用 0.1mol·L-1NaOH 溶 液、水、10mmol·L-1PBS(pH 5.13)运行缓冲溶液将石英毛细管冲洗10min,将工作电极依次用0.3,0.05μm Al2O3粉末抛光,用水冲洗,再用水超声清洗干净,吹干,将电极与毛细管安装在检测池上,用光学显微镜调节毛细管与工作电极之间的距离为(100±5)μm。
在检测池中加入5mmol·L-1Ru(bpy溶液,测定时将毛细管进样端插入10mmol·L-1PBS(pH 5.13)中,待发光信号稳定后,采用电动进样,进样电压为10kV,进样时间为10s,光电倍增管高压为800V,检测电位为1.17V,施加分离电压为15kV进行分离检测。
所有溶液在进入毛细管前经0.45μm乙酸纤维素膜过滤,每2h换一次检测池溶液,以保证试验的稳定性。
2 结果与讨论
2.1 石斛碱与三联吡啶钌发光体系的电化学发光行为
在检测池中先加入5mmol·L-1Ru(bpy溶液进行循环伏安扫描,记录电极电流和电化学发光曲线。加入3.4mg·L-1石斛碱溶液后,再进行循环伏安扫描,记录电极电流和电化学发光曲线,结果见图1。

图1 循环伏安图(a)和电化学发光曲线(b)Fig.1 Cyclic voltammograms(a)and the profile of electrochemiluminescence(b)
由图1可知:三联吡啶钌只有较小的电极电流和弱的电化学发光信号;当加入石斛碱后,电极电流和电化学发光信号都得到明显的增强。基于石斛碱对三联吡啶钌的电化学发光的增强作用,可建立毛细管电泳-电化学发光法测定石斛碱的含量。
2.2 检测条件的选择
2.2.1 检测电位
采用恒电位法在1.0~1.35V(vs.Ag/AgCl)内考察检测电位对电化学发光(ECL)强度的影响,结果见图2。
由图2可知:当检测电位升至1.17V时,石斛碱的ECL强度最大。因此,试验选择1.17V作为检测电位。

图3 Ru(bpy浓度对电化学发光强度的影响Fig.3 Effeet of concentration of Ru(bpy on ECL intensity
2.2.3 运行缓冲溶液的浓度和酸度
试验考察了5~30mmol·L-1内的运行缓冲溶液对ECL强度的影响,结果见图4。
由图4可知:随着运行缓冲溶液浓度的增大,ECL强度逐渐增大;当其浓度为10mmol·L-1时,ECL强度达到最大;浓度高于10mmol·L-1时,ECL强度逐渐减小。因此,试验选择10mmol·L-1磷酸盐缓冲溶液为运行缓冲溶液。
缓冲溶液的酸度也会影响毛细管电泳的分离效果和ECL强度,影响分析物的电离度,还会影响电渗流(EOF)的大小。试验考察运行缓冲溶液在pH 3.50~8.50内对ECL强度的影响,结果见图5。

图4 运行缓冲溶液浓度对电化学发光强度的影响Fig.4 Effect of concentration of the running buffer solution on ECL intensity
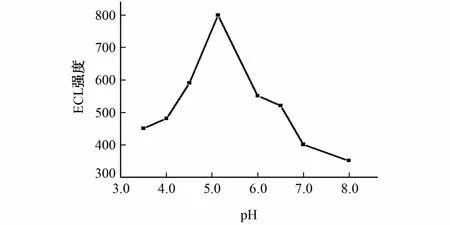
图5 运行缓冲溶液酸度对电化学发光强度的影响Fig.5 Effect of acidity of the running buffer solution on ECL intensity
由图5可知:当运行缓冲溶液pH为5.13时,ECL强度最大。因此,试验选择pH 5.13的10mmol·L-1磷酸盐缓冲溶液为运行缓冲溶液。
2.2.4 检测池中缓冲溶液的浓度和酸度
固定检测池中磷酸盐缓冲溶液浓度为60mmol·L-1,考察其 pH 在6.00~9.50内对ECL强度的影响,结果见图6。
由图6可知:pH 为6.00~8.10时,ECL强度随检测池中磷酸盐缓冲溶液pH增大而增大;pH为8.10~9.50时,ECL强度随pH 增大而减小。因此,试验选择pH 8.10的磷酸盐缓冲溶液。
选用pH 8.10磷酸盐缓冲溶液,考察其浓度在50~90mmol·L-1内对ECL强度的影响,结果见图7。
由图7可知:当检测池中磷酸盐缓冲溶液浓度为70mmol·L-1时,ECL强度达到最大。因此,试验选择检测池中磷酸盐缓冲溶液的浓度为70mmol·L-1。
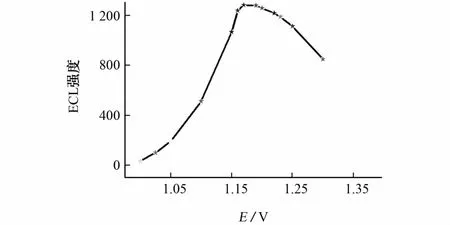
图2 检测电位对电化学发光强度的影响Fig.2 Effect of detection potential on ECL intensity
2.2.5 分离电压和进样时间
试验考察了分离电压在10~18kV内对ECL强度的影响。结果表明:当电压在10~15kV内逐渐升高时,ECL强度逐渐增大;当分离电压高于15kV时,基线噪声大。因此,试验选择分离电压为15kV。
采用电动进样,选择进样电压为10kV,考察了进样时间在5~15s内对ECL强度的影响。结果表明:随着进样时间的增加,ECL强度逐渐增大;当进样时间超过10s时,ECL强度增长缓慢且偏离线性、有拖尾现象。因此,试验选择进样时间为10s。

图6 检测池中磷酸盐缓冲溶液酸度对电化学发光强度的影响Fig.6 Effeet of acidity of PBS in detection cell on ECL intensity
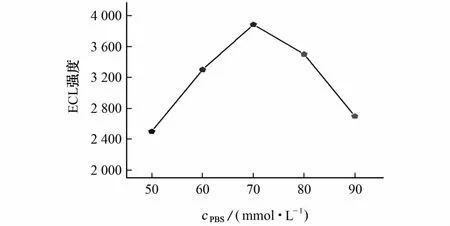
图7 检测池中磷酸盐缓冲溶液浓度对电化学发光强度的影响Fig.7 Effeet of concentration of PBS in detection cell on ECL intensity
2.3 标准曲线和检出限
在试验条件下,石斛碱质量浓度在1.0~100mg·L-1内与其峰面积呈线性关系,线性回归方程为y=374.9 x-85.81(y为ECL信号的峰面积,x为石斛碱的质量浓度),相关系数为0.999 7。
以3倍信噪比计算方法的检出限(3S/N)为0.045mg·L-1。
2.4 样品分析与加标回收试验
按试验方法测定金钗石斛样品中的石斛碱,对照品及样品的电泳图见图8。

图8 毛细管电泳图Fig.8 Capillary electrophoresis charts
图8 曲线3为金钗石斛样品的电泳图,图中只有一个峰,与对照品的出峰时间一致,且加入石斛碱标准溶液后峰信号增强,见图8曲线2,与石斛碱对照品电泳图(图8曲线1)进行比较可知,样品谱峰为石斛碱。经计算,该批金钗石斛中石斛碱质量分数为0.32%。
取已知含量的样品提取液,按试验方法进行加标回收试验,测定值与回收率结果见表1。
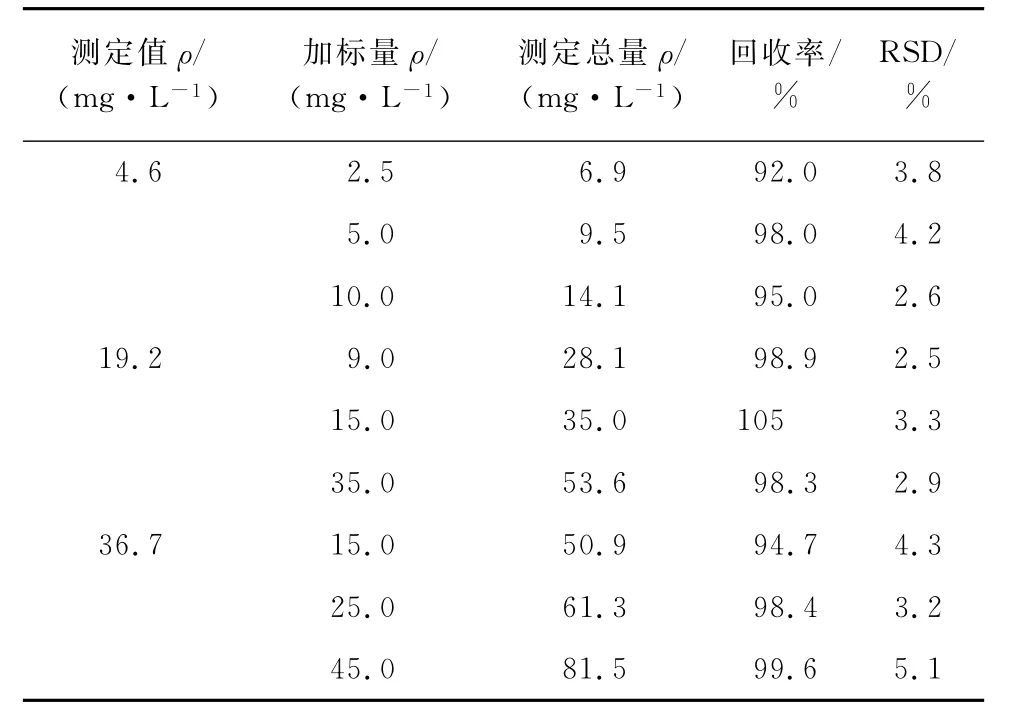
表1 样品分析结果和回收试验结果(n=5)Tab.1 Results of tests for sample analysis and recovery(n=5)
本工作采用毛细管电泳-电化学发光法测定金钗石斛中石斛碱的含量,方法简单、快速,与药典规定的测定方法相比,本方法具有进样量少、分析速率快、灵敏度高、设备低廉、装置及操作简单等优点。
[1] 管志斌,李再林.珍稀名贵中药——金钗石斛[J].中国野生植物资源,2002,21(4):36-37.
[2] 江滢,黄厚今.金钗石斛研究进展[J].云南中医中药杂志,2015,36(1):77-78.
[3] 金蓉鸾,孙继军,张远名.11种石斛的总生物碱的测定[J].中国药科大学学报,1981,16(1):9-13.
[4] 王宪楷,赵同芳.石斛属植物的化学成分与中药石斛[J].中国药学杂志,1986,21(11):666-669.
[5] 华茉莉,刘全海,庄 贤 韩,等.石 斛 碱的 新 应 用:CN101543492[P].2009-09-30.
[6] 国家药典委员会.中国药典一部2010版[M].北京:中国医药科技出社,2010.
[7] 华茉莉,杨洋,沈志伟.气相色谱法测定金钗石斛药材中石斛碱的含量[J].中药材,2006,29(4):338-339.
[8] 黄小燕,乙引.气相色谱法测定金钗石斛中石斛碱的含量[J].贵州师范大学学报(自然科学版),2007,25(4):92-94.
[9] 申刚,乙引,张习敏,等.HPLC法测定金钗石斛中石斛碱含 量 [J].安徽 农业科 学,2009,37(31):15248-15249.
[10] 李墅,王春兰,郭顺星.高效液相色谱法测定金钗石斛中石斛碱含量[J].中国药学杂志,2009,44(4):252-254.
[11] DENG B,SU C,KANG Y.Determination of norfloxacin in human urine by capillary electrophoresis with electrochemiluminescence detection[J].Analytical & Bioanalytical Chemistry,2006,385(7):1336-1341.
[12] SUN X,LIU J,CAO W,et al.Capillary electrophoresis with electrochemiluminescence detection of procyclidine in human urine pretreated by ion-exchange cartridge[J].Analytica Chimica Acta,2002,470(2):137-145.
[13] GAO Y,XU Y,HAN B,et al.Sensitive determination of verticine and verticinone in Bulbus Fritillariae by ionic liquid assisted capillary electrophoresis-electrochemiluminescence system[J].Talanta,2009,80(2):448-453.
[14] ZHOU M,LI Y,LIU C,et al.Simultaneous determination of lappaconitine hydrobromide and isopropiram fumarate in rabbit plasma by capillary electrophoresis with electrochemiluminescence detection[J].E-lectrophoresis,2012,33(16):2577-2583.
[15] ZHOU M,LI Y J,MA Y J,et al.Determination of ketotifen fumarate by capillary electrophoresis with tris(2,2′-bipyridyl)ruthenium (II)electrochemiluminescence detection[J].Luminescence,2011,26(5):319-323.
[16] LIU H,YUAN R,CHAI Y,et al.A novel solidstate electrochemiluminescence detector for capillary electrophoresis based on tris(2,2′-bipyridyl)ruthenium (II)immobilized in Nafion/PTC-NH2composite film[J].Talanta,2011,84(2):387-392.
[17] YUAN B,ZHENG C,TENG H,et al.Simultaneous determination of atropine,anisodamine,and scopolamine in plant extract by nonaqueous capillary electrophoresis coupled with electrochemiluminescence and electrochemistry dual detection[J].Journal of Chromatography A,2010,1217(1):171-174.

