中性粒细胞性哮喘小鼠气道炎症和细胞因子的变化及意义
王永彬,安 文,吴 倩,冯菲菲,车晓文⋆
(1.山东大学第二医院呼吸内科,山东 济南 250033;2.山东省菏泽市巨野县董官屯镇卫生院,山东 菏泽 274900)
支气管哮喘是气道慢性炎症性疾病。既往认为嗜酸性粒细胞气道炎症是哮喘典型的改变,TH1/TH2细胞失衡所致TH2细胞优势是介导嗜酸细胞性哮喘发病最重要的免疫学机制。但随着研究深入,显示哮喘的气道炎症存在不同的亚型,可分为嗜酸细胞性哮喘和非嗜酸细胞性哮喘,其中半数以上的非嗜酸细胞性哮喘为中性粒细胞性哮喘[1](Neutrophilic asthma,NA)。Thl7是一种以产生IL-17为主要细胞因子的辅助性T细胞,IL-17对于中性粒细胞参与的支气管哮喘气道炎症、气道高反应、气道重塑均发挥重要作用[2]。本研究通过观察NA小鼠肺组织病理改变、支气管肺泡灌洗液中炎症细胞及IL-17、IL-10水平的变化,探讨TH17/Treg细胞失衡对NA小鼠气道炎症的影响及其免疫调节作用的机制。
1 材料与方法
1.1 实验动物及分组
20只实验用C57BL/6雌性小鼠按随机数字法分为NC组、NA组,每组10只,分笼饲养。
1.2 主要试剂与设备
OVA、LPS、乙酰甲胆碱均购自美国Sigma公司。小鼠IL-10、IL-17 ELISA试剂盒由杭州联科生物技术有限公司提供。Emka动物肺功能测试系统购自法国。
1.3 实验方法
1.3.1 NA小鼠模型建立
NA组于实验第0、6、13天小鼠麻醉后予100 μgOVA及0.l μgLPS气道滴入致敏。第21天起连续2周雾化1%OVA激发,每天1次,每次激发60分。
NC组则用生理盐水代替LPS及OVA致敏及激发。
1.3.2 气道反应性测定
末次OVA雾化激发后24h,按浓度0、1、2、4、8、16mg/ml依次吸入乙酰甲胆碱,并行无创肺功能检测,记录气道反应性监测指标Penh(Enhanced pause)。
1.3.3 BALF的收集
于气道反应性测定完毕后处死小鼠,夹闭右主支气管,剪开气管用相应导管插入左主气管内,从导管注入0.3 mL生理盐水灌洗左肺,反复3次,回收率为60%~70%。将 BALF4℃3000 r/min条件下离心10 min,回收细胞进行涂片并行瑞氏-姬姆萨染色,计数白细胞数量并分类。上清液保存于-80℃,用于细胞因子的测定。
1.3.4 肺组织切片HE染色
于收集BALF后剖取右肺固定于10%福尔马林溶液内,常规取材,脱水,石蜡包埋,切片(4微米厚)、进行HE染色。
1.3.5 ELISA法测定细胞因子水平
收集BALF后按照ELISA检测试剂盒的说明书,测定BALF中IL-17、IL-10含量。
1.4 统计学分析
2 结 果
2.1 两组小鼠哮喘症状
雾化激发过程中,NA组小鼠出现抓耳挠腮、烦躁不安、呼吸急促、毛色失去光泽、腹肌抽搐等,可闻及明显的喘鸣音,而NC组未出现上述症状。
2.2 两组小鼠气道反应性测定
乙酰甲胆碱刺激小鼠,当乙酰甲胆碱浓度达16 mg/mL,NA组气道反应性较NC组升高(P<0.05)。见表1。
表1 乙酰甲胆碱刺激后两组小鼠气道反应性(±s,mg/m)

表1 乙酰甲胆碱刺激后两组小鼠气道反应性(±s,mg/m)
注:a与NC组比较P<0.05
组别 n penh 0 1 2 4 8 16 NC组 10 0.95±0.26 1.52±0.47 1.94±0.41 2.43±0.71 2.72±1.10 3.04±0.83 NA组 10 1.04±0.05 1.59±0.56 2.35±1.10 3.69±0.90 4.62±0.78 5.11±0.92a
2.3 两组小鼠BALF中细胞总数及细胞分类计数比较
NA组细胞总数,中性粒细胞(NEU)和嗜酸性粒细胞(EOS)计数均高于NC组、且NEU计数高于EOS计数(P<0.05)。见表2。
表2 两组小鼠BALF中细胞总数及白细胞分类计数(±s,105/mL)

表2 两组小鼠BALF中细胞总数及白细胞分类计数(±s,105/mL)
注:a与NC组比较P<0.05;b与EOS计数P<0.05
组别 n 细胞总数 NEU计数 EOS计数NC组 10 6.9±2.5 1.9±0.9 0.68±0.2 NA组 10 17.0±4.1a 10.1±2.2ab 1.72±0.7a
2.4 两组小鼠肺组织病理改变
NC组肺组织细支气管和肺泡结构清晰,基本无炎症细胞浸润;NA组支气管及血管周围大量炎症细胞浸润,且以中性粒细胞浸润为主,肺泡壁、支气管壁明显增厚。见图1。
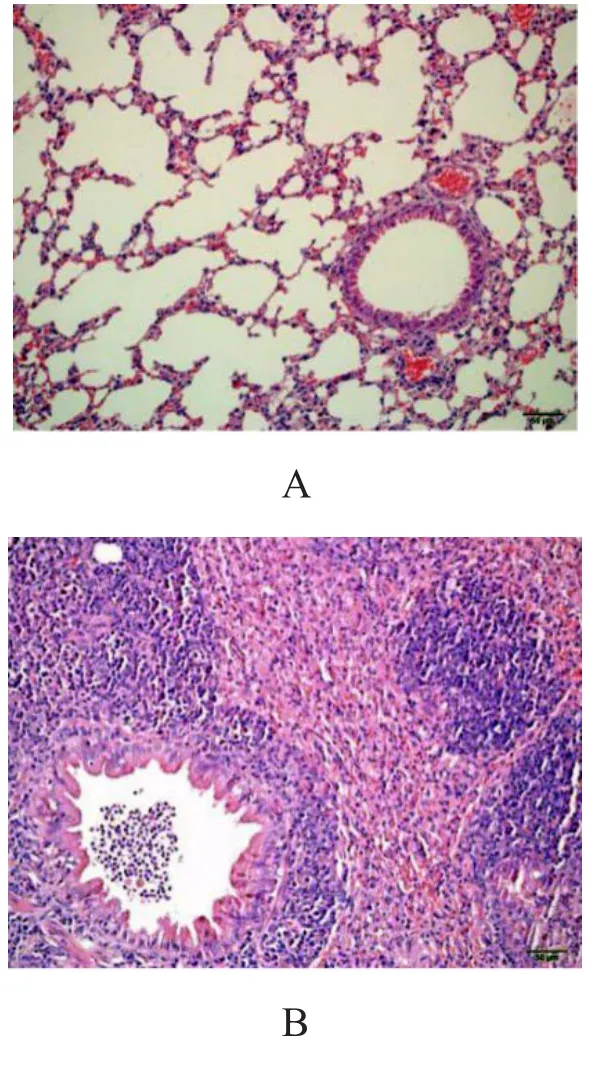
注:A:NC组;B:NA组
2.5 两组小鼠BALF中细胞因子IL-17、IL-10水平比较
NA组IL-17水平明显升高、IL-10水平明显降低,与NC组比较有明显差异(P<0.05)。见表3。
表3 两组小鼠BALF中细胞因子IL-17和IL-10水平(±s,pg/mL)

表3 两组小鼠BALF中细胞因子IL-17和IL-10水平(±s,pg/mL)
注:a与NC组比较P<0.05
组别 n IL-17 IL-10 NC组 10 41.6±7.5 118.f22.1 NA组 10 83.0±10.4a 31.5±7.2a
3 讨 论
支气管哮喘是最常见的慢性呼吸道疾病,近年研究证实支气管哮喘具有明显的异质性。过去研究显示哮喘是一种由Th2细胞驱动的“嗜酸细胞性”炎症疾病,近年的研究发现还存在除嗜酸性粒细胞哮喘外的其他炎症表型,NA、寡细胞性和混合细胞性哮喘4种亚型。而不同的炎症表型其发病机制不同。人们逐渐认识到非嗜酸细胞性气道炎症,特别是中性粒细胞性气道炎症在哮喘发病机制中的作用。我们在前人研究的基础上[3]建立了NA小鼠模型,结果显示,NA组小鼠表现为中性粒细胞浸润为主的气道炎症及气道高反应性。
支气管哮喘发病机制与免疫功能紊乱有密切联系,既往认为Th1/Th2细胞失衡是造成哮喘的免疫学发病基础,近年来研究发现Th17和调节性T细胞(Treg)及其代表性细胞因子IL-17、IL-10在哮喘发病中起着重要作用[4]。IL-17、IL-10 能在一定程度上反映Th17、Treg细胞亚群的功能状态,因而成为监测Th17/Treg 细胞功能的常用指标。IL-17具有强大的促炎和趋化免疫细胞的作用,IL-10是一种多功能负性调节因子,具有很强免疫抑制及免疫调控作用,是Treg发挥免疫调节作用的重要介质。Treg是一类具有免疫抑制作用的T细胞亚群,能负向调节免疫功能,能抑制辅助性T细胞亚群,从而防止过敏性疾病和自身免疫性疾病的发生[5]。哮喘的发作与IL-17、IL-10的水平相关,IL-17可能抑制了IL-10的产生,二者在功能上相互拮抗。本研究结果发现TH17细胞因子IL-17高于对照组,而Treg细胞因子IL-10低于对照组。
综上所述,NA小鼠BALF中细胞因子IL-17、IL-10异常变化,表现为IL-10水平降低、IL-17水平升高,TH17/Treg平衡失常,此可能为引起NA小鼠气道高反应性及气道炎症的原因。
[1]张毓娴,农光民,廖 竞,等.诱导痰液细胞学分析对儿童支气管哮喘临床分型中的应用.实用儿科临床杂志,2010,25(2):129-132.
[2]Zhao Y,Yang J,Gao YD,et al.Th17 immunity in patients with allergic asthma.International Archives of Allergy &Immunology,2010,151:297-307.
[3]刘晓微,蒋 敏,农光民,等.中性粒细胞性支气管哮喘小鼠模型的建立及其气道高反应规律的研究.中华哮喘杂志:电子版,2013,7(3):151-158.
[4]龚 臣,邓静敏.Th17/Treg在支气管哮喘发病机制中的作用及研究进展.中华哮喘杂志:电子版,2013,7(3):684-688.
[5]EusebioM,KunaP,Kraszula L, et al.The relative values of CD8+CD25+Foxp3brigh Treg cells correlate with selected lung function parameters in asthma.International Journal of Immunopathology & Pharmacology,2015,28:218-226.

