西妥昔单抗对转移性大肠癌患者血清CEA、CA199水平的影响
江璧锋,林华明
(茂名市人民医院肿瘤一科,广东 茂名 525000)
大肠癌是临床常见的恶性肿瘤之一,随着人们生活方式和饮食结构的改变,其发病率逐年增高[1]。大肠癌患者术后易出现转移和复发,增加治疗难度。全身化疗是目前临床对转移性大肠癌治疗的常用手段,FOLFOX4方案在转移性大肠癌的治疗中较为常见[2]。西妥昔单抗为单克隆抗体靶向药物(特异性靶点),能与肿瘤细胞上的表皮生长因子受体相结合,使肿瘤对放化疗的敏感性提高,加快肿瘤细胞凋亡,在大肠癌的治疗中取得良好的疗效[3]。本研究选择我院接诊的部分转移性大肠癌患者为研究对象,分组实施FOLFOX4方案和联合西妥昔单抗治疗。现报告如下。
1 资料与方法
1.1一般资料:选择我院2012年1月~2016年5月期间接诊的90例转移性大肠癌患者,根据随机数字表法分为两组,各45例。试验组:男23例,女22例;年龄34~70岁,平均(41.26±6.65)岁;病程3~8年,平均病程(5.78±1.92)年。对照组:男25例,女20例;年龄34~71岁,平均(41.27±6.68)岁;病程3~9年,平均(5.82±1.93)年。两组一般资料比较,差异无统计学意义(P>0.05)。具有可对比性。
1.2方法:对照组患者实施FOLFOX4方案治疗:第1天在250 ml的5%葡萄糖溶液中加入85 mg/m2的奥沙利铂(深圳海王药业有限公司,国药准字H20031048)行静脉滴注;第1、2天在250 ml的0.9%NaCl溶液中加入300 mg/m2氟尿嘧啶注射液(天津金耀药业有限公司 ,国药准字H12020959)行静脉滴注;第1、2天在250 ml的0.9%NaCl溶液中加入400 mg/m2亚叶酸钙注射液(重庆药友制药有限责任公司,国药准字H20010615)行静脉滴注。在此基础上,试验组予以500 mg/m2西妥昔单抗行静脉滴注治疗(BoehringerIngelheimPharmaGmbHCoKG,批准文号S20050095):初次滴注时间>2 h,而后滴注时间>1 h,每周1次。两组患者均连续治疗4个疗程,每个疗程2周。两组患者在用药前30 min均予以25 mg盐酸异丙嗪(上海禾丰制药有限公司,国药准字H31022033)行肌内注射;0.3 g西米替丁[上海现代哈森(商丘)药业有限公司,国药准字H20056905]行静脉推注,防止发生不良反应。
1.3评价指标:参考《中药新药临床研究指导原则》[4]相关标准对两组临床疗效进行评估,完全缓解(CR):病灶全部消失且维持>4周;部分缓解(PR):病灶减少1/2且维持>4周;稳定(SD):病灶减少<1/2;进展(PD):出现新病灶或病灶增加25%。CR率与PR率之和为总有效率。CR率、PR率、
SD率之和为疾病控制率。分别采集两组患者治疗前、后空腹静脉血4ml,检测血清CEA、CA199水平,均以电化学发光法测定。记录两组用药期间不良反应发生情况。

2 结果
2.1临床疗效:试验组疾病控制率与治疗总有效率均显著高于对照组,差异具有统计学意义(P<0.05)。见表1。
2.2血清CEA、CA199水平:两组治疗前血清CEA、CA199水平相比,差异无统计学意义(P>0.05);治疗后较治疗前,两组血清CEA、CA199水平治疗后均有明显降低,试验组降低幅度大于对照组,差异具有统计学意义(P<0.05)。见表2。
2.3不良反应:试验组皮疹发生率为28.89%(13/45)高于对照组的8.89%(4/45),差异具有统计学意义(P<0.05);两组其他不良反应发生率相比,差异无统计学意义(P>0.05)。见表3。
表1两组患者临床疗效对比[例(%)]

组别例数CRPRSDPD总有效疾病控制对照组458(17 78)10(22 22)14(31 11)13(28 89)18(40 00)32(71 11)试验组4511(24 44)17(37 78)12(26 67)5(11 11)28(62 22)40(88 89)χ2值4 4474 444P值<0 05<0 05


组别例数CEA(n/ml) 治疗前 治疗后 t值 P值 CA199(U/ml) 治疗前 治疗后 t值 P值 对照组45858 63±25 67317 45±16 57118 820<0 05319 57±13 47152 75±13 6258 419<0 05试验组45856 69±26 76232 54±18 31129 128<0 05318 78±13 9465 42±11 3494 580<0 05t值0 35123 0660 27333 055P值>0 05<0 05>0 05<0 05
表3两组不良反应发生率对比[例(%)]
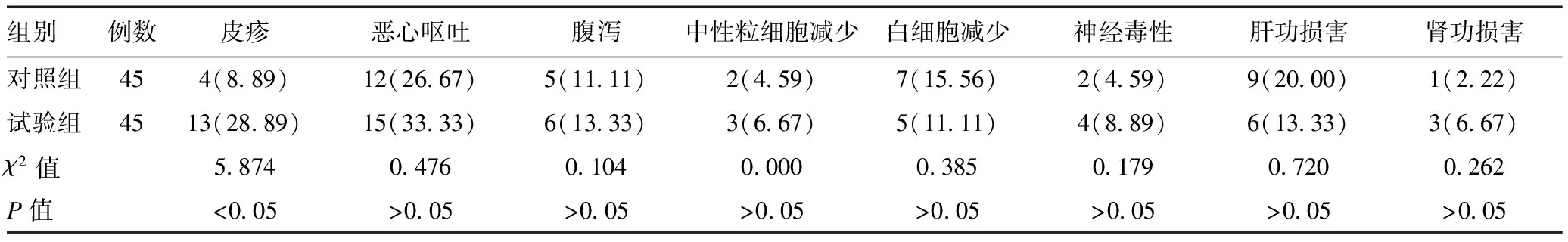
组别例数皮疹恶心呕吐腹泻中性粒细胞减少白细胞减少神经毒性肝功损害肾功损害对照组454(8 89)12(26 67)5(11 11)2(4 59)7(15 56)2(4 59)9(20 00)1(2 22)试验组4513(28 89)15(33 33)6(13 33)3(6 67)5(11 11)4(8 89)6(13 33)3(6 67)χ2值5 8740 4760 1040 0000 3850 1790 7200 262P值<0 05>0 05>0 05>0 05>0 05>0 05>0 05>0 05
3 讨论
大肠癌的发病率在我国常见肿瘤中位居第4位。本病早期诊断率较低,多数患者在确诊时已为中晚期,多为转移性[5]。目前临床治疗转移性大肠癌多以化疗药物干预为主,以将转移瘤体积缩小、提供手术切除的可能性为主要目的[6]。FOLFOX4方案是转移性大肠癌治疗的标准化疗方案,在晚期大肠癌治疗中有效率可达40%左右。其采用的奥沙利铂能经生成烷化结合物作用于脱氧核糖核酸,抑制DNA的复制和合成,防止肿瘤细胞增殖;氟尿嘧啶可在细胞内转换为5-氟尿嘧啶脱氧核苷酸,对DNA的合成造成影响[7]。
西妥昔单抗为大肠癌的靶向治疗药物,其能与肿瘤细胞上的表皮生长因子受体结合,抑制肿瘤细胞增殖信号传导,对细胞生长周期起到阻滞作用,能加快肿瘤细胞凋亡速度,进而起到防止肿瘤进展的作用。CA199为广谱肿瘤标志物,其含量在多种肿瘤组织中均有明显升高。CEA为癌胚抗原,血清中的CEA水平在肿瘤异常增殖状态时会出现明显的升高[8]。本研究中以CA199和CEA为监测指标,对大肠癌的转移和复发进行判断。结果显示,治疗后试验组血清CA199、CEA水平显著低于对照组,疾病控制率与治疗总有效率均显著高于对照组,说明联合FOLFOX4方案与西妥昔单抗治疗转移性大肠癌,能有效提高临床疗效。分析原因在西妥昔单抗存在逆转肿瘤细胞的耐药性,能有效抑制DNA修复,与氟尿嘧啶、奥沙利铂共用能起到协同作用,控制肿瘤发展。本研究中,试验组中皮疹发生率高于对照组,其他不良反应发生率相比无明显差异。皮疹是西妥昔单抗治疗中常见的不良反应,临床在治疗时应予以对症治疗,以减轻患者病痛。
综上所述,对转移性大肠癌患者实施西妥昔单抗治疗,能有效提高疾病控制率和临床疗效,改善血清CEA、CA199水平,值得临床推广与应用。
[1] 刘学伟,程龙伟,柴淑梅,等.西妥昔单抗及贝伐单抗治疗KRAS基因野生型转移性大肠癌患者的临床疗效比较[J].中国老年学杂志,2014,34(21):6003.
[2] 钱 维,陈国昌,张永镇,等.抗EGFR单抗与抗VEGF单抗联合治疗转移性大肠癌的Meta分析[J].中国肿瘤生物治疗杂志,2014,21(1):79.
[3] 曾 巍,屠宴会.奥沙利铂+5-氟尿嘧啶/希罗达联合西妥昔单抗或单纯化疗一线用于进展期大肠癌的疗效与KRAS基因状态的关系[J].中国老年学杂志,2016,36(2):363.
[4] 郑筱萸.中药新药临床研究指导原则[M].北京:中国医药科技出版社,2002.
[5] 傅军民.斑蝥酸钠维生素B6注射液联合FOLFOX4方案治疗晚期大肠癌疗效观察[J].国际肿瘤学杂志,2014,41(2):159.
[6] 宿 濛,张 睿,王 哲,等.西妥昔单抗联合FOLFIRI方案治疗大肠癌肝转移的近期疗效观察[J].肿瘤学杂志,2015,21(6):491.
[7] 徐海燕,罗 芳.西妥昔单抗联合5-氟尿嘧啶治疗晚期大肠癌临床研究[J].临床和实验医学杂志,2014,13(5):371.
[8] 秦 锐,石 燕,陈 丽,等.西妥昔单抗转化性治疗大肠癌肝转移患者的临床观察[J].解放军医学院学报,2014,35(7):696.

