CCLG-ALL2008诱导缓解方案化疗儿童急性淋巴细胞白血病的效果观察
黄欣 高清平
CCLG-ALL2008诱导缓解方案化疗儿童急性淋巴细胞白血病的效果观察
黄欣 高清平
目的 探讨CCLG-ALL2008诱导缓解方案化疗儿童急性淋巴细胞白血病(ALL)的效果。方法 回顾性选取ALL患儿134例,其中67例(观察组)给予CCLG-ALL2008诱导缓解方案化疗,另67例(对照组)给予常规多药联合化疗。观察并比较两组患儿疗效、化疗不良发应发生率、化疗后热休克蛋白90(Hsp90)表达水平、5年生存率。结果 观察组患儿治疗有效率高于对照组(P<0.05),化疗不良反应发生率与对照组比较差异无统计学意义(P>0.05),化疗后Hsp90 mRNA和蛋白表达水平均低于对照组(均P<0.05),5年生存率高于对照组(P<0.05)。结论 CCLG-ALL2008诱导缓解方案化疗儿童ALL,效果确切,预后相对较佳,值得临床应用。
CCLG-ALL2008 儿童急性淋巴细胞白血病 Hsp90 预后
急性白血病是血液系统的一类恶性肿瘤,严重危害人类健康[1]。儿童是急性白血病的高发群体,其中3/4为急性淋巴细胞白血病(ALL)。ALL的发病率和病死率均较高,在儿童病死原因中居第2位[2]。目前临床对ALL的主要治疗方法是化疗,但ALL发病原因多样、病情复杂多变,治疗相对困难,预后欠佳易复发[3]。且化疗亦严重损害人体正常组织,引发各种不良反应,加上耐药性的出现,化疗效果大打折扣[4]。如何提高化疗效果、减少不良反应是目前临床研究的热点和重点。热休克蛋白90(Hsp90)是一类分子伴侣蛋白,在肿瘤细胞中具有调节多种癌蛋白的功能,参与肿瘤细胞的生存、增殖、转移及侵袭等病理过程;有效抑制白血病细胞内Hsp90的活性,可使白血病细胞发生凋亡和分化,缓解病情[5]。CCLG-ALL2008方案是中国儿童白血病协助组(CCLG)制定的一种化疗方案。有研究显示,CCLGALL2008诱导缓解方案化疗ALL可在最短时间内杀死白血病细胞,获得有效缓解[6]。基于此,本研究旨在观察CCLG-ALL2008诱导缓解方案化疗儿童ALL的效果,现报道如下。
1 对象和方法
1.1 对象 回顾性选取2010年4月至2012年3月本院收治的经骨髓穿刺术检查确诊为ALL的患儿134例(排除既往接受过化疗者),其中67例(观察组)给予CCLG-ALL2008诱导缓解方案化疗,另67例(对照组)给予常规多药联合化疗。两组患儿性别、年龄、BMI、WBC比较差异均无统计学意义(均P>0.05),见表1。

表1 两组患者一般资料比较
1.2化疗方法
1.2.1 观察组 给予CCLG-ALL2008诱导缓解方案化疗。(1)第 1~7天:给予泼尼松片(Pred)(生产厂家:天津力生制药股份有限公司,批准文号:国药准字H12020123),用量:60mg/(m2·d);(2)第8~:停止给予Pred改为给予地塞米松(Dex),第29天开始减量,3d减半,9d减停;第8天和第15天给予柔红霉素(DNR)(生产厂家:Actavis Italy S.p.A.,批准文号:H20100552)共 2 次,每次用量:30mg/m2;第 8、15、22、29 天给予门冬酰胺酶(L-ASP)(生产厂家:贵州千红生化制药股份有限公司,批准文号:国药准字H120023613),1次/3d,每次 5 000U/m2;第 8、11、14、17、20、23、26、29 天给予长春新碱(VCR)(生产厂家:浙江海正药业股份有限公司,批准文号:国药准字H120043326)共8次,每次用量:1.5mg/m2;(3)第 1、15、33 天给予氨甲喋呤(MTX)治疗,剂量为:1~5g/m2,治疗期间进行肾功能密切监测,血清肌酐值(Scr)<1.2mg/dl,则常规给药剂量:5g/m2;Scr在 1.2~2mg/dl,则剂量减半;若>2mg/dl,则给予 1g/m2。
1.2.2 对照组 给予常规多药联合化疗。(1)第1~7天:给予Pred,用量:60mg/(m2·d);(2)第8~天:继续给予Pred,第29天开始减量,7d后减停;第8天和第9天加用DNR共2次,每次用量:30mg/m2;给予L-ASP,1次/3d,每次 5 000U/m2;第 8、15、22、29 天给予 VCR,每次用量:1.5mg/m2。
1.3 Hsp90表达水平检测 留取患儿化疗后骨髓液4ml,加入4ml淋巴细胞分离液,2 000rpm离心20min,提取单个核细胞,-80℃冰箱备存。
1.3.1 RT-PCR法检测Hsp90 mRNA表达水平 (1)严格按照Trizol试剂盒(杭州新景生物试剂开发有限公司)说明书提取组织总RNA;(2)引物设计:实验引物均由上海博亚生物技术有限公司设计合成;Hsp90引物序列为正义链 5′-GAGAGCCTGACAGACCC-3′,反义链 5′-GCCCAATCATGGAGATGT-3′;β-actin 正义链 5′-AGCGGGAAATCGTGCGTGAC-3′,反义链 5′-ACATCTGCTGGAAGGTGGAC-3′;(3)采用 Access RTPCR系统(美国Promega公司)将组织总RNA扩增成DNA目的片段,扩增条件为:95℃预变性2min,95℃变性 30s,58℃退火 30s,72℃延伸 30s,30 个循环,72℃终延伸10min;(4)PCR产物经EB染色和1.8%琼脂糖凝胶电泳后,采用紫外分析仪观察,并采用HMIAS-2000高清晰度彩色医学图文分析系统进行定量分析,用Hsp90 mRNA与β-actin的灰度比值表示Hsp90 mRNA的相对表达水平。
1.3.2 Western blot法检测Hsp90蛋白表达水平 (1)采用改良异硫氰酸胍法提取总蛋白,-80℃下冻存;(2)蛋白浓度采用NanoDrop分光光度计测量,将蛋白溶入等体积的缓冲液中煮沸10min,经聚丙烯酰胺凝胶电泳进行蛋白分离;(3)将蛋白质转印到PVDF膜上;(4)PVDF膜置入封闭液中,4℃下振荡60min,加入一抗(1∶100稀释),4℃过夜,漂洗3次(每次 10min),加入二抗(1∶1 000稀释),37℃孵育 120min,漂洗 3次(每次10min)后,与X线胶片共同放入暗盒内曝光3min,常规显影与定影,将Hsp90与β-actin蛋白的灰度值比值作为Hsp90蛋白相对表达水平。
1.4 观察指标 观察并比较两组患儿疗效、化疗不良发应发生率、化疗后Hsp90表达水平、5年生存率。
1.4.1 患儿疗效 判断标准:(1)完全缓解:临床症状消失;血象:Hb≥100g/L、PLT≤100×109/L、中性粒细胞绝对值≥1.5×109/L,原始粒细胞≤5%,外周血分类无白血病细胞,WBC及巨核细胞正常;(2)部分缓解:5%<骨髓原粒细胞≤20%,临床症状和血象中任1项未完全达标;(3)未缓解:临床症状、髓象及血象均未达到完全缓解和部分缓解。完全缓解或部分缓解视为治疗有效。
1.4.2化疗不良反应 包括恶心、呕吐、腹痛、腹泻、PLT减少及感染发生。
1.5 统计学处理 应用SPSS 19.0统计软件;计量资料以表示,组间比较采用两独立样本t检验;计数资料以频数和构成比表示,组间比较采用χ2检验;采用Kaplan-Meier法估计两组患者的生存率并绘制生存曲线,两组患者生存率的比较采用log-rank检验。P<0.05为差异有统计学意义。
2 结果
2.1 两组患儿疗效及化疗不良反应发生率比较 观察组患儿化疗后完全缓解56例,部分缓解8例,未缓解3例,发生化疗不良反应11例。对照组患儿化疗后完全缓解39例,部分缓解9例,未缓解19例,发生化疗不良反应12例。观察组治疗有效率高于对照组(95.52%vs 71.64%,P<0.05),化疗不良反应发生率与对照组比较差异无统计学意义(16.42%vs 17.91%,P>0.05)。
2.2 两组患儿化疗后Hsp90表达水平比较 见图1-2、表 2。
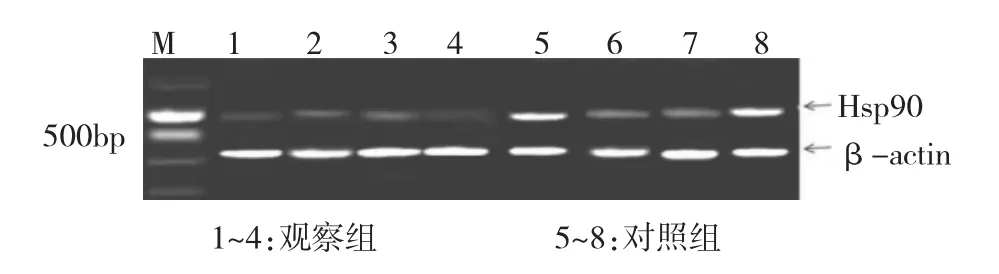
图1 两组患儿化疗后Hsp90 mRNA的凝胶电泳结果(M:DNA marker)
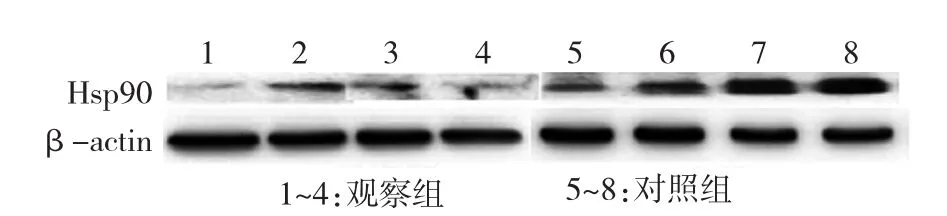
图2 两组患儿化疗后Hsp90蛋白的凝胶电泳结果
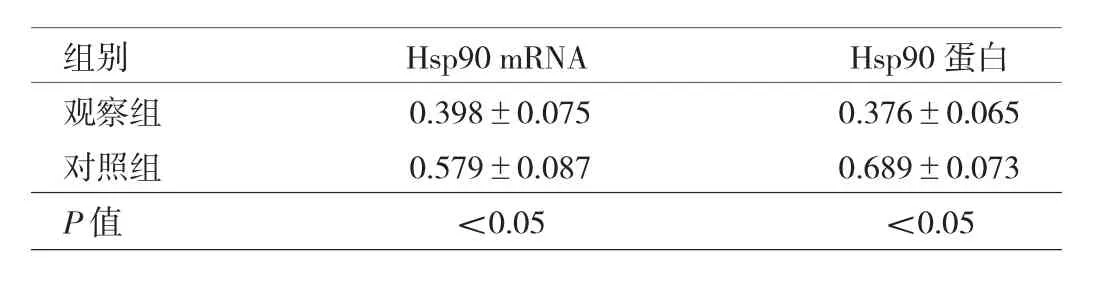
表2 两组患儿化疗后Hsp90表达水平比较
由图1-2、表2可见,观察组患儿化疗后Hsp90 mRNA和蛋白表达水平均低于对照组(均P<0.05)。
2.3 两组患儿5年生存率比较 见图3。

图3 两组患儿生存曲线比较
由图3可见,观察组患儿5年生存率高于对照组(22.39%vs 17.91%,P<0.05)。
3 讨论
白血病属于造血干细胞恶性克隆性的疾病,通常是因造血干/祖细胞发生恶变后,引起细胞增殖、分化及凋亡的异常,从而导致大量白血病细胞增加,正常造血途径受抑制[7]。白血病因基因突变的诱发而产生,通常是多个基因相互作用的结果,其突变主要表现为基因(造血细胞发育与分化基因、凋亡基因、细胞周期基因等)片段丢失或增加、点突变(ras基因)、基因融合及染色体(免疫球蛋白重链、T淋巴细胞抗原受体基因、酪氨酸激酶染色体等)易位等。这种突变是多途径的复杂过程,最终导致原癌基因被激活,而抑癌基因灭活,从而使细胞正常增殖、凋亡被干扰,相互之间平衡被破坏,白血病细胞过度聚集及分化,对正常血液细胞生成产生影响,并会侵袭其他脏器组织[8-9]。
ALL的治疗方法较多,包括生物治疗、放疗、多药联合化疗及造血干细胞移植等,目前多药联合化疗仍是主要的治疗方法[10]。诱导缓解化疗在整个ALL治疗过程中具有重要意义,CCLG-ALL2008诱导缓解化疗方案是多药联合化疗,主要包括激素、VCR、DNR及L-ASP等,可在较短时间内杀死白血病细胞,取得缓解效果[11]。本研究结果显示,观察组治疗有效率高于对照组,两组化疗不良反应发生率无统计学差异。分析原因可能是CCLG-ALL2008诱导缓解化疗方案未全程使用Pred,而是在Pred试验结束后改用Dex,且鞘内注射未选用3药联合而仅3次MTX单药鞘内注射。Dex的半衰期较长,化疗不良反应较小,尤其在ALL初治时,患者体内肿瘤负荷较高,化疗对肿瘤细胞进行破坏溶解时的不良反应会被放大,患者不耐受会影响化疗效果,并使化疗风险增高,甚至引发因化疗死亡事件的发生。在诱导缓解化疗时需平衡利弊,采取合适的化疗方案,CCLGALL2008诱导缓解化疗方案在不增加化疗不良反应的同时提高疗效[12]。另外,ALL化疗时常出现多药耐药现象,白血病细胞对某一种化疗药物产生耐药后,会继而对其他多种药物产生交叉耐药,从而使化疗失败[13]。而CCLG-ALL2008诱导缓解方案在第8天时采取Dex替代Pred,由于Dex的半衰期较长,观察组高剂量Dex的使用可大大降低耐药现象的出现,因此化疗效果更显著[14]。CCLG-ALL2008诱导缓解方案不仅减少鞘内注射的次数,更将3联药物减至单药注射,从而大大降低各种不良反应的发生,减少对器官的损伤及感染的发生。
Hsp90是Hsp家族中的成员之一,最初在升高温度的细胞中被发现,是所有真核及原核细胞生存所必需的分子伴侣,后来被证实在多种细胞中广泛存在[15]。Hsp90在信号蛋白的构象成熟及稳定和参与细胞生长中起重要作用,Hsp90含量可占正常细胞总蛋白的1%~2%,对机体具有保护作用,而在肿瘤细胞中其含量可翻倍表达,对肿瘤细胞的存活、增殖、侵袭、转移通过调节癌蛋白而参与其过程[16]。本研究结果显示,观察组患儿化疗后Hsp90 mRNA和蛋白表达水平均低于对照组。这是因为Hsp90在细胞质中无处不在,且会与多种蛋白结合形成多伴侣复合物,参与白血病细胞增殖及存活的信号传导途径,并参与白血病细胞的耐药过程[17]。而CCLG-ALL2008诱导缓解方案化疗通过Pred与Dex的适时的替代治疗,可对Hsp90进行有效抑制,阻断Hsp90对白血病细胞蛋白的释放,改变其对恶性肿瘤细胞生存和生长的潜能作用,因此Hsp90表达越低,说明缓解效果越好。
本研究结果显示,观察组患儿5年生存率明显高于对照组。分析原因可能是通过CCLG-ALL2008诱导缓解方案化疗可使患儿更加完全顺利的渡过第一阶段的治疗,缩短骨髓抑制时间的同时降低感染,可提高患儿的治疗依从性并降低复发率,利于预后。
综上所述,CCLG-ALL2008诱导缓解方案化疗儿童ALL,效果确切,化疗不良反应发生率较低,预后相对较佳,值得临床应用。
[1] Traversa G,Menniti-Ippolito F,Da C R,et al.Drug use and acute leukemia[J].Pharmacoepidemiology&Drug Safety,2015,7(2):113-123.
[2] Singh N,Frey N V,Grupp S A,et al.CAR T Cell Therapy in Acute Lymphoblastic Leukemia and Potential for Chronic Lymphocytic Leukemia[J].Current Treatment Options in Oncology,2016,17(6):28.
[3] Douer D.Efficacy and Safety of Vincristine Sulfate Liposome Injection in the Treatment of Adult Acute Lymphocytic Leukemia[J].Oncologist,2016,21(7):840.
[4] Hauner K,Maisch P,Retz M.Side effects of chemotherapy[J].Der Urologe,2015,73(6):39-44.
[5] Georgakis G V,Younes A.Heat-shock protein 90 inhibitors in cancer therapy:17AAG and beyond[J].Future Oncology,2015,1(2):273-281.
[6] 陈晓娟,邹尧,杨文钰,等.CCLG-ALL2008方案治疗儿童急性淋巴细胞白血病复发患儿的特征分析[J].中国当代儿科杂志,2015,17(4):321-326.
[7] Bleakley M,Heimfeld S,Loeb K R,et al.Outcomes of acute leukemia patients transplanted with naive T cell-depleted stem cellgrafts[J].Journalof ClinicalInvestigation,2015,125(7):2677-2689.
[8] Zhou J,Ching Y Q,Chng W J.Aberrant nuclear factor-kappa B activity in acute myeloid leukemia:from molecular pathogenesis to therapeutic target[J].Oncotarget,2015,6(8):5490-5500.
[9] Prunier C,Zhang M Z,Kumar S,et al.Disruption of the PHRF1 TumorSuppressorNetworkbyPML-RARα DrivesAcute Promyelocytic Leukemia Pathogenesis[J].Cell Reports,2015,10(6):883-890.
[10] Yilmaz M,Richard S,Jabbour E.The clinical potential of inotuzumabozogamicin in relapsed and refractory acute lymphocytic leukemia[J].Therapeutic Advances in Hematology,2015,6(5):253-261.
[11] Chen B,Xian Y,Su Y C,et al.A clinical study of drug-related toxicities of CCLG-ALL 08 protocol for childhood acute lymphoblastic leukemia[J].Chinese Journal of Contemporary Pediatrics,2013,15(9):737.
[12] Wang F,Xiao S J,Lin M.Treatment outcome of childhood standard-risk acute lymphoblastic leukemia with CCLG-08 protocol[J].Chinese JournalofPracticalPediatrics,2013,28(2):111-113.
[13] Rose-James A,Shiji R,Kusumakumary P,et al.Profiling gene mutations,translocations,and multidrug resistance in pediatric acute lymphoblastic leukemia:a step forward to personalizing medicine[J].MedicalOncology,2016,33(9):98.
[14] 王慧敏,欧阳涓,滕军旗,等.地塞米松诱导急性T淋巴细胞白血病细胞耐药及对miR-15b表达的影响[J].热带医学杂志,2016,16(6):695-698.
[15] Lamoth F,Juvvadi P R,Steinbach W J.Heat shock protein 90(Hsp90):A novel antifungal target against Aspergillusfumigatus.[J].CriticalReviews in Microbiology,2016,42(2):310-321.
[16] Liu H,Lu J,Hua Y,et al.Targeting heat-shock protein 90 with ganetespib for molecularly targeted therapy of gastric cancer[J].CellDeath&Disease,2015,6(1):e1595.
[17] Wang R,Shao F,Liu Z,et al.The Hsp90 inhibitor SNX-2112,induces apoptosis in multidrug resistant K562/ADR cells through suppression of Akt/NF-κB and disruption of mitochondria-dependent pathways[J].Chemico-biological interactions,2013,205(1):1.
Efficacy of CCLG-ALL2008 inducing remission chemotherapy in children with acute lymphoblastic leukemia
HUANG Xin,GAO Qingping.
Department of Hematology,People's Hospital of Wuhan University,Wuhan 430060,China
Objective To evaluate the efficacy of CCLG-ALL2008 induction chemotherapy in children with acute lymphoblastic leukemia(ALL). Methods One hundred and thirty four children with ALL were treated with chemotherapy,including 67 cases receiving CCLG-ALL2008 induced remission chemotherapy (study group)and 67 cases receiving conventional multi-drug combination chemotherapy (control group).The curative effect,incidence of adverse reactions,expression of heat shock protein 90 (Hsp90)after chemotherapy and the 5-year survival rate were observed and compared between the two groups. Results The effective rate in study group was higher than that in control group(P<0.05).There was no significant difference in incidence of adverse reactions between two groups(P>0.05).After chemotherapy,the expression of Hsp90 mRNA and protein in study group was lower,and the 5-year survival rate was higher than those in control group(P<0.05).Conclusion CCLG-ALL2008 inducing remission chemotherapy is more effective than conventional chemotherapy in children with ALL.
CCLG-ALL2008 Childhood acute lymphoblastic leukemia Hsp90 Prognosis
10.12056/j.issn.1006-2785.2017.39.24.2017-1178
430060 湖北,武汉大学人民医院血液科
高清平,E-mail:gaoqingping@163.com
2017-05-22)
李媚)

