多孔介质中天然气水合物生成影响因素研究进展
潘振,刘志明,刘德俊,商丽艳,李文昭,李萍
多孔介质中天然气水合物生成影响因素研究进展
潘振1,刘志明1,刘德俊1,商丽艳2,李文昭1,李萍2
(1辽宁石油化工大学石油天然气工程学院,辽宁抚顺 113001;2辽宁石油化工大学化学化工与环境学部,辽宁抚顺113001)
天然气水合物是天然气分子和水分子在低温高压条件下形成的非化学计量的笼型晶体。作为一种潜在性能源的同时,其在工业上也有广泛的应用前景。自然条件下的水合物主要存在于永冻区和海底沉积物的空隙中,实验模拟自然条件下水合物的生成,对于研究水合物的成矿机理、勘探开采以及工业应用都具有实际意义,因此许多学者在多孔介质中进行了水合物的生成实验。本文通过整理前人的研究成果,总结了多孔介质环境下介质粒径、表面特性以及添加剂(盐分和表面活性剂)的协同作用对于水合物生成速率和相平衡的影响,并归纳了不同反应条件下水合物在多孔介质中的生成位置分布情况以及几种热力学理论模型;最后提出,介质表面特性、不同种类多孔介质与盐离子的混合体系对水合物生成的影响以及多孔介质中不同的反应条件对水合物的生成位置的影响均值得进一步探讨和明确。此外,裂隙环境中不同的裂隙宽度及壁面粗糙度条件下水合物的生成情况也需要进行深入研究。
天然气水合物;多孔介质;相平衡;表面活性剂;影响因素;模型
随着石油资源的不断开采,其剩余储量在不断减少,为了保证能源供应,一种具有极大应用前景的资源逐渐进入人们的视野,即天然气水合物。天然气水合物俗称“可燃冰”,是在低温和高压条件下,由一些较小分子量气体和水分子形成的复杂笼型晶体物质[1],广泛存在于冻土带、水深大于100~250m(两极地区)和大于400~650m(赤道地区)的海床以下数百米至1000多米的沉积层内[2]。据估计,永久冻土区和海底沉积物中赋存的天然气水合物,总量可达7.6×1018m3,开采和应用前景巨大[3]。
除了资源量巨大,水合物在工业上也有着广泛的应用前景,标准状况下1单位的水合物可以储存164单位甚至更多的气体,可作为气体储存与运输的介质[4];另外,水合物晶体的形成过程中会存储大量的冷量,此性质可以应用在制冷、气体捕集及净化等行业[5-6]。自然条件下,天然气水合物存在于沉积物的孔隙中,由于孔隙中存在的毛细效应等因素的影响,其生成过程及相平衡特点将会与块状水合物有明显的差异[7]。
因此,为了进一步开发利用水合物资源,就必须深入了解沉积物孔隙中水合物的特点,同时,研究并掌握水合物在多孔介质中的生成特点,也能够早日实现水合物技术在工业上的应用。实验中为了模拟自然条件下水合物的生成过程,通常采用不同材料的多孔介质进行实验。本文就多孔介质环境中,颗粒粒径、介质表面特性、孔隙水盐度和表面活性剂等因素对水合物生成的影响进行了梳理和分析,并对多孔介质中不同反应条件下水合物的生成位置以及几种预测水合物生成条件的热力学模型进行了归纳。
1 多孔介质对水合物生成速率及相平衡的影响
由于多孔介质具有孔隙结构,会对内部液体的传热传质产生影响[8],进而影响其中水合物的生成速率与相平衡条件。LINGA等[9]分别在硅砂构成的柱状反应床和搅拌条件下的水溶液中进行水合物生成实验。结果表明,在硅砂中水合物的生成速率明显比水溶液中高。因此,在水合物生成时,不仅应该考虑水合物生成时的温度压力等本征动力学特性,还应该考虑多孔介质特性对其生成过程中传热传质的影响。本节着重对多孔介质的颗粒粒径与表面特性的影响进行整理和分析。
1.1 颗粒粒径对生成速率和相平衡的影响
不同的颗粒粒径会形成不同直径的孔隙,导致不同的毛细管力和表面张力,进而影响其中水合物的生成速率与相平衡[10]。近年来,许多学者研究了不同多孔介质颗粒粒径情况下水合物的生成特征,取得了一定的成果。但是无论是粒径对反应速率的影响还是对相平衡条件的影响,不同学者之间均存在着争议。
1.1.1 粒径对生成速率的影响
对于粒径因素对水合物生成速率的影响,其争议主要为粒径越大水合物生成速率越快还是相反。认为大粒径条件下水合物生成速率快的学者指出,小孔径产生的毛细管力大,能降低水的活度,并且阻碍气体的扩散,而大粒径由于对水分子和气体分子的束缚较小,并且相对于纯水体系增大了气-水接触面积,因此能加快水合物生成速率;而持相反观点的学者则认为,由于粒径大小与多孔介质的比表面积成反比,粒径越小意味着介质能提供更多的成核位置,进而有利于水合物生成。
(1)小粒径有利于水合物生成
BAGHERZADEH等[11]采用核磁共振的方法在硅砂介质中进行了细致的水合物生成实验,介质粒径范围分别为210~297μm、125~210μm、88~177μm和小于74μm。结果表明,水合物在这些介质中的生成情况并不统一,小粒径介质中的生成速率明显较快,如图1所示。
ZHAO等[12]同样采用了核磁共振成像的方法研究了水合物在玻璃珠中的生成。实验结果表明,随着粒径的减小,水合物的成核诱导期缩短并且生成速率增加。另外温度越低,多孔介质对于水合物成核速率的影响越明显。

图1 全饱和条件下不同粒径多孔介质中水分转化率[11]
李明川等[13]也指出多孔介质会明显减少水合物生成的诱导时间,并且随着颗粒粒径的减小,缩短的时间越长。
(2)大粒径有利于水合物生成
WROTTESLEY[14]则通过实验得出了相反的结论,他们发现水合物更容易在较大的孔径中成核。TURNER等[15]的研究成果或许能够解释这一实验现象,他们通过实验认为晶核形成的尺寸大小与温度有关,温度越低,晶核形成的尺寸就会越小。因此水合物若在较小的孔隙中形成,就需要更低的温度来形成小尺寸的晶核,即所需的温度条件相对苛刻。而水合物形成大尺寸晶核时由于所需的温度条件更容易达到,所以水合物更容易在大孔径中生成。
CHONG等[16]采用了4种粒径不同的硅砂作为多孔介质进行水合物生成实验,发现硅砂粒径越小水合物越不易生成,且生成水合物的携气率越低。同时,SUN等[17]也指出相比于大孔径,小孔径的毛细管力更强,在降低水活度的同时不利于气体分子的扩散,阻碍了气体与水分子的接触,所以水合物会优先在毛细管力较弱的大孔径中生成。
综上可知,对于同一种多孔介质而言,随着粒径变化,其表面积和毛细管力也会相应变化,而两者对于水合物生成速率的影响正好是相反的,因此本文作者认为理论上应该存在一种临界尺寸,使得两者对于水合物生成速率的影响达到平衡。大于此临界尺寸的多孔介质由于毛细管力较小并且提供了一定的成核位置,使水合物生成速率加快;小于此临界尺寸时,根据小粒径能加快水合物生成的实验现象推断,应该是由于较大的表面积提供的成核位置占主导因素,使生成速率加快;当粒径正好为此临界尺寸时,由于毛细作用产生的抑制作用和提供成核位置产生的促进作用正好平衡,宏观表现为对水合物的生成不产生影响。通过总结上述学者的研究,可以发现在他们的实验中采用的介质种类和实验条件均有所差别,而采用同一种多孔介质进行研究的也有可能因为粒径范围不够大而得出了单一结论,所以接下来可以在同种介质的条件下进行粒径范围更大的实验,明确粒径大小对水合物生成速率的影响以及此临界尺寸是否存在。
1.1.2 粒径对相平衡的影响
水合物生成需要一定的相平衡条件。当水合物在多孔介质中生成时,多孔介质提供的成核位置及其内部的孔隙,会对水合物成核的相平衡条件产生影 响[18]。目前有多位学者研究了粒径大小对于相平衡的影响,但是得出了不同的结论。有的学者指出,孔隙中的毛细作用能够降低水分子的活度,从而需要更大的过冷度和驱动力来生成水合物,使相平衡条件苛 刻[19]。得出不同结论的学者则认为,由于多孔介质增大了气液接触面积,并提供更多的成核位置,同时第三界面的存在使水分子排列更加有序,所以水合物在较高温度和较低压力的条件下即可生成,使相平衡条件相对宽松[20-21]。目前关于介质粒径对于水合物相平衡条件影响的争议,主要集中在这两点。
(1)多孔介质环境下相平衡条件更苛刻
李明川等[13]指出多孔介质的存在会使水合物生成的相平衡曲线向左上方偏移,即相平衡温度更低,压力更高,且介质粒径越小,对相平衡条件影响越大。他们认为这是由于多孔介质孔隙会产生很强的界面张力和毛细管凝聚作用,从而导致水合物在其内的生成与在纯液态环境中的生成有很大差别。
KANG[22]在硅胶中进行水合物相平衡研究时发现,硅胶在使水合物生成速率增大,气体消耗量增加的同时,会使相平衡的温度更低,压力更高。如图2所示。他同时提到,由于实验所采用的硅胶粒径为数十到上百纳米,远大于分子级别尺寸,所以在硅胶中生成的水合物结构与块状水合物并无 差异。

图2 不同粒径硅胶中甲烷水合物相平衡曲线[22]
采用逐步升温法来研究水合物相平衡条件[23],发现在给定压力下,多孔介质中水合物分解温度与块状水合物相比明显降低,即当水合物在多孔介质中生成时,其生成温度也会较块状水合物有所降低。通过实验进一步发现,介质的粒径越小温度下降的程度越大。
YONGWON等[24]则在多孔硅胶中测定了甲烷生成的相平衡条件,同时用van der Waals- Platteeuw模型进行计算,将两者结果进行比较后发现,温度一定时多孔介质中的水合物三相-w-平衡曲线将会向压力更高的方向移动。他通过NMR光谱发现了与KANG[22]相同的结果,即硅胶孔中的水合物结构和块状水合物结构一样,并且两者的水合数也是相同的。这一结果与将要在下一部分讨论的MIYAWAKI等[25]的实验结果有差异,MIYAWAKI等[25]发现活性炭微孔中水合物结构不同于块状水合物,但是经过对比可以发现,由于后者是在直径与气体分子类似的活性炭微孔中进行实验,而前者为数十纳米的硅胶,可能是因为介质孔隙的大小不同导致了他们实验结果的差异。
(2)多孔介质环境下相平衡条件更宽松
CHA等[26]认为多孔介质中水合物可以在较高的温度下生成,指出多孔介质存在时水分子会在其表面上有序排列,使之更容易形成生成水合物所需的笼形结构,从而含有第三界面的水合物生成比在纯水中快。为了解释这一促进现象,他们分别从热力学和动力学两方面进行了假设:热力学方面的促进可能是由于水分子在第三界面上的有序排列导致水合物生成时将界面作为了水合物的一部分,改变了水合物形成时需要的温度压力条件;动力学方面的促进则可能是因为第三界面的存在为水合物的生成提供了成核中心,使水合物晶核更容易生成。两方面的共同作用使水合物生成时的相平衡条件变得相对宽松。
在皂土悬浊液中生成水合物[27],发现当温度在4~6℃之间时,生成水合物所需的过压条件在纯水中必须大于4MPa,而在浓度为200mg/L的皂土悬浊液中平均仅为0.66MPa,皂土悬浊液的存在明显的降低了水合物形成所需的压力,使水合物更容易生成。由于实验中采用的是悬浊液,因此水合物生成过程中不存在孔隙的作用,由此可见,多孔介质条件下,不仅孔隙产生的毛细作用会影响水合物的相平衡条件,其界面的性质及其所提供的成核位置也会产生一定的影响。MORGAN等[28]和BLACKWELL等[29]也都通过实验,得出了多孔介质中较低的压力和较高的温度下水合物即可生成的结论。
臧小亚等[30]认为,存在上述争议的一个原因可能是没有对多孔介质进行分类。按照相关分类标准,多孔介质按照孔径大小分为微孔(孔径小于2nm)、介孔(孔径范围为2~50nm)和大孔(孔径大于50nm)三类。目前,微孔材料用于和水合物法结合以吸附的方式来储存气体;而介孔材料一般认为会对水合物的生成产生较大的影响,使相平衡压力升高和温度降低;对于大孔介质,一般认为其中的水合物的稳定性与块状水合物没有明显差异,其粒径对水合物相平衡的影响没有微孔和介孔明显,但是其对水合物生成动力学的影响不能忽略,能加快水合物结晶与生长的速率。
目前,对多孔介质条件下水合物生成的研究多集中在介质种类、粒径和温度压力等因素上。其影响原因一般认为是由于在多孔介质较大的比表面积、表面张力和毛细作用力的影响下降低了水的活度从而改变相平衡[31]。由于水合物优良的储气特性和安全性,决定了其在工业上将会有巨大的应用前景,所以利用多孔介质加快水合物的生成速率,无论是对于更好地了解水合物性质还是促进其在工业上的应用都是非常重要的。但是,在确定促进水合物生成的最佳介质种类及生成条件时,也应尽量侧重于多孔介质的运输成本问题,尤其是质量和体积等因素,以降低工业应用成本。
1.2 介质表面特性的影响
固体介质表面对水合物生成产生影响的原因可能是固-液界面处水分子排列方式的改变,进而改变了水合物的生成过程。例如实验研究表明相对于纯液体实验条件,脱斑土界面的存在使甲烷水合物的生成速率明显增加[32]。水合物生成过程分为溶解期、诱导期和生长期,其中水合物生成速率的快慢很大程度上与诱导期的成核速率有关[33]。固体表面上的成核过程,将会受到其亲水性和结晶度的不同而受到影响,而白冬生[34]的研究结果表明,由于局部水分子排列结构受到表面结晶度的影响很弱,所以水合物成核的诱导时间几乎和表面结晶度是无关的。所以本部分将会着重对成核表面的亲水性强弱对水合物成核的影响展开讨论。
在实验研究方面,LI等[35]在采用拉曼光谱的方法,研究了具有亲水、部分疏水和完全疏水性表面的玻璃颗粒对水合物生成的影响。结果表明,在疏水表面上水分子的排列有序度最高,水合物生成的平均诱导时间也越短,揭示了水分子在固体表面的有序度与水合物成核快慢之间的关系。在他的另一次实验中[36],同样采用了3种表面性质不同的玻璃珠,分别研究了水溶性的四氢呋喃和四丁基溴化铵、非水溶性的环戊烷和甲烷生成水合物的情况。发现疏水表面能显著地增加水合物成核速率,而对于部分疏水表面和亲水表面,对非水溶性材料没有促进作用而对水溶性材料有较弱的促进作用,但是其促进效果均没有疏水性表面明显。两次实验均表明疏水表面有助于水合物成核。
MIYAWAKI等[25]使用含有纳米微孔的疏水性活性炭进行了水合物生成实验,也得到了相同的结论。不同的是在纳米微孔中,由于孔径较小,通过GCMC模拟和X射线衍射的方法均发现水分子在吸附时会形成一种二维网状结构,再和甲烷生成一种新的分子化合物,其结构不同于块状水合物。在上面提到的一篇文章中,SUN等[17]在解释细砂粒对相平衡的影响时提到,硅砂表面的亲水性降低了孔隙中水的活度,使生成水合物所需温度更低,压力更高,不利于水合物的生成。
但是在数值分析方面,却得到了不同的结论。KASHCHIEV等[37]采用了结晶动力学理论,得到了水合物成核功、界面张力和基质表面润湿角的关系。最终发现,界面张力一定时,成核功与润湿角成正比,而亲水性越强,接触角越小。因此他们认为成核基质的亲水性越强,水合物越容易形成。
从吉布斯自由能的角度进行研究发现[38],当固液宏观平衡接触角大于90°时(即疏水性表面),固体表面对成核的影响非常小;当固液宏观接触角小于90°时(即亲水性表面),固体表面将会极大地促进成核过程,如图3所示。SLOAN等[39]也通过研究吉布斯自由能的变化对成核过程的影响也得出了相同的结论,即亲水性的表面对水合物成核具有促进作用。
通过总结前人的研究成果可以发现,目前关于成核基质亲水性对水合物成核的影响存在不同的结论。通过实验研究的学者得出疏水性越强,促进成核效果越好,水合物越容易生成;而通过数值模拟等方法来进行研究的学者则得出了相反的结论。水合物在固体表面的成核过程是十分复杂的,在具体的实验过程中很可能受到各种因素的作用。而建立模型进行数值模拟也未必能够将所有可能的因素加以考虑,因而会导致研究方法不同而得出不同的结论。从理论上讲,表面亲水性越弱,其对水分子的束缚也越弱,考虑到传质对于水合物生成速率的重要性,此时将更有利于水合物成核,而成核以后,水合物将会远离固体表面,此时的生长速率将不会受固体表面性质的太大影响,而主要取决于体系的温度和压力[34];再者由于此项技术的研究目的是为了以后的工业应用,所以进行具体的实验操作更加符合实际的情况,其得出的结论对于工业应用而言也将更有意义。

图3 异质形核中固体表面上水分子簇模型[38]
—液体的曲率半径;xx—分别为组分的摩尔分数;—接触角;σ、σ和σ—分别为所在位截的界面能
在接下来的工作中,应集中在争议的焦点进行研究,不断优化数值分析模型,纳入更多的影响因素,使其更接近实际情况;实验上应从更加微观的角度如接触角和界面张力等方面,对水合物在疏水性和亲水性界面的生成机理进行研究,进一步明确两种界面对水合物生成的影响。
2 多孔介质中水合物生成位置
由于多孔介质内部存在孔径很小的孔隙,产生的毛细作用会对内部反应水的迁移产生影响,而体系内不同位置水分的含量将会直接影响该处水合物的生成情况,所以多孔介质内部不同的条件会导致水合物在不同的位置生成[40]。可以对此性质进行研究,使水合物在多孔介质中快速生成的同时控制其生成位置,以便于将水合物与多孔介质进行分离。由于水合物的储气特性决定了在工业上可以通过水合物的方法进行气体的储存运输[41],若将水合物在多孔介质中生成后再分离,就可以降低生产周期和以后的运输成本,增强其在工业上的实用性。
在研究硅胶中水合物生成特点时发现,硅胶和水的质量比与水合物在多孔介质中的生成位置之间存在着密切关系[42]。当两者质量比大于1∶6时,水合物将会优先在介质顶部的气相区域中生成;当质量比小于1∶6时,水合物则在多孔介质的孔隙中生成。携气率方面,虽然生成位置随着硅胶和水的质量比不同而变化,但是水合物的携气率在各种条件下相差并不大。因此,可以在不影响水合物储气能力的前提下,控制水合物在多孔介质中的生成位置以便将两者分离,这将有助于水合物法在气体储运中的应用。
ZHANG等[43-44]在两次实验中分别研究了多孔介质在全饱和与半饱和情况下,水合物生成的位置分布和水分的运移情况,实验通过一种新型装置pF-meter传感器可测量反应釜上部、中部和下部含水量的变化。研究发现,在全饱和情况下,采用上部进气,水合物在粗砂和细沙中均先在上部生成,并且水分会在毛细管力的作用下从砂体底部迁移到上部;随着反应的进行,水合物的生成位置发生了变化,在粗砂中会逐渐在中部生成,而在细沙中却没有出现这种现象;两者的底部直到实验结束也没有发现水合物生成。
在半饱和情况下,仍采用上部进气的方式,加入了对黄土的研究。实验发现:在粗砂底部含水量最高,但是水合物在上部生成;细沙上部含水量最高,水合物主要在底部生成;粒径最小的黄土上部的含水量最高,水合物在整个范围内生成,将其从反应釜中取出时,生成的水合物将黄土整体固结在一起。如图4所示。在水分的迁移方面,发现粗砂中水分将会从底部运移到上部;细沙中正好相反;而在黄土中整个范围内没有发现明显的水分变化。由此可见,不同大小的孔径产生的毛细管力将会对内部的水分分布产生很大影响,进一步影响水合物生成位置。另外,由于两次实验均采用了上部进气的方式,因此若采用其他的进气方式是否会得到不同的实验现象也是值得研究的。
CHONG等[16]在研究粒径对水合物生长影响的同时也注意到了类似的现象。在卵石、粗砂和细沙中,水合物的生成位置有很大不同。对于卵石和粗砂粒,水合物在其顶部大量生成,而对于细沙粒,生成的水合物大都分散在多孔介质的孔隙里,如图5所示。该作者因此指出,在较大的粒径中由于毛细管力的作用导致的水分运移更加突出,导致了其顶部有更多的水合物生成。但是一般来讲,孔隙越小产生的毛细作用越大,对水分的运移和吸附作用也就越大,因此这一实验现象与理论不符,文中没有进一步明确导致这种现象产生的原因。

图4 半饱和情况下水合物在粗砂、细沙和黄土中的分布情况[44]
(a1)、(b1)、(c1)分别为粗砂、细沙和黄土中水合物生成后在反应釜内的图像;(a2)、(b2)、(c2)分别为粗砂、细沙和黄土中水合物生成后在反应釜外的侧面图像
刘锋等[45]在模拟海泥沉积物中甲烷水合物的生成实验时,发现水合物在沉积物中出现了分层生长,如图6所示。该作者认为产生这种现象的原因是实验中沉积物含水并不饱和,水会由于自重向反应釜底部聚集,所以含水量会比上部高,因此分别将两者称为富水沉积层和贫水沉积层。气体从上部进入,从生成的水合物位置进行推断,水合物层会先在含水量大的底部生成,然后再在含水量较少的上部生成,从而造成了水合物的分层生长。

图5 不同介质中水合物生成图像[16]
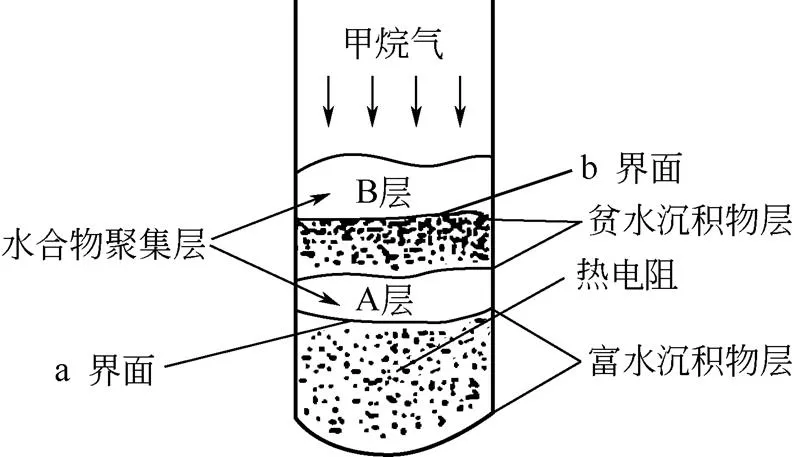
图6 水合物在沉积物中分层形成示意图[45]
由于自然环境中的水合物大都在沉积物的孔隙中生成,所以通过研究反应条件对水合物在多孔介质中生成位置的影响,不仅有助于水合物法在工业上的应用,更能通过了解这些性质,明确水合物在自然条件下的生成特点和物性,指导工业上对水合物的勘探和开采。
3 多孔介质与添加剂协同作用的影响
3.1 多孔介质与孔隙水中盐分的协同作用
自然条件下海底的水合物多为海水和天然气在海底沉积物中生成,海水中各种各样的盐离子以及沉积物复杂的壁面性质,都会对水合物生成时的相平衡条件产生影响[46]。当盐类溶于水中时将会电离出带电离子,单个带电离子会同时吸引不同的水分子簇,增加水分子的无序性。这将会改变体系内的焓和熵,根据熵的定义,水的混乱度越大系统的熵就越大,由=―知吉布斯自由能将会减少,此时体系的内能会发生变化。一般来讲,在纯水中水分子可以自由取向并与周围其他水分子形成氢键以使体系能量最低[47]。而含盐体系中由于改变了平衡体系的内能,因此溶液再达到能量最低状态时体系的热力学条件就会发生变化,并主要体现为温度和压力的改变[48-49]。因此在水合物成核时,盐分的存在无疑会改变这种热力学条件,影响水合物生成的相平衡。
由前面的分析可以知道,多孔介质界面性质及毛细作用会影响水分子的排列方式及活度,因此多孔介质和盐分都会对水合物生成的相平衡产生影响,将两者在实验条件下同时研究,不仅能更好地揭示两者对水合物生成的影响及其相互的影响关系,也能使实验条件更接近于自然界水合物生成和赋存的环境,使得研究更有意义和实用性。
杨明军等[50]在玻璃砂中研究了不同浓度的氯化钠溶液对水合物生成的影响,结果表明在同一粒径的玻璃砂中,加入盐溶液后会使水合物相平衡曲线向左移动,且盐浓度越大移动的程度越大。HAUGE等[51]则在恒压8.37MPa和4℃的条件下,研究了砂石中水合物生成速率随NaCl溶液浓度的变化情况,发现随着盐浓度从0.1%~3.5%(质量分数)逐渐升高,水合物生成速率逐渐降低。即浓度越大,对水合物的抑制效果越明显。
在用不同盐度的盐水浸湿的砂石中进行实验时发现[52],较高的盐度会延长诱导时间并且减少水合物生成,如图7所示。同时发现当采用的卤水盐度低于自然条件下海水中的盐度时,对水合物在砂石中的填充率没有太大的影响,反之填充率将会有显著降低。

图7 初始盐度不同时水合物在多孔介质中填充率曲线[52]
MEKALA等[53]在实验中发现在温度为277.2K、驱动力为4.2MPa条件下,水合物在纯水中生成时水分转化率为72%,但在质量分数为3.03%的盐水中,转化率仅为11.6%。同时通过比较纯水和盐水中的气体吸收曲线,发现在相同的压力和温度下,水合物在盐水环境下生成缓慢。所以盐分的存在,减少了气体的吸收率并且降低了水合物生成速率。
从水合物系统动力学模型出发,利用解析方法来研究盐度对水合物系统稳态的影响方面,也有学者进行了研究。杨顶辉[54]利用拟解析方法将纯甲烷气水合物系统的稳态模型推广到一种包含盐度的新稳态模型。通过数值方法来确定甲烷气水合物稳定带(MHSZ)和甲烷气水合物实际存在区(MHZ)的顶界和底界,发现甲烷水合物实际存在区的厚度随盐度的增大而变薄;盐分的存在降低了气体水合物的稳定性,引起稳定带的地界上移,所以含盐水中水合物稳定带的厚度比纯水情况下要薄,如图8所示。
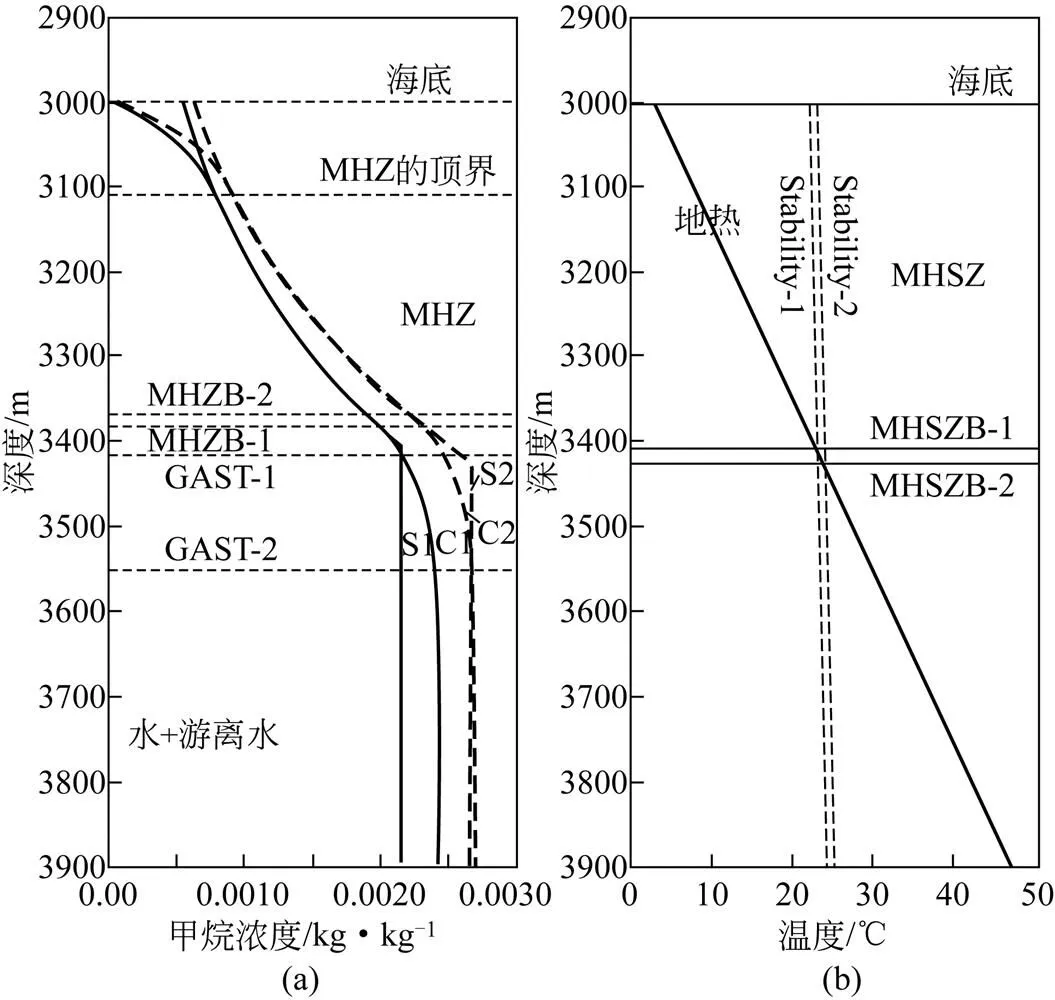
图8 在盐度为2.5%(质量分数)的盐水甲烷气水合物系统和不含盐系统两种情况下,盐度对MHZ、MHSZ以及游离气区的影响比较[54]
采用模拟退火算法来确定水合物稳定的热力学条件[55],可以得到与上述相同的结论。但是同时发现,由于体系中盐分的存在,会使甲烷气体在溶液中的溶解度下降,说明盐分存在的条件下更少量的气体就能使溶液达到过饱和状态。据此研究者认为盐分的存在实际上是有助于水合物生长的。这种看法有一定的道理,因为根据其研究结果,盐分的存在确实能够减少生成水合物时所需气体的量。但是从另一方面,盐分也会使水合物生成速率减缓,并且降低水合物在多孔介质中的填充率。再者,相对于无盐体系,少量的气体就能生成水合物意味着水合物储气密度的降低,因而从这方面来讲,盐分的存在将不利于在工业上水合物的快速生成和采用水合物法进行气体的储运。
由于自然条件下海底沉积物环境的复杂性,在实验条件下研究不同种类的盐分和不同种类的多孔介质复配体系随水合物的影响,在工业上具有很大意义,可以以此模拟各种自然环境下水合物的生成,来了解其成藏机理和赋存特点,为实际的开采工作提供指导。
3.2 多孔介质和表面活性剂的协同作用
由于目前阻碍水合物的工业应用的重要原因之一是水合物生成速率较慢,而通过改善反应过程中的传热和传质条件可以改善其生成速率,通过众多学者对多孔介质对水合物生成影响的研究,发现多孔介质的存在能够为水合物提供较大的成核位置并能够及时传导生成热,改善反应中的传热条件;而表面活性剂通过降低液体的表面张力,减小气液传质阻力,能有效改善反应中的传质条件[56-58]。因而在实际的研究中,许多研究者通过将多孔介质与表面活性剂复配,来研究此复配体系能否加快水合物的生成速率。
MOHAMMADI等[59]通过将纳米银颗粒和SDS复配进行实验。比较了分别单独使用纳米颗粒与SDS的单一体系和将两者复配的混合体系对水合物生成的效果。最终发现单独使用两者时气体的消耗量虽均有提升,但是效果并没有两者混合的体系中明显。相比于纯水中,SDS和纳米银颗粒的同时存在能将气体消耗量提升93.9%,如图9所示。另外发现在高压下同时使用两者能改善水合物的储气能力并增加最终的水分转化率。
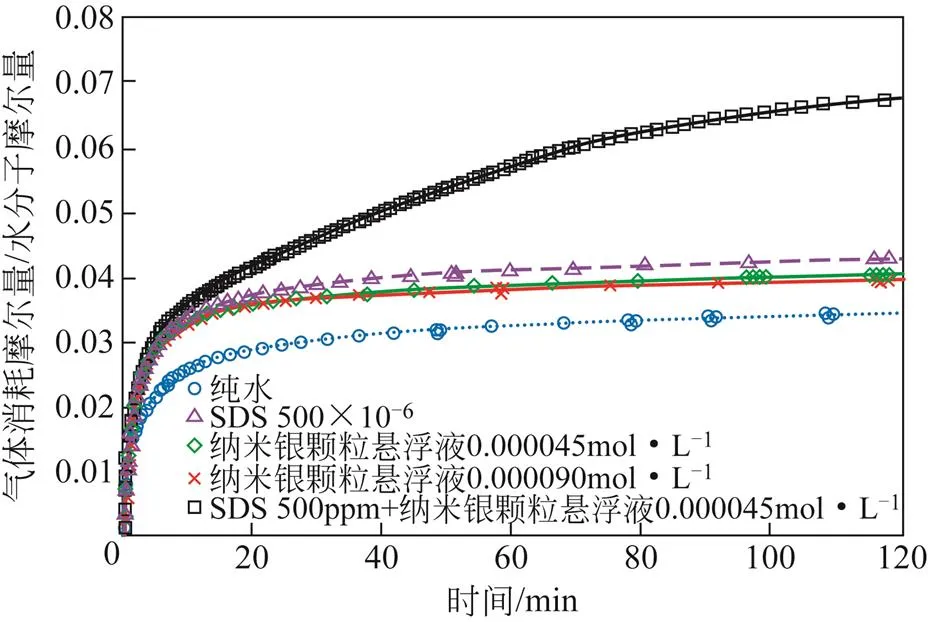
图9 初始温度273.65K和初始压力3MPa时SDS、纳米银颗粒及其复配体系对气体消耗量的影响[59]
NAJIBI等[60]通过将纳米CuO颗粒和SDS复配,在不同纳米颗粒浓度的条件下研究水合物的生成现象。最终发现气体的消耗量、消耗速率和水分转化率均增加,并且增加的程度和溶液中纳米颗粒的浓度成正比。实验结果也同时说明复配体系能减小诱导时间,但是对生成水合物的储气能力没有太大的影响。
通过比较可以发现,在复配体系下生成水合物的储气能力方面,NAJIBI等[60]和MOHAMMADI等[59]的研究结果是不同的,这可能是因为两者使用的多孔介质不同,并且MOHAMMADI等是在高压下进行实验,因此可能导致两者得出了不同的结论。
周诗岽等[61]则通过将纳米石墨颗粒和SDS复配来研究其对诱导时间的影响,结果表明,两者的引入可以使水合物生成的诱导时间相对于纯水体系明显缩短,并且其效果较于相同量的单一添加剂更好。MORAVEJI等[62]着重研究了在含SDS和纳米颗粒的溶液中甲烷的溶解度。发现由于界面张力的降低和有效接触面积的提高,甲烷的溶解度显著增大,当纳米颗粒的质量分数为1%时,甲烷溶解度在压力为1.0MPa时增大了144%;在1.5MPa时增大了77.15%,这也说明水合物生成速率和储气能力均有所增加。
袁吉[63]对表面活性剂的促进机理做出了解释,正常情况下液体界面在表面张力的作用下,具有倾向于收缩的特性,这种特性在水合反应中会减小反应物的接触面,增大传质阻力,不利于反应的快速进行。表面活性剂的引入,一方面能够改变液体的界面状态,降低表面张力,另一方面,由于其在液态环境中存在临界胶束浓度(CMC),当在溶液中的浓度大于CMC时,会产生增溶作用,增大某一组分的溶解度。这两方面的共同作用使水合反应加快,水合物成核的诱导时间缩短。
OKUTANI等[64]从生成的水合物形态上对表面活性剂的促进机理进行了解释,认为表面活性剂的存在使气-液界面处生成的水合物具有多孔结构,能够对界面下的水分子产生毛细吸力,使气体和水分子能够持续接触,促进水合物生成。
总结上述学者的研究可以发现,同时存在多孔介质和表面活性剂的体系对水合物生成的促进效果要明显优于两者单独使用的体系。同时,不同类型的多孔介质和表面活性剂对水合物也有不同的生成效果,所以其复配体系可以成为促进水合物快速生成的一种重要方法。
4 多孔介质中水合物生成热力学理论模型
液体环境下多孔介质的孔隙能够产生毛细管力并改变固液接触面处的界面状态,影响水合物成核时的温度与压力条件,即对水合物生成的相平衡条件产生影响。对于块状水合物,VAN DER WAALS和PLATEEUW[65]最初利用统计热力学的方法建立了相平衡理论模型,来预测块状水合物生成时的相平衡条件。而为了预测多孔介质中水合物的相平衡条件,许多学者在van der WAALS-PLATEERW模型的基础上纳入相关条件,建立了多孔介质中水合物相平衡预测模型。
CLARK等[66]认为孔径中的毛细作用力能够降低水的活度,因此将在模型中考虑了表面能、润湿角等多孔介质的表面性质参数,来预测水合物在多孔介质中的相平衡条件。其中,水相与气相之间的压力差由球形接触表面的Young-Laplace方程确定,如式(1)。毛细作用对水活度的影响可表示为式(2)。
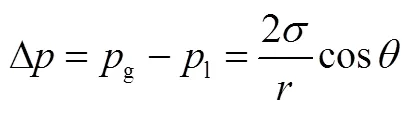
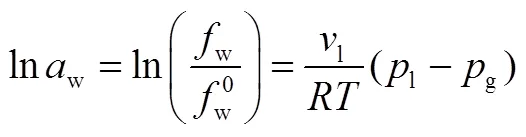

此时,多孔介质中水合物形成的相平衡关系即可用下式表示。将此模型的预测曲线与实验数据相比后发现误差较小。
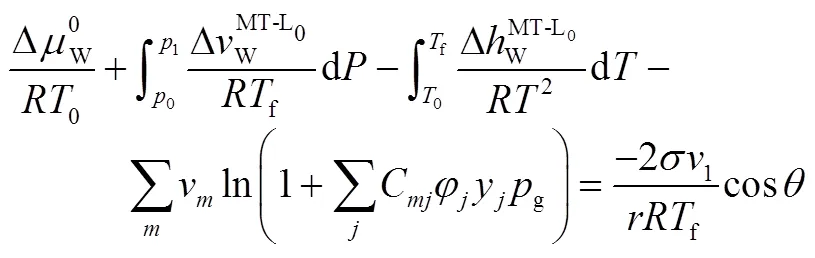
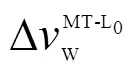
值得注意的是,WILDER等[67]也利用与此类似的模型考虑了多孔介质中气-水-冰-水合物四相点的偏移,纯水合物的四相点温度一般在冰点273.15K附近,而在多孔介质孔隙中,由于毛细管力的影响,其四相点将会向下移动,孔隙越小移动程度越大。将预测值与实验值比较后发现两者之间存在一定误差,该作者给出的原因是实验所用的多孔介质孔径分布不均匀,孔径大小只是在一定的范围内分布,而模型中参数设定的前提是在假定孔径均匀分布,所以导致了实验值和预测值的差别。
PIERRE等[68]也认为多孔介质孔隙对水合物相平衡条件的影响是由于毛细管力的存在,水合物生成过程中水的活度会因此降低,通过假设水合物相中甲烷化学势不受表面效应的影响以及水合物-水界面的表面能与占笼率无关,建立了能预测毛细作用影响下的水合物相平衡条件模型,如式(4)。

式中,L为水的化学势;β为空水合物晶格化学势;L为水的摩尔体积;为水和水合物界面的润湿角;hw为水-水合物界面张力;为多孔介质孔隙半径。
CHEN等[69]提出一种预测微孔中水合物相平衡条件的热力学模型。该模型基于水合物的反应-吸附两步形成机理,考虑了毛细作用以及温度对界面张力的影响。使用该模型对多孔介质环境下水合物相平衡条件预测后发现,当引入界面张力与温度的线性关系后,相平衡条件的绝对平均误差可降到5.08%。此模型考虑到较多水合物生成过程中的影响参数,更贴近真实情况,精度更加可靠,如式(5)~式(7)。

W=W+W+lnW(6)
式中,W为摩尔亥姆霍兹自由能;为系统压力;W为摩尔体积。

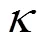
此外,KLAUDA等[70]在逸度模型中加入了多孔介质孔径分布函数,建立了预测水合物在非单一孔径中水合物相平衡条件的模型;PEDDIREDDY等[71]将多孔介质孔径内气-液接触角作为变量,建立了多孔介质内水合物相平衡模型;车雯等[72]基于孔隙网络模型模拟研究了水合物生成于壁面与中心两种方式下,多孔介质渗流特性的变化;UCHIDA 等[73]、LLAMEDO等[74]和雷晓等[75]也都对多孔介质中水合物生成模型进行了研究。
自VAN DER WAALS和PLATEERW建立了van der WAALS-PLATERW模型以来,众多研究者对其进行了优化发展,纳入更多的影响参数,使之能够更加准确地计算水合物相平衡条件。但是另一方面,模型的建立总体上是基于实验条件下的研究而建立的,但是在自然条件下,水合物稳定存在条件的影响因素远比实验室中复杂,并且水合物赋存介质孔径以及介质成分分布都相对复杂,这些都决定了所建立模型的预测结果都会与实际情况产生偏差。因此所建立的模型应该尽可能多地纳入水合物生成的影响因素,以提高其精度。不过,考虑更多的影响因素意味着计算过程更加繁琐,并且多孔介质中涉及到的一些微观参数不易直接测量。所以仍需要对自然条件下的水合物状态加以研究,明确并纳入对预测结果影响较大的参数,在保证预测精度的前提下尽量简化次要因素,使模型在实用的情况下更高效。
5 结语与展望
为了对水合物有更好的了解并方便后续的工业应用,本文总结了多孔介质的粒径、表面特性以及添加剂与多孔介质的协同作用对于水合物生成速率和相平衡的影响,并归纳了不同反应条件下水合物在多孔介质中的生成位置。
目前,对于多孔介质粒径及表面特性对于水合物的影响,不同的学者间存在不同的看法:就实验现象而言,粒径因素在影响生成速率和相平衡条件时均存在不确定性;在表面特性方面,实验现象表明疏水性越强,对水合物生成速率促进效果越大,而进行数值模拟的学者得出了相反的结论;在水合物的分布上,不同的反应条件和多孔介质能够导致水合物在不同的位置生成;对多孔介质和添加剂共存体系的研究表明,两者的协同作用对水合物生成的促进效果明显优于两者单独促进的效果。为了充分了解水合物的性质,促进其工业应用,在此对未来多孔介质环境中水合物的研究方向提出如下几点建议。
(1)多孔介质的表面特性对于水合物生成的影响尚有争议,并且,由于不同多孔介质的表面特性不同,其复配体系对水合物生成产生的影响以及促进水合物生成的最佳复配体系,都须进行进一步研究加以明确。另外,表面特性的影响是否会因为气源性质的不同而产生变化,也是值得深入研究的。
(2)充分研究多孔介质环境下温度压力、饱和度、粒径等不同反应条件对于水合物生成位置的影响,增强反应过程中水合物生成位置的可控性。同时,通过把握这些性质,可以预测自然环境中可能赋存水合物的区域,指导工业上水合物的勘探 开采。
(3)自然条件下海底沉积物的孔隙水中含有多种盐离子,并且海底沉积物成分也十分复杂,因此可以在实验条件下,研究不同种类的盐离子和多孔介质复配体系对水合物生成的影响,以明确各种自然环境下水合物的成藏机理,为实际开采工作提供参考。
(4)对于预测多孔介质中水合物生成条件的热力学模型,如何使用相对简便的同时预测精度更高的问题将是日后研究的一个重点方向,要达到这一目的,就必须对多孔介质中水合物的生成特点进行充分研究,明确其影响因素,重点把握对预测结果影响较大的因素,忽略增加模型使用难度但对预测精度影响不大的因素,不断对现有模型进行优化改进,建立更加实用高效的热力学模型。
(5)目前对多孔介质中水合物的研究多集中在孔隙中,但是通过实际勘探发现,自然条件下岩石微小裂隙环境中也存在水合物,裂隙环境的物理特征与孔隙环境不同,所以理论上对水合物生成的影响也不同,因此裂隙环境尤其是裂隙宽度以及裂隙表面粗糙度对水合物生成的影响,在接下来的工作中都值得进行分析和研究。
[1] BABU P,YEE D,LINGA P,et al. Morphology of methane hydrate formation in porous media[J]. Energy & Fuels,2013,27(6):3364-3372.
[2] WANG C C,CHEN H H,CHEN S C,et al. An introduction to the national energy program — Gas hydrate exploration in Taiwan[C]// Oceans. IEEE, 2015:318-32.
[3] ITO T,KOMATSU Y,FUJII T,et al. Lithological features of hydrate-bearing sediments and their relationship with gas hydrate saturation in the eastern Nankai Trough,Japan[J]. Marine & Petroleum Geology,2015,66:368-378.
[4] FAN S,CHEN Y,ZHENG H,et al. A combination technology of natural gas pipeline network pressure energy usage and hydrate peaking shaving[J]. Natural Gas Industry,2010,30(10):83-86.
[5] ZHANG Y,LI X S,CHEN Z Y,et al. Effects of particle and pore sizes on the formation behaviors of methane hydrate in porous silica gels[J]. Journal of Natural Gas Science & Engineering,2016,35:1463-1471.
[6] 谢振兴,谢应明,周兴法,等. 充注压力对压缩式制冷循环连续制备CO2水合物的影响[J]. 化工学报,2014,65(6):2301-2307.
XIE Z X,XIE Y M,ZHOU X F,et al. Effects of charge pressure on continuous production of CO2hydrate in compression refrigeration cycle[J]. CIESC Journal,2014,65(6):2301-2307.
[7] HASHEMI H,BABAEE S,MOHAMMADI A H,et al. Application of the clathrate hydrate of fluorinated carbons in cold storage systems[C]// The Fluoro-Chemical Expansion Initiative Conference,2016:134-138.
[8] 李莎,雍玉梅,尹小龙,等. 多孔介质的孔隙特性对气体扩散过程影响的直接数值模拟[J]. 化工学报,2013,64(4):1242-1248.
LI S,YONG Y M,YIN X L,et al. Numerical simulation for influence of pore characteristics on gas diffusion in porous media[J].CIESC Journal,2013,64(4):1242-1248.
[9] LINGA P,DARABOINA N,RIPMEESTER J A,et al. Enhanced rate of gas hydrate formation in a fixed bed column filled with sand compared to a stirred vessel[J]. Chemical Engineering Science,2012,68:617-623.
[10] LIU H,GUO P,DU J,et al. Experiments and modeling of hydrate phase equilibrium of CH4/CO2/H2S/N2,quaternary sour gases in distilled water and methanol-water solutions[J]. Fluid Phase Equilibria,2016,432:10-17.
[11] BAGHERZADEH S A,MOUDRAKOVSKI I L,RIPMEESTER J A,et al. Magnetic resonance imaging of gas hydrate formation in a bed of silica sand particles[J]. Energy & Fuels,2011,25(7):5496-5507.
[12] ZHAO J,LV Q,LI Y,et al.visual observation for the formation and dissociation of methane hydrates in porous media by magnetic resonance imaging.[J]. Magnetic Resonance Imaging,2015,33(4):485-490.
[13] 李明川,樊栓狮,赵金洲. 多孔介质中天然气水合物形成实验研究[J]. 天然气工业,2006,26(5):27-28.
LI M C,FAN S S,ZHAO J Z.Experimental study on the formation of natural gas hydrate in porous media[J]. Natural Gas Industry,2006,26(5):27-28.
[14] WROTTESLEY L. Investigation of the induction time for THF hydrate formation in porous media[J]. Journal of Natural Gas Science & Engineering,2015,24:357-364.
[15] TURNER D J,CHERRY R S,SLOAN E D. Sensitivity of methane hydrate phase equilibria to sediment pore size[J]. Fluid Phase Equilibria,2005,228(3):505-510.
[16] CHONG Z R,YANG M,KHOO B C,et al. Size effect of porous media on methane hydrate formation and dissociation in an excess gas environment[J]. Industrial & Engineering Chemistry Research,2015,55(29):7981-7991.
[17] SUN S C,LIU C L,YE Y G,et al. Phase behavior of methane hydrate in silica sand[J]. Journal of Chemical Thermodynamics,2014,69(2):118-124.
[18] NAGASHIMA H D,OHMURA R. Phase equilibrium condition measurements in methane clathrate hydrate forming system from 197.3K to 238.7K[J]. Journal of Chemical Thermodynamics,2016,102:252-256.
[19] RAMESH S,RAMADASS G A,et al. Influence of thermal stimulation on the methane hydrate dissociation in porous media under confined reservoir[J]. Journal of Petroleum Science & Engineering,2016,147:547-559.
[20] YANG M,SONG Y,LIU Y,et al. Influence of pore size,salinity and gas composition upon the hydrate formation conditions[J]. Chinese Journal of Chemical Engineering,2010,18(2):292-296.
[21] 胡亚飞,蔡晶,李小森. 环戊烷-甲烷水合物生成过程的温度特性[J]. 化工进展,2016,35(5):1418-1427.
HU Y F,CAI J,LI X S. System temperature properties in the process of the cyclopentane-methane binary hydrates formation[J].Chemical Industry and Engineering Progress,2016,35(5):1418-1427.
[22] KANG S P. Phase equilibria and formation kinetics of carbon dioxide,methane,and natural gas in silica gel pores[C]// Proceedings of the 6th International Conference on Gas Hydrates,Vancouver,British Columbia,Canada,2008.
[23] TSUTOMU U,TAKAO E A,ISHIZAKI T. Dissociation condition measurements of methane hydrate in confined small pores of porous glass[J]. Journal of Physical Chemistry B,1999,103(18):3659- 3662.
[24] YONGWON S,HUEN L A,UCHIDA T. Methane and carbon dioxide hydrate phase behavior in small porous silica gels:three-phase equilibrium determination and thermodynamic modeling[J]. Langmuir,2002,18(24):263-268.
[25] MIYAWAKI J,KANDA T,SUZUKI T,et al. Macroscopic evidence of enhanced formation of methane nanohydrates in hydrophobic nanospaces[J]. J. Phys. Chem. B,1998,102(12):2187-2192.
[26] CHA S B,OUAR H,WILDEMAN T R,et al. A third-surface effect on hydrate formation[J]. J. Phys. Chem.,1988,92(23):6492-6494.
[27] RIESTENBERG D,WEST O,LEE S,et al. Sediment surface effects on methane hydrate formation and dissociation[J]. Marine Geology,2003,198(s1/s2):181-190.
[28] MORGAN J J,BLACKWELL V R,JOHNSON D E,et al.Hydrate formation from gaseous CO2and water[J]. Environmental Science & Technology,1999,33(9):1448 -1452.
[29] BLACKWELL,VERONICA R.Formation processes of clathrate hydrates of carbon dioxide and methane[D]. California:California Institute of Technology,1998.
[30] 臧小亚,梁德青,吴能友,等. 多孔介质中甲烷水合物的生成特性研究进展[J]. 新能源进展,2015,3(2):131-138.
ZANG X Y,LIANG D Q,WU N Y,et al. Research progress on methane hydrate formation kinetics in porous media[J]. Advances in New and Renewable Energy,2015,3(2):131-138.
[31] QORBANI K,KVAMME B. Non-equilibrium simulation of CH4,production from gas hydrate reservoirs through the depressurization method[J]. Journal of Natural Gas Science & Engineering,2016,35:1544-1554.
[32] YAN L,CHEN G,PANG W,et al. Experimental and modeling study on hydrate formation in wet activated carbon[J]. Journal of Physical Chemistry B,2005,109(12):6025-6030.
[33] ZHANG B Y,QIANG W U,SUN D L. Effect of surfactant Tween on induction time of gas hydrate formation[J]. International Journal of Mining Science and Technology,2008,18(1):18-21.
[34] 白冬生.气体水合物成核与生长的分子动力学模拟研究[D]. 北京:北京化工大学,2013.
BAI D S. Molecular dynamics simulation study of the nucleation and growth of gas hydrates[D]. Beijing:Beijing University of Chemical Technology,2013.
[35] LI H,STANWIX P,AMAN Z,et al. Raman spectroscopic studies of clathrate hydrate formation in the presence of hydrophobized particles[J]. Journal of Physical Chemistry A,2016,120(3):417-424.
[36] LI H,WANG L. Hydrophobized particles can accelerate nucleation of clathrate hydrates[J]. Fuel,2015,140:440-445.
[37] KASHCHIEV D,FIROOZABADI A. Induction time in crystallization of gas hydrates[J]. Journal of Crystal Growth,2003,250(3/4):499-515.
[38] ABYZOV A S,SCHMELZER J W. Heterogeneous nucleation in solutions:generalized Gibbs' approach.[J]. Journal of Chemical Physics,2014,140(24):244706.
[39] SLOAN E D,KOH C. Clathrate hydrates of natural gases[M]. 3rd ed. New York:CRC Press,2007:258-262.
[40] 吕秋楠,宋永臣,李小森.鼓泡器中环戊烷-甲烷-盐水体系水合物的生成动力学[J]. 化工进展,2016,35(12):3777-3782.
LV Q N,SONG Y C,LI X S. Formation kinetics of cyclopentane-methane hydrate in NaCl solution with a bubbling equipment[J]. Chemical Industry and Engineering Progress,2016,35(12):3777-3782.
[41] WANG S,YANG M,LIU W,et al. Investigation on the induction time of methane hydrate formation in porous media under quiescent conditions[J]. Journal of Petroleum Science & Engineering,2016,145:565-572.
[42] VELUSWAMY H P,PRASAD P S R,LINGA P. Mechanism of methane hydrate formation in the presence of hollow silica[J]. Korean Journal of Chemical Engineering,2016,33(7):2050-2062.
[43] ZHANG P,WU Q,PU Y,et al. Water transfer characteristics during methane hydrate formation and dissociation processes inside saturated sand[J]. Journal of Natural Gas Chemistry,2010,19(1):71-76.
[44] ZHANG P,QING B,et al. Water transfer characteristics in the vertical direction during methane hydrate formation and dissociation processes inside non-saturated media[J]. Journal of Natural Gas Chemistry,2010,19(2):139-145.
[45] 刘锋,樊栓狮. 海泥石英砂沉积物中甲烷水合物的生成[J]. 天然气化工(C1化学与化工),2005,30(2):22-27.
LIU F,FAN S S. A study on formation of methane hydrate in sea mad-sand sediment[J].Natural Gas Chemical Industry,2005,30(2):22-27.
[46] KARAMODDIN M,VARAMINIAN F. Water purification by freezing and gas hydrate processes,and removal of dissolved minerals (Na+,K+,Mg2+,Ca2+)[J]. Journal of Molecular Liquids,2016,223:1021-1031.
[47] 郑艳红. 甲烷水合物在盐、醇类介质中相平衡研究[D]. 兰州:中国科学院研究生院(兰州地质研究所),2002.
ZHENG Y H. Hydrate phase equilibrium of methane in the aqueous solution of salts and methanol medium[D]. Lanzhou:University of Chinese Academy of Sciences(Lanzhou Institute of Geology),2002.
[48] SYLVA T Y,KINOSHITA C K,MASUTANI S M. Inhibiting effects of transition metal salts on methane hydrate stability[J]. Chemical Engineering Science,2016,155:10-15.
[49] SU Y,BERNARDI S,SEARLES D J,et al. Effect of carbon chain length of organic salts on the thermodynamic stability of methane hydrate[J]. Journal of Chemical & Engineering Data,2016,61(5):1952-1960.
[50] 杨明军,宋永臣,刘瑜. 多孔介质及盐度对甲烷水合物相平衡影响[J]. 大连理工大学学报,2011,51(1):31-35.
YANG M J,SONG Y C,LIU Y. Effect of porous media and salinity on phase equilibrium of methane hydrates[J]. Journal of Dalian University of Technology,2011,51(1):31-35.
[51] HAUGE L O,BIRKEDAL K,ERSLAND G,et al. Effects of initial saturation and salinity on methane hydrate growth in sandstone[C]// AGU Fall Meeting. AGU Fall Meeting Abstracts,2012.
[52] HUSEB J,ERSLAND G,GRAUE A,et al. Effects of salinity on hydrate stability and implications for storage of CO2,in natural gas hydrate reservoirs[J]. Energy Procedia,2009,1(1):3731-3738.
[53] MEKALA P,BABU P,SANGWAI J S,et al. Formation and dissociation kinetics of methane hydrates in seawater and silica sand[J]. Energy & Fuels,2014,28(4):2708-2716.
[54] 杨顶辉. 盐度对甲烷气水合物系统的影响[J]. 中国科学(地球科学),2007,37(10):1370-1381.
YANG D H. Effects of salinity on methane gas hydrate system[J].Scientia Sinica(Terrae),2007,37(10):1370-1381.
[55] ZATSEPINA O Y,BUFFETT B A. Thermodynamic conditions for the stability of gas hydrate in the seafloor[J]. Journal of Geophysical Research Atmospheres,1998,103(10):24127-24139.
[56] REZAEI E,MANTEGHIAN M,TAMADDONDAR M. Kinetic study of sthylene hydrate formation in presence of graphene oxide and sodium dodecyl sulfate[J]. Journal of Petroleum Science & Engineering,2016,147:857-863.
[57] KAKATI H,MANDAL A,LAIK S. Promoting effect of Al2O3/ZnO-based nanofluids stabilized by SDS surfactant on CH4+C2H6+C3H8hydrate formation[J]. Journal of Industrial & Engineering Chemistry,2016,35:357-368.
[58] 丁麟,史博会,吕晓方,等. 天然气水合物形成与生长影响因素综述[J]. 化工进展,2016,35(1):57-64.
DING L,SHI B H,LV X F,et al. Review of influence factors of natural gas hydrate formation and growth[J]. Chemical Industry and Engineering Progress,2016,35(1):57-64.
[59] MOHAMMADI A,MANTEGHIAN M,HAGHTALAB A,et al. Kinetic study of carbon dioxide hydrate formation in presence of silver nanoparticles and SDS[J]. Chemical Engineering Journal,2014,237(1):387-395.
[60] NAJIBI H,SHAYEGAN M M,HEIDARY H. Experimental investigation of methane hydrate formation in the presence of copper oxide nanoparticles and SDS[J]. Journal of Natural Gas Science & Engineering,2015,23:315-323.
[61] 周诗岽,张锦,赵永利,等. 纳米石墨颗粒与SDS复配对CO2水合物生成诱导时间的影响[J]. 科学技术与工程,2016(1):58-62.
ZHOU S D,ZHANG J,ZHAO Y L,et al. Effect of graphite nanoparticles and SDS oninduction time of gas hydrate formation[J]. Science Technology and Engineering,2016(1):58-62.
[62] MORAVEJI M K,GOLKARAM M,DAVARNEJAD R. Effect of CuO nanoparticle on dissolution of methane in water[J]. Journal of Molecular Liquids,2013,180(4):45-50.
[63] 袁吉. 表面活性剂对水合物生成过程影响机理的初步研究[D]. 兰州:兰州理工大学,2009.
YUAN J. Study on the effection mechanics of surfactants in the process of gas hydrate formation[D]. Lanzhou: Lanzhou University of Technology,2009.
[64] OKUTANI K,KUWABARA Y,MORI Y H. Surfactant effects on hydrate formation in an unstirred gas/liquid system:an experimental study using methane and sodium alkyl sulfates[J]. Chemical Engineering Science,2008,63(1):183-194.
[65] VAN DER WAALS J H,PLATEEUW J C. Clathrate solutions[J]. Advances in Chemical Physics,2007,2:1-57.
[66] CLARK M A,MEHRAN POOLADIDARVISH A,BISHNOI P R. A method to predict equilibrium conditions of gas hydrate formation in porous media[J]. Industrial & Engineering Chemistry Research,1999,38:2485-2490.
[67] WILDER J W,SESHADRI K,SMITH D H. Modeling hydrate formation in media with broad pore size distributions[J]. Langmuir,2001,17(21):6729-6735.
[68] PIERRE H,MICHEL T,BEN C M. Formation of natural gas hydrates in marine sediments: 2. Thermodynamic calculations of stability conditions in porous sediments[J]. Journal of Geophysical Research Atmospheres,1999,104(104022):5-23.
[69] CHEN L T,SUN C Y,CHEN G J,et al. Thermodynamics model of predicting gas hydrate in porous media based on reaction−adsorption two-step formation mechanism[J]. Industrial & Engineering Chemistry Research,2010,49(8):3936-3943.
[70] KLAUDA J B,SANDLER S I. Predictions of gas hydrate phase equilibria and amounts in natural sediment porous media[J]. Marine & Petroleum Geology,2003,20(5):459-470.
[71] PEDDIREDDY S,LEE S Y,LEE J W. Variable contact angle model for gas hydrate equilibrium in porous media[J]. AIChE Journal,2006,52(3):1228-1234.
[72] 车雯,梁海峰,孙国庆,等. 天然气水合物沉积层渗流特性的模拟[J]. 化工进展,2015,34(6):1576-1581.
CHE W,LIANG H F,SUN G Q,et al. Simulation study on the seepage characteristics of natural gas hydrate sediment[J]. Chemical Industry and Engineering Progress,2015,34(6):1576-1581.
[73] TSUTOMU U,SATOSHI T,YASUSHI K,et al. Spectroscopic observations and thermodynamic calculations on clathrate hydrates of mixed gas containing methane and ethane: determination of structure,composition and cage occupancy[J]. Journal of Physical Chemistry B,2002,106(48):12426-12431.
[74] LLAMEDO M,ANDERSON R,TOHIDI B. Thermodynamic prediction of clathrate hydrate dissociation conditions in mesoporous media[J]. American Mineralogist,2005,89(8/9):1264-1270.
[75] 雷晓,邓建强,张早校. 海底沉积物层CO2封存中水合物研究进展[J]. 化工进展,2012,31(6):1338-1346.
LEI X,DENG J Q,ZHANG Z X. Research advancement in hydrate formation during CO2sub-sea sediments sequestration[J]. Chemical Industry and Engineering Progress,2012,31(6):1338-1346.
Research progress on influence factors of natural gas hydrate formation in porous media
PAN Zhen1,LIU Zhiming1,LIU Dejun1,SHANG Liyan2,LI Wenzhao1,LI Ping2
(1Petroleum and Natural Gas Engineering,Liaoning Shihua University,Fushun 113001,Liaoning,China;2College of Chemistry,Chemical Engineering and Environmental Engineering,Liaoning Shihua University,Fushun 113001,Liaoning,China)
Nature gas hydrate(NGH)is a kind of non-stoichiometry crystal chemical clathrate,which is formed by natural gas molecules and water molecules under low temperature and high pressure. As a kind of potential energy,it has a wide application prospect in industry. Under natural conditions the hydrate mainly exists in the pore of the permafrost zone and the sea bottom sediments. Simulating the formation of hydrates under natural conditions in experiments is of practical significance for the formation mechanism of hydrate,exploration,exploitation and industrial applications. Thus,many scholars have carried out many experiments on the formation of hydrate in porous media. This paper summarizes the research achievements of predecessors,including the effect of pore size,surface properties and the synergistic reaction of additives(salts and surfactants)on hydrate formation rate and phase equilibrium in the porous environment,and the formative position of gas hydrate under different conditions and several thermodynamic models in porous medium. Finally,it is pointed out that the effects of medium surface characteristics,different types of porous medium and salt mixed system on hydrate formation and the effect of the different reaction conditions on the hydrate formative position should be deeply explored and clarified. In addition,the formation of hydrate at different crack width and wall roughness in the fracture environment is worthy of further study.
nature gas hydrate;porous media;phase equilibrium;surfactants;influence factor;models
TE 89
A
1000–6613(2017)12–4403–13
10.16085/j.issn.1000-6613.2017-0098
2017-01-17;
2017-03-21。
辽宁省自然科学基金(201602470)及辽宁省高等学校优秀人才支持计划(LJQ2014038)项目。
潘振(1981—),男,博士,副教授,主要研究方向为天然气综合利用技术。E-mail:28335719@qq.com。
刘德俊,副教授,研究方向为油水两相流输送研究。E-mail:ldj8448@163.com。

