既熟悉又陌生的金属元素
——以金属元素为背景的试题解题策略初探
赵鑫光 程子晟
吉林
既熟悉又陌生的金属元素
——以金属元素为背景的试题解题策略初探
赵鑫光 程子晟

在高考化学试卷中的非选择题必考题和选考题的物质结构部分,经常以高中教材以外的金属元素作为命题背景,这体现了不同知识点的横向联系和高考命题的综合性。以学生不太熟悉的金属单质及其化合物为载体,综合考查化合物的制备与检验、化学基本概念、化学反应原理、物质结构与性质等方面的内容。本文选择几种典型的主族金属元素加以介绍。并配以例题、解析,以期学生通过练习掌握该类试题的解题策略。
一、金属锂及其化合物
(1)在ⅠA族碱金属中,锂原子半径最小,极化能力强,表现出与Na和K等的不同性质,它与ⅡA族里的Mg相似。
(2)锂与氧气反应生成氧化物Li2O,而不形成过氧化物和超氧化物;与氮气形成氮化物Li3N,而其他碱金属不能与N2直接化合;与碳反应生成乙炔锂(Li2C2);与水反应生成氢气,但反应速率比Na或K缓慢得多。
(3)Li2CO3、Li3PO4和LiF等锂盐溶解度远远小于对应的钠盐和钾盐。
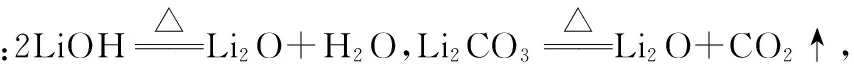

(6)LiCl·nH2O受热分解时发生水解,生成LiOH。
(7)LiCoO2一般作为锂离子电池的正极材料,发生如下反应:

【典例1】锂及锂的化合物在工业生产中有重要用途。
(1)如图为电解装置制备氢氧化锂的示意图,A、B均为惰性电极,两电极区的电解液分别为LiOH溶液和LiCl溶液中的一种。由示意图可知A极区应加入________(填化学式)电解液,该电解池的阳极反应为________,Li+的迁移方向是________(填“从A到B”或“从B到A”)。

(2)氢化铝锂(LiAlH4)是有机合成中重要的还原剂,可以还原酯、羧酸等有机化合物,则LiAlH4中,H元素的化合价为________。
(3)氢化锂和氯化铝在无水乙醚中可制得氢化铝锂,试写出制备方程式:____________。
(4)氢化铝锂与水剧烈反应生成氢气,该反应中的氧化剂是________;标准状况下生成11.2 L H2时转移的电子数为________。

二、金属钙及其化合物
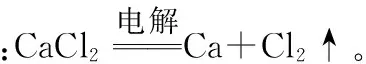


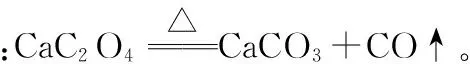
【典例2】过氧化钙(CaO2)是一种白色、无毒、难溶于水的固体,能杀菌消毒,广泛用于果蔬保鲜、空气净化、污水处理等方面。工业生产过程如下:
①在NH4Cl溶液中加入Ca(OH)2;
②不断搅拌的同时加入30%H2O2,反应生成CaO2·8H2O 沉淀;
③经过沉淀、过滤、水洗得到CaO2·8H2O,再脱水干燥得到CaO2。
(1)第①步反应的化学方程式为________。第②步反应的化学方程式为____________。
(2)可循环使用的物质是________,工业上常采用Ca(OH)2过量而不是H2O2过量的方式来生产,这是因为
____________。

(3)CaO2·8H2O加热脱水的过程中,需不断通入不含二氧化碳的氧气,目的是____________。
(4)已知CaO2在350℃迅速分解生成CaO和O2。如图是实验室测定产品中CaO2含量的装置(夹持装置省略)。若所取产品质量是mg,测得气体体积为VmL(已换算成标准状况),则产品中CaO2的质量分数为________(用字母表示)。

三、镓与铟及其化合物
(1)Ga熔点29.78℃,在手中融化,但Ga的沸点为2 403℃,是液相存在的温度范围最大的金属单质,常用于制造高温下使用的温度计。


(4)In2O3和In(OH)3几乎无两性表现,In2O3溶于酸,但不溶于碱。

【典例3】央视新闻频道2017年4月报道了由我国科学家发现的液态镓铟合金具有类生物学现象,这一发现开辟了一条构筑高性能纳米金属流体的新途径。
(1)镓是门捷列夫生前预言的“类铝”,它的原子序数为31,则它在元素周期表中的位置是________,镓铟合金熔点________(填“等于”“高于”或“低于”)金属镓。
(2)金属镓与铝类似,可以溶于氢氧化钠溶液,试写出相关的离子方程式:____________。
(3)氮化镓是新一代半导体材料,通常可由镓与氨气在1 300 K左右制备,试写出制备氮化镓的化学方程式:________________________。
(4)已知Al2S3不能在水中制备,Ga2S3与之类似,试用化学方程式解释原因:____________。
(5)GaAs也是一种半导体材料,它可由(CH3)3Ga与AsH3在1 000 K左右制得,该反应副产物是一种常见气态化合物,其在氧气中燃烧的方程式为____________。
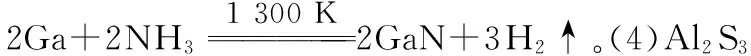
四、锡及其化合物


【典例4】硫酸亚锡(SnSO4),能溶于水,广泛用于镀锡工业,其制备路线如下图所示:

已知:①Sn在酸性溶液中存在两种形式Sn2+和Sn4+,其中Sn2+在空气中易被氧化。
②SnCl2易溶于水,在碱性条件下水解产物为Sn(OH)Cl。
③SnSO4溶解度随温度升高迅速增大。
(1)溶解SnCl2时为什么要用盐酸,请结合化学平衡移动原理加以解释:____________。
(2)加入Sn粉的作用除调节pH外还有________。
(3)若反应①得到的沉淀是SnO,则相关的离子方程式为___________;反应①后过滤的滤液中主要含________。
(4)操作①需要进行的具体操作及顺序是________。
(5)SnSO4在酸性条件下可用作H2O2的去除剂,其反应原理为________(用离子方程式表示)。

五、铅及其化合物



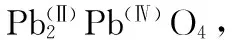


【典例5】铅及其化合物可用于蓄电池、耐酸设备及X射线防护材料等。回答下列问题:
(1)铅是碳的同族元素,比碳多4个电子层。铅在元素周期表的位置为第________周期________族;PbO2的酸性比CO2的酸性________(填“强”或“弱”)。
(2)PbO2与浓盐酸共热生成黄绿色气体,反应的化学方程式为____________。
(3)PbO2可由PbO与次氯酸钠溶液反应制得,反应的离子方程式为___________;PbO2也可以通过石墨为电极,Pb(NO3)2和Cu(NO3)2的混合溶液为电解液电解制取。阳极发生反应的电极反应式为______________,阴极上观察到的现象是_______________;若电解液中不加入Cu(NO3)2,阴极发生的电极反应式为______________,这样做的主要缺点是____________。
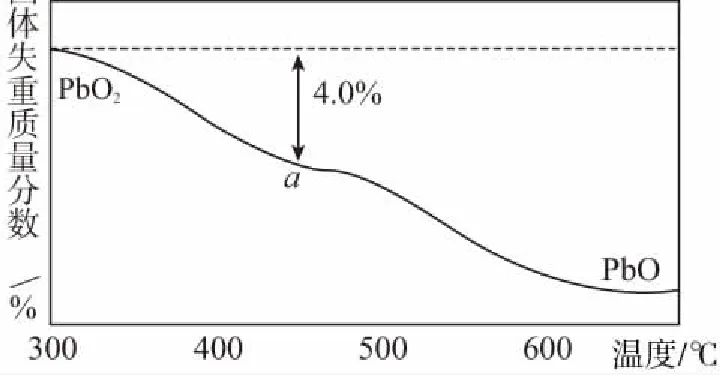
(4)PbO2在加热过程发生分解的失重曲线如图所示,已知失重曲线上的a点为样品失重的4.0%[(即样品起始质量—a点固体质量)/样品起始质量×100%]的残留固体。若a点固体组成表示为PbOx或mPbO2·nPbO,列式计算x值和m∶n值:________。

吉林省长春吉大附中实验学校)

