对罗氏Cobas Z480基因扩增仪性能的验证与分析
张 迪, 秦 苑, 左方财
(贵州省兴义市人民医院医学检验科,贵州 兴义 562400)
·检测与诊断·
对罗氏Cobas Z480基因扩增仪性能的验证与分析
张 迪, 秦 苑, 左方财
(贵州省兴义市人民医院医学检验科,贵州 兴义 562400)
目的:评价罗氏Cobas Z480基因扩增仪的性能。方法:贵州省兴义市人民医院医学检验科按照ISO15189:2012[1]和CNAS-CL36[2]的标准要求,选定乙型肝炎病毒DNA(HBV-DNA)作为检测项目,对罗氏Cobas Z480基因扩增仪检测系统的准确度、精密度及灵敏度进行验证。结果:使用本仪器对血清标本进行检测的批间精密度高值的平均值为6.19ng/ml,标准差为0.30,CV为4.81%;其批间精密度低值的平均值为3.22 ng/ml,标准差为0.15,CV为4.64%。使用本仪器对血清标本进行检测的批内精密度为:其高值的平均值为6.44 ng/ml,标准差为0.09,CV为1.47%;其低值的平均值为3.13 ng/ml,标准差为0.15,CV为4.77%。上述检测值均处于厂家推荐的允许范围内,均满足《中华人民共和国医药行业标准(YY/T 1182-2010)核酸扩增检测用试剂盒(以下简称试剂盒)》[5]技术要求中“5.7.2”条例的要求。使用本仪器对国家卫生部临床检验中心提供的质控血清进行HBV-DNA检测,获得的数据均在卫生部临床检验中心推荐的允许范围内。对本仪器检测系统进行灵敏度验证的结果为:平均值为3.43,标准差为0.25,CV为7.29%,CV处于厂家推荐的允许范围内(CV≤10%)。结论:在检测HBV-DNA方面,罗氏Cobas Z480基因扩增仪检测系统的准确度、精密度及灵敏度均较高,其批内精密度和批间精密度的变异系数均在可接受的范围内,其性能指标均与厂家提供的性能参数相符合。该仪器可以在实验室被用于进行临床检测工作。
罗氏Cobas Z480;基因扩增仪;性能验证
基因扩增仪是一种具有基因扩增功能的检测仪器。“ISO 15189:2012”规范中指出,实验室只能使用已确认的适用于预期用途的检验程序,以满足给定用途或某特定领域的应用要求。“GB/T22578-2008”规范[3]中指出,在临床实验室使用厂家严格评估的检验方法或试剂盒前,应验证其分析性能,以证实其能达到厂家声明的性能指标。我国卫生行业标准“WS/T420-2013”标准[4]中指出,临床实验室应对所用的检验方法或商品试剂盒进行验证。“CNASCL36”准则中指出,对临床实验室所用的检验方法、仪器或商品试剂盒进行性能验证的项目至少应包括其准确度、精密度等。笔者根据最新的相关文件、“ISO 15189:2012”规范、“YY/T 1182-2010”说明书中的相关要求及对HBVDNA试剂盒产品性能的基本要求,使用本实验室的罗氏Cobas Z480基因扩增仪定量测定HBV-DNA,以验证该仪器检测系统的性能。
1 资料与方法
1.1 一般资料
1)本试验所用的仪器为罗氏Cobas Z480荧光扩增仪、广东珠海黑马医学仪器有限公司生产的16K型台式高速离心机、杭州奥盛仪器有限公司生产的干式恒温器、生物安全柜等。2)本试验所用的试剂为广州中山达安基因股份有限公司提供的“乙型肝炎病毒核酸定量检测试剂盒”,国食药监械(准)字2012第3400078号,有效期为四年;试剂批号为2016001(有效期为20170111);校准品批号为20160503(有效期至20170502)。3)本试验中标本的来源为广州中山达安基因HBV-DNA检测试剂盒自带标准品(浓度为2.0E6)。质控血清由国家卫生部临床检验中心提供。本试验中所用的样本来源于在本院进行健康体检者的100份新鲜血清标本。
1.2 方法
1.2.1 精密度验证 根据试剂说明书、本实验室制定的标准操作程序(SOP)及美国临床实验室标准化协会(CLSI)制定的评价标准EP15A中的相关要求,以1:10的比例将100份血清标本的浓度分别稀释为E6、E3,并在同一天、同一条件下对这些血清标本进行20次的批内精密度测定。所有试验均在5个小时内完成,并计算平均值和变异系数(CV)。对本组标本每天进行一次的批间精密度测定,连续检测20天,并计算平均值和变异系数。
1.2.2 准确度验证 对国家卫生部临床检验中心发放的5份室间质控品血清进行检测,分析本实验室的测定值是否处于国家卫生部临床检验中心给定靶值的允许范围内。
1.2.3 灵敏度验证 取广州中山达安基因HBV-DNA检测试剂盒自带(浓度为2.0E6)的标准品,严格按照试剂说明书的要求进行操作,将标本上机连续检测10次,计算平均值、标准差及变异系数(CV),并根据厂家提供的检测限(1.00×103IU/ml),检测其CV是否处于厂家提供的允许范围内(CV≤10%)。
2 结果
2.1 进行精密度验证试验的结果
使用本仪器对血清标本进行检测的批间精密度高值的平均值为6.19ng/ml,标准差为0.30,CV为4.81%;其批间精密度低值的平均值为3.22 ng/ml,标准差为0.15,CV为4.64%。使用本仪器对血清标本进行检测的批内精密度为:其高值的平均值为6.44 ng/ml,标准差为0.09,CV为1.47%;其低值的平均值为3.13 ng/ml,标准差为0.15,CV为4.77%。上述检测值均处于厂家推荐的允许范围内,均满足《中华人民共和国医药行业标准(YY/T 1182-2010)核酸扩增检测用试剂盒(以下简称试剂盒)》[5]技术要求中“5.7.2”条例的要求。该条例明确规定,标本的精密度应符合检测浓度对数值的变异系数(CV≤5%)。
2.2 进行准确度验证试验的结果
使用本仪器对2015年9月由国家卫生部临床检验中心提供的质控血清进行HBV-DNA检测,检测结果均在卫生部临床检验中心提供的上限、下限允许的范围内。详情见表1。评均通过审核,准确度均符合标准。
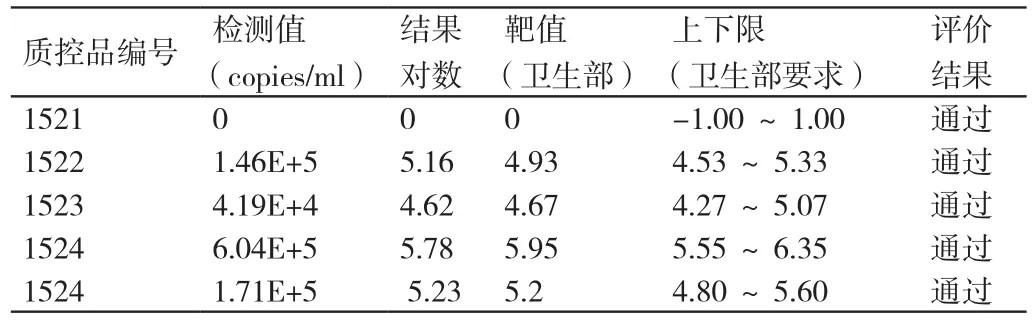
表1 进行本次HBV-DNA测定结果的分析
2.3 进行灵敏度验证试验的结果
对本仪器检测系统进行灵敏度验证的结果为:平均值为3.43,标准差为0.25,CV为7.29%,CV处于厂家推荐的允许范围内(CV≤10%)。
3 讨论
《医学实验室质量和能力认可准则》(ISO15189准则)中指出,实验室必须对其所用的检测系统进行性能验证。笔者根据ISO15189准则及CNAS-CL36准则在基因扩增检验方面的相关要求及罗氏Cobas Z480基因扩增仪性能指标的相关要求,结合本实验室质量体系在仪器性能指标方面的要求,对该仪器的批内精密度、批间精密度、检测的准确度及灵敏度进行验证。
笔者所在单位对罗氏Cobas Z480基因扩增仪检测系统进行性能验证的结果显示,该仪器的精密度、灵敏度及准确度均较高,操作的重复性好,其批内和批间变异系数均在可接受的范围内,能够有效地进行乙型肝炎病毒定量检测。我们对该仪器3项性能的验证结果与相关文献[6-8]报道的结果相一致。
乙型病毒性肝炎是一种因感染乙型肝炎病毒(HBV)引起的肝炎。我国属于HBV感染的流行区。我们居民进行乙型肝炎表面抗原(HBsAg)检测结果的阳性率约为9.09%[9]。近年来,我国针对乙型病毒性肝炎的流行情况采取一系列的防疫措施,使该病的流行病学特点发生了显著的变化[10]。传统的HBV血清学标志物检测法属于定性检测法,可间接了解患者体内HBV复制的情况。但当该病毒发生变异时,对其进行定性检测的效果可显著变差。目前,临床上主要采用PCR技术进行HBV-DNA检测,以获取分子生物学实验方面的诊断依据。该技术不仅可以对HBV进行定性检测,还可定量检测患者体内HBV的复制情况。进行HBV-DNA检查可从血清中直接检测HBV的存在与否[11],其操作快速、灵敏度较高、获取试验报告的周期较短。根据对患者进行HBV-DNA检查的结果进行分析,可判断其体内HBV的复制情况及传染性,有助于临床医师为其设计治疗方案、选用药物、观察疗效及评估预后。
进行仪器性能的验证是ISO15189准则中要求完成的重要工作之一。根据新版ISO15189认可准则和《医学实验室质量和能力认可准则在分子诊断领域的应用说明》的要求,笔者对本实验室罗氏Cobas Z480基因扩增仪检测系统的准确度、精密度及灵敏度进行验证。验证的结果显示,该仪器检测系统的精密度、敏感度、准确度均较高,重复操作性好,其批内精密度和批间精密度的变异系数均在可接受范围内,其3项性能的指标均与厂家提供的性能参数相符合,可以在实验室被用于进行临床检测工作。
[1] 中国合格评定国家认可委员会.ISO15189:2012医学实验室质量和能力的专用要求[S].北京:中国合格评定国家认可委员会,2012.
[2] 中国合格评定国家认可委员会.CNAS-CL36医学实验室质量和能力认可准则在基因扩增检验领域的应用说明[S].北京:中国合格评定国家认可委员会,2012.
[3] 中华人民共和国国家质量监督检验检疫总局,中国国家标准化管理委员院会.GB/T22576.2008医学实验室一质量和能力的专用要求[S].北京:中国标准出版社,2008.
[4] 中华人民共和国卫生行业标准,WS/T420-2013临床实验室对商品定量试剂盒分析性能的验证[S]. 北京:中国标准出版社,2013.
[5] 国家食品药品监督管理局.YY/T 1182-2010核酸扩增检测用试剂(盒)[S].北京:中国标准出版社,2010.
[6] 罗卉丽,袁杭,毛源,等. 分子诊断定量项目分析性能验证程序探讨[J].国际检验医学杂志, 2015,36(16): 2360-2362.
[7] 王治国. 临床检验方法确认与性能验证[M]. 北京:人民卫生出版社, 2009.
[8] 康凤凤,王治国.ISO15189:2012与临床检验定量检测方法确认和性能验证[J].临床检验杂志,2013,31(12):881-884.
[9] Zhang F,Fan YC,Mu NN,et al.Rapid.Exportin 4 gene expression an d DNA promoter methylation status in chronic hepatitis B viru s[J].J Viral Hepat,2014,21(4):241-250.
[10] 朱科伦,朱郇悯,曾文铤,等.乙型肝炎流行病学的研究新进展[J].广州医药,2010,41(4):1-2.
[11] 倪艳,蒋凤,徐华,等.四环素调控表达肿瘤坏死因子α抗乙型肝炎病毒的实验研究[J].中华肝病杂志,2014,22(3):213-218.
R446.1
B
2095-7629-(2017)14-0134-02

