葡萄籽油的氧化稳定性
秦亚南,王玲,谢远东,邹积赟,杨华峰,王建国,康健*
1(新疆大学 生命科学与技术学院,新疆 乌鲁木齐,830046) 2(新疆合普联科检测技术研究院,新疆 乌鲁木齐,834000) 3(新疆海瑞盛生物工程股份有限公司,新疆 库尔勒,843000)
葡萄籽油的氧化稳定性
秦亚南1,王玲2,谢远东2,邹积赟3,杨华峰3,王建国3,康健1*
1(新疆大学 生命科学与技术学院,新疆 乌鲁木齐,830046) 2(新疆合普联科检测技术研究院,新疆 乌鲁木齐,834000) 3(新疆海瑞盛生物工程股份有限公司,新疆 库尔勒,843000)
以葡萄籽毛油作为研究对象,分析了葡萄籽毛油依次经过精炼的各个环节后,油脂的氧化稳定性变化。并采 Rancimat 标准法,以诱导期作为油脂稳定性的评价指标,考察叔丁基对苯二酚(TBHQ)、丁基羟基茴香醚(BHA)、抗坏血酸棕榈酸钠、dl-a-生育酚、迷迭香提取物等抗氧化剂单独使用及复合抗氧化剂对葡萄籽油氧化稳定性的影响。结果显示,对葡萄籽油酸值影响最大的工艺流程为脱酸工艺;对过氧化值影响最大的工艺为脱臭工艺;而诱导期在整个精炼过程中整体呈下降趋势。在葡萄籽精炼油中添加抗氧化剂时,TBHQ、BHA、抗坏血酸棕榈酸钠及迷迭香提取物这四种抗氧化剂单独使用效果较好,能明显提高葡萄籽油氧化稳定性。对4种抗氧化剂进行复配,除TBHQ外,复合抗氧化剂比抗氧化剂单独使用时效果更好,其中以m(TBHQ)∶m(BHA)=3∶1时效果最佳。
葡萄籽油;精炼;抗氧化剂;稳定性
葡萄籽油中含有丰富的不饱和脂肪酸,主要是以亚油酸为主,含量在58% ~ 78%[1]。亚油酸作为一种人体必需脂肪酸,在动脉硬化以及心脏病的治疗方面具有显著的疗效;不仅如此,葡萄籽油中还含有多种微量营养,可用于人体营养元素的补充。是一种不可多得的高品质植物油[2]。另外,葡萄籽油因其优良的特性常被应用到化妆品和药品的制作中[3]。
由于葡萄籽油中具有较高含量的不饱和脂肪酸,所以在葡萄籽精制油的生产加工过程中,葡萄籽油极易受到不良环境的影响而发生氧化酸败,酸败不仅会破坏葡萄籽油中所含的必需脂肪酸,还有可能产生异味以及有毒物质,对消费者的健康带来不利影响。因此,有效的防止或延缓油脂在生产加工过程中发生氧化酸败至关重要。
目前,除了使用密封包装储存油脂外,在油脂中添加抗氧化剂也是一种简单、经济的方法[4-5]。葡萄籽油作为一种新兴的植物油资源,目前研究主要在成分分析、提取方法、功能评价等方面[6-9],有关葡萄籽油稳定性影响的报道较少。
本文采用Rancimat 法考察叔丁基对苯二酚(TBHQ)、丁基羟基茴香醚(BHA)、抗坏血酸棕榈酸钠、dl-a-生育酚、迷迭香提取物等[10-14]抗氧化剂单独使用及复合抗氧化剂对葡萄籽油氧化稳定性的影响。
1 材料与方法
1.1试样、试剂
葡萄籽油,由新疆海瑞盛生物工程股份有限公司提供;柠檬酸、活性白土、可溶性淀粉均为分析纯,由郑州康帆生物科技有限公司提供;无水乙醇、KOH、异辛烷、石油醚、冰乙酸、HCl均为分析纯,由天津市富宇精细化工有限公司提供;KI、酚酞、ICl、十二烷酸乙酯、Na2S2O3均为分析纯,由成都市科龙化工试剂公司提供;TBHQ、BHA、抗坏血酸棕榈酸钠、dl-a-生育酚、迷迭香提取物均为食品级,由德州汇洋生物科技有限公司提供。
1.2主要仪器设备
892Rancimat氧化稳定仪,瑞士万通 Metrohm 公司;DZF-6505 型真空恒温干燥箱,上海安亭科学仪器厂;电子天平,上海福玛实验设备有限公司;ICI-S 型恒温水浴锅,郑州长城科工贸有限公司;WYA 阿贝折射仪,上海光学仪器厂;离心机,河南智诚科技发展有限公司;WFZ-UV 2000紫外可见分光光度计,尤尼柯上海有限公司;RE-52AA 旋转蒸发仪,上海精宏实验设备有限公司;SHB-III循环式多用真空泵,巩义市英峪予华仪器厂。
1.3试验方法
1.3.1 精炼各环节氧化稳定性变化
精炼各环节的葡萄籽油,按照 GB/T 5538—2005 测定过氧化值, 按照 GB/T 5530—2005 测定酸值,诱导期按照标准 Rancimat 法测定。
1.3.2 葡萄籽精炼油质量评价
酸值: GB/T 5530—2005;不溶性杂质:GB/T 5688—2008;皂化值:GB/T 5534—2008;水分及挥发物:GB/T 5528—2008;碘值:GB/T 5532—2008;折光指数:GB/T 5527—2010;过氧化值;GB/T 5538—2005;透明度、气味、滋味:GB/T 5525—2008;相对密度:GB/T 5526—1985。
1.3.3 葡萄籽油货架期的预测
取4份葡萄籽油,分别在 100、110、120、130 ℃ 的条件下使用 892 Rancimat 氧化稳定仪测定葡萄籽油的诱导期,然后利用温度外推法得到诱导期随温度变化的氧化曲线,从而推算出葡萄籽油在 25 ℃下的储存期。
分析条件:控制温度100、110、120、130 ℃;空气流量20.0 L/h。
1.3.4 单一抗氧化剂对油脂稳定性的影响
取若干份 100 mL 的葡萄籽油分别装入 250 mL 的三角烧瓶中,将TBHQ、BHA、抗坏血酸棕榈酸钠、dl-a-生育酚、迷迭香提取物几种抗氧化剂按照 0.01%、0.015%、0.02%、0.04% 的添加量分别加入葡萄籽油中,同时做一组对照实验。每组油样分别取(3.0+0.01)g放置于 892 Rancimat 氧化稳定仪中,分别测定其诱导期并计算其抗氧化系数。
分析条件:温度 120 ℃;空气流量20.0 L/h。
1.3.5 复合抗氧化剂对油脂稳定性的影响
根据5种抗氧化剂在单独使用时对葡萄籽油氧化稳定性影响的结果,综合考虑抗氧化剂在油脂中的溶解性和抗氧化剂对葡萄籽油氧化稳定性影响的实验结果这两方面因素,选择符合条件的抗氧化剂进行复配实验[15-18],每组油样分别取(3.0 + 0.01)g放置于 892 Rancimat 氧化稳定仪中,分别测定其诱导期并计算其抗氧化系数。
分析条件:温度120 ℃;空气流量20.0 L/h。
1.3.6 诱导期及抗氧化系数的测定
诱导期:反应池中的油脂在气流和高温的作用下加速氧化,生成许多小分子有机酸,这些小分子有机酸随着气流被带入测量池中,大量的小分子有机酸导致测量池中溶液的电导率发生变化,测量池内的电极可感受到电导率的变化,并记录下电导率与反应时长的氧化曲线,电导率二阶导数最大时作为测定终点,又将其称为诱导期[19]。诱导期可以作为表示样品抗氧化能力的一个参数,当被测定样品的诱导期越长时,表示样品越稳定。
抗氧化系数(protection factor,PF):抗氧化剂在油脂中对油脂抗氧化能力的强弱,可以通过抗氧化剂加入油脂后的诱导期与未加入抗氧化剂油脂的诱导期的比值表示。该比值用抗氧化系数(PF)来表示, PFgt;1 时,表明抗氧化剂的抗氧化能力一般; 4gt;PFgt;2 时,表明抗氧化剂具有较为显著的抗氧化能力; PFgt;4,则表明抗氧化剂的抗氧化能力极显著[20]。

(1)
2 结果与分析
2.1葡萄籽油精炼过程中基本指标的变化
如图1所示,由于葡萄籽毛油在进行精炼之前己储藏较长时间,且夏季温度高,品质发生劣变。因此酸值高达 6.32 mg KOH/kg。经脱胶后,葡萄籽油的酸价略微升高至 6.68 mg KOH/kg,其原因可能是因为由于脱胶过程中温度升高,产生更多游离酸,也有可能是因为脱胶过程中加入柠檬酸,使酸价增高。当葡萄籽油经过脱酸工艺后,葡萄籽油的酸值降低至 0.38 mg KOH/kg。随后脱色油酸值略微升高,其原因可能是葡萄籽油在脱色工艺过程中所使用的吸附剂表面有很多活性位点,这些活性位点可以促使甘油三酯水解;也有可能是由于葡萄籽油在脱色工艺过程中所用的吸附剂将皂中的钠离子吸附,并生成了一些游离脂肪酸,因而使葡萄籽油的酸价略微升高[21]。最终葡萄籽油在脱臭工艺后,由于高温的作用使它的酸值降至 0.30 mg KOH/kg。
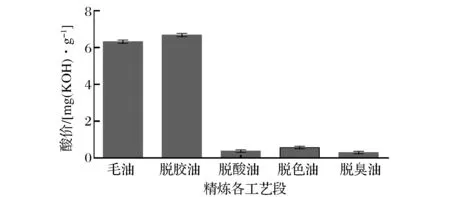
图1 葡萄籽油精炼过程酸价变化Fig.1 The process of change of acid value refined grape seed oils
由图2可知,由于葡萄籽毛油在进行精炼之前己储藏较长时间,且夏季温度高,品质发生劣变。因此过氧化值高达 8.47 mmol/kg,在经过脱胶工艺、脱酸工艺后过氧化值升高至约 10.74 mmol/kg,原因可能是在葡萄籽油脱酸过程反应温度较高,从而导致葡萄籽油继续氧化。相对于脱酸油,脱色油的过氧化值大幅降低。其过氧化值降低的原因[22]主要由于葡萄籽油在脱色过程中所使用吸附剂的活性位点可以将脱酸葡萄籽油中的过氧化物吸附,从而使其过氧化值降低。在经过脱臭工艺后,葡萄籽油在高温条件的作用下,大部分的过氧化物发生裂解并生成许多小分子物质并蒸出,使得过氧化值进一步降至最低 1.76 mmol/kg。

图2 葡萄籽油精炼过程过氧化值变化Fig.2 Changes of peroxide value in refining process of grape seed oil
在120 ℃,空气流量20.0 L/h的条件下测定各工艺阶段油脂的诱导期,诱导期为电导率测定值的二阶导数,与电导率的测定息息相关。因此未精炼前油脂中的游离脂肪酸以及金属离子、水分、皂角等极性物质均对电导率产生影响。从图3可知,葡萄籽油的诱导期在精炼过程中总体上呈下降趋势。未经精炼的毛油诱导期为3.17 h,其诱导期较高的原因可能是由于其中含有较多的天然抗氧化剂(如生物类黄酮、VE、生物类黄酮、白黎芦醇、原花青素等),因此诱导期相对较高[23]。与毛油相比,脱胶油诱导期略微升高,可能是由于脱胶过程中去除了大量磷脂与金属离子。经过脱酸工艺后,葡萄籽油诱导期大幅下降,可能是由于在此反应过程后,脂质氧化产物含量最高,且经过水化后的皂角、水分等极性杂质不利于其氧化稳定性[24]。葡萄籽毛油经过脱胶、脱酸、脱色等一系列工艺过程后,诱导期下降至 0.72 h。在经过脱臭工艺后,诱导期略微增高至0.92 h,这主要是由于脱臭工艺是在高温真空下进行,葡萄籽油中的小分子氧化产物被大量除去,即使葡萄籽油中脂肪伴随物含量较少,其诱导期仍略高于脱色油。

图3 葡萄籽油精炼过程诱导期变化Fig.3 Change of induction period of grape seed oil refining
2.2葡萄籽精炼油的质量评价
由表1和表2可以看出,经过精炼后的葡萄籽油,无论在感官鉴定和理化指标上都达到国家标准,葡萄籽精炼油的不溶性杂质含量较低,满足食用油脂的要求。
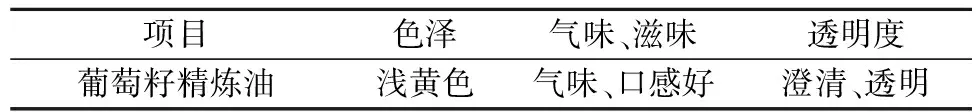
表1 葡萄籽精炼油的感官评价
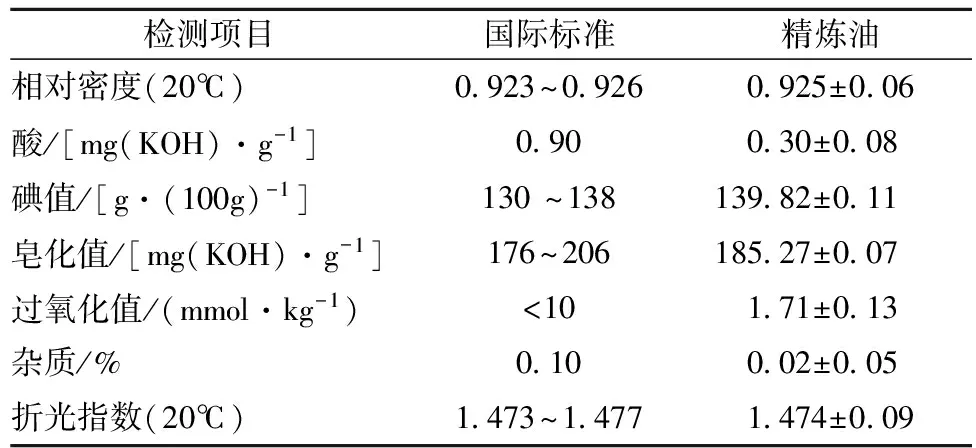
表2 葡萄籽精炼油理化指标
2.2葡萄籽油货架期的预测
在100、110、120、130 ℃,流量为20 L/h的条件下使用892 Rancimat氧化稳定仪分别测定葡萄籽油的诱导期,根据温度与lg(诱导期)的关系推测作图,由图4及公式Y=4.593 2-0.038 7×推测:当温度为 25 ℃时,葡萄籽精炼油的储存时间为176 h。

表3 不同温度下葡萄籽油氧化稳定性
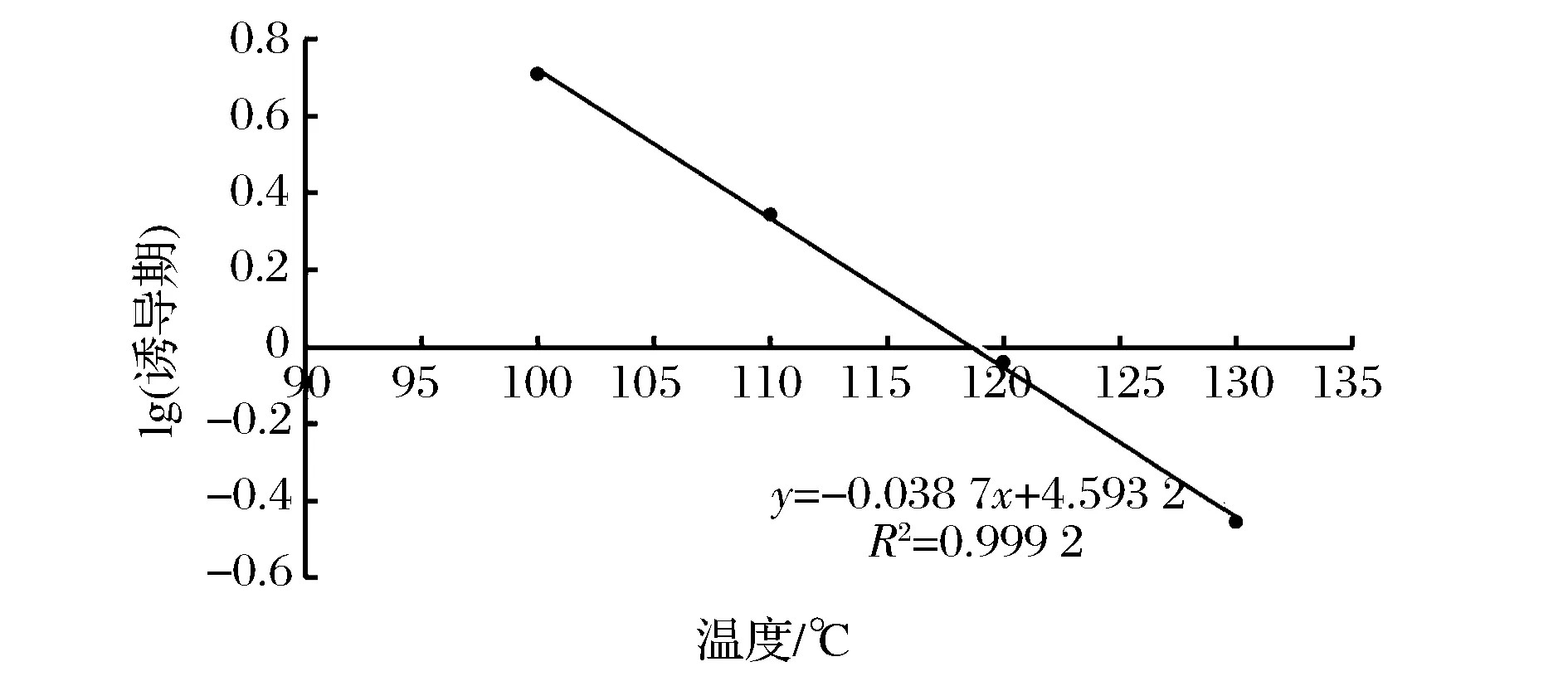
图4 诱导期和温度关系图Fig.4 Induced phase and temperature diagram
2.3单一抗氧化剂对葡萄籽油氧化稳定性的影响
诱导期在温度 120 ℃,空气流量为 20 L/h 的条件下测定,当不添加任何抗氧化剂时,葡萄籽精炼油诱导期为 0.91 h,将其作为空白对照,由表4可知,在葡萄籽油中添加不同种类的单一抗氧化剂时,各抗氧化剂对葡萄籽油的诱导期均高于空白对照。说明这5种抗氧化剂均具有延缓葡萄籽油氧化酸败的作用。但添加不同种类的抗氧化剂时,各抗氧化剂对葡萄籽油诱导期的影响不同。在添加同等剂量的抗氧化剂情况下,在葡萄籽油中抗氧化效果排名依次为TBHQgt;BHAgt;迷迭香提取物gt;APgt;dl-a-生育酚,说明TBHQ在葡萄籽油中的抗氧化效果最优。

表4 添加单一抗氧化剂葡萄籽油的诱导期
注:结果以(Mean±SD)表示;用最小显著差法(LSD法)进行多重比较,同行小写字母不同表示差异显著(plt;0,05);同列大写字母不同表示差异显著(plt;0.05)。表5同。
当5种抗氧化剂分别按 100、150、200、400 mg/kg 的添加量加入葡萄籽油中时,由表4可知,葡萄籽油的抗氧化能力随着抗氧化剂添加量的增加而增强。其中以TBHQ的抗氧化效果最优,当TBHQ在葡萄籽油中的添加量为100、 150、200 mg/kg时,如表5所示,在温度120 ℃下对葡萄籽油的PF分别为2.25、2.47、2.86,具有很好的抗氧化活性。考虑到生产成本以及食品安全,最终选用TBHQ(200 mg/kg)作为葡萄籽精炼油中添加的单一抗氧化剂。

表5 不同抗氧化剂对葡萄籽油的抗氧化系数(PF)
2.4复合抗氧化剂对油脂稳定性的影响
诱导期在温度120 ℃,空气流量为20 L/h的条件下测定,根据单一抗氧化剂对葡萄籽油氧化稳定性的影响,综合考虑单一抗氧化剂对葡萄籽油氧化稳定性影响的实验结果和抗氧化剂在油脂中的溶解性这两方面因素,选择迷迭香提取物、TBHQ、BHA三种抗氧化剂进行复配,结果如表6所示。将其与表4和表5比较,除TBHQ单独使用效果优于复合使用效果外,其余抗氧化剂复合后,抗氧化效果均比单独使用好。原因可能是由于抗氧化剂复合使用过程中,在抗氧化剂之间产生的游离基生产了新的酚类化合物[25],这些酚类化合物可以进一步与过氧化白由基结合生成相对稳定的物质,产生抗氧化作用,因而使其抗氧化效果得以增强。在葡萄籽油中添加复合抗氧化剂时,以TBHQ:BHA为3∶1时效果最佳。但单纯添加TBHQ(200 mg/kg)的效果更优。
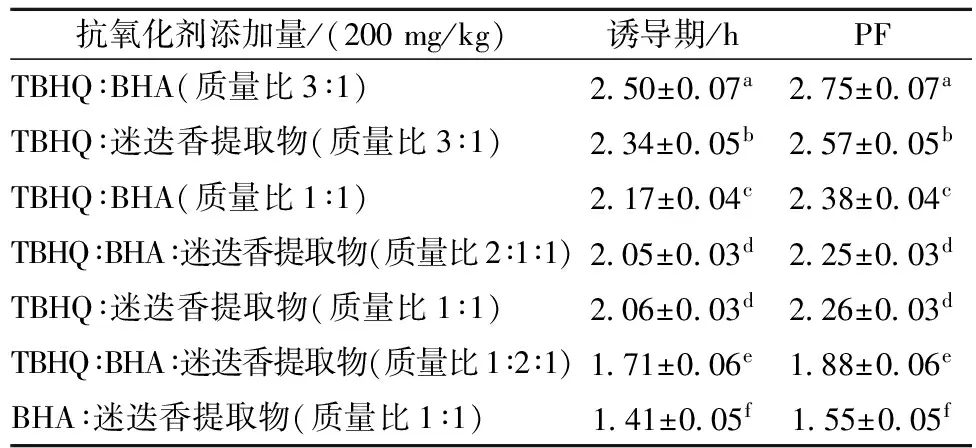
表6 添加复合抗氧化剂的葡萄籽油的诱导期及抗氧化系数(PF)诱导期
注:结果以(Mean±SD)表示;用最小显著差法(LSD法)进行多重比较,同列小写字母不同表示差异显著(plt;0.05)。
3 结论
(1)对葡萄籽油酸值影响最大的工艺流程为脱酸工艺,对葡萄籽油过氧化值影响最大的工艺为脱臭工艺,而诱导期在整个精炼过程中整体呈下降趋势。
(2)葡萄籽油经过精炼各工艺后,无论在感官鉴定和理化指标上都达到国家标准,葡萄籽精炼油的不溶性杂质含量较低,满足食用油脂的要求。无论在感官鉴定和理化指标上都满足食用油脂的要求。
(3)通过Rancimat法测定葡萄籽油样品的诱导期,在5种抗氧化剂质量浓度相同的条件下,分别对葡萄籽油抗氧化性能进行测定和分析,结果表明,5种抗氧化剂对葡萄籽油均具有一定的抗氧化效果,但添加不同抗氧化剂时,对于葡萄籽油氧化稳定性影响具有差异,当5种抗氧化剂质量浓度相同时,抗氧化能力由强到弱的顺序为:TBHQgt;BHAgt;迷迭香提取物gt;APgt;dl-a-生育酚。当5种抗氧化剂质量浓度不同时,随着添加量的增加,葡萄籽油的抗氧化能力也逐渐增强。
(4)6种抗氧化剂的复配实验表明:与复合抗氧化剂相比,TBHQ 单独使用效果更优,除此之外,其余各抗氧化剂复合后,抗氧化效果均比单独使用好,对于葡萄籽油而言,复合抗氧化剂的最佳组合为 TBHQ∶BHA (质量比3∶1)。
(5)用Rancimat法分别测定在100、110、120、130 ℃下葡萄籽油的诱导期,根据温度T与lg(诱导期)的关系作图,得lg(诱导期)和温度T线性相关,其方程式为1g(诱导期)=4.593 2-0.038 7X,R2=0.999 2,经外推葡萄籽油在 25 ℃ 的货架期为 176 d。
[1] 田淑芬.中国葡萄产业态势分析[J].中外葡萄与葡萄酒,2009(1):64-66.
[2] 任秋壮.葡萄籽毛油的精炼工艺研究[D].杨凌:西北农林科技大学,2012.
[3] 于红霞,宋家玉.葡萄籽中功效成分的测定[J].预防医学文献信息,2000,6(1):14-15.
[4] 徐芳,卢立新.油脂氧化机理及含油脂食品抗氧化包装研究进展[J].包装工程,2008,29(6):23-26.
[5] 边凤霞,郑旭煦,殷钟意.植物油氧化稳定性研究进展[J].重庆工商大学学报:自然科学版,2013,30(1):69-75.
[6] 任秋壮.葡萄籽毛油的精炼工艺研究[D].杨凌:西北农林科技大学,2012.
[7] 张国治,韩宝丽,土伟玲,等.葡萄籽油中脂肪酸成分分析[M].粮食科技与经济,2011,1(1): 49-50.
[8] 赵巍,王军,沈育杰,等.不同方法提取的山葡萄籽油理化指标和营养成分的对比[J].中国粮油学报,2008,23(6):127-130.
[9] 史晓东,吴彩娥.超声波提取葡萄籽油工艺的研究[J].粮食与食品工业,2007,14(2):17-20.
[10] 赵功玲.不同抗氧化剂对萝卜籽油氧化稳定性的影响[J].粮油食品科技,2016,24(2):39-42.
[11] 王茜茜.菜籽油储藏稳定性研究[D].南京:南京财经大学,2012.
[12] 李兴元,董福生,孙凤华.四种天然抗氧化剂对大豆油贮藏稳定性影响研究[J].粮食与油脂,2014,27(2):57-61.
[13] 翟柱成,吴克刚,柴向华,等.天然抗氧化剂对葵花籽油抗氧化作用的研究[J].食品工业科技,2010(3):148-150.
[14] 李素玲,张子德,王强,等.抗氧化剂对杏仁油贮藏稳定性的影响[J].中国油脂,2009,34(11):59-61
[15] 胡国华.食品添加剂应用基础[M].北京:化学工业出版社,2005.
[16] 张洁,杨国龙,毕艳兰,等.抗氧化剂对几种冷榨植物油氧化稳定性的影响[J].河南工业大学学报(自然科学版),2012,33(3):33-35,69.
[17] 徐金瑞,邓翌凤,列丽坤.几种抗氧化剂协同作用对葵花籽油稳定性的影响[J].中国油脂,2009,34(8):40-42.
[18] 盛雪飞,彭燕,陈健初.天然抗氧化剂之间的协同作用研究进展[J].食品工业科技,2010(7):64-66
[19] 朱振宝,刘梦颖,易建华.2种方法测定核桃油脂氧化稳定性相关性[J].中国粮油学报,2016,31(4):85-88.
[20] 肖仁显.山核桃油的提取工艺及其氧化稳定性研究[D].杭州:浙江大学,2012.
[21] 刘悦.油脂脱色过程及其机理的研究[D].无锡:江南大学,2007.
[22] 曹小峰.精炼过程及储藏条件对高酸价米糠油品质的影响[D].武汉:武汉轻工大学,2014.
[23] 谢丹.精炼及储藏对菜籽油品质的影响[D].无锡:江南大学,2012.
[24] 朱晋萱.茶叶籽制油过程中油的品质变化研究[D]:无锡:江南大学,2013.
[25] 郝利平,夏延斌,陈永泉,等.食品添加剂[M].北京:中国农业大学出版社,2002: 63-81.
Studyonoxidativestabilityofgrapeseedoil
QIN Ya-nan1,WANG Ling2,XIE Yuan-dong2,ZOU Ji-bin3, YANG Hua-feng3,WANG Jian-guo3,KANG Jian1*
1(College of Life Science and Technology, Xinjiang University,Urumqi 830046,China) 2(Xinjiang Pulian Department Detection Technology Research Institute,Urumqi 834000,China) 3(Xinjiang Hai Sheng Biological Engineering Limited by Share Ltd, Korla 843000,China)
Oxidative stability of grape seed oil was analyzed after refining. Rancimat method was used and the induction period was the index in oil stability evaluation. Effects of single usage and compound antioxidants such as tert butyl hydroquinone (TBHQ) and butylated hydroxyanisole (BHA), ascorbic acid palmitic acid sodium, dl-a- tocopherol, and rosemary extract on the oxidative stability of grape seed oil were studied. The results showed that the process of the greatest influence on the acid value was the acid removal process, and the most influential technology for the peroxide value was the deodorization process, while the induction period showed a downward trend in the whole refining process. Adding TBHQ, BHA, ascorbic acid, sodium palmitate and rosemary extract individually all has a better effect in refining oil and can improve oxidative stability of grape seed oil significantly. Except TBHQ, the oxidative effect of four antioxidant compound is better than any single one. The best ratio for TBHQ:BHA is 3∶1.
grape seed oil; refining; antioxidant; stability
10.13995/j.cnki.11-1802/ts.013770
硕士研究生(康健副教授为通讯作者,E-mail:1468501684@qq.com)。
2017-01-06,改回日期:2017-05-02


