美洛昔康联合氨甲环酸对腰椎骨折手术患者隐性失血和深静脉血栓的影响
陈文坚, 林 阳
(华中科技大学同济医学院附属同济医院, 湖北 武汉, 430022)
美洛昔康联合氨甲环酸对腰椎骨折手术患者隐性失血和深静脉血栓的影响
陈文坚, 林 阳
(华中科技大学同济医学院附属同济医院, 湖北 武汉, 430022)
美洛昔康; 氨甲环酸; 腰椎; 骨折; 隐性失血; 深静脉血栓
美洛昔康是一类烯醇酸类抗炎镇痛药,对于骨科术后疼痛具有良好的缓解作用,且无显著不良反应[1]。氨甲环酸是一种抗纤溶类药物,在临床的应用中具有明确的止血效果[2]。腰椎骨折手术是下肢深静脉血栓(DVT)发生的高危手术[3-4]。本研究探讨美洛昔康和氨甲环酸联合应用对减少腰椎骨折术后术后出血量及凝血功能的影响,现报告如下。
1 资料与方法
1.1 一般资料
选取本院2015年3月—2017年3月收治的60例腰椎骨折的患者,其中男33例,女27例,年龄32~67岁,平均年龄(45.6±7.3)岁。全部患者随机分为观察组30例和对照组30例。观察组男19例,女11例,年龄32~62岁,平均年龄(41.2±5.9)岁。对照组男14例,女16例,年龄38~67岁,平均年龄(46.7±7.1)岁。入选标准: 全部患者均诊断为腰椎骨折,其他各项检查指标均正常;术前2周均未服用抗凝药物或影响凝血功能的药物;术前经下肢血管彩色多普勒超声检查无明显异常。排除标准: 严重肝肾功能异常患者; 既往合并溃疡病史; 有凝血功能障碍性疾病和血管栓塞史的患者; 对氨甲环酸和美洛昔康过敏的患者。
1.2 处理方法
对照组患者于麻醉后、切皮前10 min, 静脉输入氨甲环酸注射液10 mg/kg。观察组在给予氨甲环酸注射液的基础上联合应用美洛昔康注射液15 mg ,肌肉注射, 1次/d, 术后开始连用5 d。全部患者均在手术前、后检查血常规,检查指标有纤维蛋白原、凝血酶原时间(PT)及活化部分凝血活酶时间(APTT)。患者术后的失血情况以总失血量、术中失血量和隐性失血量来表示。隐性失血量的计算方法为: 隐性失血量为理论失血量与机体输入血量之和,并扣除显性失血量[5]。
1.3 评价标准
2组患者的术后疼痛情况均应用视觉模拟疼痛程度评分(VAS)进行评估: 评分从0分至10分疼痛程度依次加深。记录全部患者术后6、12、24、48和72 h的VAS评分。
1.4 统计学方法
采用SPSS 18.0统计软件处理数据,采用配对t检验比较2组患者手术前后凝血指标及深静脉血栓发生率的比较,计数资料的比较采用卡方检验,P<0.05为差异有统计学意义。
2 结 果
与对照组相比,观察组患者的术后各时间点的VAS评分均显著下降,提示美洛昔康用于胸腰骨折术后患者能显著改善疼痛症状。见表1。观察组患者的总失血量、术中失血量和隐性失血量丢失依次为(1 735.8±263.5)、(535.26±87.35)、(432.6±63.5) mL, 与对照组的(1 813.6±206.7)、(546.75±72.69)、(438.7±59.6) mL比较,差异无统计学意义(P>0.05)。提示美洛昔康和氨甲环酸联合应用对患者失血情况无显著影响。2组患者术前和术后的纤维蛋白原、PT和APTT均无显著差异,提示美洛昔康和氨甲环酸联合应用对患者凝血功能无显著影响。见表2。观察组DVT发生率为6.67%, 对照组DVT发生率为3.33%, 2组比较无显著差异(P>0.05)。
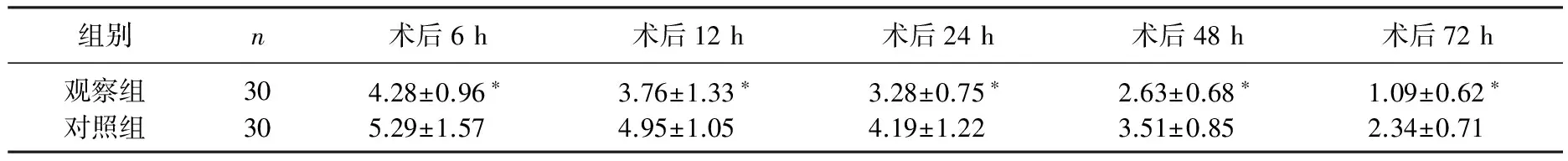
表1 2组患者术后各时间点的VAS评分 分
与对照组比较, *P<0.05。

表2 2组手术前后凝血指标及深静脉血栓发生情况比较
3 讨 论
手术后疼痛是一种常见的临床疼痛类型,手术本身和手术器械造成的组织损伤使机体释放大量的前列腺素,并刺激发生炎症反应,释放炎性因子和致痛物质[6], 同时由于机体外周感受器大量疼痛信号的传入,影响到患者的循环、呼吸、消化和免疫等机体功能,易造成术后并发症的发生,严重者会发生关节僵硬、肌肉萎缩等并发症[7],甚至增加深静脉血栓的发生率。
相关研究[8]显示,非选择性的非甾体抗炎药(NSAIDs), 除具有抗炎镇痛作用外,还能不同程度地影响血小板功能,延长出血时间,增加出血量。美洛昔康对COX-2具有一定的选择性,是其对COX-1的选择性的约10倍[9],显著高于其他常用的非甾体类药物,如布洛芬,阿司匹林等。因此推测美洛昔康比其他类非选择性 NSAIDs药物的安全性更好,对体内血小板功能抑制作用更小[10]。
腰椎部位依靠丰富的肌肉韧带组织保护,发生的骨折常为高能量性损伤,再经手术进一步创伤,会造成较大的隐性失血量,其发生隐性失血的机制推测为血液能够由微小血管渗入周围组织间隙和皮下等部位。此外,脊柱的生理腔隙和椎体间腔隙等部位会发生血液滞留,以上多个原因均能导致隐性失血的发生。若手术时间较长,机体受到的创伤更多,会同时增加机体的隐性失血量。隐性失血虽具有一定的隐蔽性,但不能被忽视,以防止术后患者出现红细胞压积及血红蛋白明显下降的现象,防止影响机体的愈合和修复[11]。因此术后的镇痛用药应尽量减少对隐性失血的影响。本研究比较了两组患者的失血情况,观察组和对照组患者的总失血量、术中失血量和隐性失血量丢失均无显著性差异(P>0.05), 提示将美洛昔康和氨甲环酸联合应用于腰椎骨折术后的抗凝止痛治疗,对患者失血情况无显著影响,未增加患者的隐性失血。
本研究通过对血小板计数和凝血指标观察, 2组患者的纤维蛋白原、PT和APTT水平相比差异无统计学意义,提示美洛昔康对于腰椎骨折术后应用氨甲环酸抗凝的患者的凝血功能无显著影响,未增加失血风险。Rinder HM[12]研究显示,通过对患者出血时间和凝血酶原时间观察,美洛昔康能阻断TXA2的形成,且不影响血小板功能,该特点有异于其他非甾体类药物,本研究结果与之相似。纤维蛋白原是凝血反应过程中的关键凝血因子,患者在术中血液凝血系统被激活,机体处于高凝状态[13], 2组患者的纤维蛋白原水平相比无明显差异,提示美洛昔康未显著影响术后患者体内的凝血状态。
术中的器械和操作能造成骨折部位的血管和内皮细胞的损伤,凝血过程启动,循环系统中由于术中组织因子的进入,且大量炎症因子的释放,共同作用使血液呈高凝状态,造成下肢深静脉血栓(DVT)的发生[14]。DVT能引起静脉回流障碍,如血栓脱落后有引发肺栓塞的危险,从而成为围术期常见的一种并发症。本研究结果显示,美洛昔康和氨甲环酸的联合用药组与单用氨甲环酸组相比的DVT的发生率无显著性差异,提示美洛昔康未显著增加DVT的发生率,在围术期应用安全有效。
[1] Altman R, Hochberg M, Gibofsky A, et al. Efficacy and safety of low-dose SoluMatrix meloxicam in the treatment of osteoarthritis pain: a 12-week, phase 3 study[J]. Current medical research and opinion, 2015, 31(12): 2331-2343.
[2] 王浩洋, 康鹏德, 裴福兴,等. 氨甲环酸减少全髋关节置换术围术期失血的有效性及安全性研究[J]. 中国骨与关节杂志, 2015(8):649-654.
[3] 王浩洋, 康鹏德, 杨静,等. 氨甲环酸减少全髋关节翻修术围术期失血的安全性及有效性研究[J]. 中华关节外科杂志:电子版, 2013, 7(5):11-15.
[4] Rappold J F, Pusateri A E. Tranexamic acid in remote damage control resuscitation[J]. Transfusion,2013,53(Suppl 1): 96S-99S.
[5] 杜绍良, 张锡光, 滕兆伟,等. 腰椎骨折手术相关隐性失血[J]. 临床和实验医学杂志, 2013, 12(19):1575-1575.
[6] 姚红. 骨科患者术后疼痛护理干预[J]. 中国民族民间医药, 2012, 21(12):141-141.
[7] 张婧. 骨科围术期超前镇痛及护理干预的疗效观察[J]. 实用药物与临床, 2013, 16(6):501-503.
[8] Moore N, Pollack C, Butkerait P. Adverse drug reactions and drug-drug interactions with over-the-counter NSAIDs [J]. Therapeutics & Clinical Risk Management, 2015, 11:1061-1075.
[9] Park J H, Park Y S, Lee J B, et al. Meloxicam inhibits fipronil-induced apoptosis via modulation of the oxidative stress and inflammatory response in SH-SY5Y cells[J]. Journal of Applied Toxicology, 2016, 36(1):10-7.
[10] Aurini L, Borghi B, White P F, et al. Treatment of chronic cervicobrachial pain with periradicular injection of meloxicam[J]. Minerva anestesiologica, 2016, 82(4): 411-418.
[11] 杜绍良, 张锡光, 滕兆伟,等. 腰椎骨折手术相关隐性失血[J]. 临床和实验医学杂志, 2013, 12(19):1575-1575.
[12] Rinder H M, Tracey J B, Souhrada M, et al.Effects of meloxicam on platelet function in healthy adults: a randomized, double-blind, placebo-controlled trial[J].J Clin Pharmacol, 2002,42(8):881- 886.
[13] Takami Y, Eguchi S, Tateishi M, et al. A randomised controlled trial of meloxicam, a Cox-2 inhibitor, to prevent hepatocellular carcinoma recurrence after initial curative treatment[J]. Hepatology International, 2016, 10(5):799-806.
[14] Yoon Y C, Sim J A. Prophylaxis and Management of Deep Vein Thrombosis in Trauma Patients[J]. Journal of the Korean Fracture Society, 2015, 28(1):82-8.
R 683
A
1672-2353(2017)19-172-02
10.7619/jcmp.201719060
2017-05-22
湖北省自然科学基金(2012FFB02405、2016CFB659)

