不同降糖方案对初诊2型糖尿病患者胰高血糖素样肽-1的影响及与β细胞功能的相关性
马淑芳, 杜志坡, 王运兴, 王玉宵, 侯冰洁
(河北省唐县人民医院, 河北 唐县, 072350)
不同降糖方案对初诊2型糖尿病患者胰高血糖素样肽-1的影响及与β细胞功能的相关性
马淑芳, 杜志坡, 王运兴, 王玉宵, 侯冰洁
(河北省唐县人民医院, 河北 唐县, 072350)
目的观察不同降糖方案对初诊2型糖尿病(T2DM)患者的胰高血糖素样肽-1(GLP-1)水平的影响及其与β细胞功能的相关性。方法将76例初诊T2DM患者随机分为诺和锐30组和口服药物组,治疗前后进行OGTT试验,测定0、30、120 min时血糖,检测GLP-1、C肽、胰岛素等指标,计算HOMA胰岛素分泌指数(HOMA-IS)及抵抗指数(HOMA-IR)。以健康者30例作为对照组,比较GLP-1水平,分析治疗前后各指标变化。结果不同降糖治疗方案的各时间点比较,血糖及其曲线下面积(AUCg)显著降低(P<0.05); 胰岛素、C肽及其曲线下面积(AUCins、AUCc-p)显著升高(P<0.05); HOMA-IR显著降低(P<0.05), HOMA-IS、△INS30/G30、△INS120/G120显著升高(P<0.05)。与治疗前比较,诺和锐30组和口服药物组各时间点GLP-1水平及AUCglp(GLP-1曲线下面积)均显著升高(P<0.05), 在120 min达峰值,接近对照组曲线。结论初诊T2DM患者GLP-1水平低于正常值。不同降糖治疗均使GLP-1升高。胰岛素、C肽及AUCins、AUCc-p、HOMA-IS、HOMA-IR等明显改善,提示β细胞功能恢复,胰岛素抵抗减轻。
2型糖尿病; 胰高血糖素样肽-1; 胰岛素; β细胞功能
胰高血糖素样肽-1(GLP-1)是一种肠促胰岛素,主要由回肠末端、结肠中L细胞分泌,由葡萄糖等营养物质刺激释放,可促进胰岛素合成及分泌,改善早期胰岛素应答能力,还可抑制胰岛β细胞凋亡和促进其增殖,抑制胰高血糖素分泌等。本研究探讨不同降糖方案对初诊2型糖尿病(T2DM)患者胰高血糖素样肽-1的影响及与β细胞功能的相关性,现报告如下。
1 资料与方法
1.1 一般资料
随机选取2010年4月—2013年8月本院的初诊T2DM患者共76例,其中男35例,女41例。随机分为诺和锐30治疗组36例,其中男17例,女19例; 口服药物治疗组40例,其中男18例,女22例。以同期本院健康体检者30例作为对照组,男15例,女15例。本研究经本院医学伦理委员会批准,患者知情同意。糖尿病诊断及分型参考1999年WHO标准,均为初诊T2DM患者,未服用任何降糖药物,未行饮食及运动治疗。3组年龄、体质量指数、收缩压、舒张压、总胆固醇等比较,差异无统计学意义(P>0.05)。见表1。
1.2 方法
受试者均于清晨禁食水10 h以上,脱鞋、免冠,测量身高及体质量,行葡萄糖耐量(OGTT)试验,采集空腹及餐后30、120 min静脉血液标本,分别检测血糖、GLP-1、C肽及胰岛素水平。采用ELISA法检测活性GLP-1、C肽,化学发光法测定胰岛素(INS); 氧化酶法检测血糖水平。HOMA-IS=20×INS0/(G0-3.5); HOMA-IR=G0×INS0/22.5; AUCC-PC肽曲线下面积= 25(C0+4×C30+3×Cl20); AUCg =0.25 ×(G0+4×G30+3×Gl20); AUCins=0.25×(INS0+4×INS30+3×INSl20); AUCglp =0.25×(GLP0+4×GLP30+3×GLPl20); 早相胰岛素分泌△INS30/△G30=INS30-INS0/G30-G0; △INS120/△Gl20=INSl20-INS0/G120-G0。

表1 3组患者一般资料比较
1.3 统计学处理
应用SPSS 17.0软件进行统计分析,正态分布计量资料以均数±标准差表示,组间比较采用方差分析,不同降糖治疗方案的治疗前后指标水平比较用配对t检验。所有检验均为双侧检验,以P<0.05为差异有统计学意义。
2 结 果
与对照组相比,诺和锐30组和口服药物组治疗前各时间点的血糖显著升高,胰岛素、C肽及GLP-1显著降低(P<0.05)。与治疗前比较,经格列吡嗪、二甲双胍及诺和锐30治疗4周后,患者OGTT各时间点血糖浓度均显著下降,葡萄糖曲线下面积(AUCg)明显减少; 反映胰岛功能的胰岛素、C肽及其曲线下面积(AUCins、ACUc-p)显著增加,反映胰岛素抵抗的HOMA-IR均较治疗前显著降低, HOMA-IS及△INS30/G30、△INS120/G120显著升高(P<0.05)。与治疗前比较,各组的GLP-1水平, OGTT 30、120 min均较0 min显著升高,不同降糖治疗4周后,其各自0、30、120 min的GLP-1及AUCglp均显著升高(P<0.05), 均接近对照组曲线。见表2、3。
3 讨 论
T2DM是一种异质性疾病,具有胰岛素抵抗和胰岛素分泌缺陷双重病理机制,糖毒性和脂毒性的持续存在,导致β细胞功能进行性衰退。GLP-1作为一种多肽类肠促胰素,能改善早期胰岛素应答,促进β细胞增殖、抑制凋亡,可由进餐诱导分泌。糖尿病患者的GLP-1分泌在餐后120 min有明显下降[1], 其类似物已用于临床治疗2型糖尿病,并获较好疗效。血浆总GLP-1及其变化水平,在OGTT试验30~120 min各时间点明显低于正常糖耐量组及糖耐量减低组[2]。本研究显示,初诊T2DM患者降糖治疗前,空腹及OGTT所诱导的GLP-1水平在糖负荷后30、120 min均低于正常人。
本研究显示,初诊T2DM患者的GLP-1分泌水平在空腹及糖负荷后30、120 min均低于正常人; 经格列吡嗪、二甲双胍联合应用及诺和锐30治疗后, GLP-1水平升高,接近正常人水平。表明格列吡嗪、二甲双胍联合治疗有提高血GLP-1水平的作用。反映β细胞功能的胰岛素、C肽及其曲线下面积(AUCins、AUCc-p)等指标升高, HOMA-IS明显升高,提示β细胞功能明显改善, HOMA-IR降低则提示胰岛素抵抗减轻。格列吡嗪、二甲双胍及诺和锐30治疗后,初诊T2DM患者的血清GLP-1升高。本研究结果显示,两种不同的降糖方案在治疗后的GLP-1水平较治疗前均明显升高,在120 min达峰值,接近正常人。GLP-1分泌模式受损状态也有改善。二甲双胍通过提高GLP-1水平对T2DM发挥降糖作用,具体机制至今未明。推测其抑制DPP-4活性[3], 增加β细胞内的GLP-1 受体表达[4-6], 提高外周组织对GLP-1的敏感性[7], 直接和/或间接延长GLP-1半衰期,从而发挥更好的降糖作用。
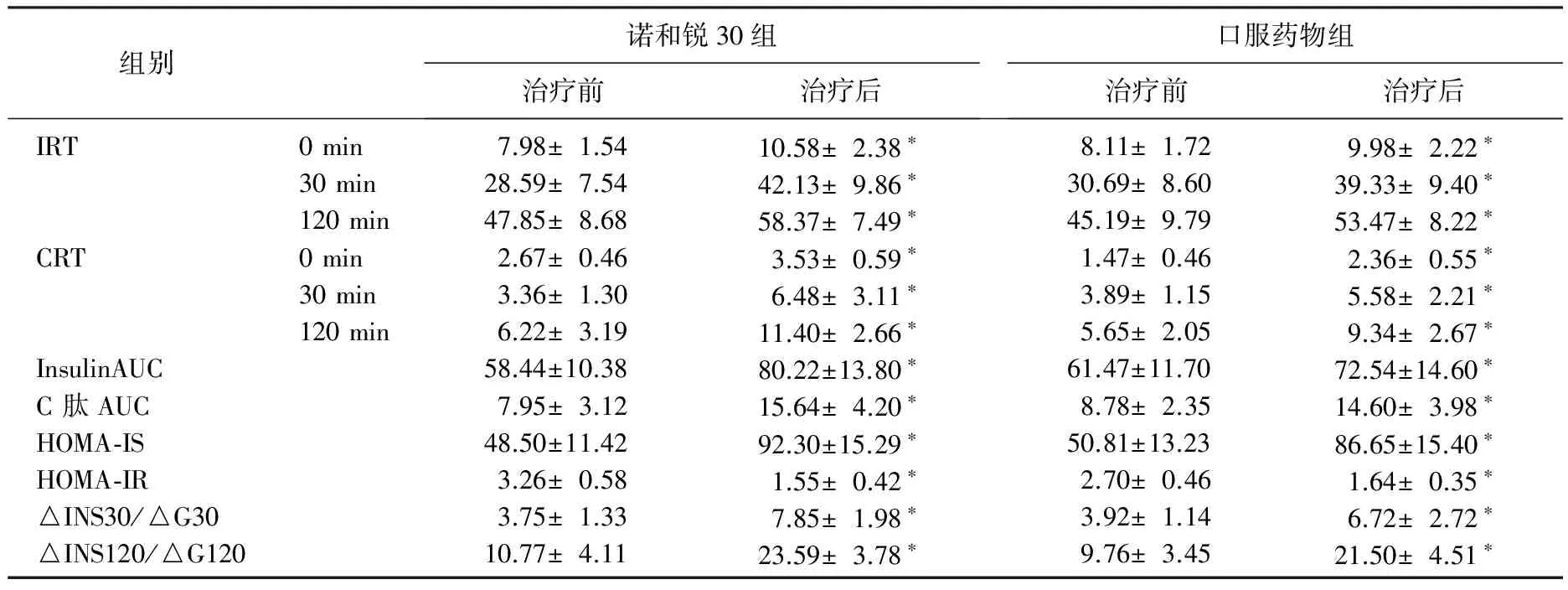
表2 诺和锐30组和口服药物组降糖治疗前后各β细胞功能指标的比较
与治疗前比较, *P<0.05。IRT: 胰岛素释放试验; CRT: C肽释放试验。

表3 T2DM组不同降糖方案治疗前后与对照组OGTT试验中GLP-1水平的变化 pmol/L
与对照组比较, *P<0.05; 与治疗前比较, #P<0.05。
GLP-1的下降是造成IR的决定性因素。胰岛素强化治疗可解除高糖毒性,提高GLP-1基础浓度,达到改善胰岛素抵抗和胰岛β细胞功能的效果。赵晶等研究发现,与健康人群比较,初诊T2DM患者的GLP-1水平和HOMA-IS明显降低, HOMA-IR明显升高,促使GLP-1和C肽水平明显回升。有研究[8]显示经2周的胰岛素强化降糖治疗后, OGTT试验显示GLP-1分泌水平明显改善。
[1] Zhang F, Tang X, Cao H, et al. Impaired secretion of total glucagon-like peptide-1 in people with impaired fasting glucose combined impaired glucose tolerance[J]. Int J Med Sci, 2012, 9(7): 574-581.
[2] Wang X L, Ye F, Li J. Impaired secretion of glucagon-like peptide 1 during oral glucose tolerance test in patients with newly diagnosed type 2 diabetes mellitus[J]. Saudi Med J, 2016, 37(1): 48-54.
[3] Cuthbertson J, Patterson S, O′Harte FP, et al. Addition of metformin to exogenous glucagon-like peptide-1 results in increased serum glucagon-like peptide-1 concentrations and greater glucose lowering in type 2 diabetes mellitus[J]. Metabolism, 2011, 60(1): 52-6.
[4] 倪敏, 袁群. 艾塞那肽联合二甲双胍治疗口服降糖药控制不佳的2型糖尿病疗效观察[J]. 中国临床研究, 2012, 25(9): 835-837.
[5] 李洁, 王扬天, 许一新, 等. 二甲双胍加用艾塞那肽治疗2型糖尿病20例疗效分析[J]. 重庆医学, 2013, 42( 14): 1630-1632.
[6] 陈彬, 张星光, 程千鹏, 等. 艾塞那肽联合二甲双胍对初诊成人2型糖尿病患者血糖控制效果观察[J]. 解放军医药杂志, 2016, 28(5): 66-69.
[7] Bahne E, Hansen M, Brønden A. Involvement of Glucagon-like Peptide-1 in the Glucose-lowering effect of Metformin[J]. Diabetes Obes Metab, 2016, 18(10): 955-61.
[8] 熊静, 莫朝晖, 谢艳红, 等. 新诊断的2型糖尿病患者短期胰岛素强化治疗后肠促胰岛素的变化[J]. 中国糖尿病杂志, 2012, 20(2): 120-123.
Effectsofdifferenthypoglycemictreatmentsonglucagon-likepeptide-1anditscorrelationwithβcellsfunctioninnewlydiagnosedtype2diabetesmellitus
MAShufang,DUZhipo,WANGYunxing,WANGYuxiao,HOUBingjie
(DepartmentofEndocrinology,TangCountyPeople′sHospital,TangCounty,Hebei, 072350)
ObjectiveTo observe different hypoglycemic treatments on glucagon-like peptide-1(GLP-1) and its correlation with β cells function in newly diagnosed type 2 diabetes mellitus(T2DM).MethodsA total of 76 patients with newly diagnosed T2DM were randomly divided into insulin aspart 30 group and oral drugs group. OGTT test were measured at 0, 30, 120 min, the serum levels of GLP-1 and corresponding C peptide, and insulin levels were measured, HOMA insulin secretion and insulin resistance index were calculated. Then 30 healthy cases were as the control group, GLP-1 levels were analyzed, and the changes of the index were compared.ResultsAt each time point, blood glucose and glucose area under the curve (AUCg) was significantly decreased (P<0.05). Insulin and C-peptide and the AUC (AUCins, AUCc-p)were increased (P<0.05). HOMA-IR was statistically decreased compared with pre-therapy(P<0.05), HOMA-IS and △INS30/G30, △INS120/G120 were significantly increased (P<0.05). Compared with pre-therapy, GLP-1 levels and AUCglp (area under the curve GLP-1) were significantly increased (P<0.05), and reached the peak at 120 min, closed to secretion curve of the control group.ConclusionGLP-1 levels were lower than normal in newly diagnosed T2DM patients, and different hypoglycemic drugs makes GLP-1 levels increase. Insulin, C-peptide and AUCins, AUCc-p, HOMA-IS, HOMA-IR, etc., suggest that β-cell function is restored and insulin resistance is reduced.
type 2 diabetes mellitus; GLP-1; insulin; β cell function
R 587.1
A
1672-2353(2017)19-056-03
10.7619/jcmp.201719016
2017-04-11
河北省卫生厅青年科技项目(20100547)

