电感耦合等离子体原子发射光谱法测定植物中钾、钠、钙和镁*
刘泽斌 ,刘守廷 ,蒋天成 ,宋业成 ,吴婷 ,黄殿贵 ,王有兵 ,王玉清 ,邓捷
(1.广西辐射环境监督管理站,南宁 530222; 2.广西分析测试研究中心,南宁 530022;3.广西中医药大学,南宁 530001; 4.广西桂宏环境监测科技有限公司,南宁 530021)
电感耦合等离子体原子发射光谱法测定植物中钾、钠、钙和镁*
刘泽斌1,刘守廷2,蒋天成2,宋业成3,吴婷2,黄殿贵2,王有兵4,王玉清2,邓捷2
(1.广西辐射环境监督管理站,南宁 530222; 2.广西分析测试研究中心,南宁 530022;3.广西中医药大学,南宁 530001; 4.广西桂宏环境监测科技有限公司,南宁 530021)
采用硝酸–高氯酸湿法消解或硝酸–双氧水微波消解植物样品,以电感耦合等离子体原子发射光谱法同时测定样品溶液中钾、钠、钙和镁含量。用该法测定灌木枝叶和茶叶标准样品,测定值均在标准值范围内,测定结果的相对标准偏差为0.45%~4.05% (n=8)。钾、钠、钙、镁的加标回收率分别为94.4%~107.6%,92.6%~107.9%,93.7%~105.4%,92.9%~107.2%。该方法操作简便,测量精密度和准确度完全满足植物中钾、钠、钙和镁含量的测定要求。
电感耦合等离子体原子发射光谱法;植物;钾;钠;钙;镁
钾、钠、钙、镁是植物生长过程中不可缺少的重要元素,其中钾元素可提高植物光合作用的强度,增强作物的抗逆性和抗病能力;钠元素可促进植物细胞体积增大和细胞数目增多,使植物生长得更快,发育得更好;钙元素对碳水化合物和蛋白质的合成过程以及植物体内生理活动的平衡起着重要作用;镁元素则是叶绿素的重要组分之一。
目前植物中钾、钠含量的测定通常采用火焰光度法[1–5],也有报道采用示波极谱法[6]和原子吸收光谱法[7–15]。植物中钙、镁的含量测定通常采用原子吸收法和EDTA络合滴定法[11–18],也有报道采用光度法测定植物中的钙含量[19–20]。上述检测方法钾、钠、钙、镁元素均单独测定,操作繁琐,试剂消耗量大,检测时间长。目前有报道采用微波消解–电感耦合等离子体发射光谱(ICP–AES)法测定大米中铜、锰、铁、锌、钙、镁、钾、钠 8 种元素[21]。随着精密大型分析仪器的逐渐普及,开发建立一批利用大型仪器的标准分析方法代替工作量大、操作繁琐、环境污染大的分析方法,势在必行。
笔者对测定条件进行优化,建立了同时测定植物中钾、钠、钙、镁含量的ICP–AES法,该法操作简单快捷,灵敏度高,线性范围宽,重复性好,准确度高,环境污染少,特别适用于大批量样品的检测。
1 实验部分
1.1 实验原理
将植物试样在电热板上以硝酸–高氯酸湿法消解或硝酸–过氧化氢微波消解后定容。用检测元素的标准物质溶液配制系列标准工作溶液,用电感耦合等离子体原子发射光谱仪同时测定标准工作溶液、样品及空白溶液的谱线强度,以待测元素质量浓度为横坐标,谱线强度为纵坐标,绘制标准工作曲线,利用标准工作曲线计算出试样中钾、钠、钙和镁含量。
1.2 主要仪器与试剂
电感耦合等离子体原子发射光谱仪:ICAP 6300DUO型,美国热电仪器公司;
氩气:纯度为99.99%;
电子微量天平:BT125D型,感量为0.1 mg,赛多利斯科学仪器(北京)有限公司;
电热板:ML–2.4–4可调式,广西南宁融仪实验设备有限公司;
微波消解系统:CEM MARS型,美国培安科技公司;
盐酸、硝酸、高氯酸、过氧化氢:分析纯;
氯化钾、氯化钠、碳酸钙、氧化镁:基准试剂,上海试剂一厂;
钾标准溶液:1.0 mg/mL,称取 1.907 0 g于(550±50)℃灼烧至恒重的基准试剂氯化钾,置于500 mL烧杯中,用适量水溶解,冷却,移入1 000 mL容量瓶中,用水稀释至标线,混匀,贮于聚乙烯瓶中;
钠标准溶液:1.0 mg/mL,称取 2.542 0 g于(550±50)℃灼烧至恒重的基准试剂氯化钠,置于100 mL烧杯中,用适量水溶解,移入1 000 mL容量瓶中,用水稀释至标线,混匀,贮于聚乙烯瓶中;
钙标准溶液:1.0 mg/mL,称取0.249 7 g于110℃干燥至恒重的基准试剂准碳酸钙,置于100 mL烧杯中,用少量盐酸溶解,移入100 mL容量瓶中,用水稀释至标线,混匀,贮于聚乙烯瓶中;
镁标准溶液:1.0 mg/mL,称取0.165 8 g于800℃灼烧至恒重的基准试剂氧化镁,置于100 mL烧杯中,加入3 mL盐酸溶液(1+6),完全溶解后,移入100 mL容量瓶中,用水稀释至标线,混匀,贮于聚乙烯瓶中;
灌木枝叶标准物质:编号为GBW 07602(GSV–1),含钾 (0.85±0.02)%,钠 (1.10±0.10)%,钙(2.22±0.13)%,镁(0.287±0.018)%,地矿部物化探研究所;
茶叶标准物质:编号为GBW 10016 (GSB–7),含钾(1.63±0.07)%,钠(0.009±0.001)%,钙(0.326±0.008)%,镁(0.186±0.11)%,地球物理地球化学勘查研究所;
实验所用其它试剂均为分析纯(或以上);
实验用水为实验室二级水。
1.3 仪器工作条件
中阶梯光栅,二维交叉色散系统;CID86电荷注入固体检测器;高频发生器功率:1 150 W;冷却气流量:12 L/min;辅助气:氩气,流量为0.5 L/min;辅助雾化气:氩气,流量为0.75 L/min;冲洗泵转速:75 r/min;分析泵转速:50 r/min;泵稳定时间:5 s;积分时间:25 s;分析谱线:钾 766.4,769.8 nm,钠 588.9,589.5 nm,钙 317.9,431.8 nm,镁 279.5,285.2 nm。
1.4 钾、钠、钙、镁系列混合标准工作溶液的配制
分别移取钾、钠、钙、镁标准溶液各0.00,0.10,0.50,1.00,2.00,3.00 mL 于 6只 50 mL 容量瓶中,分别加入3 mL盐酸,用水稀释至标线,摇匀,配制成含钾、钠、钙、镁均分别为 0,2.00,10.0,20.0,40.0,60.0 μg/mL的系列混合标准工作溶液。
1.5 样品消解
1.5.1 湿法消解
称取试样0.40 g(精确至0.000 1 g),置于125 mL三角烧杯中,以少许水润湿,加入10 mL硝酸、1 mL高氯酸,盖上表面皿,放置10 min左右,于电热板上低温加热消解,待样品中大量浓氮气体挥发后,将电热板升温至150~180℃消解至冒高氯酸白烟。若样品冒高氯酸白烟前有颜色,需补加2~4 mL硝酸消解至溶液基本无色。打开表面皿,待冒完高氯酸白烟至湿盐状时取下,加入3 mL盐酸,温热溶解,冷却至室温,将试样溶液转移至100 mL容量瓶中,用水稀释至标线,摇匀,待测。同时做空白试验。
1.5.2 微波消解
称取试样0.20 g(精确至0.000 1 g),于微波消解罐中,以少许水湿润,先加入5 mL硝酸,再加入3 mL过氧化氢,按照表1参数设定微波消解条件并进行消解,消解完毕后,用水少量多次洗入50 mL容量瓶中,加入1 mL盐酸,定容至标线,摇匀待测。同时做空白试验。

表1 微波消解条件
1.6 测定
根据试样溶液中待测元素的浓度范围,导入标准工作溶液,用电感耦合等离子体原子发射光谱仪测定标准工作溶液的谱线强度,以待测元素的质量浓度为横坐标,谱线强度为纵坐标,绘制标准工作曲线,标准工作曲线的线性相关系数应不小于0.999 5。
测定前预热仪器40~60 min以增强其稳定性。根据各元素推荐分析谱线响应的相对强度和干扰情况,为待测元素选择适当的分析谱线。
1.7 结果计算
试样中钾、钠、钙、镁的含量按式⑴进行计算:

式中:X——试样中的钾、钠、钙或镁含量,mg/kg;
c——从标准工作曲线上查得试样溶液中钾、钠、钙或镁的质量浓度,µg/mL;
c0——从标准工作曲线上查得试剂空白溶液中钾、钠、钙或镁的质量浓度,µg/mL;
V——试样溶液的定容体积,mL;
m——试样的质量,g。
2 结果讨论
2.1 样品处理方法的选择
植物主要成分由碳、氢、氧、氮四大元素组成,植物样品的消解通常采用碱熔、酸熔和微波消解3种消解体系。
碱熔通常采用Na2CO3和NaOH高温熔融消解,测定植物中钾、钠、钙和镁时会引入杂质及对钠的测定产生干扰;酸熔消解若只使用硝酸,消解速度慢且消解不完全,若以硝酸为主加入0.5~1 mL高氯酸在电热板上消解,则消解快速且完全,但高氯酸加入量不宜过多,否则在有机物未消解完全、硝酸耗尽、冒高氯酸烟雾时易发生爆炸;微波消解只使用硝酸作消解液则消解速度慢且消解不完全,若加入高氯酸则易发生爆炸,用硝酸和强氧化剂双氧水混合消解,消解既快又完全。故湿法酸熔消解采用硝酸和少许高氯酸体系,微波采用硝酸和双氧水体系。
2.2 实验条件的优化
钾、钠、钙、镁分别选择 4,3,10,6 条谱线进行测定,比较不同谱线的仪器响应情况,最终每种元素选择两条灵敏度相对较高、干扰小、峰形好、重复性好的谱线作为分析谱线。
仪器功率在900~1 300 W之间可调,钾、钠、钙、镁同时测定时,采用1 150 W功率可以保证每种元素都能得到较高的原子化率。
以火焰锥形较好、不波动为依据选定冷却气流量为12 L/min。
选择雾化气流量为0.75 L/min,此条件下雾化率较高。
以钾、钠、钙、镁分析谱线强度均较强为依据选定火焰观察高度为14 mm。
以连续测定10次重复性和稳定性较好为依据选择积分时间为25 s。
2.3 干扰试验
植物中的主要无机元素有Fe,Al,Ca,Mg,K,Na,P,Si等,经硝酸和高氯酸消解后,除Si外全部溶解在溶液里。为了考察溶出的基体元素对植物中钾、钠、钙和镁测定结果的影响,进行了基体元素S,P,Al,Fe对所选分析谱线的干扰试验,试验结果见表2。由表2可知,基体元素S,P,Al,Fe对钾、钠、钙和镁分析谱线的强度几乎没有影响。
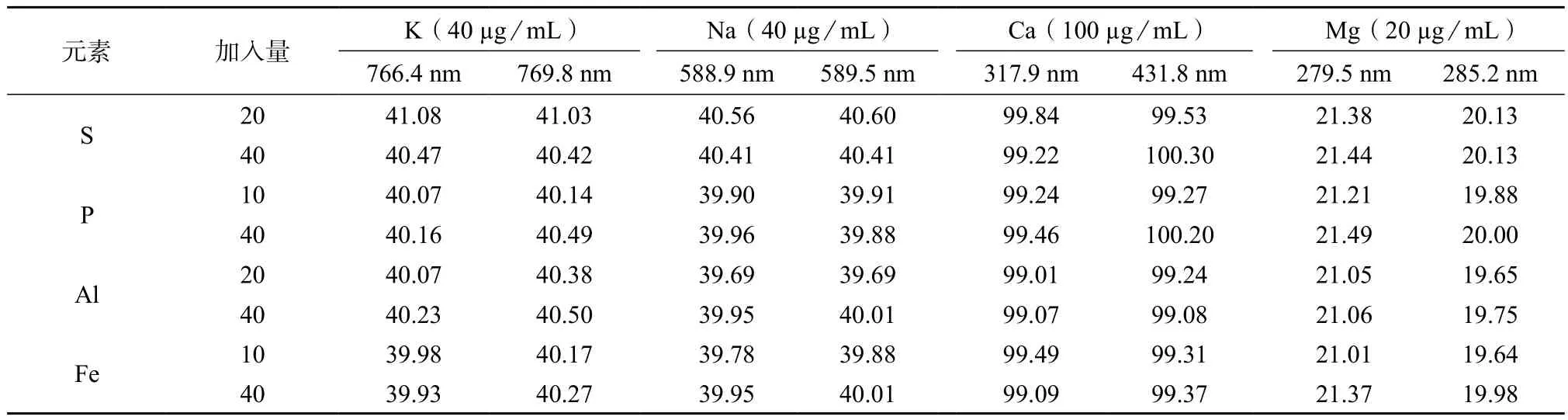
表2 S,P,Al,Fe不同加入量时钾、钠、钙、镁的测定结果 µg/mL
2.4 线性方程和检出限
用电感耦合等离子体原子发射光谱仪依次测定钾、钠、钙、镁系列混合标准工作溶液,以标准工作溶液的质量浓度X为横坐标,光谱强度Y为纵坐标,绘制标准工作曲线,以样品空白11次连续测定结果标准偏差的3倍作为方法检出限。
该方法钾、钠、钙、镁4种元素的线性范围、线性方程、相关系数和检出限见表3。
2.5 样品测定
选取灌木枝叶和茶叶标准物质进行测定,每种样品称取8个平行样,按1.5和1.6方法进行样品消解和测定,测定结果见表4。由表4可知,钾、钠、钙、镁4种元素测定值在标准值范围内,相对标准偏差为0.45%~4.05%,表明方法的准确度、精密度良好。
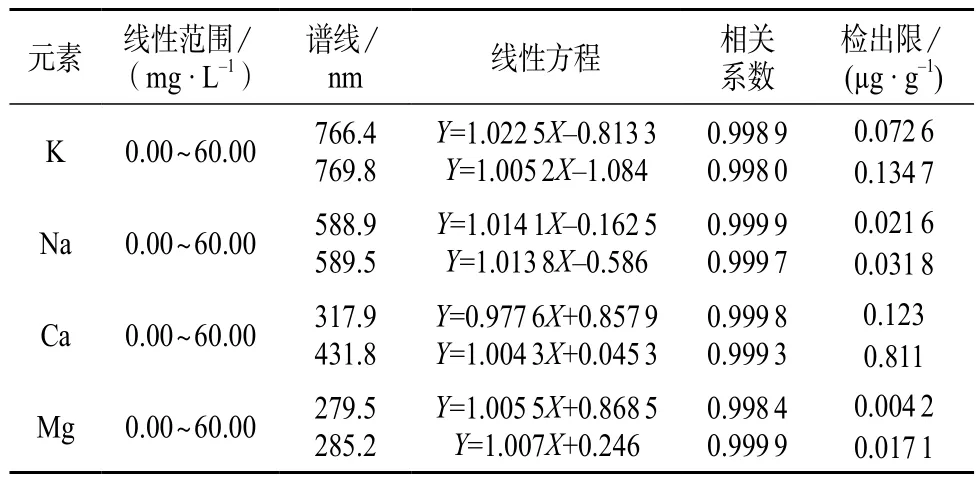
表3 钾、钠、钙、镁的线性范围、线性方程和相关系数

表4 标准样品测定结果
2.6 加标回收试验
选择灌木枝叶标准物质、茶叶标准物质,各称取一定质量(每种标准物质称取3份平行样品),分别加入不同量的钾、钠、钙、镁标准储备液,按照1.5和1.6方法进行消解、定容、测定,计算钾、钠、钙、镁4种元素的回收率,测定结果见表5~表8。由表5~表8可知,灌木枝叶、茶叶两种标准样品钾、钠、钙、镁3个浓度水平的加标回收率分别为94.4%~107.6%,92.6%~107.9%,93.7%~105.4%,92.9%~107.2%,表明本法测量准确度较高。

表5 钾的加标回收试验结果

表6 钠的加标回收试验结果
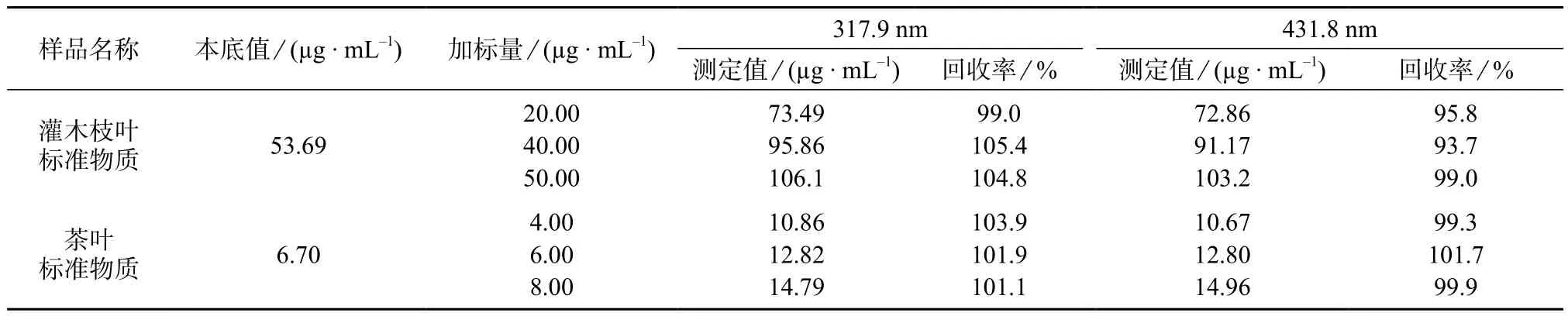
表7 钙的加标回收试验结果

表8 镁的加标回收试验结果
3 结语
用电感耦合等离子体原子发射光谱法测定灌木枝叶及茶叶标准物质中钾、钠、钙、镁的含量,测定结果均在标准值范围内,测量精密度良好,4种元素加标回收率较高,说明本方法准确、可靠,可满足植物中钾、钠、钙和镁含量的测定要求。
[1]南京农业大学.土壤农化分析[M]. 2版.北京:农业出版社,1992: 216.
[2]中国土壤学会农业化学专业委员会.土壤农业化学常规分析方法[M].北京:科学出版社,1989: 276–283.
[3]LY/T 1270–1999 森林植物与森林枯枝落叶层全硅、铁、铝、钙、镁、钾、钠、磷、硫、锰、铜、锌的测定[S].
[4]鲍士旦.土壤农化分析[M].北京:中国农业出版社,2005:270–275.
[5]张行峰.实用农化分析[M].北京:化学工业出版社,2005:196–200.
[6]牛家淑.示波极谱滴定法测定植物中钾含量的研究[J].植物学通报,1997(2): 56–58.
[7]NY/T 2017–2011 植物中氮、磷、钾的测定[S].
[8]张翠兰,梁伟.土壤、植物中钾、钠的原子吸收光谱测定[J].分析化学,1982(6): 382–383.
[9]张翠兰,董永涛.土壤、植物中铜、锌、铁、锰、钾、钠的原子吸收光谱测定[J].光谱学与光谱分析,1982(Z1): 86–87.
[10]LY/T 1271–1999 森林植物与森林枯枝落叶层全氮、磷、钾、钠、钙、镁的测定[S].
[11]张素纯,孙励敬,姜恒春,等.流动注射原子吸收法测定土壤、植物中的铜、锌、铁、锰、钠、钾、钙、镁[J].光谱学与光谱分析,1984(3): 42–47.
[12]魏复盛,齐文启.原子吸收光谱法及其在环境分析中的应用[M].北京:中国环境科学出版社,1988: 365–367.
[13]中国林业科学研究院分析中心.现代实用仪器分析方法[M].北京:中国林业出版社,1994: 14–16.
[14]王秀敏,谢令琴,刘艳苏,等.原子吸收光谱法测定小麦品种子粒中钾钠钙镁的含量[J].河北农业大学学报,2003(4): 90–92,97.
[15]李朝英,郑路.一种检测植物中钾、钙、镁含量的方法.CN104931437A[P]. 2015–09–23.
[16]董顺玲.原子吸收火焰法测定合用稀盐酸提取法测定植物的钙、镁、锌和锰力康粉剂中钾、钠、钙、镁、锌、铁的含量[J].中国药科大学学报,2003(6): 60–62.
[17]Sahrawal K L,王正银.用稀盐酸提取法测定植物的钙、镁、锌和锰[J].云南农业科技,1990(6): 43–45.
[18]王颖.苹果叶片中全量钙、镁的测定——EDTA钠盐滴定法[J].北方果树,1978(2): 13–15.
[19]曹德菊.原子吸收分光光度法测定茶叶中钙[J].茶业通报,1995(4): 7–8.
[20]丘星初.钙色素光度法测定植物中的钙[J].分析测试通报,1987(6): 67–68.
[21]叶润,刘芳竹,刘剑,等.微波消解–电感耦合等离子体发射光谱法测定大米中铜、锰、铁、锌、钙、镁、钾、钠8种元素[J].食品科学,2014(6): 117–120.
一种色谱仪用溶液杂质过滤装置获国家专利
由中国水产科学研究院黑龙江水产研究所孙言春等人申请的“一种色谱仪用溶液杂质过滤装置”获国家实用新型专利授权,专利号为ZL 2016 2 0734991.0。
本实用新型结构简单,可对进入色谱仪的溶液进行杂质过滤,防止有未溶化的颗粒进入色谱仪中堵塞管路,导致仪器故障停机,保证检测工作的顺利进行,满足高通量检测工作要求,进而提高工作效率。
( 林)
Determination of Potassium, Sodium, Calcium and Magnesium Content in Plant by Inductively Coupled Plasma Atomic Emission Spectrometry
Liu Zebin1, Liu Shouting2, Jiang Tiancheng2, Song Yecheng3, Wu Ting2, Huang Diangui2, Wang Youbing4, Wang Yuqing2, Deng Jie2
(1. Guangxi Station of Radiation Environment Supervision, Nanning 530222, China;2. Guangxi Center of Analysis and Test Research, Nanning 530022, China;3. Guangxi University of Chinese Medicine, Nanning 530001, China;4. Guangxi Guihong Environmental Monitoring Technology Limited Company, Nanning 530021, China)
The contents of potassium, sodium, calcium and magnesium in the sample solution were determined by ICP–AES with nitric acid and perchloric acid wet digestion or nitric acid and hydrogen peroxide microwave digestion.Certified reference materials of Shrubs and tea leaves were determined by this method, the measured values were within the allowable error of the standard value, and the relative standard deviations were 0.45%–4.05%(n=8). The recoveries of potassium, sodium, calcium and magnesium were 94.4%–107.6%, 92.6%–107.9%, 93.7%–105.4%, 92.9%–107.2%,respectively. The method is easy to operate, and it can meet the determination requirement of potassium, sodium, calcium and magnesium in plants with qualified precision and accuracy.
ICP–AES; plant; potassium; sodium; calcium; magnesium
O657.31
A
1008–6145(2017)05–0023–05
10.3969/j.issn.1008–6145.2017.05.006
*广西壮族自治区直属公益性科研院所基本科研业务费专项(2015ACZ10)
联系人:刘守廷;E-mail: Liushouting@163.com
2017–06–27

