芬顿氧化法对抗生素废水深度处理的实验研究*
福建省环境科学研究院 吴锡峰 杨 恺
芬顿氧化法对抗生素废水深度处理的实验研究*
福建省环境科学研究院 吴锡峰 杨 恺
研究了芬顿氧化法对抗生素废水SBR出水的深度处理效果,考察了pH值、H2O2投加量、FeSO4·7H2O投加量及H2O2和FeSO4·7H2O的投加比对废水中COD去除率的影响。结果表明:在pH值为3.0、0.6 g FeSO4·7H2O、1.4 mL H2O2,反应时间为3h、室温条件下,芬顿氧化法对抗生素废水SBR出水的COD去除率达77.8%,为今后难处理有机废水的深度处理提供了新思路。
抗生素废水 芬顿氧化法 深度处理
医药工业废水主要包括中药废水、化学制药废水、抗生素类废水制药废水[1],其中抗生素生产废水是一种成分复杂、色度高、生物毒性大、含多种抑制物质的难降解高浓度有机废水,含有残留着不同种类和浓度的抗生素及其中间代谢产物,以及较多的悬浮物、硫酸盐等污染物。目前,抗生素制药废水的处理工艺有物理法、好氧生物处理法、厌氧生物处理法、好氧—厌氧生物组合工艺[2]。由于抗生素废水的水质复杂特性,传统处理方法特别是生物法处理后,出水水质仍然含有较高的COD和色度,无法做到达标排放的问题。因此,寻求一种经济而有效的抗生素制药废水深度处理技术变得非常必要。
近年来,高级氧化技术在处理高浓度、难降解废水应用中取得了良好效果,而芬顿氧化法是一种高级氧化技术,是在pH值为2~5的环境体系中,利用H2O2被Fe2+催化产生了强氧化性的羟基自由基(·OH),可以氧化分解水中难降解的有机物,由此产生的Fe3+具有絮凝沉淀效果,协同去除水中有机污染物[3]。本研究以福兴抗生素制药厂SBR生化出水(SBR出水COD含量为254~298mg/L)为研究对象,考察了pH值、H2O2投加量、FeSO4投加量及H2O2和FeSO4的投加比对芬顿氧化法处理生化出水的影响,为芬顿氧化法在医药废水深度处理技术的应用研究提供参考。
1 实验部分
1.1 实验药品与仪器
1.1.1实验药品
H2SO4(AR,国药集团化学试剂有限公司);NaOH(AR,国药集团化学试剂有限公司);FeSO4·7H2O(AR,西陇化工股份有限公司);30% H2O2(AR,西陇科学股份有限公司)。
1.1.2实验仪器
六联电动搅拌器(HJ-6S型,金坛市友联仪器研究所);COD快速测定仪(5B-3A(V7)型,兰州连华环保科技有限公司);万分之一电子分析天平(BS224S型,赛多利斯);pH测定仪(PHBI-260型,上海仪电科学仪器股份有限公司)。
1.2 实验方法
1.2.1芬顿氧化原理
芬顿氧化反应体系复杂,关键是Fe2+与H2O2之间的链反应催化生成·OH自由基,·OH自由基的氧化能力仅次于氟,氧化电势高达2.80V。另外,·OH自由基具有很高的电负性,其电子亲和能力高达569.3 kJ,具有很强的加成反应特性,其反应机理为[4-5]:
Fe2++H2O2→Fe3++·OH+OH-
Fe3++H2O2→Fe2++·HO2+H+
Fe2++·OH→Fe3++OH-
Fe3++·HO2→Fe2++O2+H+
1.2.2芬顿氧化处理废水反应
取一定体积的抗生素制药废水SBR出水,调节pH值,加入一定量的FeSO4·7H2O和H2O2,在机械搅拌器上,机械搅拌。每个一段时间取样,滤纸过滤,滤液用COD快速测定仪测定其COD值。在同一反应条件下,考察不同影响因素对芬顿氧化法处理抗生素制药废水SBR出水中COD去除效果的影响。
2 结果与讨论
2.1 初始pH值的影响
在1.0 L水样、0.5g FeSO4·7H2O、1.5 mL H2O2、反应时间3h、室温条件下,考察初始pH值对芬顿氧化法处理废水中COD的影响,如图1所示。
由图1可知,抗生素废水中COD随着初始pH值升高而去除率相应增大。初始pH值在2.5~4.0范围内,芬顿氧化法对抗生素废水中COD具有良好的去除效果,反应时间在120 min时,去除率均超过62.7%。酸性条件下,溶液中Fe2+主要以Fe(OH)2+的形态存在,Fe(OH)2+在自然光照下容易产生·OH促进Fenton主反应的进行[6]。而当初始pH值低于2.0时,去除效果明显降低,但初始pH值分别为1.4和2.0时,反应时间在120 min时,COD去除率分别仅为21.4%和36.6%。因此,初始pH值对芬顿氧化过程影响显著。由反应方程式Fe2++H2O2→ Fe3++·OH+OH-可知,当pH值较低时,Fe2+容易被氧化成Fe3+,破坏了Fe2+和Fe3+之间的转换平衡,降低了催化剂的量和减少了·OH的产生量,进而影响了催化氧化反应的进行。然而,pH值过高也导致·OH转化成O-,失去·OH的强氧化能力[7, 8],而且,Fe2+也易生成氢氧化物沉淀而失去催化能力。芬顿氧化反应去除COD过程主要通过·OH自由基的强氧化性,·OH自由基越多越有利于去除COD。因此,芬顿氧化法的最佳pH值为3.00。
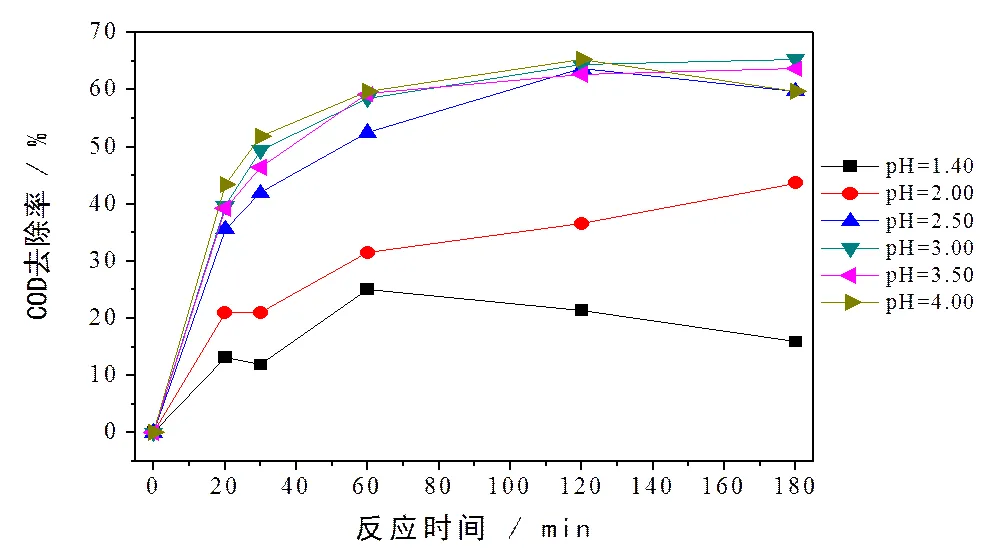
图1 初始pH值对芬顿氧化法处理废水中COD的影响
2.2 FeSO4·7H2O投加量的影响
在1.0 L水样、初始pH值为3.00、1.4 mL H2O2、反应时间3h、室温条件下,考察FeSO4·7H2O的投加量对芬顿氧化法处理废水中COD的影响,如图2所示。
由图2可知,废水中COD的去除率先随FeSO4·7H2O投加量的增加而增大,当反应时间超过90 min后,COD去除率差异不大。FeSO4·7H2O的投加量在0.3g、0.4g、0.5g、0.6g、0.7g、0.8g范围时,反应时间为10min,COD的去除率依次为22.7%、31.4%、35.7%、43.3%、49.8%和53.8%,此时,FeSO4·7H2O投加量对芬顿氧化法处理抗生素废水中COD去除效果的影响显著。随着反应时间的延长,COD的去除率不断升高,在120 min时,去除率均为70%左右。在H2O2投加量相同的条件下,反应体系产生的·OH自由基潜在总数是相同的,因而当反应处于平衡时的COD去除率几乎相同。徐琪琪等人[8]认为,在Fe2+浓度较低时,单位量H2O2产生的·OH随Fe2+浓度增加而增加,所产生的·OH全部参与有机物的氧化反应。因此,在此投加范围内,Fe2+初始浓度越大,所产生的·OH初始总量越大,初始芬顿氧化反应速率也更快,但随着反应继续进行,限制于H2O2的投加量相同,最终的COD去除率也基本相同。
2.3 H2O2投加量的影响
在1.0 L水样、初始pH值为3.00、0.5 g FeSO4·7H2O、反应时间3h、室温条件下,考察H2O2投加量对芬顿氧化法处理废水中COD的影响,如图3所示。
由图3可知,反应时间在0~30 min时,COD的去除率随着H2O2的投加量增加而降低。投加量为0.5 mL时,10min时的COD去除率达到了58%,而投加量为2.0 mL时,相应的COD去除率仅为16.2%。随着反应的进行,H2O2的投加量为0.5 mL时,20min时基本达到了反应平衡,COD的去除率达到了64%。而当投加量分别为0.50mL、0.80mL、1.10mL、1.40mL、1.70mL、2.00mL,反应时间为60min时,COD的去除率分别为66.8%、75.1%、71.8%、66.8%、64.6%和61.4%。较低浓度的H2O2和相同的Fe2+浓度体系中,Fe2+可充分地将H2O2催化生成·OH自由基,获得更高的初始·OH,因而表现出芬顿氧化反应过程的初始速率也更快,但因H2O2的低浓度限制,生成的·OH总数也更少,导致COD的最终去除率比高浓度的低。相同的Fe2+和H2O2投加量较少体系中,·OH的产生量随H2O2投加量的增加而增加,所产生的·OH几乎全部参与有机物的氧化反应[9]。而当H2O2投加量过大时,一开始便将Fe2+氧化成Fe3+,破坏了Fe2+和Fe3+的平衡反应,大大降低了Fe2+的总量[10],导致催化反应显著地降低,进而影响·OH自由基的产生量和COD去除率。范拴喜等人[11]发现,根据反应方程式·OH+H2O2→H2O+HO2,H2O2投加量过多,既消耗了H2O2的用量又抑制了·OH的产生。同时,H2O2具有较强的氧化性,但当它遇到氧化性更强的氧化剂时就会表现出还原性。残留的H2O2会部分增加芬顿氧化反应的出水中COD含量。例如,重铬酸钾是一种强氧化剂,在强酸性体系中,H2O2会被重铬酸钾氧化而表现出还原性[12]。
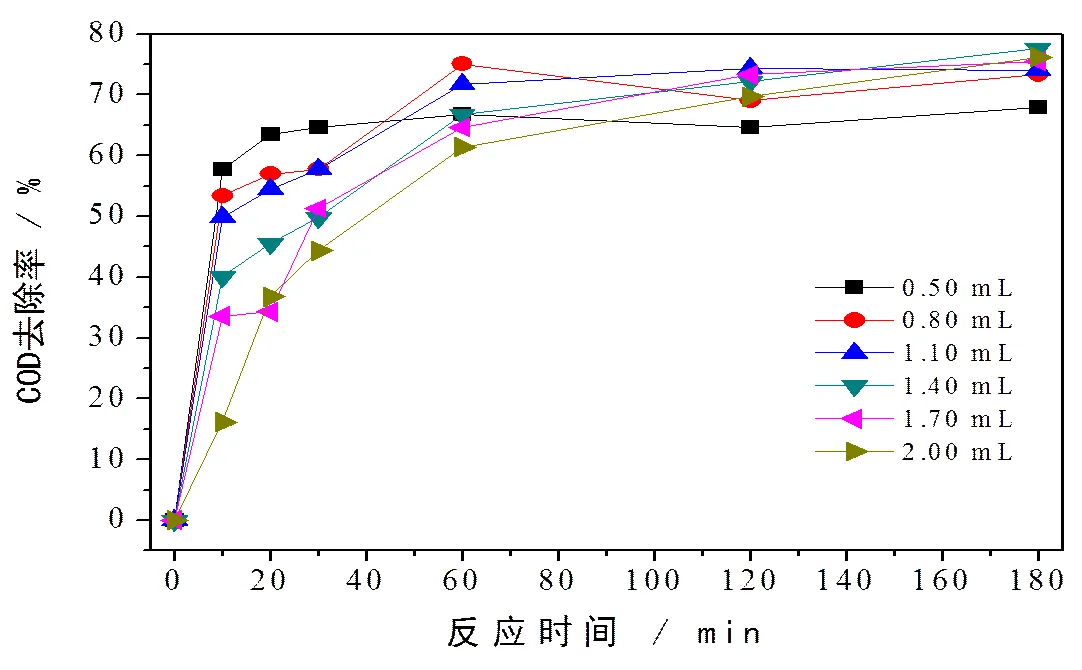
图3 H2O2投加量对芬顿氧化法处理废水中COD的影响
2.4 H2O2和FeSO4·7H2O之间的配比的影响
在1.0 L水样、初始pH值为3.00、反应时间3h、室温条件下,考察H2O2和FeSO4·7H2O之间的配比对芬顿氧化法处理废水中COD的影响,如表1所示。
由表1可以看出,H2O2和FeSO4·7H2O之间的配比对芬顿氧化法处理抗生素废水中COD的影响差异大,当添加1.40 mL H2O2和0.60 g FeSO4·7H2O,即摩尔比为6.35时,芬顿氧化法对抗生素废水中COD去除率最高,达到77.8%。

表1 H2O2和FeSO4·7H2O的配比对废水中COD去除率的影响
3 结论
(1)初始pH值和H2O2投加量对芬顿氧化法处理抗生素废水中COD的影响显著,而FeSO4·7H2O投加量的影响较低。
(2)相同浓度的Fe2+体系中,芬顿氧化法处理抗生素废水中COD的去除率随着H2O2投加量增大而初始反应速率呈反相关趋势,但COD的去除率与芬顿试剂的用量和反应时间有关。
(3)芬顿氧化法处理抗生素制药废水SBR出水的最佳实验条件为:1.0L水样、初始pH值为3.00、1.40 mL H2O2、0.6g FeSO4·7H2O、室温,在此条件下,COD去除率高达77.8%。
[1] 黄胜炎. 医药工业废水处理现状与发展[J]. 医药工程设计杂志,2005, 26(3): 41-50.
[2] 汤超. 论述抗生素废水处理工艺的运用[J]. 资源节约与环保, 2015(8): 55, 58.
[3] 江传春, 肖蓉蓉, 杨平. 高级氧化技术在水处理中的研究进展[J]. 水处理技术, 2011, 37(7): 12-15.
[4] 张玲玲, 李亚峰, 孙明, 等. Fenton氧化法处理废水的机理及应用[J]. 辽宁化工, 2004, 33(12): 734-737.
[5] 唐文伟,曾新平,胡中华.芬顿试剂和湿式过氧化氢氧化法处理乳化液废水研究[J].环境科学学报,2006,26(8):1265-1270.
[6] 吴彦瑜,郑可,陈东宇,等.Fenton试剂氧化降解腐殖酸动力学[J].环境科学,2010,31(9):2085-2091.
[7] 董蓓, 颜家保, 庄容, 等. Fenton试剂·OH生成率的影响因素研究[J]. 化学工程师, 2009, 3:14-16.
[8] 徐祺琪, 陈维芳, 沈晓慧, 等. Fenton高级氧化技术去除水中有机污染物2-MIB的影响因素研究[J]. 水资源与水工程学报, 2014, 23(2): 158-161.
[9] 高林霞, 皮科武, 万端极. Fenton试剂+SBR法处理纤维素废水的研究[J]. 环境科学与技术, 2011, 34(6): 82-84.
[10] 胡洁, 王乔, 周珉. 芬顿和臭氧氧化法深度处理化工废水的对比研究[J]. 四川环境, 2015, 34(4): 23-26.
[11] 范拴喜, 江元汝. Fenton法的研究现状与进展[J]. 现代化工, 2007, 27(1): 104-107.
[12] 姜科军, 唐啸天. 双氧水对废水化学需氧量测定的影响[J]. 石油化工环境保护, 2003, 26(1): 36-38.
福建省省属公益类科研院所基本科研专项(编号:2014R1004-2)。

