离子液体用于燃油萃取脱硫的选择与过程优化
方静,张淑婷,李婷婷,李春利
离子液体用于燃油萃取脱硫的选择与过程优化
方静,张淑婷,李婷婷,李春利
(河北工业大学化工学院,天津 300130)
针对基于COSMO-SAC模型分子设计方法的准确性问题,采用离子液体脱硫机理分析和实验的方法对其进行了验证,即对[HMIM][BF4]、[HMIM][PF6]、[BMIM][BF4]、[BMIM][PF6]、[EMIM][BF4]、[EMIM][PF6] 6种离子液体作萃取剂时的脱硫效果进行了脱硫机理的分析和实验的验证,得到的脱硫性能排序与离子液体分子设计结果基本一致,且均认为[HMIM][PF6]脱硫率较高。以[HMIM][PF6]为萃取剂,通过液相色谱法测定萃取后的液相组成,考察萃取时间、萃取温度、剂油比3个因素对脱硫率、分配系数和选择性系数的影响。通过正交实验设计确定了萃取时间40 min、萃取温度20℃、剂油比2:1为较优操作条件,单次脱硫率为72.74%,四级萃取可将模型油的含硫量由1200 μg·g−1降至6.98 μg·g−1,符合国Ⅴ标准。
离子液体;萃取;脱硫;模拟;正交实验
引 言
汽车尾气中含硫氧化物是城市空气的主要污染物之一。脱除燃油中的含硫化合物成为遏制汽车尾气污染大气的主要途径[1-4]。
萃取脱硫(extraction desulfurization,EDS)是利用硫化物在萃取剂与燃料油中溶解度不同而进行分离的脱硫工艺[5]。萃取脱硫的操作条件温和(低温、低压或常温、常压),脱硫后油品的性质不发生改变,不需要消耗氢气、氧化剂等额外的物质,设备简单,流程短,投资成本低。然而由于受到萃取剂性质的限制,该方法的脱硫效率较低,而且传统溶剂对环境的污染也较为严重[6-7]。因此,对于溶剂萃取脱硫工艺而言,开发一种高效、低污染的绿色溶剂是当前的研究重点。
离子液体作为一种绿色溶剂,对传统的加氢脱硫方法难以去除的噻吩类硫化物有较好的脱除效果,而且离子液体萃取脱硫可在室温下进行,操作简单,离子液体易于回收利用,克服了传统脱硫方法工艺复杂、设备投资大等缺点[8-11]。因此,离子液体萃取脱硫具有良好的工业应用前景[12]。
1995年Klamt[13]提出了COSMO-RS模型,即真实溶剂似导体屏蔽模型,该模型只需知道分子的结构信息,便可利用分子表面屏蔽电荷密度分布计算得到体系的物理化学性质,如饱和蒸气压和活度因子等[14-16]。其后Lin等[17-19]提出了与之类似的COSMO-SAC片段活度因子模型,通过引入Staverman-Guggenheim组合项克服了COSMO-RS在预测汽液平衡数据时不符合热力学一致性原理的缺点[20]。但基于COSMO-SAC模型的离子液体设计方法是一种估算方法,在计算无限稀释活度因子时存在一定误差[21]。
本文通过离子液体脱硫机理和实验的方法对基于COSMO-SAC模型的分子设计方法的准确性进行验证,并就[EMIM][BF4]、[EMIM][PF6]、[BMIM][BF4]、[BMIM][PF6]、[HMIM][BF4]、[HMIM][PF6] 6种离子液体中模拟萃取效果最好的[HMIM][PF6]作为萃取脱硫溶剂,对不同操作条件下脱除燃油中的含硫化合物的效果进行研究,旨在找出简单操作下能达到高脱硫率的最佳操作条件。
2 实验材料和方法
2.1 实验材料
苯并噻吩,纯度98%,天津希恩思生化科技有限公司;正辛烷,分析纯,天津福晨化学试剂厂;1-乙基-3-甲基咪唑四氟硼酸盐[EMIM][BF4],纯度99%,上海成捷化学有限公司;1-乙基-3-甲基咪唑六氟磷酸盐[EMIM][PF6],纯度99%,上海成捷化学有限公司;1-丁基-3-甲基咪唑四氟硼酸盐[BMIM][BF4],纯度99%,上海成捷化学有限公司;1-丁基-3-甲基咪唑六氟磷酸盐[BMIM][PF6],纯度99%,上海成捷化学有限公司;1-己基-3-甲基咪唑四氟硼酸盐[HMIM][BF4],纯度99%,上海成捷化学有限公司;1-己基-3-甲基咪唑六氟磷酸盐[HMIM][PF6],纯度99%,上海成捷化学有限公司。
选择苯并噻吩为含硫化合物,正辛烷为溶剂,配制模型油。在精确度为0.0001 g的电子天平上准确称取1.0000 g苯并噻吩,在250 ml的锥形瓶中加入198 g正辛烷,与苯并噻吩配制成含硫量1200 μg·g−1的模型油。
2.2 仪器设备和方法
集热式恒温加热磁力搅拌器,DF-101S型,上海翔雅仪器设备有限公司;高效液相色谱,SPD-M20A型,日本岛津公司;旋转蒸发器,RE-5299型,天津科诺仪器设备有限公司;电子天平,TC328A型,上海天平仪器厂。
实验中苯并噻吩和离子液体的测定采用液相色谱法。分别配置苯并噻吩含量为1、2、3、4、5 mg·L−1,[HMIM][PF6]含量为400、600、720、800、980 mg·L−1的标准溶液,在流动相90%甲醇、10%水,流速1 ml·min−1下进样分析,以峰面积为纵坐标,各物质质量浓度(mg·L−1)为横坐标,通过线性回归,分别得到苯并噻吩和[HMIM][PF6]的线性回归方程为
= 46088.7− 2705.9(= 0.99993)
= 12976.1+ 2.4(= 0.99912)
利用所得回归方程,即可将检测结果中的峰面积转化为苯并噻吩和[HMIM][PF6]的浓度。
常压下,在50 ml的锥形瓶中加入含硫量为1200 μg·g−1的模型油和离子液体,一定温度下密闭磁力搅拌,萃取平衡后室温下静置,待模型油与离子液体萃取剂清晰分层。用注射器抽取0.1 ml上、下层溶液并称重,再分别稀释至50、100倍,即可用液相色谱仪检测稀释后苯并噻吩、离子液体的含量A和S,正辛烷含量B=−50A−100S。由此可得上下层溶液三相组成。
实验中离子液体在正辛烷中的溶解度同样采用液相色谱法测定。配制25℃下离子液体-正辛烷饱和溶液,取0.1 ml并称重,稀释至100倍用液相色谱仪检测稀释后离子液体的含量S,正辛烷含量B=−100S,25℃下离子液体在正辛烷中的溶解度为P=100SB。
3 结果与讨论
3.1 基于COSMO-SAC模型分子设计方法的准确性验证
3.1.1 COSMO-SAC模型[20]及分子设计 Lin等[17]在2002年提出COSMO-SAC活度系数模型,认为混合物中组分的活度系数可以分解为两个部分,即表面电荷片段对活度系数的贡献和分子形状大小差异对活度系数的贡献。前者采用与COSMO-RS模型类似的片段活度系数计算方法表示,后者则采用Staverman-Guggenheim组合项来表示,即

式中,γ/S、分别为组分在混合物中的活度系数和Staverman-Guggenheim组合项活度系数;n为混合物中组分的物质的量;p()为组分的表面电荷密度分布函数,即-Profile,该模型中纯物质的-Profile取自文献[22];s()、Г()分别为混合物和纯物质中表面电荷密度等于的片段对活度系数的贡献值大小,均可按式(2)计算
(2)
式中,下标S/表示混合物S或组分;Δ(σ,σ)为交换能,即从中性对中得到(σ,σ)荷电对所需的能量;为气体常数;为体系温度。
混合物中的表面电荷密度分布函数S()为所有纯组分P()的加权和,即

式中,x为混合物中组分的摩尔分数;A为组分中所有表面电荷的空穴表面积。
Staverman-Guggenheim组合项活度系数则由式(4)计算

式中,为配位数,通常取值为10;θ和φ分别为组分的表面积分数和体积分数
(5)
式中,r和分别为组分的量纲1分子体积和表面积,可以通过COSMO计算得到。l按式(6)计算
l=(/2)[(r-q)(r-1)] (6)
用COSMO-SAC模型对[EMIM][BF4]、[EMIM][PF6]、[BMIM][BF4]、[BMIM][PF6]、[HMIM][BF4]、[HMIM][PF6] 6种离子液体在30℃下进行量子化学计算,得到其无限稀释活度因子。选取分配系数A、选择性系数、溶解度P作为萃取剂的性能指标[23],计算公式如式(7)~式(9)所示

(8)
(9)
式中,∞A,B为组分A在组分B中的无限稀释活度因子;∞A,S为组分A在萃取剂S中的无限稀释活度因子;∞B,S为组分B在萃取剂S中的无限稀释活度因子。
分配系数A表示萃取达到平衡时,组分A在萃取剂S和组分B中的比值,比值越大,萃取能力越强;选择性系数越大,萃取剂对两组分的分离效果越好;溶解度P表示组分A在萃取剂S中的溶解能力,溶解度越大,分离效果也越好。
根据王秀丽等[24]提出的模糊综合评判方法,对6种离子液体的脱硫性能进行评价和排序。设萃取剂评判因素集= {A,,P},对中所有因素均设评语集= {优}。萃取剂的模糊综合评判公式为== {1,2,…,},其中为权重分配集,反映的是各因素的权重,这里考虑到选择性系数、分配系数和溶解度的重要性基本相同,因此令= [1/3, 1/3, 1/3][21];为综合评判因子;为模糊转换矩阵
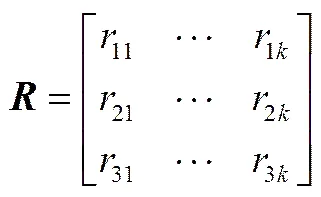
是第个被评判对象中第个元素对的隶属度。这里规定隶属函数如式(11)~式(13)所示
(11)
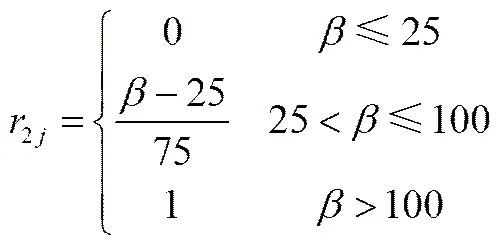
(13)
基于COSMO-SAC模型的分子设计结果见表1,从6种离子液体的综合评判因子大小可以看出,离子脱硫性能顺序为:[HMIM]+> [BMIM]+> [EMIM]+,PF6−> BF4−,且离子液体中综合性能较好的为[HMIM][PF6]。6种离子液体结构如图1所示。
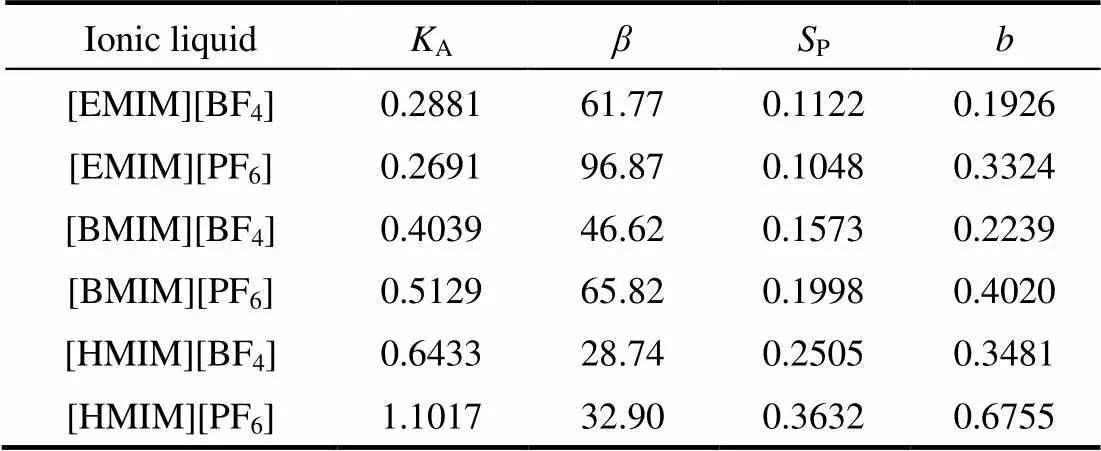
表1 离子液体作为萃取脱硫剂的分子设计结果
3.1.2 离子液体脱硫机理验证 Zhang等[25]采用NMR光谱研究了噻吩在离子液体中的吸附作用,结果表明离子液体在溶解噻吩分子过程中进行重新组装,这种重新组装的能力主要取决于噻吩和离子液体中阳离子的相互作用,这主要归因于咪唑阳离子与噻吩分子的芳香环间的电流作用[26]。
由Mochizuki等[27]、Nie等[28]的研究可知,在阴离子相同的情况下,随着阳离子上烷基链取代基中碳原子个数的增加,离子液体脱硫能力增强。这是因为,一方面随着阳离子上烷基链取代基的增长,离子液体分子结构增大,阴阳离子之间的库仑作用减弱,有利于噻吩分子插入离子液体的动态分子结构中,形成液相包合物,促进萃取过程的进行;另一方面,咪唑环的对称性越差,阳离子极化性就越强,与噻吩类硫化物的络合作用就越强,并且烷基是给电子基,可以增强硫原子与咪唑环的π-π作用[29]。所以阳离子脱硫效果顺序为:[HMIM]+> [BMIM]+> [EMIM]+。
Mochizuki等[27]、胡松青等[30]也发现,在阳离子相同的情况下,阴离子体积增大也会使脱硫率增大。对此的解释是,硫化物在离子液体中的溶解度受空间效应的影响,阴离子体积增大使得阳离子不会靠得很近,离子液体与芳香环间的电流作用降低,“堆垛”结构没有那么紧密了,可插入的硫化物分子数增多,脱硫率提高[31]。所以,阴离子脱硫效果顺序为PF6−> BF4−。
由此可见,离子液体的结构影响其萃取脱硫效果,在一定限度内增大阴阳离子的体积有助于提高脱硫率[31]。所以从脱硫机理来看,脱硫性能排序为[HMIM]+> [BMIM]+> [EMIM]+,PF6−> BF4−。且6种离子液体中,[HMIM][PF6]的脱硫性能最好,这与基于COSMO-SAC模型的分子设计结果保持一致,证明基于COSMO-SAC模型的离子液体设计方法是有效的。但是需要注意的是,由于COSMO-SAC模型是一种估算方法,在计算无限稀释活度因子时存在一定误差,因此该萃取剂分子设计方法是一种初步选择方法,萃取剂的综合性能仍需要实验进行验证[21]。
3.1.3 脱硫实验验证 在锥形瓶中分别加入等物质的量的离子液体和一定量的模型油,在30℃下密闭磁力搅拌进行脱硫实验,萃取达到平衡后室温下静置。用液相色谱检测反应前后模型油相中的硫含量,考察脱硫率(由于[EMIM][PF6]常温下呈固态,其萃取温度设为50℃)。6种离子液体的脱硫率数据见表2。
从表2中6种离子液体的脱硫率大小可以看出,其脱硫性能排序与基于COSMO-SAC模型的分子设计结果基本一致,均认为[HMIM]+> [BMIM]+> [EMIM]+,PF6−> BF4−,且[HMIM][PF6]的脱硫效果最好。
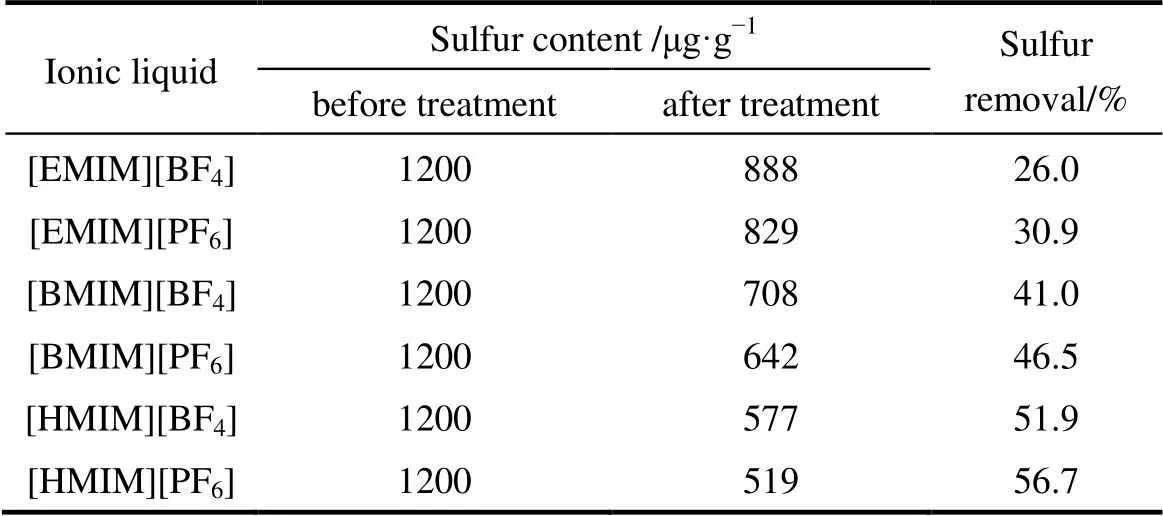
表2 6种离子液体单次脱硫率
综上所述,通过离子液体脱硫机理和实验两种方法对基于COSMO-SAC模型分子设计方法的准确性进行验证,证明基于COSMO-SAC模型分子设计方法具有一定的准确性。
6种离子液体在正辛烷中的溶解度数据见表3。从表中可以看出,6种离子液体在正辛烷中的溶解度都非常小,虽然[HMIM][PF6]在正辛烷中的溶解度较其他5种离子液体略大,但这并不影响分离过程中对萃取剂溶解度的要求。
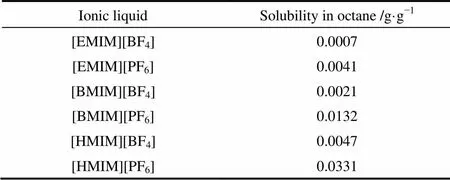
表3 298.15 K离子液体在正辛烷中的溶解度
下面将采用分子设计方法得出的综合评判因子最高的[HMIM][PF6]离子液体作为萃取剂,对脱除模型油中的苯并噻吩过程进行优化。
3.2 [HMIM][PF6]脱硫的过程优化
3.2.1 萃取温度对脱硫效果的影响 以质量比1:1加入一定量的[HMIM][PF6]和模型油,在不同温度下密封搅拌30 min后,室温下静置,测定上下层中的三相组成。分析萃取温度对脱硫效果的影响,实验结果见表4。

表4 温度对萃取效果的影响
从表4可以看出,从20℃到60℃,随着温度的升高,离子液体脱硫率逐渐降低,这是因为随着温度的升高,两相间互溶度增大,不利于萃取过程的进行,且高温条件会造成油品收率的降低。
3.2.2 萃取时间对脱硫效果的影响 以质量比1:1分别加入一定量的模型油和离子液体,在30℃下密封磁力搅拌10、20、30、40、50、60 min后,室温下静置,测定上下层中的三相组成,分析随萃取时间变化,脱硫率、分配系数及选择性系数的变化。实验结果见表5。
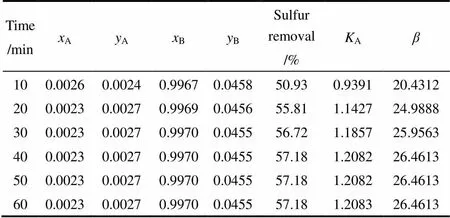
表5 萃取时间对萃取效果的影响
从表5可以看出,从10 min到40 min,随着时间的延长,脱硫率逐渐增加,40 min时脱硫率达到最大值,萃取40 min后脱硫率不再变化。这是因为随着时间的延长,含硫化合物不断地从油品中萃取到离子液体中,导致离子液体中的含硫化合物逐渐趋于饱和,达到萃取平衡,从而使得脱硫率不再变化。因此,萃取时间选择40 min为较优萃取时间。
3.2.3 剂油比对脱硫效果的影响 分别以质量比4:1、2:1、1:1、1:2加入一定量的模型油和离子液体,在30℃下密闭磁力搅拌30 min后室温下静置,测定上下层中的三相组成,分析随剂油比的变化,脱硫率、分配系数及选择性系数的变化。实验结果见表6。

表6 剂油比对脱硫率和萃取效果的影响
由表6可知,随着离子液体与模型油质量比的增大,离子液体脱硫率逐渐增大,这是因为随着萃取剂用量的增加,苯并噻吩的溶解的量增大,脱硫率升高,因此增加萃取剂用量有利于脱硫率的提高。
3.2.4 萃取级数对脱硫效果的影响 以质量比1:2加入一定量的模型油和离子液体,在30℃下密闭磁力搅拌30 min,结束后室温静置,待清晰分层后,测定其中的含硫量,再对其重复多次萃取,分析随萃取次数增加,脱硫效果的变化。模型油中含硫量和脱硫率随萃取级数的变化如图2所示。
由图2可看出随着萃取级数的增加,脱硫率显著增大,一级萃取脱硫率为70.72%,含硫量降至351.36 μg·g−1,经过四级萃取之后,脱硫率达到99.27%,模型油含硫量降至8.87 μg·g−1,符合国Ⅴ标准。因此,离子液体可用于燃油深度脱硫,并具有较好的效果。
3.2.5 离子液体的回收利用 将脱硫后的离子液体置于在旋转蒸发仪中,90℃下抽真空(真空度0.1 MPa)蒸馏60 min,得到回收离子液体。用回收的离子液体进行萃取实验,测定回收离子液体的脱硫效果,如图3所示。
由图3可以看出回收离子液体的脱硫效果并无很大的变化,重复使用4次脱硫率仍可达到51.89%。虽然离子液体价格略高,但其重复使用性提高了其综合利用价值,这也使得离子液体优于其他脱硫溶剂。值得注意的是,在本实验中,虽然多级萃取能够将大部分硫脱除,但同时会造成一小部分模型油的损失,因此,如何在深度脱硫的同时保证燃油的收率值得继续研究。
3.3 正交实验设计
通过正交试验来优化萃取脱硫条件,设计三因素三水平的正交试验,以脱硫率为考察指标,正交实验因素和水平见表7,实验及优化结果见表8。

表7 正交实验影响因素和水平
由表8可以看出,各因素对脱硫率的影响顺序为:C(剂油比) > A(萃取温度) > B(搅拌时间),较优操作条件为A1B3C1,而该操作条件并未出现在表8的9次试验中,按照得出的较优方案进行实验验证,在剂油比为2:1,萃取温度20℃,密闭搅拌40 min条件下,得到该条件下离子液体单次脱硫率为72.74%。经过四级脱硫实验之后,模型油含硫量降至6.98 μg·g−1,符合国Ⅴ标准。
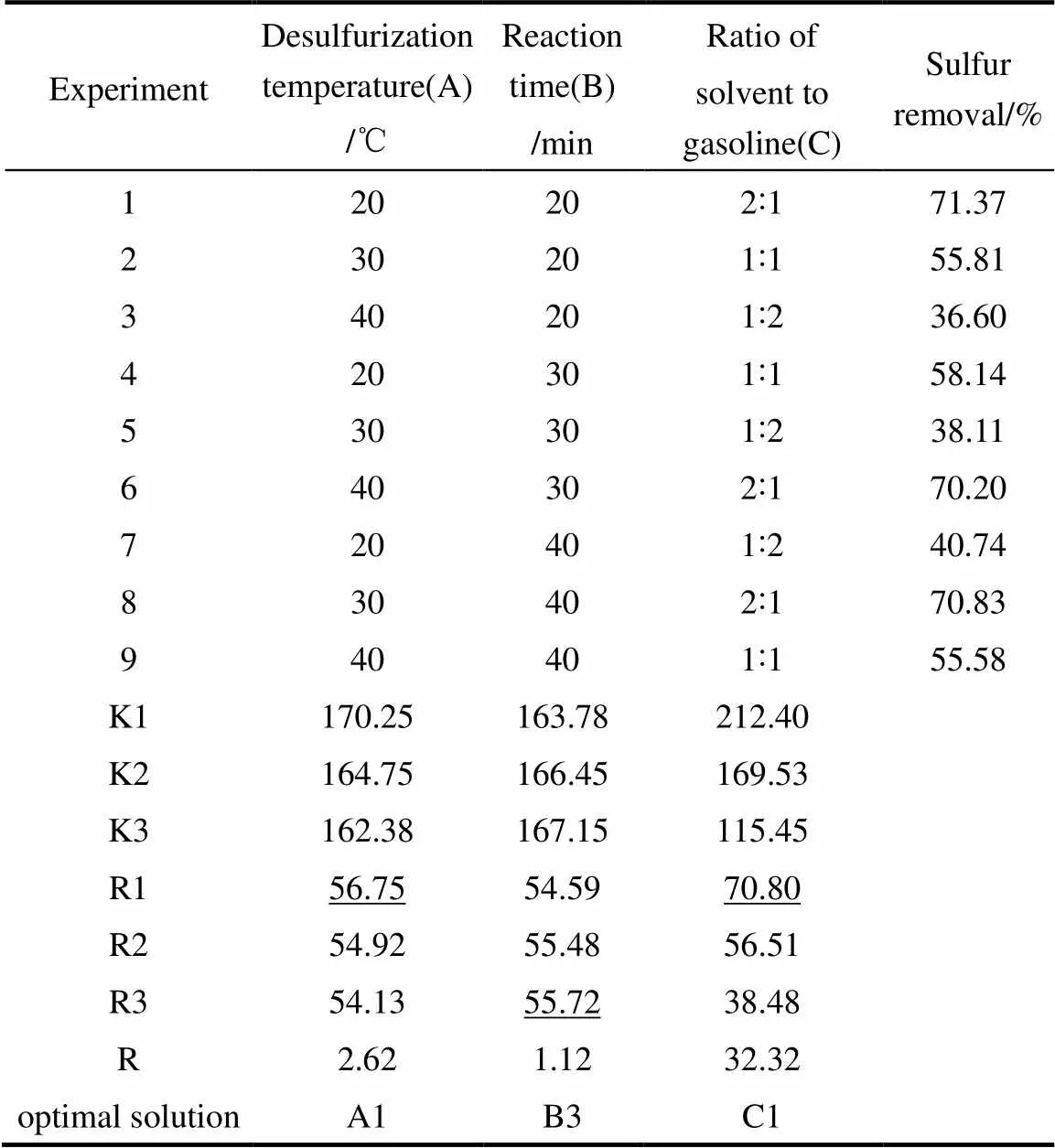
表8 正交实验结果及分析
4 结 论
(1)通过离子液体脱硫机理和实验两种方法,对基于COSMO-SAC模型分子设计方法的准确性进行验证,即:对[HMIM][BF4]、[HMIM][PF6]、[BMIM][BF4]、[BMIM][PF6]、[EMIM][BF4]、[EMIM][PF6] 6种离子液体作萃取剂时的脱硫效果进行了脱硫机理的分析和实验的验证,得到的离子液体脱硫效果排序都与基于COSMO-SAC模型的分子设计结果基本一致,证明该分子设计方法具有一定的准确性。
(2)[HMIM][PF6]作为萃取脱硫剂,通过液相色谱法测定了萃取脱硫后的液相组成,同时考察了萃取温度、萃取时间、剂油比3个因素对脱硫率、分配系数及选择性系数的影响。
(3)通过正交试验设计确定了萃取温度20℃、萃取时间40 min、剂油比2:1为较优操作条件,得到该条件下离子液体单次脱硫率为72.74%,四级脱硫可将模型油中的含硫量由1200 μg·g−1降至6.98 μg·g−1,符合国Ⅴ标准。
符 号 说 明

A——分子表面积,nm2 b——模糊综合评判因子 F——随机变量 f——自由度 K——分配系数 m——质量,g n——物质的量,mol P(σ)——表面电荷密度分布函数 q——表面积参数 R——气体常数,J·mol-1·K-1 r——体积参数 SP——溶解度,g·g−1 T——体系温度,K ΔW——交换能,J x——萃余相中组分的质量分数 xi——组分i的摩尔分数 y——萃取相中组分的质量分数 z——配位数 β ——选择性系数 Г(σ)——表面电荷密度为σ的片段活度系数 γ——活度系数 θ——表面积分数 σ——屏蔽电荷密度,e·nm−2 φ——体积分数 上角标 SG——Staverman-Guggenheim组合项 ∞——无限稀释 下角标 A——苯并噻吩 B——正辛烷 i——组分i S——萃取剂
References
[1] 崔文广, 周二鹏, 赵地顺, 等. 催化裂化汽油脱硫技术研究进展[J]. 河北工业科技, 2004, 21(2): 1-4+12. CUI W G, ZHOU E P, ZHAO D S,. Technology progress of desulfurization of FCC gasoline[J]. Hebei Journal of Industral Science & Technology, 2004, 21(2): 1-4+12.
[2] 庞新梅, 孙书红, 高雄厚. 生产低硫汽油新型FCC催化剂研究进展[J]. 石化技术与应用, 2001, 19(6): 384-388+397-350. PANG X M, SUN S H, GAO X H. New FCC catalysts for gasoline desulfurization[J]. Petrochemical Technology & Application, 2001, 19(6): 384-388+397-350.
[3] 王军民, 袁铁. 超低硫清洁汽油的生产技术进展[J]. 天然气与石油, 2001, 19(4): 14-17+1. WANG J M, YUAN T. Research progress in technology for super low sulfur gasoline production[J]. Natural Gas and Oil, 2001, 19(4): 14-17+1.
[4] 王鹏, 傅军, 何鸣元. 含噻吩烷烃在分子筛上裂化脱硫的研究[J]. 石油炼制与化工, 2000, 31(3): 58-62. WANG P, FU J, HE M Y. Cracking-desulfurization of thiophene contained paraffin over zeolites[J]. Petroleum Processing and Petrochemicals, 2000, 31(3): 58-62.
[5] 寇晓撒, 史丽娟. 汽油萃取脱硫技术进展[J]. 广州化工, 2013, 41(3): 30-31. KOU X S, SHI L J. The progress of gasoline extraction desulfurization technology[J]. Guangzhou Chemical Industry, 2013, 41(3): 30-31.
[6] 曾丹林, 胡义, 王可苗, 等. 燃料油萃取脱硫技术研究进展[J]. 石油炼制与化工, 2012, 43(5): 98-102. ZENG D L, HU Y, WANG K M,. Research advance in desulfurization of transportation fuels by extraction process[J]. Petroleum Processing and Petrochemicals, 2012, 43(5): 98-102.
[7] 张伟伟, 侯侠. 汽油萃取脱硫技术的应用研究与进展[J]. 兰州石化职业技术学院学报, 2015, 15(4): 5-9. ZHANG W W, HOU X. Progress on research and application of gasoline extraction desulphurization technology[J]. Journal of Lanzhou Petrochemical College of Technology, 2015, 15(4): 5-9.
[8] SWATLOSKI R P, HOLBREY J D, ROGERS R D. Ionic liquids are not always green: hydrolysis of 1-butyl-3-methylimidazolium hexafluorophosphate[J]. Green Chemistry, 2003, 5(4): 361-363.
[9] WASSERSCHEID P, HAL R V, BÖSMANN A. 1--Butyl-3 -methylimidazolium ([BMIM]) octylsulfate — an even ‘greener’ ionic liquid[J]. Green Chemistry, 2002, 4(4): 400-404.
[10] 周瀚成, 陈楠, 石峰, 等. 离子液体萃取脱硫新工艺研究[J]. 分子催化, 2005, 19(2): 94-97. ZHOU H C, CHEN N, SHI F,. Studies on desulfurization of gasoline by extracting with ionic liquids[J]. Journal of Molecular Catalysis (China), 2005, 19(2): 94-97.
[11] 冯婕, 李春喜, 孟洪, 等. 磷酸酯类离子液体在燃油深度脱硫中的应用[J]. 石油化工, 2006, 35(3): 272-276. FENG J, LI C X, MENG H,. Application of phosphate ionic liquids in deep desulfurization of fuel[J]. Petrochemical Technology, 2006, 35(3): 272-276.
[12] 王坤, 刘大凡, 何爱珍, 等. 离子液体萃取脱硫的研究[J]. 石油化工, 2010, 36(6): 675-680. WANG K, LIU D F, HE A Z,. Extractive desulfurization of simulative oil with ionic liquids[J]. Petrochemical Technology, 2010, 36(6): 675-680.
[13] KLAMT A. Conductor-like screening model for real solvents: a new approach to the quantitative calculation of solvation phenomena[J]. Journal of Physical Chemistry, 1995, 99(7): 2224-2235.
[14] KLAMT A, VOLKER J, THORSTEN A B,. Refinement and parametrization of COSMO-RS[J]. Journal of Physical Chemistry A, 1998, 102(26): 5074-5085.
[15] KLAMT A, ECKERT F. COSMO-RS: a novel and efficient method for the a priori prediction of thermophysical data of liquids[J]. Fluid Phase Equilibria, 2000, 172(172): 43-72.
[16] KLAMT A, KROOSHOF G J P, TAYLOR R. COSMOSPACE: alternative to conventional activity-coefficient models[J]. AIChE Journal, 2002, 48(10): 2332-2349.
[17] LIN S T, SANDLER S I. A priori phase equilibrium prediction from a segment contribution solvation model[J]. Industrial & Engineering Chemistry Research, 2002, 41(5): 899-913.
[18] LIN S T, CHANG J, WANG S,. Prediction of vapor pressures and enthalpies of vaporization using a COSMO solvation mode[J]. Journal of Physical Chemistry A, 2004, 108(36): 7429-7439.
[19] HSIEH C M, SANDLER S I, LIN S T. Improvements of COSMO-SAC for vapor-liquid and liquid-liquid equilibrium predictions[J]. Fluid Phase Equilibria, 2010, 297(1): 90-97.
[20] 吴选军, 余永富, 袁继祖. COSMO结合状态方程预测汽液平衡及可视化[J]. 武汉理工大学学报(信息与管理工程版), 2011, 33(3): 354-358. WU X J, YU Y F, YUAN J Z. Prediction and visualization of vapor -liquid equilibria based on COSMO model and state equation[J]. Journal of WUT (Information & Management Engineering), 2011, 33(3): 354-358.
[21] 李瑞, 崔现宝, 吴添, 等. 基于COSMO-SAC模型的离子液体萃取剂的选择[J]. 化工学报, 2013, 64(2): 452-469.LI R, CUI X B, WU T,. Selection of ionic liquid solvent for liquid-liquid extraction based on COSMO-SAC model[J]. CIESC Journal, 2013, 64(2): 452-469.
[22] MULLINS E, OLDLAND R, LIU Y A,. Sigma-profile database for using COSMO-based thermodynamic methods[J]. Industrial & Engineering Chemistry Research, 2006, 45(12): 4389-4415.
[23] PRETEL E J, LOPEZ P A, BOTTINI S B,. Computer-aided molecular design of solvents for separation process[J]. AIChE Journal, 1994, 48(8): 1349-1360.
[24] 王秀丽, 孙伟, 宋海华. 萃取精馏溶剂的模糊综合评判[J]. 天津大学学报, 2003, 36(4): 478-481.WANG X L, SUN W, SONG H H. Fuzzy comprehensive judgement on extractive distillation solvents[J]. Journal of Tianjin University, 2003, 36(4): 478-481.
[25] ZHANG S G, ZHANG Z C. Novel properties ofionic liquids in selective sulfur removal from fuels atroom temperature[J]. Green Chemistry, 2002, 4(4): 376-379.
[26] SU B M, ZHANG S G, ZHANG Z C. Structuralelucidation of thiophene interaction with ionic liquidsby multinuclear NMR spectroscopy[J]. Journal ofPhysical Chemistry B, 2004, 108(50): 19510-19517.
[27] MOCHIZUKI Y, SUGAWARA K. Removal of organic sulfur fromhydrocarbon resources using ionic liquids[J]. Energy & Fuels, 2008, 22(5): 3303-3307.
[28] NIE Y, LI C X, HONG M,.,-Dialkylimidazoliumdialkylphosphate ionic liquids: their extractive performance forthiophene series compounds from fuel oils versus the length of alkylgroup[J]. Full Processing Technology, 2008, 89(10): 978-983.
[29] 黄廷昌, 苑建. 离子液体应用于燃油脱硫技术的研究进展[J]. 河北化工, 2011, 34(5): 44-47+67.HUANG T C, YUAN J. Development on desulfurization of fuel oil by ionic liquids[J]. Hebei Huagong, 2011, 34(5): 44-47+67.
[30] 胡松青, 张军, 刘冰, 等. 离子液体萃取脱硫的探索性研究[J]. 石油学报(石油加工), 2007, 23(1): 100-103. HU Q S, ZHANG J, LIU B,. Feasibility study of extraction desulfurization with ionic liquids[J]. ACTA Petroleisinica (Petroleum Processing Section), 2007, 23(1): 100-103.
[31] 林燕, 王芳, 张志庆, 等. 离子液体绿色脱硫机理及应用进展[J]. 化工进展, 2013, 32(3): 549-557. LIN Y, WANG F, ZHANG Z Q,. Mechanism and application of ionic liquids in environmental friendly oil desulphurization[J]. Chemical Industry and Engineering Progress, 2013, 32(3): 549-557.
Selection and process optimization of ionic liquids for desulfurization
FANG Jing, ZHANG Shuting, LI Tingting, LI Chunli
(School of Chemical Engineering, Hebei University of Technology, Tianjin 300130, China)
To verify the reliability of ionic liquids’ molecular design method based on COSMO-SAC model, ionic liquids desulfurization mechanism analysis and experimental results are compared with COSMO simulation.By analyzing [HMIM][BF4], [HMIM][PF6], [BMIM][BF4], [BMIM][PF6], [EMIM][BF4] and [EMIM][PF6] on mechanism level, [HMIM][PF6] was considered as a better extractive desulfurization agent than others, and the order of desulfurization efficiency was consistent with the calculation results from COSMO-SAC model. The experimental result shows that the difference between the COSMO simulation and experiments is not significant. In this study, [HMIM][PF6] was used as an extractive desulfurization agent to remove benzothiophene from fuels, and the change of sulfur content in model oil was determined by liquid chromatography. Through considering the effect of extraction temperature, time and the ratio of solvent to oil, the optimal operating conditions, 20℃, 40 min and 2:1 respectively, were determined in orthogonal experiment with an efficiency over 72.74%. With [HMIM][PF6] used as the deep extraction desulfurization solvent, the sulfur content decreased from 1200 μg·g−1to 6.98 μg·g−1by 4-stages extraction, which met the Phase Ⅴ Emission Standards in China.
ionic liquids; extraction; desulfurization; simulation; orthogonal experiment
10.11949/j.issn.0438-1157.20170182
TQ 028.3
A
0438—1157(2017)09—3434—08
2017-02-24收到初稿,2017-05-31收到修改稿。
李春利。
方静(1977—),女,博士,教授。
教育部博士点基金项目(20131317120014)。
2017-02-24.
Prof. LI Chunli, ctstfj@163.com
supported by the Ph.D Program Foundation of Ministry of Education of China (20131317120014).

