Cd2+在改性橙皮上的吸附及其动力学
杨为森,简绍菊,林维晟
(1.福建省生态产业绿色技术重点实验室, 福建 武夷山 354300;2.福建省竹材工程技术研究中心, 福建 武夷山 354300;3.武夷学院 生态与资源工程学院, 福建 武夷山 354300)
Cd2+在改性橙皮上的吸附及其动力学
杨为森1,2,3,简绍菊1,2,3,林维晟1,2,3
(1.福建省生态产业绿色技术重点实验室, 福建 武夷山 354300;2.福建省竹材工程技术研究中心, 福建 武夷山 354300;3.武夷学院 生态与资源工程学院, 福建 武夷山 354300)
以橙皮为基体,经环氧氯丙烷和氢氧化钠改性处理制备橙皮生物质吸附剂,用红外光谱及SEM对改性橙皮结构及形貌进行表征,研究了改性橙皮对Cd2+溶液的吸附性能,考察了Cd2+溶液的pH值、初始浓度、吸附时间和吸附剂用量等对吸附效果的影响。结果表明:当Cd2+溶液初始浓度为100 mg/L、pH=6、吸附时间为60 min、投加量为0.2 g时,在室温条件下,改性橙皮对Cd2+的去除率和吸附容量分别为90%和11.03 mg/g;改性橙皮对Cd2+的等温吸附平衡符合Langmuir模型,以单层化学吸附为主;对Cd2+的吸附动力学符合准二级动力学方程。
橙皮;生物质吸附剂;Cd2+溶液;环氧氯丙烷;动力学
Abstract: Orange peel was modified by epichlorohydrin and sodium hydroxide to obtain an orange peel absorbent. The morphology and structure of modified orange peel were characterized by FTIR and SEM, and the absorption of modified orange peel on Cd2+solution was studied. The effects of initial pH, initial concentration, absorbent dosage and reaction time on the adsorption efficiencies of Cd2+were investigated. The result showed that the adsorption of Cd2+was the best when the initial pH was 6, initial concentration was 100 mg/L, absorbent dosage was 0.2g and reaction time was 60 min in room temperature, the decolorization rate and absorption capacity of Cd2+were about 90% and 11.03 mg/g respectively. The experimental isotherm data fits well in the Langmuir equations, indicating monolayer chemical adsorption on the absorbent. The adsorption process can be well described by the pseudo-second-order kinetic equation.
Keywords: orange peel; biological adsorbent; Cd2+solution; epichlorohydrin; kinetics
随着国民经济和现代工业的飞速发展,重金属污染日益严重。重金属因毒性和致癌性较强且不能被生物降解,可通过食物链在生物体内富集,从而给人体的生命健康带来了巨大的危害。对重金属污染的治理已成为当今国际世界亟待解决的问题之一。镉是一种毒性很大的重金属,在电镀、电子、冶金和电池等领域应用广泛。镉可以通过食物、水、被污染的空气经消化道或呼吸道进入人体,富集在肾脏和肝脏中,使蛋白质变性,对肾脏和肝脏造成损害。长期摄入镉会阻碍人体对钙的吸收,从而导致骨质疏松、脆化和脊柱畸形等。目前处理重金属废水的方法主要有化学法、物理化学法和生物吸附法等[1-2]。生物吸附法是一种新兴的处理重金属废水的方法[3],具有价格低廉、吸附速率快、去除效率高、原料丰富、操作简单以及不产生二次污染且易再生的优点[4]。近年来,国内外学者已经研究并发展了利用农林废弃物如秸秆[5]、茶渣[6]、花生壳[7]、甘草渣[3]、柿子粉[8]、小麦壳[9]、橙皮渣[10]、甘蔗渣[11]及豆渣[12]等来治理重金属离子废水的方法。
我国盛产脐橙,脐橙被食用后,其橙皮作为废料被填埋或焚烧,这使得脐橙的资源利用率低且易造成环境污染。橙皮主要由富含羟基和羧基等官能团的纤维素、半纤维素、木质素和果胶等化合物组成,并且疏松多孔,是一种良好的生物吸附材料,在重金属废水处理领域具有广阔的应用前景。但未经处理的橙皮存在吸附容量较低,对重金属废水的处理效率不高等缺点[13],通过化学改性可以提高橙皮的比表面积和增加吸附活性位点,从而提高其吸附容量[14-18]。本研究以橙皮为原料,经环氧氯丙烷及氢氧化钠改性制备改性橙皮,并研究其对Cd2+的吸附,探讨pH、初始浓度、反应时间和吸附剂投加量单因素对生物吸附过程的影响,研究了吸附过程的动力学特征。
1 实验原料与方法
1.1 主要试剂和仪器
主要试剂:硝酸镉、环氧氯丙烷、氢氧化钠和盐酸(36%~38%)均为分析纯,实验用水为二次蒸馏水。
主要仪器:AVATAR 330FT-IR傅里叶红外光谱仪、SHA-B水浴恒温振荡器、FZ102型微型植物粉碎机、S312数显恒速搅拌器、PK-S24恒温水浴锅、SHBⅢ型循环水真空泵和AA-6300F原子吸收分光光度计。
1.2 改性橙皮的制备
参照文献[16,19]制备改性橙皮,主要操作方法为:将新鲜橙皮用蒸馏水洗涤3~4遍后,置于60 ℃烘箱中烘干48 h,粉碎,过100目筛,取筛下物保存备用。取5 g未处理的干橙皮粉于250 mL三口烧瓶中,加入5 mL的环氧氯丙烷和100 mL 1 mol/L NaOH,置于40 ℃恒温水浴锅中搅拌反应30 min,过滤,用蒸馏水洗至pH=7,50 ℃真空干燥后,用研钵磨碎,过100目筛,即得改性橙皮,置于干燥器中备用。
1.3 吸附实验方法
在100 mL干燥洁净的具塞锥形瓶中加入25 mL一定质量分数的Cd2+重金属溶液,再加入一定量的环氧氯丙烷改性橙皮,一定温度下于恒温水浴振荡器中振荡吸附一定时间后,静置,离心取上清液稀释至适宜浓度,在火焰原子吸收分光光度计上于Cd2+特定吸收波长处测定吸光度。与该重金属的标准工作曲线(y=0.179x-0.002 4,R=0.999 9)对照,求出残余重金属的浓度,按式(1)和式(2)计算出橙皮对重金属的去除率(R)和平衡吸附量(Qe)。
R=(C0-Ce)/C0×100%
(1)
Qe=(C0-Ce)V/W
(2)
式中:R为去除率(%);C0为Cd2+初始浓度(mg/L);Ce为吸附平衡时浓度(mg/L);Qe为平衡吸附量(mg/g);V为溶液体积(L);W为橙皮投入量(g)。
2 结果与讨论
2.1 红外光谱(FT-IR)分析
橙皮和环氧氯丙烷改性橙皮的红外光谱如图1所示。由图1可知:3 370 cm-1处的宽吸收峰是橙皮中纤维素和木质素等分子上O-H和N-H的伸缩振动吸收峰,1 740 cm-1处为橙皮中果胶等分子上羰基的吸收峰,1 268 cm-1处的吸收峰归属于C-O的伸缩振动,1 600 cm-1和1 516 cm-1的吸收峰归属于苯环的骨架振动,1 370 cm-1处的吸收峰归属于半纤维素和纤维素中C-H的变形振动。对比橙皮和改性橙皮的红外光谱图,可以看出:改性后的橙皮于1 740、1 516、1 370、1 268 cm-1处的吸收峰逐渐减弱甚至消失,说明改性过程中橙皮中大量的半纤维素和木质素被脱除了。而在1 417 cm-1处出现了强的-CH2-的吸收峰,说明改性后环氧氯丙烷的碳链已成功地接在了纤维素分子上,碳链有所增长。
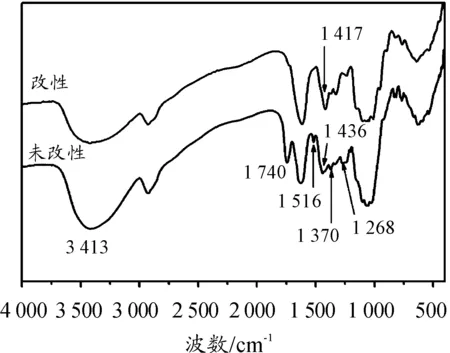
图1 改性前后橙皮的红外光谱
2.2 表面形貌分析
图2是未改性橙皮(a)和环氧氯丙烷改性橙皮(b)的扫描电镜图。由图2可知,橙皮的表面凹凸不平且松散多孔。与未改性橙皮相比,改性过程中经碱处理后橙皮中的半纤维素、木质素等组分溶解并被水冲洗掉,使橙皮的表面结构产生了变化,孔隙更小更多,这大大地提高了橙皮的比表面积。同时,剧烈的环氧化反应使得橙皮表面出现了更多的褶皱,有突起部分,增加了更多的活性基团,从而更有利于吸附过程的进行。

图2 改性前后橙皮的SEM图
2.3改性橙皮对Cd2+吸附实验的影响因素
2.3.1 溶液初始pH对吸附效果的影响
溶液pH值既影响金属离子的存在形态,又影响吸附剂的吸附位点,同时H+本身也是一个强的竞争吸附剂[20],是影响吸附效果的一个重要因素。在不同pH值下,镉离子以不同羟合离子形式存在,当pH值小于6时主要以游离的Cd2+和少量Cd(OH)+的化学形态存在。用0.2 g改性橙皮于室温条件下处理25 mL 100 mg/L的Cd2+溶液,振荡吸附3 h,调节溶液pH值,得到pH值对Cd2+吸附效果的影响,如图3所示。由图3可知,pH值对改性橙皮吸附Cd2+的影响显著。当溶液pH值在3~6时,改性橙皮对Cd2+的吸附效果随pH值的升高而呈逐渐增加的趋势,主要是H+浓度随pH值升高而降低,减少了H+的竞争吸附,有利于金属离子吸附在吸附剂的活性位点上[21];当pH值大于6时,Cd2+将以氢氧化物的形式存在,不利于吸附的进行,改性橙皮对Cd2+的吸附性能降低。因此,吸附实验应控制溶液的pH=6。
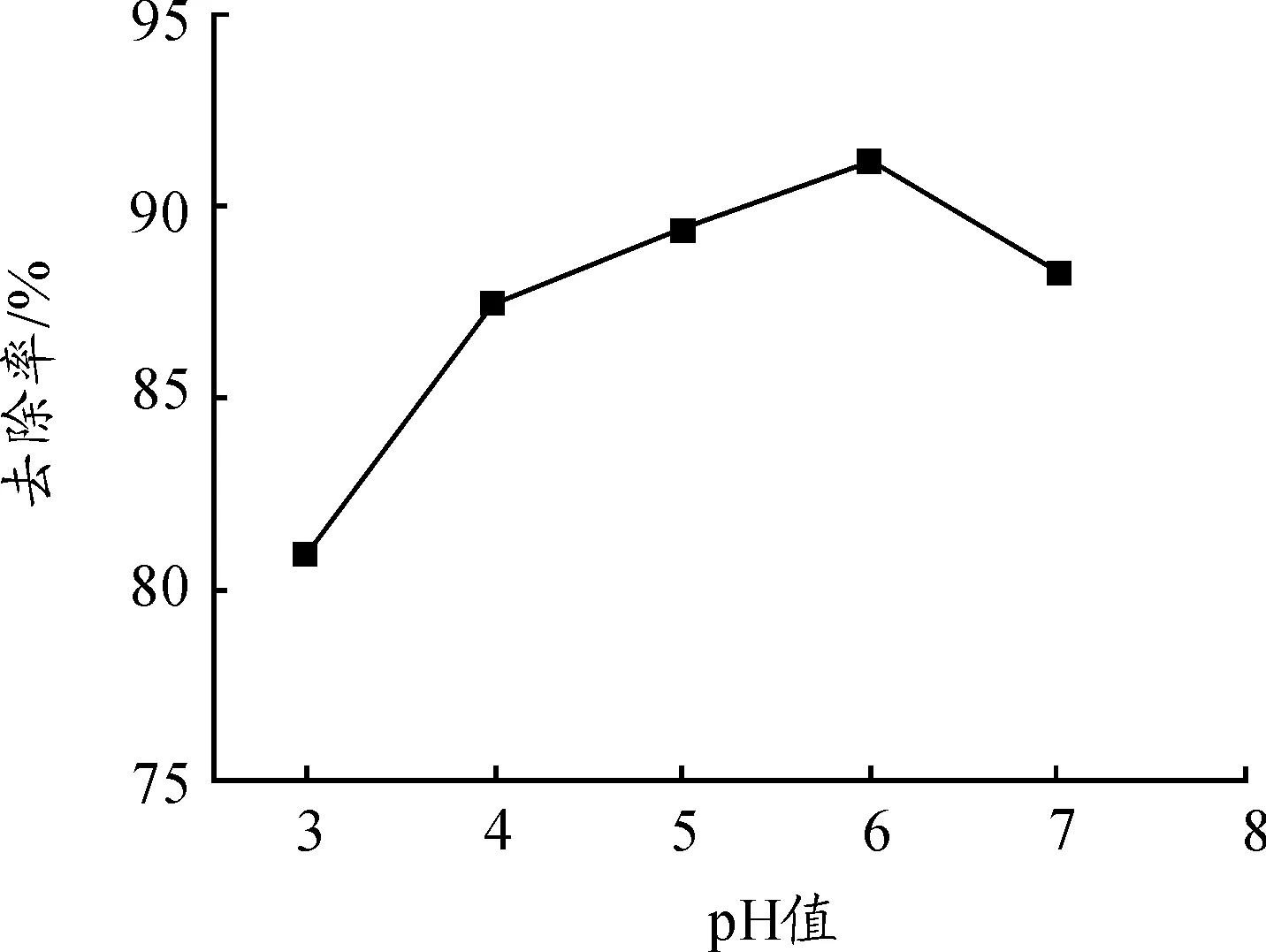
图3 溶液初始pH值对改性橙皮吸附Cd2+的影响
2.3.2 吸附剂投加量对吸附效果的影响
吸附剂投加量是影响吸附效果的另一个重要因素。吸附剂投加量太少,就不能有效地去除Cd2+,而投加量太多,又会造成资源浪费,降低经济效益。
因此,为了合理有效地利用吸附剂,研究了吸附剂投加量对去除率的影响。在pH=6、初始浓度为100 mg/L、吸附时间为3 h、室温条件下,测定不同吸附剂投加量对Cd2+的吸附效果的影响,结果见图4。
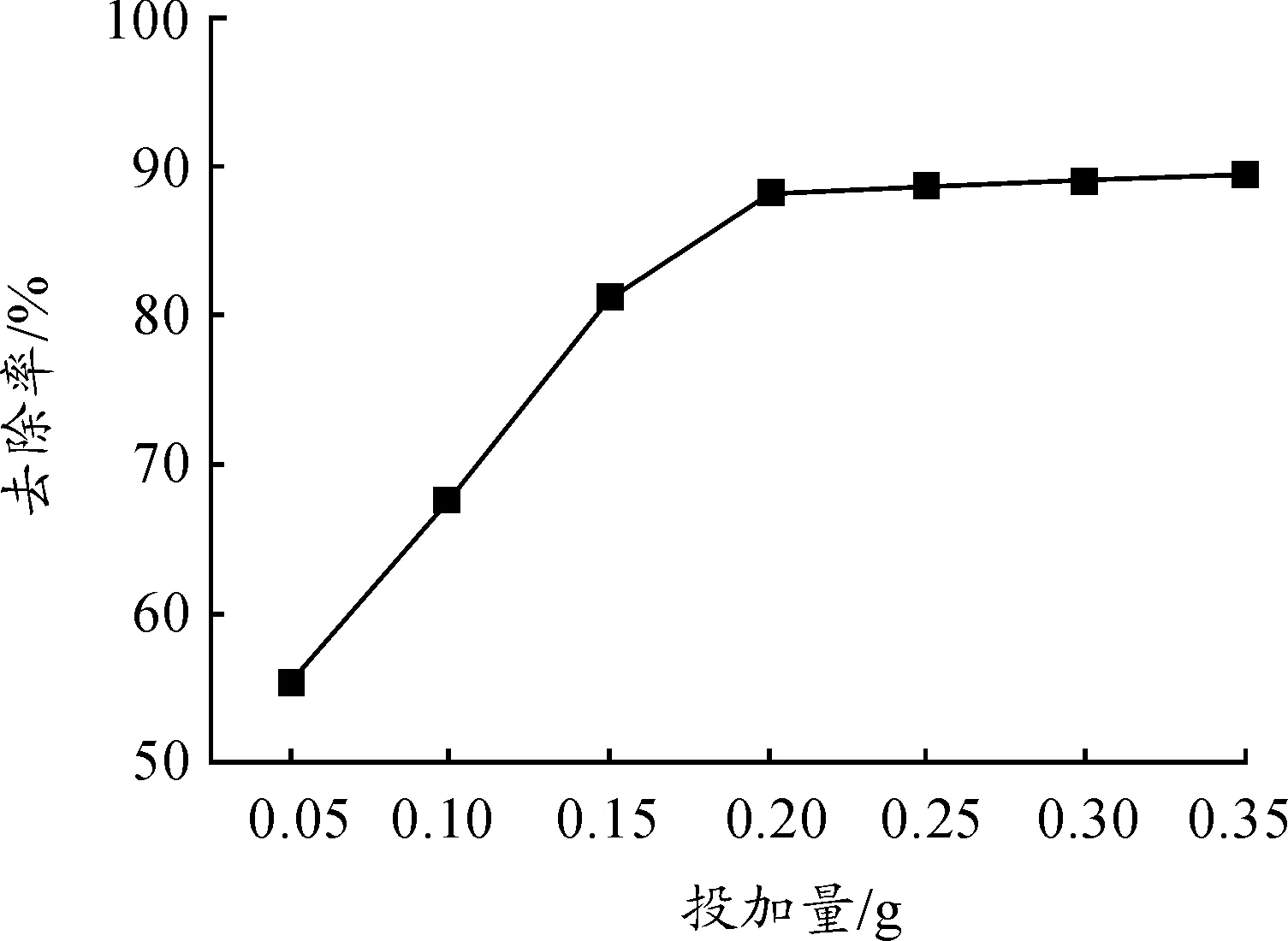
图4 吸附剂投加量对改性橙皮吸附Cd2+的影响
由图4可知:当改性橙皮投加量低于0.2 g时,Cd2+的去除率随着投加量的增加而增加;当投加量等于0.2 g时,去除率最高,约为90%(而氢氧化钠改性橙皮对低浓度的Cd2+(3 mg/L) 在pH=6时吸附200 min后除去率为97.0%[22]);随着投加量的进一步增加,Cd2+的去除率基本不变。这是因为Cd2+初始浓度一定时,投加量的增加提高了活性吸附位点的数量,从而提高了Cd2+的去除率;当改性橙皮投加量增加到一定程度时,去除率基本不变,可能是达到了吸附平衡。因此,最佳投入量为0.2 g。
2.3.3 吸附动力学
吸附时间是影响生物吸附剂对重金属吸附效果的又一个重要因素。在pH=6、吸附剂投加量为0.2 g、室温条件下处理25 mL 100 mg/L的Cd2+溶液,测定不同时间内对Cd2+的吸附效果,结果见图5。由图5可知:在吸附初始阶段,改性橙皮对Cd2+的去除率随时间的延长而急剧上升。40 min内对Cd2+的去除率高达80%以上,吸附60 min时,去除率接近90%,60 min后去除率基本不变,达到吸附平衡。这可能是改性橙皮刚投入使用时,吸附剂表面有大量的活性位点,Cd2+的吸附主要在改性橙皮的表面进行;随着时间的延长,吸附剂表面的活性位点基本被Cd2+占据,Cd2+逐渐进入改性橙皮的微孔内,传质速率减慢,使得去除率增速缓慢并趋于稳定。因此,最佳吸附时间为60 min。
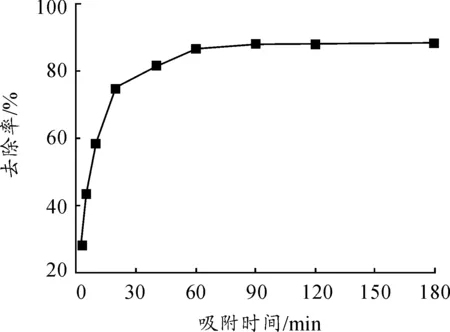
图5 吸附时间对改性橙皮吸附Cd2+的影响
采用准二级动力学[23-25]和Weber-Morris粒子内部扩散模型[26]对图5的实验数据进行拟合,以研究改性橙皮对Cd2+的吸附动力学机理。
准二级动力学方程如式(3)所示。
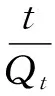
(3)
颗粒内部扩散模型的表达式如式(4)所示。
Q=kidt1/2+C
(4)
式中:k2为二级反应速率常数,kid为扩散因子,如果式(4)中C不为零,则颗粒内部扩散不是吸附速率的唯一控制步骤[27]。拟合结果如图6所示,由图6(a)可知:改性橙皮对Cd2+的吸附符合准二级动力学模型,相关系数为0.999 7,Qe(计算)为11.38 mg/g,与实验数据11.03 mg/g接近。这表明改性橙皮对Cd2+的吸附是以化学吸附为主。由图6(b)可知:C不为零,颗粒内部扩散模型拟合曲线不通过原点,且线性相关系数很低(R2=0.764 6),因此改性橙皮对Cd2+的吸附不仅受粒子内部扩散控制,还受颗粒外部扩散等其他因素的控制[28]。
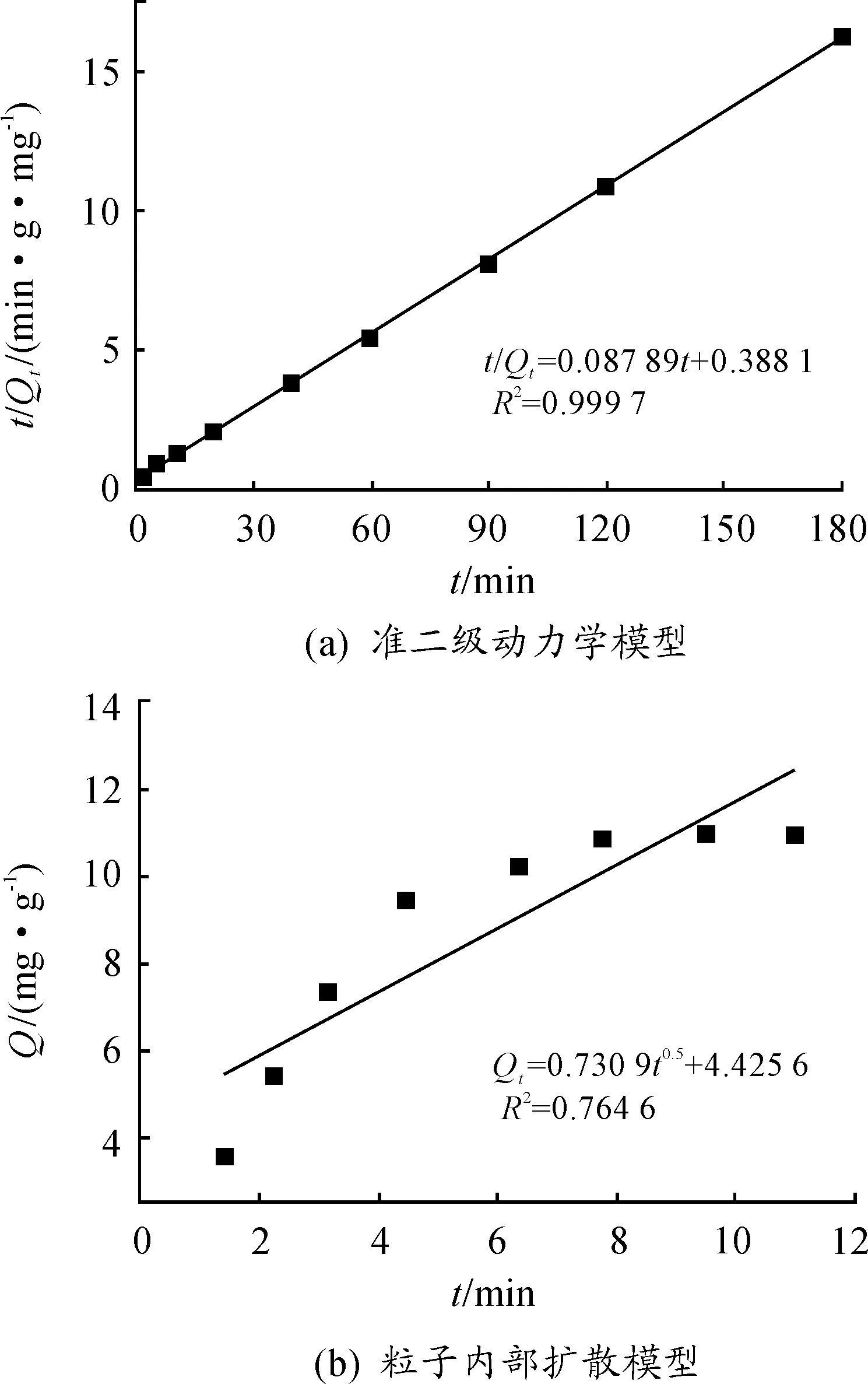
图6 吸附动力学拟合
2.3.4 吸附等温线
吸附等温线是指吸附平衡时重金属浓度与吸附容量的关系,是研究吸附热力学的重要组成部分。在pH=6、t=60 min、吸附剂投加量为0.2 g、室温条件下处理25 mL不同质量浓度的Cd2+溶液,初始浓度对吸附效果的影响见图7。当Cd2+溶液浓度为50 mg/L时,改性橙皮对Cd2+的去除率高达91.37%,吸附量(5.71 mg/g)最小。随着初始浓度的增加,Cd2+的去除率呈下降趋势,而吸附量呈递增趋势。这是因为吸附剂投加量一定时,吸附活性位点是有限的,当Cd2+的浓度增加到一定程度时,超过了吸附剂的饱和容量,无法吸附多余的金属离子,故去除率下降。
Langmuir模型主要用来描述单层均相吸附体系,而Freundlich模型主要用来描述非均相吸附体系。本研究分别采用Langmuir[29]和Freundlich[30]等温模式对实验数据进行拟合来研究吸附剂对Cd2+溶液的吸附机理。
Langmuir等温吸附模型的线性方程式如式(5)所示。
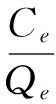
(5)
Freundlich等温吸附模型的线性方程式如式(6)所示。
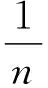
(6)
式中:Ce为平衡浓度(mg/L);Qe为平衡吸附量(mg/g);Qmax为最大吸附量(mg/g);b为Langmuir常数(L/mg);n、k为经验常数。
采用上述2种模型对图6实验数据进行线性拟合,结果见图8。Langmuir(图8(a))模型拟合的参数为:b=0.069 3,R2=0.981 7,Qmax=41.32 mg/g(硝酸质子化改性橙皮对Cd2+的最大吸附量为13.7 mg/g[25];氢氧化钠、酯化和硫酸改性的橙皮对Cu2+的最大吸附容量仅为1.56 mg/g、1.73 mg/g和1.69 mg/g[24]);Freundlich(图8(b))模型拟合的参数为:k=4.4,n=3.2992,R2=0.828 5。比较2种模型的相关系数(R2),可知Langmuir模型对Cd2+的吸附拟合效果更好,说明Cd2+在改性橙皮上的吸附以单层化学吸附为主。
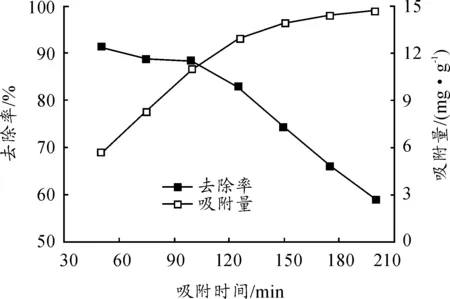
图7 Cd2+初始浓度对改性橙皮吸附Cd2+的影响

图8 Langmuir (a) 和Freundlich (b) 模型拟合
2.3.5 吸附剂的再生和重复使用
取在最佳试验条件下剩余的滤渣,即改性橙皮投入量0.2 g、pH=6、吸附时间为60 min、初始浓度为100 mg/L,在室温条件下吸附,达到吸附平衡后将改性橙皮与溶液离心分离,即得滤渣。将滤渣用0.1 mol/L HCl溶液洗涤几遍后,再在100 mL浓度为0.1 mol/L HCl溶液中于50 ℃下振荡脱附3 h,过滤,用蒸馏水洗涤滤渣至中性,烘干磨碎,过100目筛,即得再生改性橙皮。将此再生吸附剂在相同的条件下进行吸附实验,实验结果表明,再生吸附剂经3次再生和重复后对Cd2+的去除率仍在85%以上,说明该改性橙皮再生性能好,可重复使用。
3 结论
采用环氧氯丙烷和氢氧化钠对橙皮进行了改性,制备了改性橙皮吸附剂。FTIR的测试结果表明,改性橙皮结构发生了变化,环氧氯丙烷的碳链已成功地接在了纤维素分子上,增加了活性吸附位点数;SEM测试结果表明,改性后橙皮表面变得更加凹凸不平,提高了吸附剂与Cd2+的接触面积,有利于提高对Cd2+的去除率。
改性橙皮对Cd2+有较好的去除效果,其吸附剂投加量、pH值、吸附时间和Cd2+初始浓度对吸附效果影响显著。在室温条件下,当改性橙皮投加量为0.2 g、pH=6、吸附时间为60 min、初始浓度为100 mg/L时,改性橙皮对Cd2+的去除率高达90%,吸附量为11.03 mg/g。与氢氧化钠[22]、氢氧化钠和柠檬酸[31]、磷酸[32]、异丙醇[33]改性的橙皮吸附剂仅对低浓度Cd2+(3 mg/L)、Cr6+(10 mg/L)、Fe2+(10 mg/L)、Pb2+(20 mg/L)有较高的去除率相比,本文制备的改性橙皮的优势表现为对高浓度的Cd2+具有较好的处理效果。
与Freundlich模型相比,改性橙皮对Cd2+的吸附更符合Langmuir模型,最大吸附容量较高(41.32 mg/g),吸附过程以单层化学吸附为主;动力学研究结果表明,改性橙皮对Cd2+的吸附遵循准二级动力学方程。
改性橙皮具有良好的再生性能,重复使用性能优良,在工业废水处理中具有较好的应用前景。
[1] 张玉梅.含镉废水处理的试验研究[J].环境工程,1995,13(1):15-21.
[2] 熊佰炼,崔译霖,张进忠,等.改性甘蔗渣吸附废水中低浓度Cd2+和Cr3+的研究[J].西南大学学报(自然科学版),2010,32(1):118-123.
[3] 马春芳,时洋,刘建平,等.硫酸改性甘草废渣生物吸附剂对Pb2+离子的吸附[J].高等化学工程学报,2015,29(3):716-723.
[4] WANG X S,QIN Y.Equilibrium sorption isotherm for Cu2+on rice bran[J].Process Biochemistry,2005,40(2):677-680.
[5] 刘恒博,徐宝月,李明明,等.改性小麦秸秆对水中Cd2+吸附的研究[J].水处理技术,2013,39(4):15-19.
[6] 郭昌建.茶叶对重金属的吸附性能研究[D].大连:大连理工大学,2010.
[7] LI Q,ZHAI J P,ZHANG W YI,et al.Kinetic studies of adsorption of Pb (II),Cr (III) and Cu (II) from aqueous solution by sawdust and modified peanut husk[J].Journal of Hazardous Materials,2007,141(1):163-167.
[8] 郭学益,肖彩梅,梁莎,等.改性柿子粉吸附剂对Cd2+的吸附性能[J].中南大学学报(自然科学版),2012,43(2):412-417.
[9] 梁东旭,罗春燕,周鑫,等.改性小麦壳对水溶液中Cd2+的吸附研究[J].农业环境科学学报,2015,34(12):2364-2371.
[11] 齐亚凤,何正艳,余军霞,等.改性甘蔗渣对Cu2+和Zn2+的吸附机理[J].环境工程学报,2013,7(2):585-590.
[12] 李莲.新型生物吸附剂豆渣对水中Cd2+和Zn2+的吸附[D].长沙:湖南大学,2008.
[13] ANNADURAI A,JUANG R S,LEE D J.Adsorption of heavy metals from water using banana and orange peel[J].Water Science and Technology,2002,47(1):185-190.
[14] FENG N C,GUO X Y,LIANG S.Adsorption study of copper (II) by chemically modified orange peel[J].Journal of Hazardous Materials,2009,164(2-3):1286-1292.
[15] 简绍菊,杨为森.改性橙皮对水中中性红的吸附及其动力学[J].安徽农业大学学报,2013,40(3):514-518.
[16] 杨为森,简绍菊.环氧氯丙烷改性橙皮对含Pb2+废水的吸附研究[J].长江大学学报(自然科学版),2017,14(05):11-15.
[17] 马沛勤,陈莉.酸碱改性橙皮渣对Pb2+的吸附性能研究[J].中国南方果树,2015,44(01):36-39.
[18] ZHANG L X,YANG Z Q,LI T,et al.Perchlorate adsorption onto orange peel modified by cross-linking amine groups from aqueous solutions[J].Water Science and Technology,2015,71(11):1629-1637.
[19] 孙小梅,刘勇,李步海,等.改性花生壳粉对Mn2+的吸附[J].中南民族大学学报(自然科学版),2009,28(4):23-27.
[20] ARPITA G,KEKA S,PAPITA D S.Central composite design optimization and artificial neural network modeling of copper removal by chemically modified orange peel[J].Desalination and Water Treatment,2013,51(40/42):2444-2450.
[21] FENG N C,GUO X Y,LIANG S,et al.Biosorption of heavy metals from aqueous solutions by chemically modified orange peel[J].Journal of Hazardous Materials,2011,185(1):49-54.
[22] KUMAR A,KUMAR V.Equilibrium and thermodynamic studies of Cd (II) biosorption by chemically modified orange peel[J].Journal of Environmental Biology,2016,37(2):201-206.
[23] MUNAGAPATI V S,KIM D SU.Adsorption of anionic azo dye Congo Red from aqueous solution by cationic modifiedorange peel powder[J].Journal of Molecular Liquids,2016,220:540-548.
[24] KHALFAOUI A,MENIAI A H.Application of chemically modified orange peels for removal of copper(II) from aqueous solutions[J].Theoretical Foundations of Chemical Engineering,2012,46(6):732-739.
[25] LASHEEN M R,AMMAR N S,IBRAHIM H S.Adsorption/desorption of Cd(II),Cu(II) and Pb(II) using chemically modified orange peel:Equilibrium and kinetic studies[J].Solid State Sciences,2012,14(2):202-210.
[26] GEETHAMANI C K,RAMESH S T,GANDHIMATHI R,et al.Fluoride sorption by treated fly ash:Kinetic and isotherm studies[J].Journal of Material Cycles and Waste Management,2013,15(3):381-392.
[27] DOGAN M,ABAK H,ALKAN M.Adsorption of methylene blue onto hazelnut shell:kinetics,mechanism and activation parameters[J].Journal of hazardous Materials,2009,164(1):172-181.
[28] 吴洁,张娟,冯辉霞,等.鞣酸模板交联壳聚糖/凹凸棒粘土复合树脂的吸附性能[J].高分子材料科学与工程,2012,28(10):81-85.
[29] LIANG S,GUO X Y,FENG N C,et al.Adsorption of Cu2+and Cd2+from aqueous solution by mercapto-acetic acid modified orange peel[J].Colloids and Surfaces B:Biointerfaces,2009 73(1):10-14.
[30] FENG N C,GUO X Y,LIANG S.Kinetic and thermodynamic studies on biosorption of Cu(II) by chemically modified orange peel[J].Transactions of Nonferrous Metals Society of China,2009,19(5):1365-1370.
[31] 张玮,刘雪琴,陈旭章.改性橙皮对废水中Cr6+的吸附效果[J].湖北农业科学,2011,50(12):2429-2431.
[32] 张玮,詹燕,石灵慧.改性橙皮对水溶液中Fe2+的吸附性能[J].湖北农业科学,2013,52(1):71-73.
[33] 张玮,张冬.改性橙皮静态吸附模拟废水中的Pb2+[J].化工环保,2012,32(3):201-204.
(责任编辑林 芳)
StudyontheAdsorptionofCd2+inAqueousSolutionbyModifiedOrangePeelanditsBiosorptionKinetics
YANG Weisen1,2,3, JIAN Shaoju1,2,3, LIN Weisheng1,2,3
(1.Fujian Provincial Key Laboratory of Eco-Industrial Green Technology, Wuyishan 354300, China;2.Fujian Provincial Bamboo Engineering Technology Reserach Center, Wuyishan 354300, China;3.College of Ecology and Resources Engineering, Wuyi University, Wuyishan 354300, China)
2017-04-12
福建省科技厅区域重大项目(2012Y3008);福建省科技厅资助项目(JK2011058);福建省大学生创新创业训练项目(201510397033);武夷学院一般项目(XL201301);武夷学院校级科研基金(XL201402)
杨为森(1983—),男,博士研究生,讲师,主要从事纳米材料和有机合成研究,E-mail:yangweisen@126.com。
杨为森,简绍菊,林维晟.Cd2+在改性橙皮上的吸附及其动力学[J].重庆理工大学学报(自然科学),2017(9):103-109.
formatYANG Weisen,JIAN Shaoju,LIN Weisheng.Study on the Adsorption of Cd2+in Aqueous Solution by Modified Orange Peel and its Biosorption Kinetics[J].Journal of Chongqing University of Technology(Natural Science),2017(9):103-109.
10.3969/j.issn.1674-8425(z).2017.09.017
X703.1
A
1674-8425(2017)09-0103-07

