纳米TiO2/硬脂酸超疏水材料的制备与表征
曹坤丽,吴燕*,曹福才,朱彦涛,朱文凯
(1.南京林业大学家居与工业设计学院,南京 210037; 2.江苏纬信工程咨询有限公司,南京 210014;3.天津大学内燃机燃烧学国家重点实验室,天津 415400)
纳米TiO2/硬脂酸超疏水材料的制备与表征
曹坤丽1,吴燕1*,曹福才2,朱彦涛3,朱文凯1
(1.南京林业大学家居与工业设计学院,南京 210037; 2.江苏纬信工程咨询有限公司,南京 210014;3.天津大学内燃机燃烧学国家重点实验室,天津 415400)
为探究适合工业化生产的纳米TiO2疏水修饰工艺,以便宜无毒的钛酸四丁酯、硬脂酸、无水乙醇等为原料进行了研究。通过对光学接触角测量仪的数据分析,得出水接触角最优的纳米TiO2疏水材料制备工艺为:将0.2 g TiO2放入70 mL无水乙醇中超声1 h,再加入1 g硬脂酸,继续超声30 min;接着将超声后的混合液70℃磁力搅拌12 h,然后常温磁力搅拌使得混合溶液稳定6 h,再加入等体积无水乙醇后离心去除上清液,120℃鼓风干燥,最终得到超疏水材料,水接触角166°。该工艺操作简单方便,成本低、疏水性好,适应工业化生产,极具商业价值。通过傅里叶变换红外光谱仪(FT-IR)和场发射扫描电子显微镜(SEM)等对内部机理进行探究,得出表面修饰物硬脂酸以化学方式吸附于材料表面。
修饰工艺;纳米TiO2;疏水修饰;硬脂酸;超疏水
纳米TiO2具有催化活性高、催化范围广[1-3],抗紫外线、抗老化[4],能够有效去除多种有机污染物[5-7]等优良特点,但纳米TiO2具有大的比表面积,高表面能,极易发生团聚[8],在应用时很难分散,不能体现纳米TiO2的特殊功能。同时,纳米TiO2的极性较强,表面容易吸附水分子极化成表面羟基[9],宏观上表现出亲水特性,限制其应用范围。因此,对纳米TiO2粉体的有机表面修饰是纳米材料科学的一个研究热点。
前人为制备更具实用价值的纳米TiO2做出了诸多尝试,其中包括对纳米TiO2进行疏水修饰。王百年等[10]用十六烷基三甲基溴化铵(CTAB)对纳米TiO2进行湿法表面改性,以疏水度为考察指标,通过控制体系pH、CTAB用量、反应时间、温度等,使得纳米TiO2疏水度由13%提高至59%;何丽红等[11]以硅烷偶联剂KH-570为改性剂,对TiO2进行表面有机改性,经测试改性后的TiO2涂层与水的接触角为152.5°;潘洪波等[12]采用有机硅改性聚氨酯与纳米TiO2复合,通过控制纳米TiO2与聚氨酯的质量比、分散剂添加量以及紫外光照射时间,制备出静态接触角为156°的超疏水材料。目前,对TiO2的疏水研究普遍存在原材料昂贵、过程有毒、工艺复杂、疏水度不高、无法适应工业化生产等问题。据此,笔者以低价、无毒的钛酸四丁酯、硬脂酸和无水乙醇为原料,研究纳米TiO2超疏水材料的制备工艺,以期为纳米TiO2超疏水材料的工业化生产提供依据。
1 材料与方法
1.1 试验材料
本试验所用化学试剂主要有:硬脂酸(分析纯AR,上海凌峰化学试剂有限公司);钛酸四丁酯(质量分数98%,南京大光明化学试剂有限公司);聚乙二醇(质量分数98%,广东光华科技股份有限公司);乙醇(质量分数≥99.7%,南京大光明化学试剂有限公司)。
1.2 试验设备
磁力恒温搅拌机(S312-60,上海梅颖浦仪器仪表制造有限公司);电子天平(JA21002,上海良平仪器仪表有限公司);电热恒温鼓风干燥箱(DHG-9523A,上海精宏实验设备有限公司);真空干燥箱(DZF-6020,南京先欧仪器制造有限公司);箱式电阻炉/马弗炉(SX2-4-10,上海嘉展仪器设备有限公司);激光粒度分析仪(Winner 2005,济南微纳仪器有限公司);傅里叶变换红外光谱仪(尼高力360,美国尼高力仪器公司);场发射扫描电子显微镜(JSM-7600F,日本电子株式会社);台式离心机(TDL-40B,上海安亭科学仪器厂);超声破碎仪(BILON-500,上海比郎仪器有限公司);Attension光学接触角测量仪器(Theta Lite,瑞典百欧林科技有限公司)。
1.3 试验方法
1.3.1 纳米TiO2的制备
将反应容器置于恒温槽中,在20℃恒温条件下,将30 mL钛酸四丁酯乙醇溶液在强力搅拌下滴加于40 mL质量分数为2%的聚乙二醇溶液中,反应30 min后用离心机离心分离沉淀,用蒸馏水洗涤4次,然后80℃真空干燥4 h,500℃煅烧2 h得锐钛矿型TiO2,研磨成粉待用。
1.3.2 纳米TiO2/硬脂酸功能复合材料的制备
为探索纳米TiO2/硬脂酸超疏水材料的制备工艺,本试验分别制备了12份处理方式不同的样品,每份样品重复制备3次,依次标号为a、b、c,并设置一份不经任何处理的纳米TiO2空白对照样。具体方法如下:将0.2 g TiO2放入70 mL无水乙醇中超声1 h;再加入1 g硬脂酸,继续超声30 min,接着按表1进行处理;最后将制得的测试样粉末及未处理的纳米TiO2空白样喷洒于粘有双面胶的载玻片上,待测。
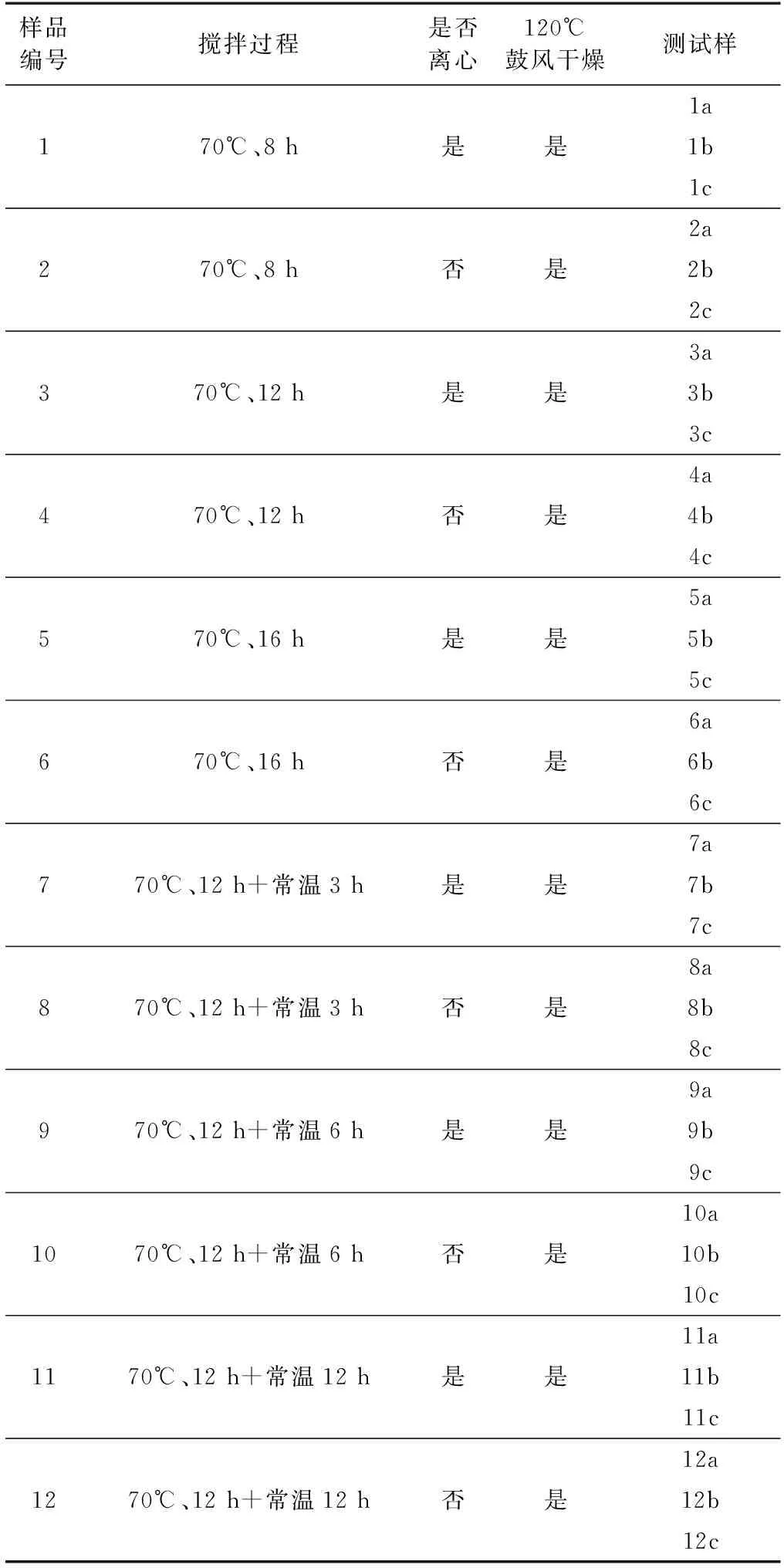
表1 样品制备过程Table 1 Sample preparation process
注:制备过程中的“是否离心”具体操作方式为,是否加入与混合液等体积的无水乙醇后离心去除上清液。
2 结果与分析
2.1 样品水接触角
先对空白对照样进行3次不同点的水接触角测试,水接触角分别为27°,27°,28°;26°,27°,28°;28°,27°,28°。平均水接触角为27.33°。对处理的12份样品的每个测试样都进行了3个不同点的水接触角测试,并取得每个测试样的水接触角平均值。根据表2中的数据及空白对比样的数据可以得出:
1)样品的疏水性与是否用硬脂酸对纳米TiO2进行疏水修饰有很大关系。未经处理的纳米TiO2即空白对比样水接触角均小于90°,表现亲水的特性,而经硬脂酸修饰后的样品水接触角均大于90°,表现疏水特性。
2)样品的疏水性与是否做离心处理有很大关系。样品2,4,6,8,10,12均不做离心处理,可以看出它们的水接触角稳定在137°左右,不做离心处理的样品间差异不显著(P=0.30>0.05);而样品1,3,5,7,9,11均经过离心处理,样品间差异极显著(P=4.23×10-19<0.01)。由此可知,如果用硬脂酸对纳米TiO2进行改性后不做离心处理,其他处理条件将不对疏水性产生有效影响,所以在用硬脂酸改性样品后需对样品做离心处理。
3)探究制备工艺需要考虑时间和成本,尽量选择节能高效的方式。对样品1和3进行方差分析,两者水接触角差异极显著(P=4.49×10-6<0.01),对照下表可以得出,加热搅拌12 h比8 h疏水效果好;对样品3和5进行方差分析,P=0.000 5,对样品3和7进行方差分析,P=1.17×10-6,虽然两组P值均小于0.05,但是样品5在3的基础上增加了4 h的加热处理,然而水接触角增幅仅3°,而样品7在3的基础上增加了3 h的常温搅拌处理,增幅明显高于10°,因此,在实际生产中样品5的处理方案较样品7无显著差异,即当样品热处理12 h后应转为常温搅拌处理。
4)对样品7和9进行方差分析,两者疏水性差异显著(P=1.15×10-5<0.05),即常温处理6 h比3 h疏水效果好;对样品9和11进行方差分析,两者疏水性差异不显著(P=0.07>0.05),即样品常温处理12 h与处理6 h疏水性无显著性差异,因此,制备疏水材料时常温处理6 h即可。
综上所述,从节省时间节约成本方面考虑,纳米TiO2/硬脂酸超疏水复合材料的备工艺选择样品9的制备方法:将0.2 g TiO2放入70 mL无水乙醇中超声1 h;再加入1 g硬脂酸,继续超声30 min;接着将超声后的混合液70℃磁力搅拌12 h,然后在常温条件下进行磁力搅拌使得混合溶液稳定6 h,再加入等体积无水乙醇后离心去除上清液,120℃鼓风干燥,得到超疏水材料。最终水接触角成像图及实物图如图1所示。
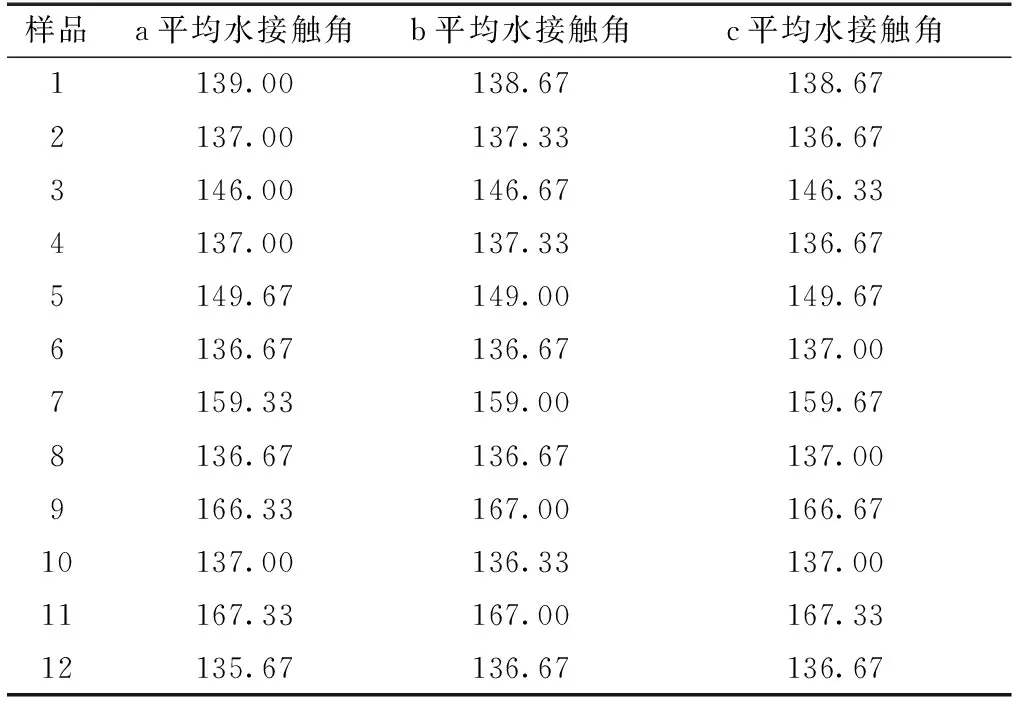
表2 样品水接触角Table 2 Water contact angle of the samples /(°)

图1 水接触角166°图像Fig.1 The image of water droop with a contact angle of 166°
2.2 傅里叶红外光谱分析
傅里叶红外光谱图见图2。在图2的TiO2/硬脂酸谱线中,2 848和2 915 cm-1处的尖峰分别对应于—CH2和—CH3中C—H的伸缩振动[13];而1 470 cm-1处的尖峰则主要是—CH2的剪切振动或—CH3的对称变形振动的贡献,1 430 cm-1为—OH的弯曲振动吸收峰[14]。以上吸收峰都是由硬脂酸中的非极性部分即脂肪族长碳链基团引起的,这表明产物中确实存在因纳米TiO2与硬脂酸反应而形成的长碳链,而相应的硬脂酸谱线上的2 658 cm-1处二聚体之间的氢键肩峰,1 702 cm-1处C—O键伸缩振动吸收峰,及1 430 cm-1处O—H弯曲振动吸收峰等硬脂酸中极性部分的吸收峰却明显减弱或消失,说明纳米TiO2表面吸收的硬脂酸很少且产物中已无游离的脂肪酸[14]。表面修饰后纳米TiO2在1 635 cm-1处出现新的强吸收峰,为羧酸根(COO—)的不对称伸缩振动和对称伸缩振动吸收峰,说明硬脂酸根和纳米TiO2是以双齿配位的方式结合的[15]。
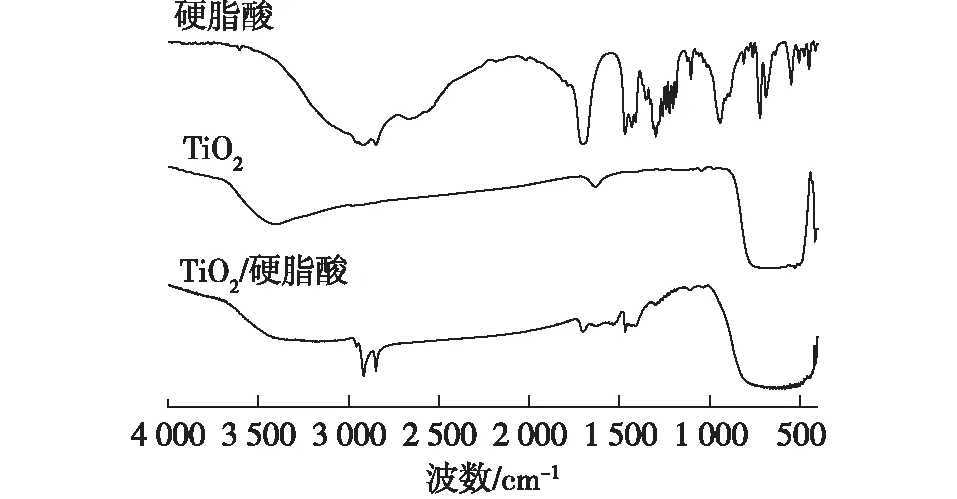
图2 傅里叶红外光谱图Fig.2 Fourier transform infrared spectroscopy
2.3 场发射扫描电子显微镜分析
2.3.1 纳米TiO2的微观形貌分析
不同放大倍数下纳米TiO2的场发射扫描电镜图见图3。由图可知,微观形貌下的纳米TiO2呈类球形,粒径非常小,经激光粒径仪测试得到纳米TiO2的粒径分布范围在7~60 nm之间,高峰是10 nm,平均粒径为13.5 nm,30%的粒径在9.8 nm以下,50%的粒径在13 nm以下,由此可知纳米粒子粒径不均,某些大粒子是某些小粒子粒径的几倍。从电镜图片中可以看出,虽然多数纳米TiO2粒子粒径较小,但其中会夹杂一些大粒径粒子,这是因为单个纳米TiO2粒子粒径较小,比表面积大,表面能高,所以会出现一些团聚现象。

图3 纳米TiO2的SEM图Fig.3 The SEM images of nano TiO2
2.3.2 硬脂酸改性纳米TiO2的微观形貌分析
对比硬脂酸改性纳米TiO2前后的微观形貌图(图4)可以看出,硬脂酸改性前后的纳米TiO2没有发生形貌上的变化,依然是类球形。用激光粒径仪对改性后的纳米TiO2进行粒径分析,得到改性后的纳米TiO2的粒径分布范围在10~18 nm之间,高峰是14 nm,平均粒径为14.4 nm,90%的粒径在16.7 nm以下,由此可知,纳米粒子粒径分布较为均匀,结合改性后的纳米TiO2扫描电镜图片,可以得出低表面能物质硬脂酸的加入有效防止了纳米TiO2粒子团聚现象的发生。

图4 硬脂酸改性纳米TiO2粉末的SEM图Fig.4 The SEM images of stearic-acid-modified nano TiO2
3 结 论
1)以钛酸四丁酯为前驱体制备的纳米TiO2,微观状态下呈分散的类球形且粒径非常小。由红外光谱图结果得出,硬脂酸的疏水长链烷基成功接枝到了纳米TiO2表面,纳米TiO2表面吸收的硬脂酸很少且产物中已无游离的脂肪酸。硬脂酸根和纳米TiO2是以双齿配位的方式结合的,对纳米TiO2进行了疏水修饰。场发射扫描电镜结果进一步证明了纳米TiO2表面包覆了硬脂酸。
2)纳米TiO2/硬脂酸超疏水材料的最优制备工艺为:将0.2 g TiO2放入70 mL无水乙醇中超声1 h;再加入1 g硬脂酸,继续超声30 min;接着将超声后的混合液70℃磁力搅拌12 h;然后在常温条件下进行磁力搅拌使得混合溶液稳定6 h,再加入等体积无水乙醇后离心去除上清液,120℃鼓风干燥,最终得到静态水接触角为166°的纳米TiO2超疏水材料。
[1]王姝.改性纳米二氧化钛的光催化性能研究[D].长春:吉林大学,2014.WANG S.The photocatalytic property of modified TiO2nanocrystals[D].Changchun:Jilin University,2014.
[2]DIEBOLD U.The surface science of titanium dioxide[J].Surface Science Reports,2003,48(5):53-229.
[3]CARP O,HUISMAN C L,RELLER A.Photoinduced reactivity of titanium dioxide[J].Progress in Solid State Chemistry,2004,32(1):33-177.
[4]范崇政,肖建平,丁延伟.纳米TiO2的制备与光催化反应研究进展[J].科学通报,2001,46 (4):265-273.
[5]严新,吴俊,陈华,等.TiO2光催化降解甲基橙废水性能研究[J].合肥工业大学学报(自然科学版),34(3):429-432.YAN X,WU J,CHEN H,et al.Photocatalytic degradation property of TiO2in treating methyl orange wastewater[J].Journal of Hefei University of Technology (Natural Science),2011,34(3):429-432.
[6]RADECKA M,ZAKRZEWSKA K,WIERZBICKA M,et al.Study of the TiO2-Cr2O3system for photoelectrolytic decomposition of water[J].Solid State Ionics,2003,157(1):379-386.
[7]KARVINEN S,LAMMINMKI R J.Preparation and characterization of mesoporous visible-light-active anatase[J].Solid State Sciences,2003,5(8):1159-1166.
[8]姚超,高国生,林西平,等.硅烷偶联剂对纳米二氧化钛表面改性的研究[J].无机材料学报,2006,21(2):315-321.YAO C,GAO G S,LIN X P,et al.Surface modification of nanosized TiO2with silane coupling reagent[J].Journal of Inorganic Materials,2006,21(2):315-321.
[9]魏绍东.纳米二氧化钛的现状与发展[J].中国涂料,2005,20(2):9-10.WEI S D.Present status and development of nano-TiO2[J].China Paint,2005,20(2):9-10.
[10]王百年,何晓婷,刘磊.二氧化钛的疏水改性及其表征[J].化学工业与工程技术,2013,34(4):36-40.WANG B N,HE X T,LIU L,et al.Hydrophobic modification and characterization of titanium dioxide[J].Journal of Chemical Industry &Engineering,2013,34(4):36-40.
[11]何丽红,周超,李力,等.硅烷偶联剂表面改性二氧化钛粒子超疏水性能[J].精细化工,2014,31(9):1061-1064.HE L H,ZHOU C,LI L,et al.Superhydrophobicity of surface-modified TiO2with silane coupling agent[J].Fine Chemicals,2014,31(9):1061-1064.
[12]潘洪波,汪存东,刘建新,等.二氧化钛/聚氨酯超疏水涂层的制备及性能[J].高分子材料科学与工程,2015,31(5):62-65.PAN H B,WANG C D,LIU J X,et al.Preparation and properties of titanium oxide/polyurethane superhydrophobic coating[J].Polymer Materials Science and Engineering,2015,31(5):62-65.
[13]颜海涛.等离子体辅助球磨对船用润滑油添加剂的表面修饰[D].厦门:集美大学,2016.YAN H T.Surface modification of marine lubricating oil additives by plasma assisted ball milling [D].Xiamen:Jimei University,2016.
[14]曹坤丽,吴燕,吴兆旭,等.硬脂酸改性纳米纤丝化纤维素的制备与表征[J].科技创新与应用,2016(28):32-33.
[15]姚超.纳米TiO2合成、表面处理及其防团聚研究[D].南京:南京理工大学,2006.YAO C.Study on nano-TiO2synthesis,surface treatment and anti-agglomeration [D].Nanjing:Nanjing University of Science &Technology,2006.
Preparation and characterization of nano TiO2/stearic acidsuperhydrophobic material
CAO Kunli1,WU Yan1*,CAO Fucai2,ZHU Yantao3,ZHU Wenkai1
(1.College of Furnishings and Industrial Design,Nanjing Forestry University,Nanjing 210037,China;2.Jiangsu Wei Xin Engineering Consultants Co.Ltd.,Nanjing 210014,China;3.State Key Laboratory of Engines,Tianjin University,Tianjin 415400,China)
In order to study the industrial-scale nano titanium dioxide (TiO2) hydrophobic modification process,the low cost nontoxic tetrabutyl titanate,stearic acid and anhydrous ethanol were chosen as raw materials.Through the analysis of the optical contact angle data,the process for preparing the nano titanium dioxide superhydrophobic composite material with the optimal water contact angle was obtained: 0.2 g nano titanium dioxide and 70 mL anhydrous ethanol were mixed and ultrasonically dispersed for 1 h.Then,1 g stearic acid was added into the mixed liquid,and the ultrasonic dispersion was carried out again for 30 min.Thereafter,the mixed liquid was stirred first at 70℃ for 12 h and then at room temperature for 6 h.Finally,the same volume of anhydrous alcohol was added into the mixture,and the supernatant was removed by centrifugation.The residue was dried in an oven at 120℃.The water contact angle of the hydrophobic material obtained was 166°.The process is simple and cost-effective,and the product shows good hydrophobicity.It is suitable for industrial application and has great commercial value.The underlying mechanism was investigated by using Fourier transform infrared spectroscopy (FT-IR),field emission scanning electron microscopy (SEM) and so on,and the results showed that stearic acid was chemically adsorbed on the surface of the material.
modification process;nano TiO2;hydrophobic modification;stearic acid;super hydrophobic
TS664
A
2096-1359(2017)05-0031-05
2016-11-16
2017-01-07
江苏省2016年度普通高校研究生实践创新计划项目(SJLX16-0360);中国博士后特别资助项目(2014T70529)。
曹坤丽,女,研究方向为家具材料改性与性能开发。
吴燕,女,副教授。E-mail:30887772@qq.com

