咪唑离子液体氯化物水溶液的密度、折光率和体积性质
唐 静,金利华,李淑妮,翟全国,蒋育澄,胡满成,张黎明
(1.陕西国际商贸学院医药学院,陕西 西安 710246;2.陕西师范大学化学化工学院,陕西 西安 710062;3.西北有色金属研究院,陕西 西安 710016)
咪唑离子液体氯化物水溶液的密度、折光率和体积性质
唐 静1,2,金利华3,李淑妮2*,翟全国2,蒋育澄2,胡满成2,张黎明1
(1.陕西国际商贸学院医药学院,陕西 西安 710246;2.陕西师范大学化学化工学院,陕西 西安 710062;3.西北有色金属研究院,陕西 西安 710016)
常压下,测定了咪唑离子液体氯化物([C2mim]Cl、[C4mim]Cl、[C6mim]Cl、[C8mim]Cl)与水的二元混合溶液在288.15 K、298.15 K、308.15 K下的密度和折光率,计算获得了过量摩尔体积和折光率偏差,并用Redlich-Kister方程对衍生性质数据进行拟合,通过过量摩尔体积研究了二元混合溶液中离子液体与水分子之间的相互作用,同时采用多项式方程对二元混合溶液的密度及折光率随组成的变化进行了拟合。结果表明,二元混合溶液的密度和折光率随离子液体质量分数的增加而增大,随离子液体阳离子烷基链的增长、温度的升高而减小;二元混合溶液的过量摩尔体积为负值而折光率偏差为正值;离子液体与水分子之间具有较强的相互作用。
咪唑;离子液体;密度;折光率;过量摩尔体积;折光率偏差
离子液体作为目前最受关注的三大绿色溶剂(离子液体、超临界CO2和双水相)之一,又被称为“液体分子筛”,具有蒸气压低、不挥发、液程宽、溶解性好等独特性能,被广泛应用于催化合成、分离萃取等领域[1-3]。2002年,Rogers课题组[4]报道了1-丁基-3-甲基咪唑氯盐离子液体对纤维素具有较好的溶解能力,离子液体作为绿色溶剂为纤维素资源的利用提供了新的选择;此外,基于水及一些传统有机溶剂与离子液体互不相溶而形成可调控的两相溶液体系在生物活性物质的萃取应用也引起了人们的广泛关注[5-7]。但是由于构成离子液体的离子间存在较强的静电作用,导致其具有极性[8],且其黏度较传统有机溶剂大,从动力学方面来看影响了溶质的扩散。如果将小分子溶剂(如水或醇)加入到离子液体中使其成为黏度较小的混合溶剂将会拓宽离子液体在传输方面的应用。
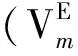
1 实验
1.1 试剂与仪器
氯化1-乙基-3-甲基-咪唑离子液体([C2mim]Cl)、氯化1-丁基-3-甲基-咪唑离子液体([C4mim]Cl)、氯化1-己基-3-甲基-咪唑离子液体([C6mim]Cl)、氯化1-辛基-3-甲基-咪唑离子液体([C8mim]Cl)均由上海成捷离子液体有限公司提供,质量分数≥99%,使用前于60 ℃真空干燥箱中干燥48h,保存在硅胶干燥器中。实验用水为二次蒸馏水。
DMA4500型密度仪(精确度±1×10-5g·cm-3,控温精度±0.02 ℃)、RXA170型折光率仪(精确度±4×10-5,控温精度±0.02 ℃),奥地利AntonPaar公司;AL204型电子天平(精确度±0.0001g),上海梅特勒-托利多公司;YS-10A型超纯水机(25 ℃时水电阻率≥18.2MΩ·cm),上海摩科科技集团。
1.2 方法
采用直接称重法配制质量分数(ωIL)分别为0.0、0.1、0.2、0.3、0.4、0.5、0.6、0.7、0.8的系列咪唑离子液体氯化物水溶液。将配制好的二元混合溶液用封口膜封好后固定在半微量相平衡装置的载样盘上旋转搅拌24 h使之混合均匀,静置。在温度为288.15 K、298.15 K和308.15 K下分别用密度计和折光率仪测定二元混合溶液的密度和折光率,平行测定3次,取平均值。密度计和折光率仪在使用前用二次蒸馏水和干燥空气在常压下进行校正。
2 结果与讨论
2.1 [Cnmim]Cl(n=2、4、6、8)+H2O二元混合溶液的密度及折光率
离子液体[Cnmim]Cl(n=4、6、8)在288.15 K、298.15 K、308.15 K下的密度及折光率列于表1。
表1 离子液体[Cnmim]Cl(n=4、6、8)在288.15 K、298.15 K、308.15 K下的密度及折光率

Tab.1 Density and refractive index of ionic liquid [Cnmim]Cl(n=4,6,8) at 288.15 K,298.15 K,and 308.15 K
注:括号内为文献值。
从表1可以看出,实验值与文献值基本一致,实验数据比较可靠。离子液体的密度随着阳离子烷基链的增长而减小,这是由于有机阳离子烷基链越长其体积越大,离子液体的密度相应越小。离子液体的密度随着温度的升高而减小,这符合温度对一般液体密度的影响规律,温度升高粒子间的距离增大、体积膨胀,从而导致密度减小[9]。
[Cnmim]Cl(n=2、4、6、8)+H2O二元混合溶液在288.15 K、298.15 K和308.15 K下的密度及折光率列于表2,二元混合溶液的密度及折光率与温度、离子液体质量分数之间的关系如图1所示。
表2 [Cnmim]Cl(n=2、4、6、8)+H2O二元混合溶液在288.15 K、298.15 K和308.15 K下的密度及折光率
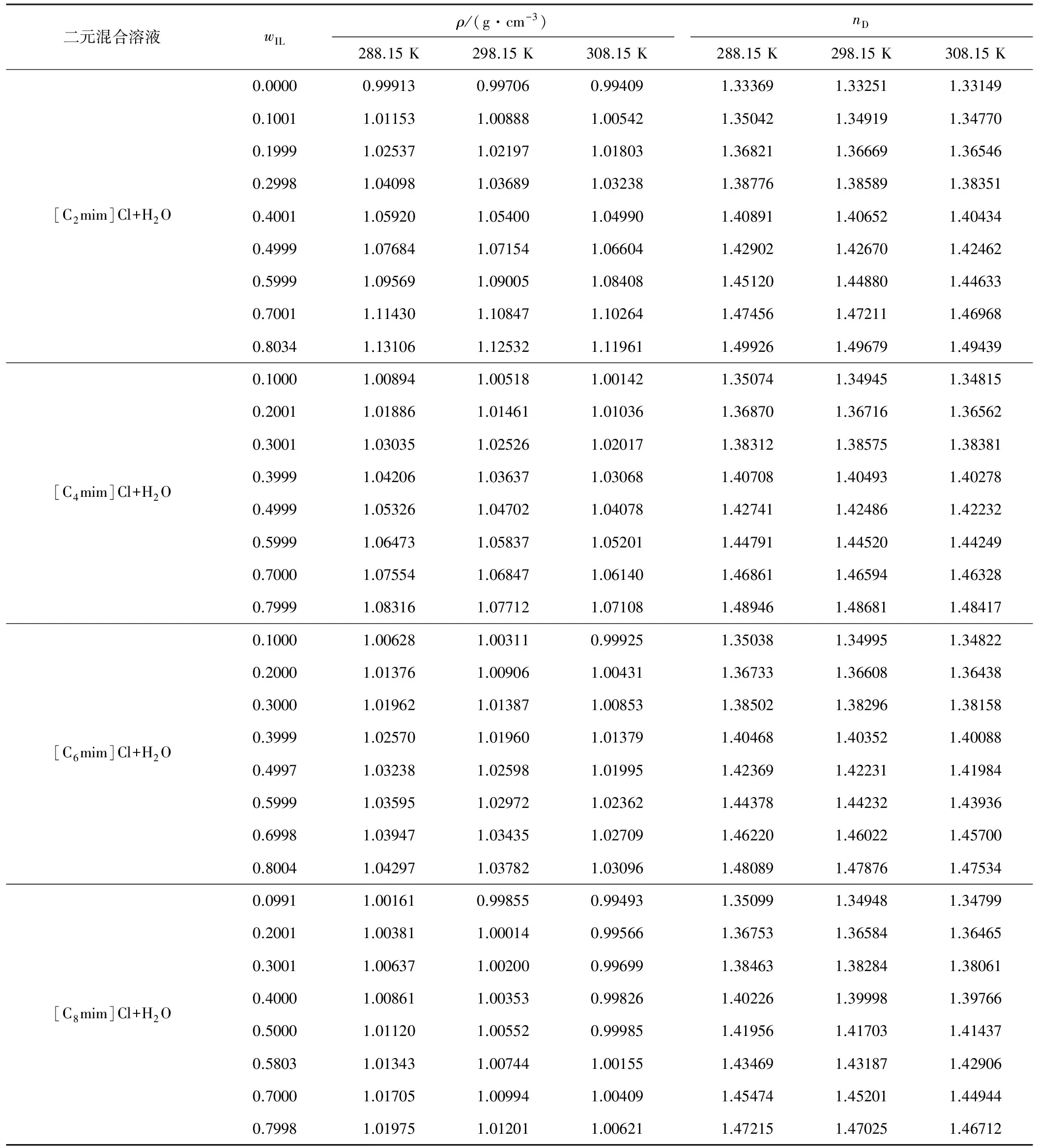
Tab.2 Density and refractive index of the binary mixture solution [Cnmim]Cl(n=2,4,6,8)+H2O at 288.15 K,298.15 K,and 308.15 K
从图1可以看出:(1)二元混合溶液的密度及折光率均随着离子液体质量分数的增加平稳增大,这是因为离子液体[Cnmim]Cl(n=2、4、6、8)密度比纯水略大。(2)随着离子液体阳离子烷基链的增长,二元混合溶液的密度及折光率均逐渐减小,其变化趋势为[C2mim]Cl>[C4mim]Cl>[C6mim]Cl>[C8mim]Cl,
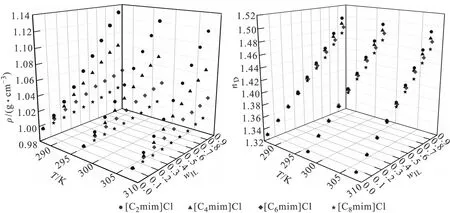
图1 [Cnmim]Cl(n=2、4、6、8)+H2O二元混合溶液的密度及折光率与温度、离子液体质量分数之间的关系
与纯离子液体的密度变化趋势一致[13]。这是因为,烷基链增长使离子液体分子体积增大,分子间距离增大,有效堆积程度降低。(3)二元混合溶液的密度及折光率均随着温度的升高而减小,这是由于温度升高,离子液体和水的体积均有不同程度膨胀,导致其混合溶液密度及折光率减小;此外升高温度引起分子间作用力改变,分子间距离增大,二元混合溶液的密度及折光率减小。
为了更好地描述离子液体质量分数与密度、折光率的关系,采用四参数经验方程对实验数据进行拟合[14]:
(1)
式中:Y为平衡时溶液的密度或折光率;A、B、C、D为方程的回归参数。
采用最小二乘法对表2数据进行拟合,得到的回归参数及标准偏差(s)列于表3。
表3 由方程(1)拟合所得到的回归参数(A、B、C、D)及标准偏差
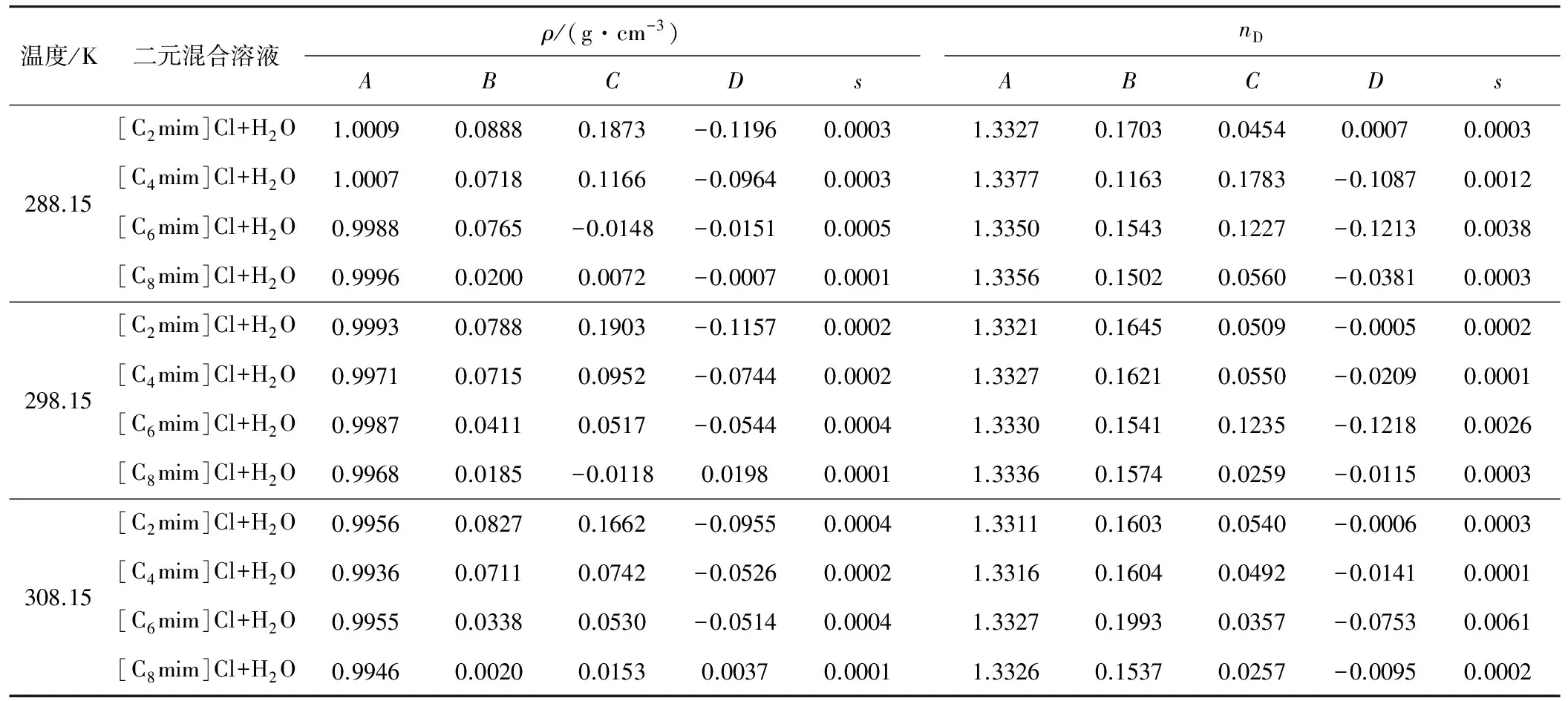
Tab.3 Regression parameters(A,B,C,D) and standard deviations by fitting of equation(1)
对四参数经验方程(1),当wIL为0时,A的理论值为纯水的密度值(或折光率值)。表3中的参数A与纯水的密度(288.15 K、298.15 K和308.15 K下纯水的密度分别为0.99913 g·cm-3、0.99706 g·cm-3和0.99409 g·cm-3)非常相近,说明该四参数经验方程适用于[Cnmim]Cl(n=2、4、6、8)+H2O二元混合溶液密度及折光率的计算。表3中的标准偏差均小于0.0061,说明实验数据是可靠的。
2.2 [Cnmim]Cl(n=4、6、8)+H2O二元混合溶液的过量摩尔体积
过量摩尔体积是指在温度、压强和组成一定的条件下,多个纯组分混合的真实溶液摩尔体积与理想溶液摩尔体积的差值。过量摩尔体积可以提供混合溶液中各组分分子之间相互作用信息,其值受各组分分子形状大小、各组分分子的重新取向及各组分分子间相互作用的影响。[Cnmim]Cl(n=4、6、8)+H2O二元混合溶液的过量摩尔体积可以用下式计算:
(2)
式中:MIL和MW分别为离子液体和水的摩尔质量;xIL和xW分别为离子液体和水的摩尔分数;ρ、ρIL和ρW分别为二元混合溶液、离子液体及水的密度。
图2是[Cnmim]Cl(n=4、6、8)+H2O二元混合溶液的过量摩尔体积随离子液体摩尔分数的变化曲线,图中实线表示Redlich-Kister多项式拟合得到的值,点表示实验值。
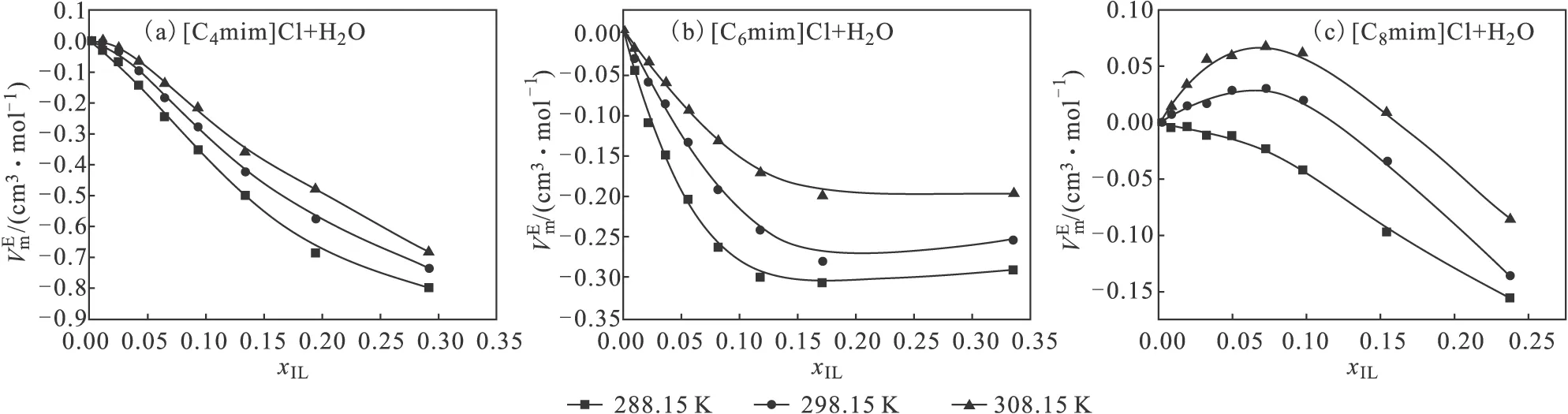
图2 [Cnmim]Cl(n=4、6、8)+H2O二元混合溶液的过量摩尔体积随离子液体摩尔分数的变化曲线
从图2可以看出:(1)二元混合溶液[C4mim]Cl+H2O、[C6mim]Cl+H2O和[C8mim]Cl+H2O的过量摩尔体积是负值,说明二元混合溶液体系中离子液体与水分子之间的相互作用起主要作用,混合溶液体积主要表现为压缩性质。[Cnmim]Cl(n=4、6、8)+H2O二元混合溶液表现出负的过量摩尔体积是由于体系内离子液体与水分子形成氢键所致。离子液体极性大于传统有机溶剂使其有较强的偶极矩和氢键作用;水作为一种高介电性质溶剂加入离子液体后会使其部分解离成离子,导致中性水分子与带电离子液体微粒间存在不对称力。随着水的加入,离子液体本身的网络结构被打破,溶液的局部组成可以理解为水分子与离子液体阴阳离子之间的氢键作用。(2)二元混合溶液的过量摩尔体积随着离子液体摩尔分数的增加而减小,这种现象说明二元混合溶液体系中除了存在[Cnmim]+-H2O、Cl--H2O间相互作用外,还存在着阴离子-阳离子间的相互吸引作用。(3)随着温度的升高,过量摩尔体积逐渐增大,即混合溶液体积收缩程度减弱使其偏离理想体积的程度减小。产生此结果的原因可能是:第一,水的介电常数随着温度的升高而减小,当温度从288.15 K升至308.15 K时,水的介电常数由81.82减小到74.80。具有高介电性质的水可以使离子液体部分解离成离子,从而导致中性水分子与带电的离子液体颗粒之间存在高度的不对称力。随着水的介电常数减小,离子液体的解离程度减小,离子液体更倾向于中性分子,水分子与离子液体间作用力减弱,导致二元混合溶液体系的过量摩尔体积随着温度的升高而增大。第二,温度升高使混合溶液中各种粒子的热运动加快,导致离子液体与水分子之间的氢键作用遭到破坏,对过量摩尔体积有正的贡献,所以温度较高时的过量摩尔体积比温度较低时的要大一些。第三,随着温度的升高,水与离子液体体积均有不同程度的膨胀,使得二元混合溶液的过量摩尔体积随着温度的升高而增大。
图3是298.15 K下离子液体阳离子烷基链长对[Cnmim]Cl(n=4、6、8)+H2O二元混合溶液过量摩尔体积的影响。
从图3可以看出,当离子液体的摩尔分数相同时,二元混合溶液过量摩尔体积随着离子液体阳离子烷基链的增长逐渐增大,即[C4mim]Cl<[C6mim]Cl<[C8mim]Cl。
二元混合溶液的过量摩尔体积随组成的变化可用Redlich-Kister多项式[15]进行拟合:
(3)
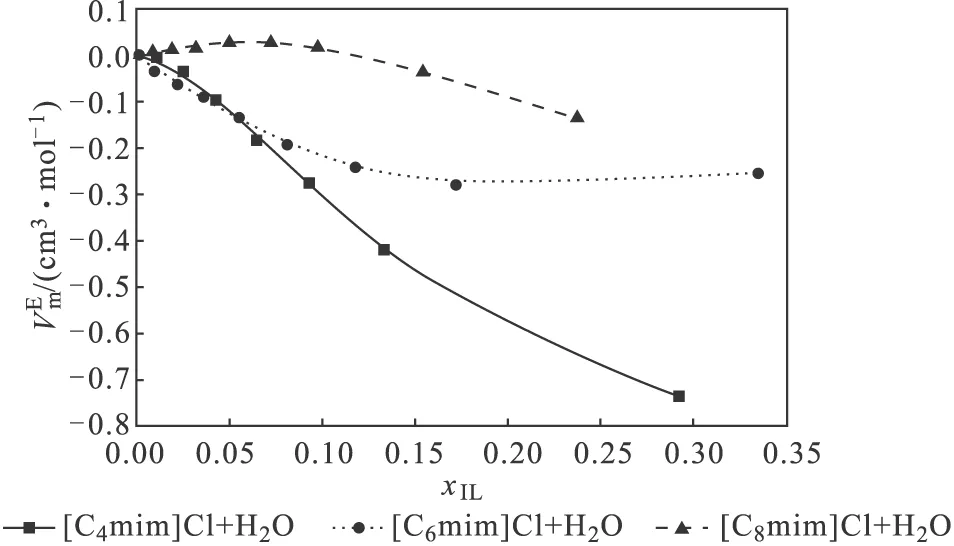
图3 298.15 K下离子液体阳离子烷基链长对[Cnmim]Cl(n=4、6、8)+H2O二元混合溶液过量摩尔体积的影响
式中:j为多项式的次数;Aj(j=0~4)为多项式的可调参数,可通过最小二乘法拟合得到。
采用Redlich-Kister多项式对二元混合溶液过量摩尔体积进行拟合,关联所得到的参数Aj及标准偏差列于表4。
从表4可以看到,拟合的标准偏差都很小,均在0.0066以下,说明Redlich-Kister多项式可以较好地关联[Cnmim]Cl(n=4、6、8)+H2O二元混合溶液的过量摩尔体积。
2.3 [Cnmim]Cl(n=6、8)+H2O二元混合溶液的折光率偏差
混合溶液的折光率和折光率偏差与溶液色散相互作用有着紧密联系[16],折光率偏差可用下式计算获得:
表4 采用Redlich-Kister多项式拟合[Cnmim]Cl(n=4、6、8)+H2O二元混合溶液所得到的参数Aj及标准偏差
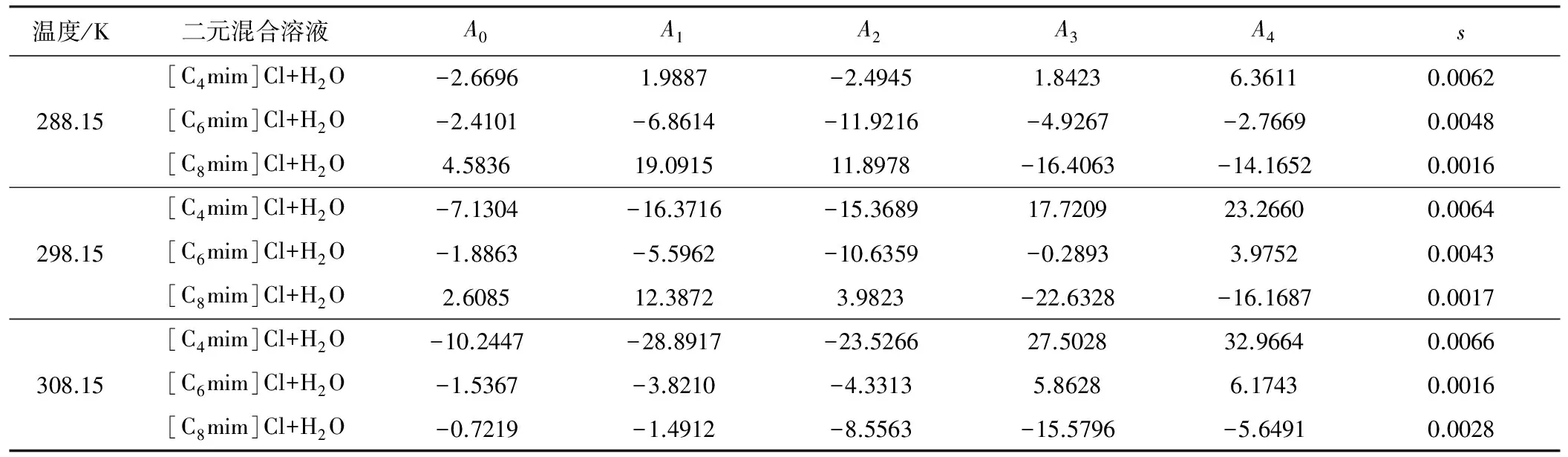
Tab.4 Parameter Aj and standard deviations by fitting of Redlich-Kister equation for the binary mixture solution [Cnmim]Cl(n=4,6,8)+H2O
(4)
式中:nDi为混合溶液组分i的折光率;xi为组分i的摩尔分数。
[Cnmim]Cl(n=6、8)+H2O二元混合溶液的折光率偏差随离子液体摩尔分数的变化曲线如图4所示。
从图4可以看出:(1)二元混合溶液[C6mim]Cl+H2O和[C8mim]Cl+H2O的折光率偏差均为正值,且随着离子液体摩尔分数的增加而增大,说明混合溶液中离子液体与水分子间的色散相互作用比纯组分的更高。(2)温度对二元混合溶液的折光率偏差影响较小。
3 结论
测定了常压下288.15K、298.15K、308.15K时4种咪唑离子液体氯化物([C2mim]Cl、[C4mim]Cl、[C6mim]Cl、[C8mim]Cl)与水的二元混合溶液的密度、折光率、过量摩尔体积和折光率偏差;并采用四参数方程对密度和折光率进行拟合,采用Redlich-Kister多项式对衍生性质数据进行拟合,通过过量摩尔体积研究了二元混合溶液中离子液体与水分子之间的相互作用。结果表明,二元混合溶液的密度和折光率随着离子液体质量分数的增加而增大,随着离子液体阳离子烷基链的增长、温度的升高而减小;二元混合溶液的过量摩尔体积为负值而折光率偏差为正值;离子液体与水分子之间具有较强的相互作用。该研究为[Cnmim]Cl(n=2、4、6、8)+H2O二元混合溶液的开发应用提供了基础数据。
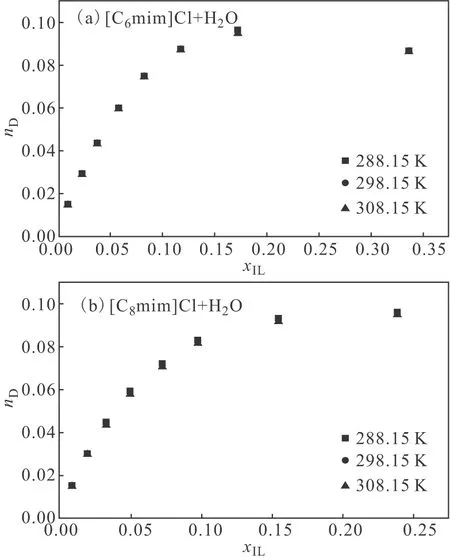
图4 [Cnmim]Cl(n=6、8)+H2O二元混合溶液折光率偏差随离子液体摩尔分数的变化曲线
[1] 胡应喜,张彧,潘欣欣.氯铝酸型离子液体催化合成环己酮(苯甲醛)乙二醇缩酮(醛)[J].化学与生物工程,2015,32(10):42-44.
[2] WANG Z,PEI Y,ZHAO J,et al.Formation of ether-functionalized ionic-liquid-based aqueous two-phase systems and their application in separation of protein and saccharides[J].The Journal of Physical Chemistry B,2015,119(12):4471-4478.
[3] YANG X,ZHANG S,YU W,et al.Ionic liquid-anionic surfactant based aqueous two-phase extraction for determination of antibiotics in honey by high-performance liquid chromatography[J].Talanta,2014,124:1-6.
[4] SWATLOSKI R P,SPEAR S K,HOLBREY J D,et al.Dissolution of cellose with ionic liquids[J].Journal of the American Chemical Society,2002,124(18):4974-4975.
[5] 巩育军,牛盛童,黄学锋,等.离子液体双水相萃取山楂黄酮和多糖的研究[J].化学与生物工程,2014,31(7):27-29.
[6] PRATIWI A I,YOKOUCHI T,MATSUMOTO M,et al.Extraction of succinic acid by aqueous two-phase system using alcohols/salts and ionic liquids/salts[J].Separation and Purification Technology,2015,155:127-132.
[7] 李兰杰,李绪文,丁健,等.超声辅助结合离子液体双水相提取-高效液相色谱法测定三七中5种稀有人参皂苷的含量[J].高等学校化学学报,2016,37(3):454-459.
[8] WAKAI C,OLEINIKOVA A,OTT M,et al.How polar are ionic liquids?Determination of the static dielectric constant of an imidazolium-based ionic liquid by microwave dielectric spectroscopy[J].The Journal of Physical Chemistry B,2005,109(36):17028-17030.
[9] 郭斌,高亮,段二红,等.[bmim][BF4]、[bmim][PF6]离子液体及其与DMF二元体系在293.15~353.15 K下的密度和体积性质[J].河北科技大学学报,2012,33(2):135-141.
[10] KUMAR B,SINGH T,KUMAR A,et al.Thermodynamic and spectroscopic studies on binary mixtures of imidazolium ionic liquids in ethylene glycol[J].The Journal of Chemical Thermodynamics,2012,43(1):121-127.
[11] GOMEZ E,GONZALEZ B,DOMINGUEZ A,et al.Dynamic viscosities of a series of 1-alkyl-3-methylimidazolium chloride ionic liquids and their binary mixtures with water at several temperatures[J].Journal of Chemical and Engineering Data,2006,51(2):696-701.
[12] HUDDLESTON J G,VISSER A E,REICHERT W M,et al.Characterization and comparison of hydrophilic and hydrophobic room temperature ionic liquids incorporating the imidazolium cation[J].Green Chemistry,2001,3(4):156-164.
[13] SU W C,CHOU C H,WONG D S H,et al.Diffusion coefficients and conductivities of alkylimidazolium tetrafluoroborates and hexafluorophosphates[J].Fluid Phase Equilibria,2007,252(1):74-78.
[14] CARTON A,SOBRON F,BOLADO S,et al.Composition and density of saturated solutions of lithium sulfate+water+methanol[J].Journal of Chemical and Engineering Data,1994,39(1):61-62.
[15] IVANIS G R,VUKSANOVIC J,CALADO M S,et al.Liquid-liquid and solid-liquid equilibria in the solutions of poly(ethylene glycol) with several organic solvents[J].Fluid Phase Equilibria,2012,316:74-84.
[16] PINEIRO A,BROCOS P,AMIGO A,et al.Prediction of excess volumes and excess surface tensions from experimental refractive indices[J].Physics and Chemistry of Liquids,2000,38(2):251-260.
版权声明
为适应我国信息化建设,扩大本刊及作者知识信息交流渠道,本刊已被《中国学术期刊网络出版总库》及CNKI系列数据库、《万方数据——数字化期刊群》、《中文科技期刊数据库(全文版)》、超星域出版平台、《台湾华艺数据库》等收录。如作者不同意论文被收录,请在来稿时向本刊声明,本刊将作适当处理。
《化学与生物工程》编辑部
Density,Refractive Index and Volume Propertyof Imidazolium Chloride Ionic Liquid Aqueous Solution
TANG Jing1,2,JIN Li-hua3,LI Shu-ni2*,ZHAI Quan-guo2,JIANG Yu-cheng2,HU Man-cheng2,ZHANG Li-ming1
(1.SchoolofMedicine,ShaanxiInstituteofInternationalTrade&Commerce,Xi′an710246,China;2.SchoolofChemistry&ChemicalEngineering,ShaanxiNormalUniversity,Xi′an710062,China;3.NorthwestInstituteforNonferrousMetalResearch,Xi′an710016,China)
Wemeasureddensityandrefractiveindexofthebinarymixturesolutionofimidazoliumchlorideionicliquid([C2mim]Cl,[C4mim]Cl,[C6mim]Cl,[C8mim]Cl)withwateratatmosphericpressureand288.15K,298.15K,and308.15K,respectively.Wecalculatedexcessmolarvolumeandrefractiveindexdeviation,usedRedlich-Kisterequationtofitthederivativepropertydata,andinvestigatedtheinteractionbetweenionicliquidandwaterbyexcessmolarvolume.Additionally,wefittedthevariationofdensityandrefractiveindexwiththecompositionofthebinarymixturesolutionbypolynomialequation.Theresultsshowedthat,thedensityandrefractiveindexincreasedwiththeincreaseofmassfractionofionicliquid,anddecreasedwiththeincreaseofionicliquidcationalkylchainlengthandtemperature.Thevaluesofexcessmolarvolumewerenegative,butthevaluesofrefractiveindexdeviationwerepositive.Therewasastronginteractionbetweenionicliquidandwater.
imidazole;ionicliquid;density;refractiveindex;excessmolarvolume;refractiveindexdeviation
国家自然科学基金项目(21571120,21301114),陕西省教育厅专项科研计划项目(16JK2036),2016陕西省大学生创新创业训练计划项目(2958),陕西国际商贸学院校级课题(SMXY201605),陕西国际商贸学院人才引进科研启动经费项目
2017-03-27
唐静(1982-),女,陕西西安人,讲师,博士研究生,研究方向:溶液化学,E-mail:tangjing224@126.com;通讯作者:李淑妮,副教授,E-mail:lishuni@snnu.edu.cn。
10.3969/j.issn.1672-5425.2017.08.008
TQ013.1
A
1672-5425(2017)08-0037-07
唐静,金利华,李淑妮,等.咪唑离子液体氯化物水溶液的密度、折光率和体积性质[J].化学与生物工程,2017,34(8):37-43.

