六水合三氯化铁中亚铁的检测方法探讨
白晓光,王正达,邬旭东,段书芬,刘爱华,程 晓
(1.上海拱极化学有限公司,上海 201302; 2.青岛国风药业股份有限公司,山东 青岛 266000)
·检验检测·
六水合三氯化铁中亚铁的检测方法探讨
白晓光1,王正达1,邬旭东1,段书芬1,刘爱华1,程 晓2
(1.上海拱极化学有限公司,上海 201302; 2.青岛国风药业股份有限公司,山东 青岛 266000)
目的 建立测定六水合三氯化铁中亚铁含量的分光光度法。方法 通过比较欧洲药典、美国药典和中国化工行业《化学试剂六水合三氯化铁(三氯化铁)》(HG/T3474-2014)等资料中关于六水合三氯化铁中亚铁的检测方法,发现后2个方法不易操作。以欧洲药典为基础,拟订了用H3PO4掩蔽Fe3+、用分光光度法检测Fe2+的方法,并用样品对方法进行了验证。结果与结论 所建立的分光光度法容易操作、重复性好。
亚铁离子;六水合三氯化铁;分光光度法;质量控制
六水合三氯化铁作为制药原料,早已被英国药典、欧洲药典(2008)和美国药典(2015)所收录,其中都有关于质量标准和检测方法的详细论述。六水合三氯化铁至今尚未被中国药典收录,但已被国内许多制药企业广泛用作制药原料。关于其质量指标和检测方法,国内各制药企业都有自己的企业标准,但因各企业质检人员的理解不同而有所差异,且检测方法也不尽相同。关于六水合三氯化铁中亚铁含量的测定方法,国内外基本分为2种,一是以美国化学会(ACS)为代表的铁氰化钾直接显色法,二是以欧洲药典为代表的磷酸掩蔽-铁氰化钾显色法。本研究中就这2种方法作了详细探讨,并据此提出了检测六水合三氯化铁中亚铁含量的分光光度法。现报道如下。
1 仪器与试药
1.1 仪器
722型分光光度计(上海菁华科技仪器有限公司)。
1.2 试药
铁氰化钾(上海强顺化学试剂有限公司,批号为1401107),5%的铁氰化钾溶液要在试验当日配制;磷酸(上海凌峰化学试剂有限公司,批号为20151009);七水合硫酸亚铁(FeSO4·7H2O,国药集团化学试剂有限公司,批号为10012118)。
Fe2+质量浓度为0.1 g/L的贮备液(称取0.250 g FeSO4·7H2O,加H2SO45 mL溶解并稀释至500 mL容量瓶中);Fe2+质量浓度为0.01 g/L的溶液(取10 mL Fe2+质量浓度为0.1 g/L的贮备液,稀释至100 mL容量瓶中,现配现用)。
六水合三氯化铁溶液(FeCl3·6H2O,国药集团化学试剂有限公司,批号为10011918);盐酸(国药集团化学试剂有限公司,批号为10011018)。
2 方法与结果
2.1 方法的原理
K3Fe(CN)6溶液和二价铁盐作用,立即生成滕氏蓝沉淀,其组成为Fe3[Fe(CN)6]2,此时三价铁不会发生干扰,因Fe3+与K3Fe(CN)6仅仅生成淡绿褐色溶液,况且又用H3PO4将Fe3+络合掩蔽了,使其无色。化学反应式如下:
3FeCl2+2K3Fe(CN)6→Fe3[Fe(CN)6]2+6KCl
2.2 方法的建立
2.2.1 ACS的检测方法
方法:称取样品0.5 g,溶于20 mL盐酸(1→19),再加入0.05 mL新配制的5%K3Fe(CN)6,若在1 min内未出现蓝绿色,则认为该样品的 Fe2+含量不大于0.002%。
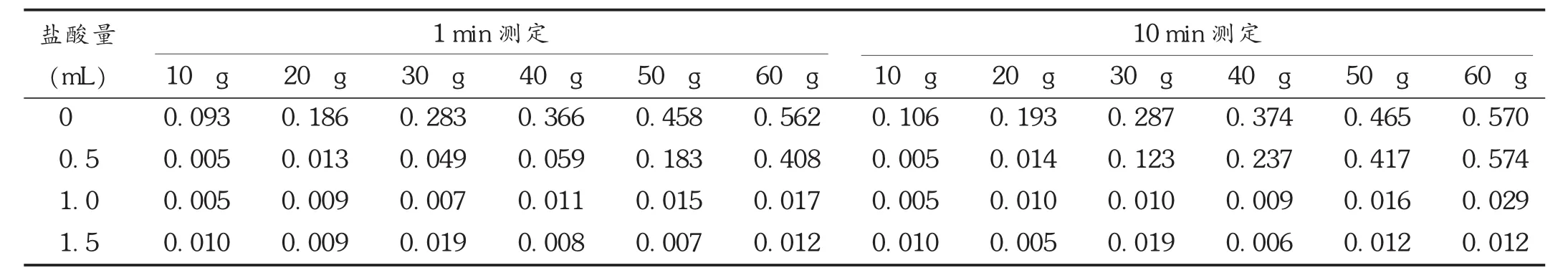
表1 1 min和10 min时不同亚铁含量条件下的吸光度
探索试验一:取不同量的Fe2+,加不同量的盐酸,加入2滴5%K3Fe(CN)6,于1 min和10 min时测定显色后的吸光度。入射光波长为黄色(λ=570 nm),比色皿长度为5 mm,用722型分光光度计测定。结果见表1。可见,当在25 mL试液中加入1 mL盐酸后基本上都不显色,尤其Fe2+含量低至10 μg时吸光度更低,这种情况下靠目测无法辨别。

表2 不同条件下亚铁的吸光度
探索试验二:按以下条件进行试验。条件 A,取10 μg Fe2+标准液,不加盐酸,稀释至25 mL,加1滴5% K3Fe(CN)6;条件B,取10 μg Fe2+标准液,加1 mL盐酸,稀释至25 mL,加1滴5%K3Fe(CN)6;条件C,取50 μg Fe2+标准液,加 1 mL盐酸,稀释至25 mL,加 1滴 5% K3Fe(CN)6;条件 D,取 0.5 g FeCl3·6H2O,加 1 mL盐酸,稀释至25 mL,不加 K3Fe(CN)6;条件E,取0.5 g FeCl3·6H2O,加1 mL盐酸,稀释至25 mL,加1滴5% K3Fe(CN)6。用722型分光光度计测定溶液吸光度,结果见表2。可见,在1 mL盐酸存在条件下,不仅10 μg Fe2+标准液的吸光度极低,就连50 μg Fe2+标准液的吸光度也低于0.02,但样品溶液(条件E)的吸光度(>0.2)是如何产生的。这就是ACS法的最大问题。另外,没有蓝绿色,也不能肯定Fe2+含量不大于0.002%,这么少量的Fe2+(10 μg)靠目测,随意性太大,这是ACS法的第2个问题。而且,由于三价铁的颜色太深,检测取样量也不能过大。
2.2.2 中国化工行业标准的检测方法
方法:中国化工行业标准中六水合三氯化铁的质量指标和检测方法[1],基本上是由ACS法演变而来。称取0.5 g样品,溶于 20 mL无氧水中,加入1 mL盐酸及1滴新配制的5%K3Fe(CN)6,摇匀,放置10 min,溶液所呈蓝绿色不得深于标准比色溶液。其中,标准比色溶液的配制是称取0.5 g不含亚铁的六水合三氯化铁(按上述方法操作,溶液不呈现蓝绿色)及0.01 mg Fe2+(分析纯)或0.025 mg Fe2+(化学纯)的亚铁(Fe2+)标准溶液,与样品同时同样处理。
问题:该方法的缺点首先是沿用了ACS法的1 mL盐酸,其次是取样量太少,第三是要采用不含亚铁的六水合三氯化铁。不含亚铁的六水合三氯化铁难以找到。ACS法认为,不出现绿色仅表明亚铁含量不大于0.002%,并不是不含亚铁。而且笔者的试验显示,不出现蓝绿色,样品中亚铁的含量仍可能大于0.002%甚至更高,只是目测测不出。
2.2.3 欧洲药典的检测方法
方法(磷酸掩蔽-铁氰化钾显色法):往10 mL样品溶液(内含1 g样品)中,加入1 mL H2O和1滴5%K3Fe(CN)6溶液,接着加入4 mL H3PO4。10 min后,试液中的蓝色不应深于标准溶液。标准溶液为1 mL新鲜配制的硫酸亚铁溶液(0.25 g/L的FeSO4·7H2O)和10 mL H2O,与样品同时同样处理。
分析欧洲药典的检测方法,用H3PO4掩蔽了三氯化铁,方法简单、明确。但若用分光光度计来检测,还应配制样品空白溶液,即将样品(FeCl3·6H2O)溶液与同样的H3PO4混合即可。计算亚铁含量时,应从样品溶液的吸光度中减去样品空白溶液的吸光度。
2.2.4 H3PO4掩蔽Fe3+试验
于4个比色管中各加入1 g FeCl3·6H2O和25 mLH2O,再分别加入4,6,8,10 mL H3PO4,摇匀,测定吸光度。结果见表 3。可见,10 mL H3PO4的掩蔽效果最好。为了节约H3PO4,以及与欧洲药典方法尽量保持一致,笔者选择了 8 mL H3PO4(加 H3PO4前的溶液体积为25 mL),而欧洲药典方法在加4 mL H3PO4前的溶液体积为11 mL。

表3 H3PO4掩蔽Fe3+试验的吸光度结果( =570 nm,h=50 mm)
2.2.5 分光光度法检测亚铁含量
根据欧洲药典方法拟订了六水合三氯化铁中亚铁的检测方法。取4个50 mL的比色管,编号为A,B,C,D,往A管、D管中加入50 μg Fe2+标准溶液;往B管、C管、D管中各加1 g样品,用少量H2O溶解;将4管溶液用H2O稀释至25 mL,摇匀;往A管、C管、D管中各加2滴5%K3Fe(CN)6溶液,摇匀;再往4管中各加8 mL H3PO4,摇匀[其中D管只起到监督样品的作用,其颜色必须深于 A管,否则样品中可能有氧化剂(如Cl2)存在,若已知样品中无氧化剂则可不用D管]。10 min后,用722型分光光度计测定吸光度 λ=570 nm,h=50 mm,按以下公式计算样品中亚铁的含量:

2.3 验证试验
取国药集团化学试剂有限公司FeCl3·6H2O样品,按2.2.5项下方法测定,结果见表4。
由于50 μg Fe2+标准溶液和样品溶液的吸光度随时间变化而变化,故应人为规定取值时间,仍以欧洲药典的10 min为准。按公式一计算,即得样品中亚铁的含量。
3 讨论
样品中Fe2+的含量在要求很严的情况下,如Fe2+不能大于50×10-6,甚至不能大于20×10-6时,应考虑到六水合三氯化铁并不是很稳定。六水合三氯化铁是相当强的氧化剂,并且很活跃,有比较明显的歧化现象。在电炉上直接加热其水溶液,甚至用滤纸滤布、PP微孔滤膜滤过其热溶液都会产生Fe2+。六水合三氯化铁尤其对光线比较敏感,光照下很容易发生歧化现象,自动产生亚铁。如将Fe2+含量为0.002%的六水合三氯化铁装于试管中,在室外放置 10 d后,Fe2+含量变为0.22%,可增加100倍。因此,其产品的包装、贮存就显得很重要,要绝对避光保存,才能使亚铁不再产生或增速减缓。检验产品中亚铁含量时,应新打开包装,不要从已打开包装多时的产品取样。如果生产时亚铁检测要求很严,也尽量不要采用打开包装多时的六水合三氯化铁。
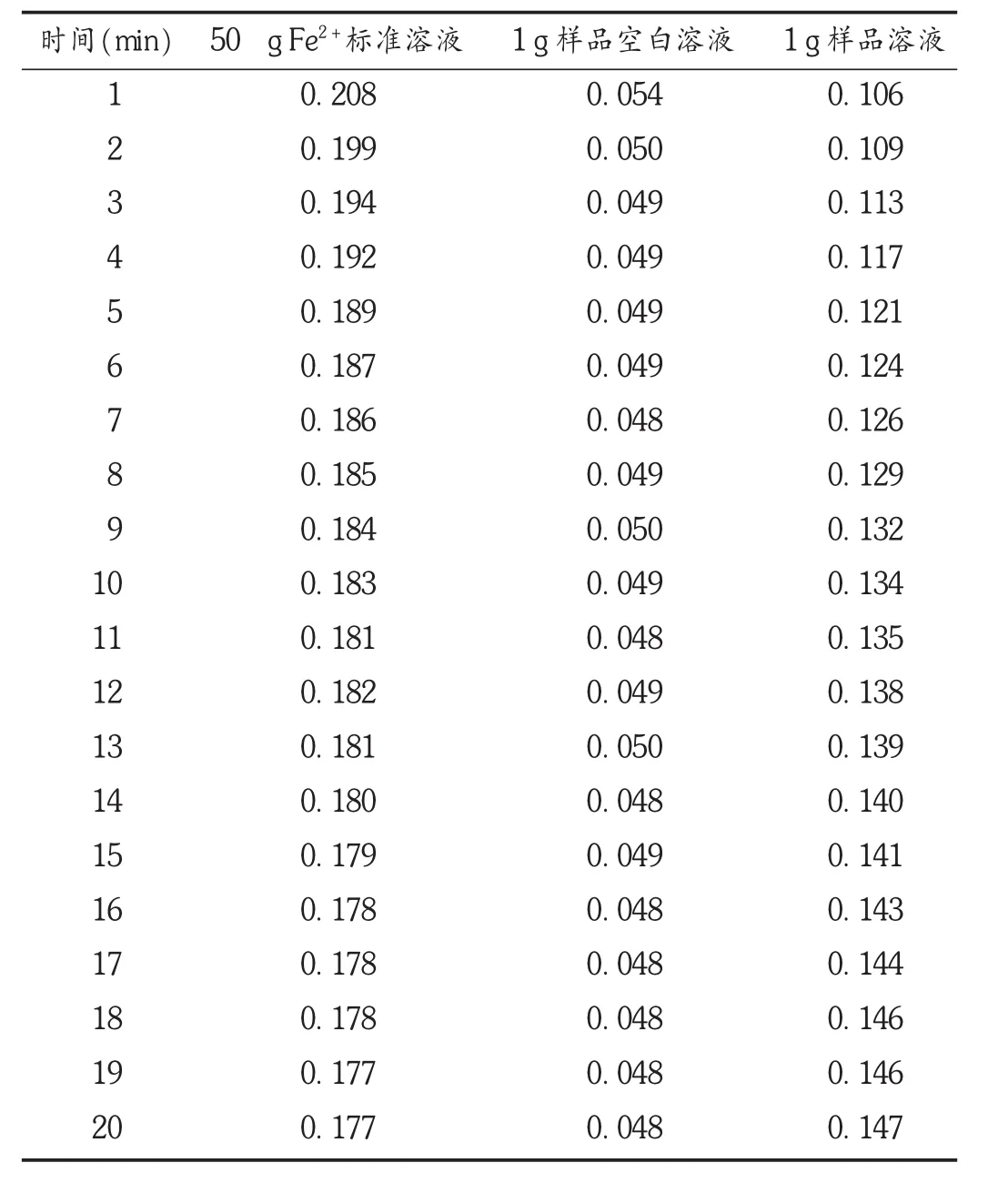
表4 验证试验结果(吸光度)
欧洲药典的检测方法中取50 μg Fe2+标准溶液,是ACS法(10 μg)的5倍,呈现的蓝绿色很明确,目测时不存在似是而非、模棱两可的感觉,用分光光度计测定吸光度也很可靠。
欧洲药典的检测方法巧妙地采用H3PO4掩蔽三价铁的颜色,消除了FeCl3的底色,与无FeCl3的标准溶液基本上处同一颜色水平,用两者比较蓝绿色,更容易、更明确、更合理。
用H3PO4掩蔽三价铁、分光光度法测定亚铁离子的含量,可以半定量地计算出亚铁的含量。因此,本研究中建立的方法可更明确地检测六水合三氯化铁中亚铁含量是否达标。
[1]HG/T3474-2014,化学试剂六水合三氯化铁(三氯化铁)[S].
Determination of Ferrous Iron in Ferric Chloride Hexahydrate
Bai Xiaoguang1,Wang Zhengda1,Wu Xudong1,Duan Shufen1,Liu Aihua1,Cheng Xiao2(1.Shanghai Gongji Chemical Co.,Ltd.,Shanghai,China 201302; 2.Qingdao Guofeng Pharmaceutical Co.,Ltd.,Qingdao,Shandong,China 266000)
Objective To establish a spectrophotometric method for the determination of ferrous iron in ferric chloride hexahydrate.Methods The detection methods on ferrous iron in ferric chloride hexahydrate among European Pharmacopoeia,United States Pharmacopoeia and Chemical Reagent Ferric Chloride Hexahydrate(HG/T3474-2014)of China′s Chemical Industry were compared.The last twomethodswerenoteasy tooperation.On the basisof the European Pharmacopoeia,a method wasproposed thatafter Fe3+were screened with H3PO4,Fe2+wasmeasured by spectrophotometry,and the method wasverified by experiments.Resultsand Conclusion The spectrophotometry method is easy to operate and has good reproducibility.
ferrous ion;ferric chloride hexahydrate;spectrophotometry;quality control
R927.1
A
1006-4931(2017)16-0029-03
2017-03-15)
10.3969/j.issn.1006-4931.2017.16.009
白晓光(1937-),男,高级工程师,研究方向为铁化学,(电子信箱)languanghuaxue@126.com。

