替格瑞洛对阿托伐他汀治疗急性冠脉综合征的影响
赵雪银 王晓 严研 范婧尧 聂绍平
作者单位:100071 北京市,北京大学第一医院北京丰台医院CCU(赵雪银);首都医科大学附属北京安贞医院急诊危重症中心(王晓、严研、范婧尧、聂绍平)
替格瑞洛对阿托伐他汀治疗急性冠脉综合征的影响
赵雪银 王晓 严研 范婧尧 聂绍平
作者单位:100071 北京市,北京大学第一医院北京丰台医院CCU(赵雪银);首都医科大学附属北京安贞医院急诊危重症中心(王晓、严研、范婧尧、聂绍平)
目的 观察对CYP3A4酶有抑制作用的替格瑞洛联合经CYP3A4酶代谢的阿托伐他汀治疗急性冠脉综合征(ACS)短期内的安全性及对降脂作用的影响。方法 共收集ACS患者244例,随机分为阿托伐他汀+替格瑞洛组(以下简称为替格瑞洛组)和阿托伐他汀+氯吡格雷组(以下简称为氯吡格雷组)。收集入院24 h内和出院后1个月内胆固醇(TC)、甘油三酯(TG)、低密度脂蛋白胆固醇(LDL-C)、丙氨酸转氨酶(ALT)、天门冬氨酸转氨酶(AST)、肌酸激酶(CK)及血清肌酐(Scr)水平,同时计算LDL-C达标率。结果 替格瑞洛组在肝功能损害、肌肉毒性及肾功能损害的发生率上均高于氯吡格雷组(2.8%比0.7%,1.9%比0.7%,4.47%比3.04%),但均未见统计学差异。替格瑞洛组LDL-C达标率为53.3%,明显高于氯吡格雷组的38.0%(P=0.017,P<0.05)。在降低TC、TG水平上,替格瑞洛组要略优于氯吡格雷组(18.09%比17.93%,6.23%比2.58%),但未见统计学差异(P>0.05)。结论 短期内替格瑞洛对经肝酶CYP3A4代谢的阿托伐他汀的安全性影响较小,且使用相同剂量的阿托伐他汀,替格瑞洛组在LDL-C达标率上更有优势。
阿托伐他汀; 替格瑞洛; CYP3A4; 急性冠脉综合征; 肝功能损害; 肌肉毒性; 低密度脂蛋白胆固醇
在ACS患者的治疗中,抗血小板及降脂、稳定斑块是基本并且重要的治疗措施。羟甲基戊二酰辅酶A(HMG.CoA)还原酶抑制剂即他汀类药物良好的降脂疗效和心血管获益已被指南和大量证据反复证实[1]。随着他汀类药物在临床的广泛使用,其安全性也日益受到临床医生的重视。替格瑞洛作为一种新型的非噻吩吡啶类的二磷酸腺苷受体(P2Y12)拮抗剂,相比较氯吡格雷而言,起效更迅速,血小板抑制作用更加显著[2,3]。
他汀类药物中的阿托伐他汀主要经肝细胞色素P450(CYP450)3A4代谢,阿托伐他汀与对CYP3A4有抑制作用的药物合用时,可致阿托伐他汀血药浓度增加,而他汀类药物不良事件的发生率与剂量明显相关[4,5]。替格瑞洛口服后主要由肝酶CYP3A4转化生成活性代谢产物ARC124910XX和非活性代谢产物AR-C133913XX,替格瑞洛是CYP3A的底物,同时也是CYP3A酶的抑制剂或诱导剂[6,7]。有研究表明,同时服用阿托伐他汀和替格瑞洛可使前者的血浆药物峰浓度(Cmax)和血药浓度-时间曲线下面积(AUC)增加[8,9],从而有可能增加阿托伐他汀临床不良事件的发生率。
本研究通过收集急性冠脉综合征患者病例,比较常规剂量的阿托伐他汀分别与替格瑞洛及氯吡格雷联合应用时,短期内临床使用的安全性,同时进一步了解对血脂水平变化的影响。
1 对象与方法
1.1 研究对象 连续入选2016年1月至2016年6月北京安贞医院急诊科收治的ACS患者共244例。入选标准:符合2016年中国医师协会急诊医师分会、中华医学会心血管病学分会、中华医学会检验医学分会制定的急性冠脉综合征诊断标准[10],包括ST段抬高型心肌梗死(STEMI)、非ST段抬高型心肌梗死(NSTEMI)及不稳定型心绞痛(UA)。排除标准:①年龄>75岁。②任何原因的肝病史,无论目前伴或不伴有转氨酶升高。③既往任何原因的肌病史,确诊或可疑曾出现与他汀类药物相关的肌肉疼痛、肌肉无力症状,以及肌酸激酶升高。④具有抗血小板治疗禁忌证、血液疾病或伴有恶性肿瘤。⑤心功能Ⅲ~Ⅳ级。⑥严重肾功能不全。⑦既往服用或目前正在服用任何他汀类药物。⑧入院时LDL-C≤70 mg/dl(1.8 mmol/L)。
1.2 研究方法 入选患者随机分为阿托伐他汀+替格瑞洛组(以下简称为替格瑞洛组)和阿托伐他汀+氯吡格雷组(以下简称为氯吡格雷组)。两组患者均口服阿托伐他汀20 mg,1次/d。替格瑞洛组入院时给予替格瑞洛180 mg负荷量后,继续90 mg 2次/d口服;氯吡格雷组入院时予氯吡格雷300 mg或600 mg负荷量后,继续接受氯吡格雷75 mg 1次/d治疗。所有入选患者均常规口服冠心病二级预防用药。分别收集患者入院24 h内和出院后1个月胆固醇(TC)、甘油三酯(TG)、低密度脂蛋白胆固醇(LDL-C)、丙氨酸转氨酶(ALT)、天门冬氨酸转氨酶(AST)、肌酸激酶(CK)及血清肌酐(Scr)水平,同时计算LDL-C达标率。
1.3 研究终点
1.3.1 主要终点事件 ⑴肝功能损害,定义为转氨酶≥正常值上限的3倍。⑵肌肉毒性,其中肌肉毒性分类及定义如下。①肌痛:CK水平正常,表现包括肌肉疼痛、肌肉酸软、肌肉僵直、肌肉压痛、运动时或运动不久后肌肉痉挛(非夜间痉挛)。②肌病肌肉无力(非疼痛所致且不一定与CK升高相关)③肌炎:肌肉炎症、肌坏死,表现为肌酶升高或高CK血症。轻度,>3×ULN;中度,≥10×ULN;重度,≥50×ULN。④临床横纹肌溶解:肌坏死伴肌红蛋白尿或急性肾衰竭(血清肌酸酐升高≥0.5 mg/dl)。
1.3.2 次要终点事件 ①比较患者院外1个月LDL-C达标率。LDL-C达标率定义为LDL-C水平达到≤70 mg/dl(1.8 mmol/L)或降幅≥50%。②比较两组胆固醇、甘油三酯及肌酐水平院外1个月较入院时的变化是否具有统计学意义。
1.4 统计学方法 所有数据采用SPSS 22.0统计软件。计量资料以±s表示,两组间计量资料均数的比较采用t检验。两组间分类变量资料率的比较采用χ2检验或Fisher′s确切概率法。以P<0.05为差异有统计学意义。
2 结果
2.1 两组患者一般临床特征 两组患者在年龄性别及基础疾病方面比较未见统计学差异,见表1。
2.2 两组患者肝功能损害发生率比较 替格瑞洛组转氨酶升高≥3倍正常上限有3例,发生率2.8%,其中>5倍正常上限有1例;氯吡格雷组转氨酶升高≥3倍正常上限有1例,发生率0.7%。替格瑞洛组肝功能损害发生率高于氯吡格雷组,但经卡方检验比较,未见统计学差异(P>0.05)。同时本研究进一步统计了两组转氨酶升高≥1倍正常上限的人数,替格瑞洛组有15例,发生率14.0%,其中11例发生于住院期间;氯吡格雷组有13例,发生率9.5%,其中3例发生于住院期间。替格瑞洛组除转氨酶升高发生的时间要早于氯吡格雷组外,两组在发生率上比较未见统计学差异(P>0.05)。见表2、3。
表1 入选病例一般情况比较[±s,例数及百分率(%)]

表1 入选病例一般情况比较[±s,例数及百分率(%)]
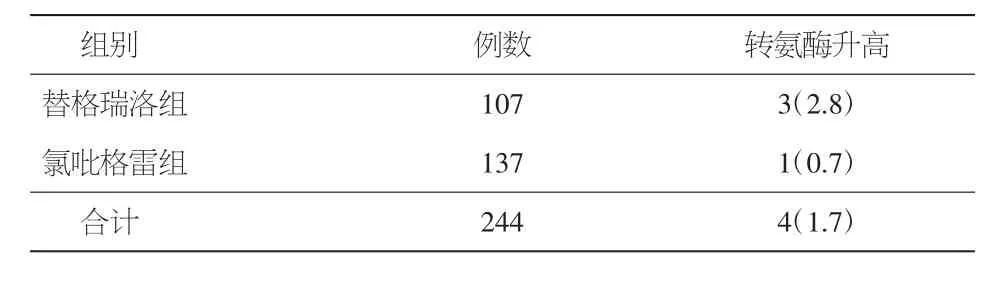
表2 两组患者转氨酶升高≥3倍正常上限人数比较[例数及百分率(%)]
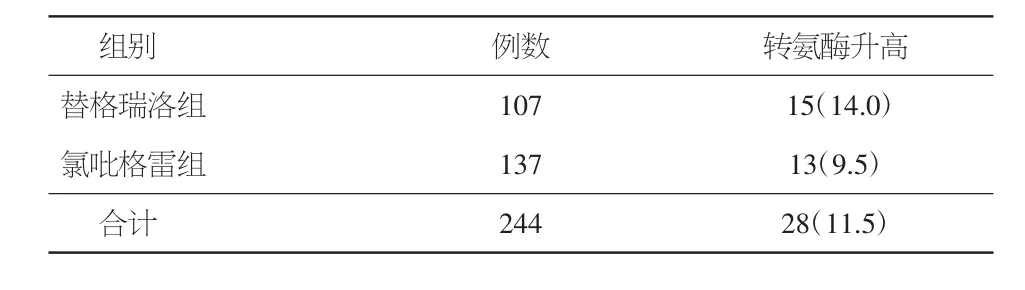
表3 两组患者转氨酶升高≥1倍正常上限人数比较[例数及百分率(%)]
2.3 两组患者肌肉毒性发生率比较 替格瑞洛组有1例肌酸激酶轻度升高,1例出现他汀类药物相关的肌肉疼痛症状,发生率1.9%;氯吡格雷组有1例肌酸激酶轻度升高,发生率0.7%。两组肌酸激酶升高均<5倍正常上限。替格瑞洛组肌肉毒性发生率高于氯吡格雷组,但两组比较未见统计学差异(P>0.05)。见表4。

表4 两组肌肉毒性发生率比较[例数及百分率(%)]
2.4 两组低密度脂蛋白胆固醇达标率比较 两组患者在院外1个月时血LDL-C均较入院时下降,替格瑞洛组LDL-C达标率明显优于氯吡格雷组(53.3%比38.0%,P=0.017<0.05)。见表5。
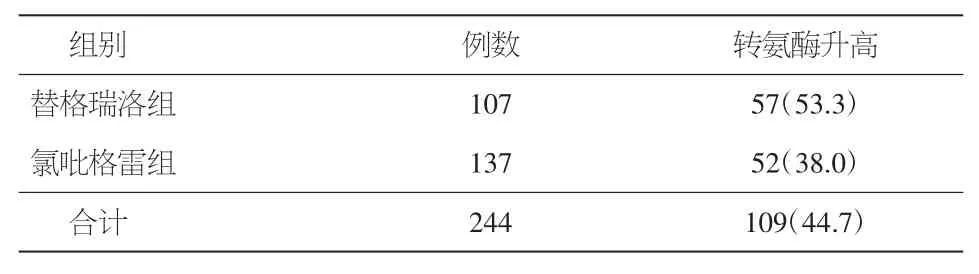
表5 两组患者LDL-C达标率比较[例数及百分率(%)]
2.5 胆固醇、甘油三酯及肌酐水平变化比较 两组患者院外1个月时TG、TC水平均较入院时下降,Cr水平均有所升高(P均<0.05)。替格瑞洛组胆固醇及甘油三酯在院外1个月分别较入院时下降了18.09%和6.23%,降低幅度略大于氯吡格雷组;血清肌酐水平院外1个月较入院时升高了4.47%,升高幅度大于氯吡格雷组,但两组比较未见统计学差异(P>0.05)。见表6。
表6 两组患者TC、TG、Cr治疗前后变化比较(±s)
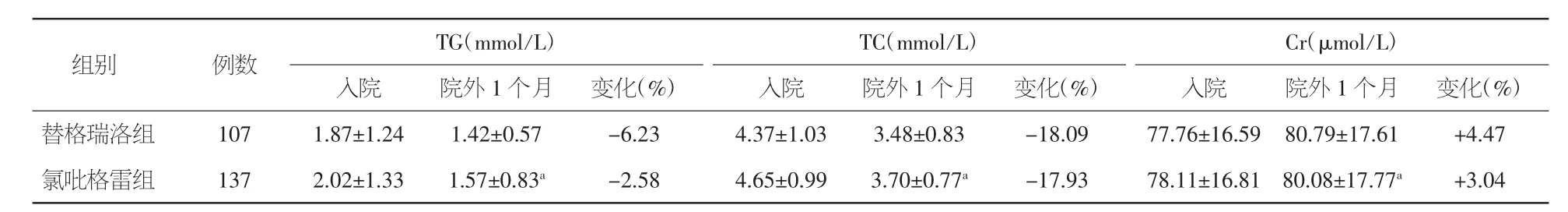
表6 两组患者TC、TG、Cr治疗前后变化比较(±s)
注:-:下降;+:升高;TG:甘油三酯;TC:总胆固醇;Cr:肌酐。与本组入院时比较,aP<0.05
组别 例数替格瑞洛组 107氯吡格雷组 137 TG(mmol/L) TC(mmol/L) Cr(μmol/L)入院 院外1个月 变化(%) 入院 院外1个月 变化(%) 入院 院外1个月 变化(%)1.87±1.24 1.42±0.57 -6.23 4.37±1.03 3.48±0.83 -18.09 77.76±16.59 80.79±17.61 +4.47 2.02±1.33 1.57±0.83a-2.58 4.65±0.99 3.70±0.77a-17.93 78.11±16.81 80.08±17.77a+3.04
3 讨论
ACS是临床最常见的冠心病类型之一,由于其并发症多、致残率高、病死率高,严重威胁着人类的健康。ACS的病理生理基础为斑块破裂、继发血栓形成,在这一过程中,斑块的易损性是ACS发病的重要基础。
他汀类药物是目前使用非常广泛的调血脂药物,通过抑制HMG-CoA还原酶减少胆固醇的合成,从而起到降低胆固醇、低密度脂蛋白胆固醇及甘油三酯,升高高密度脂蛋白的作用。研究表明,他汀类药物在发挥降脂作用之前即可发挥明显的稳定斑块作用,还有降低炎症因子水平、抗动脉粥样硬化、改善内皮功能等作用[11]。近些年的一系列大规模临床研究,如ALLHAT-LLT、PROSPER、AFCAPS/TexCAPS、MEGA[12-15]等已相继证实,应用他汀类药物可明显降低血清总胆固醇和LDL-C水平,同时能显著降低冠心病发病率及心血管病死亡率,因此他汀类药物在冠心病的治疗中具有不可替代的作用。
他汀类药物根据其体内代谢酶的不同可大致分为两类,即主要经过细胞色素P450CYP3A4代谢的阿托伐他汀、辛伐他汀、洛伐他汀和不以细胞色素P450CYP3A4为主要代谢酶的瑞舒伐他汀、氟伐他汀、普伐他汀。经CYP3A4途径代谢的阿托伐他汀是一种脂溶性强效他汀类药物,其临床疗效和安全性已经过多项随机对照研究得到证实,目前已成为全球销量较大的他汀类药物[16,17]。鉴于阿托伐他汀在临床应用的广泛性及我国庞大的用药人群基数,其在临床使用的安全性也日益受到临床医生的重视。
文献报道,他汀类药物的不良反应主要涉及消化系统和骨骼肌肉系统[16,18]。在消化系统反应中,肝损害为主要症状,包括转氨酶升高,伴或不伴有肝功能受损的相关的临床症状;在肌肉毒性反应中,主要表现肌酸激酶或其同工酶升高,临床症状有肌痛、肌病、肌炎、横纹肌溶解等。从不良反应发生的时间上分析,分别约有66%及90%的不良反应发生在用药后7 d和30 d内,提示在阿托伐他汀治疗初期,就应该警惕有可能出现的不良反应,监测各项生化指标,最迟30 d后应进行肝功能等生化指标检查,以确保临床用药的安全性。
替格瑞洛是一种新型的抗血小板药物,PLATO试验结果显示,替格瑞洛在心血管死亡、心肌梗死、全因死亡的整个复合终点事件中,与氯吡格雷比较均有统计学差异,同时不增加整体性的大出血发生率。替格瑞洛口服后由肝酶CYP3A4及CYP3A5(主要是前者)转化生成活性代谢产物ARC124910XX和非活性代谢产物ARC133913XX,同时替格瑞洛对CYP3A4酶有一定抑制作用[8,19,20]。有研究表明,同时服用阿托伐他汀与替格瑞洛可使前者的血浆药物峰浓度Cmax和AUC分别增加23%~55%和36%~67%[8,9]。
现已明确的是,阿托伐他汀与CYP3A4抑制剂如大环内酯类抗生素、伊曲康唑等康唑类抗真菌药物、吉非贝齐等贝特类药物、胺典酮等药物合用时可发生药物间的相互作用,导致阿托伐他汀血药浓度升高,增加发生不良反应的风险。替格瑞洛作为一种新型的抗血小板药物,随着越来越普遍地与阿托伐他汀联合使用治疗ACS患者,两药间的相互作用也越来越受到临床医生的重视。国外已有相关文献[21-23]报道替格瑞洛联合大剂量他汀在治疗ACS患者时,出现急性肾功能衰竭或肌溶解,不排除与两药联合使用有关。
本研究共纳入了244例ACS患者,从入院开始至院外1个月终止,观察替格瑞洛对阿托伐他汀治疗ACS患者的影响。研究结果提示,常规剂量的阿托伐他汀联合替格瑞洛较阿托伐他汀联合氯吡格雷,在肝损害及肌肉毒性等安全性终点事件方面没有统计学差异,短期内两者联合应用的整体安全性较好。但是替格瑞洛组肝酶升高有11例发生在住院2~4 d,而氯吡格雷组仅有3例发生于住院期间,并且替格瑞洛组转氨酶≥3倍正常上限的发生率也高于氯吡格雷组。考虑到由于院外有可能出现混杂因素,如饮食、其他药物等对肝功能产生影响故替格瑞洛与阿托伐他汀联合应用时仍需引起临床医生的注意。此外,在血清肌酐水平升高上,替格瑞洛组的发生率要略高于氯吡格雷组。所以一些高危患者,如高龄、合并肝肾功能不全者,仍需警惕两药联用带来的副作用。
另一方面,替格瑞洛与阿托伐他汀联合应用时,由于增加了阿托伐他汀的血浆药物浓度,从而相对地增加了他汀类药物的使用剂量,在LDL-C达标率上明显优于氯吡格雷组,降低TC和TG上也略优于氯吡格雷组。这也进一步证实了国外相关文献报道对PLATO试验的解读,即替格瑞洛在降低ACS患者的MACE事件时,除其本身优越的抗血小板的药理学特性及临床疗效外,还有其相对增加了CYP3A4途径代谢的他汀类药物的血药浓度亦为重要的原因[24]。
在ACS患者的治疗中,他汀类药物与抗血小板药物的合并使用不可避免,临床医生在选择联合使用药物时应慎重。由于门诊患者的流动性、地区医疗条件的差异、依从性欠佳或经济问题等原因同时缺乏有效的随访,以及相应的药物不良反应报告制度尚不够完善,这些都有可能导致患者在院外发生不良反应后不能及时发现和就诊。所以,临床医生在选择用药时应谨慎,既要根据病情选择用药,同时也要兼顾在用药剂量的选择及药物代谢上有可能产生的相互作用,必要时尽量避免联合使用具有相同代谢途径CYP3A4介导的药物。同时告知患者,要警惕有可能发生的不良反应或风险,做好随访。
综上所述,在急性冠脉综合征患者的治疗中,短期内替格瑞洛对20 mg/d的阿托伐他汀使用剂量的安全性影响较小,整体安全性较好;同时能更好地降低LDL-C水平,达到更好的临床疗效,但对于高危患者,应加强随访,定期监测生化指标。同时,由于本研究中ACS患者使用阿托伐他汀的剂量为中等强度20 mg/d,与指南[25]推荐的强化他汀治疗的剂量40~80 mg/d相比,剂量偏小,所以尚需临床进一步开展大剂量他汀类药物的相关研究。两类药物在临床上合用的有效性和安全性仍需要不断的探索和验证,从而制订最佳的药物使用策略,在改善冠心病患者的预后和经济负担的同时,减少不良事件的发生。
[1]Kavalipati N,Shah J,Ramakrishan A,et al.Pleiotropic effects of statins.Indian J Endocrinol Metab,2015,19:554-562.
[2]Storey RF.Pharmacology and clinical trials of reversibly-binding P2Y12 inhibitors.Thromb Haemost,2011,105:7581.
[3]Wallentin L,Befcker RC,Budaj A,et al.Ticagrelor versus clopidogrel in patients with acute coronary syndromes.N Engl J Med,2009,361:1045-1057.
[4]Jose J.Statins and its hepatic effects:Newer data,implications,and changing recommendations.J Pharm Bioallied Sci,2016,8:23-28.
[5]张冰,王莉莉.他汀类药物的临床应用及不良反应研究进展.国际药学研究杂志,2013,40:560-564.
[6]Ferri N,Corsini A,Bellosta S.Pharmacology of the new P2Y12 receptor inhibitors:insights on pharmacokinetic and pharmacodynamic properties.Drugs,2013,73:1681-1709.
[7]Dobesh PP,Oestreich JH.Ticagrelor:Pharmacokinetics,Pharmacodynamics,Clinical Efficacy,and Safety Pharmacotherapy. Pharmacotherapy,2014,34:1077-1090.
[8]Teng R.Pharmacokinetic,pharmacodynamic and pharmaco genetic profile of the oral antiplatelet agent ticagrelor.Clin Pharmacokinet,2012,51:305-318.
[9]Teng R,Mitchell PD,Butler KA.Pharmacokinetic interaction studies of co-administration of ticagrelor and atorvastatin or simvastatin in healthy volunteers.Eur J ClinPharmacol,2013,69:477-487.
[10]中国医师协会急诊医师分会,中华医学会心血管病学分会,中华医学会检验医学分会.急性冠脉综合征急诊快速诊疗指南.中华危重症医学杂志,2016,9:73-80.
[11]徐辉,杨跃进.他汀类药物多效性的临床研究进展.心血管病学进展,2011,32:649-652.
[12]Shepherd J,Blauw GJ,Murphy MB,et al.Pravastatin in elderly individuals at risk of vascular disease(PROSPER):a randomised controlled trial.Lancet,2002,360:1623-1630.
[13]The ALLHAT officers and coordinators for the ALLHAT collaborative research group.The Antihypertensive and Lipid-Lowering Treatment to Prevent Heart Attack Trial.Major outcomes in moderately hypercholesterolemic,hypertensive patients randomized to pravastatin vs usual care:The Antihypertensive and Lipid-Lowering Treatment to Prevent Heart Attack Trial(ALLHAT-LLT).JAMA,2002,288:2998-3007.
[14]Nakamura H.Primary prevention trial by lowering hyperlipidemia on the cardiovascular disease(MEGA Study).Nippon Ronen Igakkai Zasshi,2009,46:18-21.
[15]Gotto AM Jr.Establishing the benefit of statins in low-to-moderate-risk primaryprevention:the Air Force/Texas Coronary Atherosclerosis Prevention Study (AFCAPS/TexCAPS).Atheroscler Suppl,2007,8:3-8.
[16]Athyros VG,Tziomalos K,Karagiannis A,et al.Atorvastatin:safety and tolerability.Expert Opin Drug Saf,2010,9:667-674.
[17]Rabar S,Anthony W,Lindsay B,et al.Lipid modification and cardiovascular risk assessment for the primary and secondary prevention of cardiovascular disease:summary of updated NICE guidance.BMJ,2014,349:g4356.
[18]Sakaeda T,Kadoyama K,Okuno Y.Statin-associated muscular and renal adverse events:data mining of the public version of the FDA adverse event reporting system.PLoS One,2011,6:e28-124.
[19]Zhou D,Andersson TB,Grimm SW.In vitro evaluation of potential drug-drug interactions with ticagrelor:cytochrome P45 reaction phenotyping,inhibition,induction,and differential kinetics.Drug Metab Dispos,2011,39:703-710.
[20]Thachil J.Antiplatelet therapy-a summary for the general physicians.Clin Med,2016,16:152-160.
[21]van Vuren AJ,de Jong B,Bootsma HP,et al.Ticagrelor-induced renal failure leading to statin-induced rhabdomyolysis. Neth J Med,2015,73:136-138.
[22]Kido K,Mary B,Seratnahaei A,et al.Rhabdomyolysis precipitated by possible interaction of ticagrelor with high-dose atorvastatin.J Am Pharm Assoc,2015,55:320-323.
[23]Holbrook A,Wright M,Sung M,et al.Statin-associated rhabdomyolysis:is there a dose-response relationship?Can J Cardiol,2011,27:146-151.
[24]James J,DiNicolantonio Victor L.Serebruany Exploring the Ticagrelor-Statin Interplay in the PLATO Trial.Cardiology,2013,124:105-107.
[25]霍勇,葛均波,韩雅玲,等,急性冠状动脉综合征患者强化他汀治疗专家共识.中国介入心脏病学杂志,2014,22:4-6.
The influence of Ticagrelor on Atorvastatin in the patients with acute coronary syndrome
ZHAO Xue-yin*,WANG Xiao,YAN Yan,et al.*CCU,Peaking University First Hospital Fengtai Hospital,Beijing 100071,China
NIE Shao-ping,E-mail:spnie@126.com
Objective To observe the clinical safety of Atorvastatin metabolized by the CYP3A4 enzyme combined with the CYP3A4 enzyme inhibitor Ticagrelor in the treatment of patients with acute coronary syndrome,meanwhile evaluate the efficacy of lipid-lowering.Methods A total of 244 patients with ACS were collected,and randomly divided into Atorvastatin+Ticagrelor group(Ticagrelor group)and Atorvastatin+Clopidogrel group(Clopidogrel group).Then collected the laboratory and clinical data with admission in 24 hours and out of the hospital a month,including cholesterol,triglycerides,low density lipoprotein cholesterol,glutamic-pyruvic transaminase,glutamic-oxalacetic transaminase,creatine kinase and serum creatinine,and the LDL-C compliance rate was calculated.Results The Ticagrelor group incidence of liver function damage,muscle toxicity and impaired renal function were higher than Clopidogrel group(2.8%vs 0.7%,1.9%vs 0.7%,4.47%vs 3.04%).The difference did not reach statistical significance.The LDL-C compliance rate had significant difference between two groups,Ticagrelor group was more effective than Clopidogrel group with the same dose Atorvastatin(53.3%vs 38%,P<0.05). Cholesterol and triglyceride levels of two groups outside the hospital a month were compared with admission decreased significantly(P<0.05).Creatinine level is higher than that of the admission(P<0.05),between the two groups differences no statistical significance(P>0.05).Conclusion The effects of Ticagrelor on the safety of Atorvastatin metabolized by the CYP3A4 enzyme is less,and in the same dose of Atorvastatin,Ticagrelor combined with Atorvastatin has more advantage in LDL-C compliance rate.
Atorvastatin; Ticagrelor; CYP3A4; Acute coronary syndrome; Liver function damage;Muscle toxicity; Low-density lipoprotein cholesterol
聂绍平,E-mail:spnie@126.com
10.3969/j.issn.1672-5301.2017.05.020
R543.3
A
1672-5301(2017)05-0458-05
2016-11-29)

