In625合金和316L不锈钢在NaCl-CaCl2-MgCl2熔盐中的腐蚀机理
刘波,魏小兰,王维龙,宋明,丁静
In625合金和316L不锈钢在NaCl-CaCl2-MgCl2熔盐中的腐蚀机理
刘波1,魏小兰1,王维龙2,宋明1,丁静2
(1华南理工大学化学与化工学院,广东广州 510640;2中山大学工学院,广东广州 510006)
为了解Cr元素对含铬合金在三元NaCl-CaCl2-MgCl2氯化物熔盐中腐蚀的影响机理,选择两种含铬合金镍基Inconel 625(In625)和铁基奥氏体316L型不锈钢,采用全浸没法分别研究它们在500~700℃下于三元氯化物NaCl-CaCl2-MgCl2低共熔盐中的腐蚀行为,以及接触空气程度与温度对腐蚀的影响。绘制了In625合金和316L不锈钢在熔盐中600℃下浸没21 d的腐蚀速率曲线。采用XRD(X射线衍射仪)、SEM(扫描电镜)和EDX(X射线能谱仪)对In625合金和316L不锈钢的腐蚀产物和截面形貌进行分析。结果表明:两种金属的腐蚀程度随着接触空气的量和腐蚀温度的增加而加大;600℃下腐蚀21 d后金属表面和截面的元素及形貌分析表明,Cr具有优先脱溶性;600℃下腐蚀21 d后在合金截面形成了贫Cr区域;致密的腐蚀层可以降低金属的腐蚀速率;在NaCl-CaCl2-MgCl2三元氯化物熔盐中镍基合金In625拥有比奥氏体不锈钢更好的耐腐蚀性能。
氯化物熔盐;腐蚀;不锈钢;Inconel 625镍基合金
引 言
提高能量转换和利用效率是太阳能热发电技术需要解决的核心问题,其中提高蓄热系统的蓄热温度是重要环节,研制高温传热蓄热介质是关键[1]。理想的高温蓄热介质应能够储存600℃以上的热量[2]。碱金属、碱土金属氯化物以其高温化学稳定、储量丰富、无毒、黏度小和比热容大等优势满足600℃以上高温传热蓄热要求[3-6]。但高温氯化物熔盐会加速金属材料的腐蚀,因此储热系统设计必须考虑熔盐的腐蚀性[7-8]。
氯化物熔盐的腐蚀性研究一直都是热点。Wang等[9]研究了304、316L不锈钢和Q235A 3种金属材料450℃下在LiCl-KCl熔盐中的腐蚀行为,结果表明含Mo的316L不锈钢拥有更好的耐腐蚀性。Lu等[10]在研究Cr基、Fe基和Ni基合金850℃在NaCl熔盐中的腐蚀行为时发现,Cr基合金的耐腐蚀性最差,Cr元素从金属基体内向外扩散致使Cr流失,是合金质量损失的主要原因。Vignarooban等[11]采用浸没法和电化学方法,研究了Hastelloys C-276、C-22和304不锈钢在NaCl-KCl-ZnCl2熔盐中的腐蚀行为,结果表明上述金属在隔绝空气的情况下在熔盐中的腐蚀速率明显降低。Vignarooban等[12]也研究了Hastelloy C-276、C-22和N型合金浸没在250、500℃的三元NaCl-KCl-ZnCl2共晶氯化物熔盐中的腐蚀行为。结果表明,C-276合金的耐腐蚀性能最好,N型合金的腐蚀速率最大;C-276和C-22合金中较高的Cr含量使它们拥有比N型合金更好的耐腐蚀性。Gomez-Vida等[13]通过质量损失法和电化学方法研究了氩气氛围下经预氧化过的Inconel 702、Haynes 224和Kanthal APMT合金在MgCl2-KCl熔盐中的腐蚀行为,结果表明:高的Ni含量可以增强合金在氯化物熔盐耐腐蚀性;腐蚀后合金中的Cr和Fe元素进入熔盐中的量最多,其次是Al、Ni,然后是Mo。Judith等[14]研究了650~700℃下SS347、SS310、Incoloy 800H和Inconel 625合金在NaCl-LiCl熔盐中的腐蚀性,结果表明Inconel 625合金的耐腐蚀性最好。宋明[15]研究了201、304、310S和316L型奥氏体不锈钢在三元氯化物NaCl-CaCl2-MgCl2熔盐中的腐蚀性,发现316L不锈钢的耐腐蚀性最好。
“活化氧化”(active oxidation)机理[16-18]常被用来解释高温氯化腐蚀。Grabke等[19]在研究低于850℃的温度下氯化物熔盐中的腐蚀机理时提出:熔盐可以与金属表面氧化物或者与熔盐中的水分反应生成氯气;这些氯气具有高度流动性,可以穿透氧化层和与金属形成金属氯化物,生成的金属氯化物在实验温度下是非常易挥发的;这些气态金属氯化物将通过氧化层扩散,直到它们达到较高的含氧环境被氧化并释放出氯气,之后氯气又可以向金属/金属氧化物界面扩散引起进一步的腐蚀。但氯化物熔盐的腐蚀是一个复杂的过程,包括化学腐蚀、电化学腐蚀以及界面反应和氧化物的溶解[20]。需要结合不同的实验条件进行机理分析。
比较316L不锈钢和镍基Inconel 625合金在三元氯化物NaCl-CaCl2-MgCl2熔盐中腐蚀性的差异,探讨温度和空气对腐蚀的影响,分析腐蚀产物特性,研究腐蚀机理,为该熔盐优选合适的容器材料提供借鉴。
1 实验材料和方法
1.1 实验材料与仪器
用于制备三元氯化物熔盐的无水NaCl(广州化学试剂厂)、无水CaCl2(广州化学试剂厂)和无水MgCl2(上海百灵威科技有限公司)皆为分析纯试剂。在腐蚀速率曲线测定过程用来处理钢片的无水乙醇、丙酮、HNO3和HCl溶液也皆为分析纯试剂或由分析纯试剂溶于纯水中配制。研究用的316L型奥氏体不锈钢(简称316L)和Inconel 625型镍基合金(简称In625)被截为40 mm×15 mm×2 mm的片状试样,两种金属的化学组成见表1。

表1 In625合金和316L不锈钢的主要化学组成[21]
腐蚀实验所用坩埚为200 ml柱状刚玉坩埚,分为加盖(有阻接触空气)和无盖(无阻接触空气)两种,用来区别腐蚀过程熔盐接触空气的程度。腐蚀前处理好的金属片在WGL-30B电热鼓风干燥箱中干燥;其质量测量在电子天平(美国丹佛仪器公司)上进行,量程为110 g,精度为0.1 mg。腐蚀过程在SX-4-10型箱式电阻炉(天津泰斯特有限公司)中进行。腐蚀后金属片上腐蚀层的物相在德国Bruker D8 ADVANCE型X射线衍射仪(XRD)上分析;腐蚀层表面和剖面形貌以及相关元素分布,在日立S3700N型扫描电镜(SEM)上进行。
1.2 实验方法
将片状金属试样用砂纸由粗及细打磨光滑除去表面氧化层,再经水、丙酮、酒精清洗完成前处理,然后干燥备用。
按照文献[4]采用静态熔融法制备三元氯化物NaCl-CaCl2-MgCl2熔盐。将称重后的金属片放入刚玉坩埚内并加入所制熔盐到坩埚几乎装满,然后将坩埚置于箱式电阻炉中,待温度升高到指定值后保温并开始计时。改变实验条件重复上述实验。
1.2.1 空气和温度对腐蚀性的影响研究 将装有In625镍基合金和熔盐的加盖和无盖坩埚置于马弗炉内500℃下恒温腐蚀40 h后取出,测量其经过超声水洗和酸洗后的质量损失[22],计算其总质量损失率。用316L不锈钢代替In625镍基合金重复上述实验,比较空气对两种金属腐蚀的影响。
将两种金属分别在加盖坩埚中于600、700℃重复上述实验,研究有阻接触空气(坩埚加盖)条件下温度对两者在熔盐中腐蚀性的影响。
1.2.2 有阻接触空气条件下的腐蚀速率研究 在编号为1~12号的加盖坩埚中分别放入In625镍基合金片与熔盐,然后于600℃恒温腐蚀数天。其中第1~4号、6~9号和11号坩埚各放入1片金属,第5、10和12号坩埚中分别各放3片。每隔1 d从炉中取出一个坩埚直到第10号,然后在第14天和21天取出第11和12号坩埚。按文献[22]所述的标准方法进行腐蚀后处理,计算合金的质量损失率,以损失率为纵坐标,时间为横坐标作图,得In625镍基合金在熔盐中的腐蚀速率曲线。用316L不锈钢代替In625合金重复上述实验,同样得到316L不锈钢腐蚀速率曲线。将第5、10和21天坩埚内的另外两片In625合金或316L不锈钢仅进行超声水洗并干燥,分别进行XRD分析和SEM观察。
文中相关化学反应的标准反应Gibbs自由能计算数据由文献[23]查得。
2 结果与讨论
2.1 空气和温度对金属腐蚀的影响
图1是In625合金和316L不锈钢分别在有阻和无阻接触空气情况下浸入500℃镁基三元氯化物NaCl-CaCl2-MgCl2熔盐中腐蚀40 h后的总质量损失。由图1可以看出,两种金属在无阻接触空气情况下的腐蚀质量损失均明显大于有阻接触空气情况。Vignarooban等[11]在研究NaCl-KCl-ZnCl2熔盐的腐蚀性时,证明空气是引发熔盐/合金体系发生腐蚀的重要因素,隔绝空气可以很大程度减小熔盐对金属的腐蚀。Groll等[24]在研究KCl-LiCl熔盐对金属容器的腐蚀行为时发现水分含量的增加会加剧熔盐对金属的腐蚀性。这些研究结论与图1所示实验结果一致。当坩埚加盖时,空气中的O2和H2O溶入熔盐过程受阻,腐蚀过程消耗的O2和H2O得不到及时补充,因此腐蚀程度低。可见,氯化物熔盐作为传热蓄热介质在实际应用中应该尽量避免与空气的接触,严格控制熔盐的纯度。
在有阻接触空气条件下,316L不锈钢和In625合金在不同温度熔盐中分别浸没40 h后的质量损失如图2所示。
由图2可知,随着温度的升高,熔盐对两种金属的腐蚀性都有所增强。温度升高,不仅加快熔盐中腐蚀性气体的扩散,更能加快腐蚀反应速率,致使相同腐蚀时间内,金属的腐蚀质量损失随温度升高而增大。
2.2 浸没21 d的腐蚀结果
2.2.1 腐蚀动力学 图3为In625合金和316L不锈钢在有阻接触空气情况下于600℃的NaCl-CaCl2- MgCl2熔盐中浸没21 d的腐蚀动力曲线。从图3可以看出,两种金属的腐蚀动力曲线都表现为先增加然后趋于平稳的态势。主要的质量损失源于氧化层中的疏松氧化物。In625合金从第7天开始疏松氧化物才呈现急剧增加现象,9 d后增加量趋于减小。整个过程中合金形成的碱性氧化物的量基本没变。316L不锈钢在14 d和21 d的疏松氧化层还在不断增加,表明其腐蚀产物较为疏松,容易脱落。计算[25]求得In625合金和316L不锈钢有阻接触空气条件下在600℃熔盐中的腐蚀速率分别为0.1211~0.1384、0.2639~0.5407 mm·a−1。按照金属腐蚀10级标准评估[26],两种金属在本实验条件下的腐蚀等级分别为为6级和6~7级,都属于尚耐蚀。
从图3所示两种金属腐蚀14 d后质量损失趋于平缓可以看出,金属表面的腐蚀层基本稳定,接触熔盐的腐蚀外层的减少速率与接触金属基底的腐蚀内层形成速率基本达到平衡。
2.2.2 腐蚀产物的物相 图4(a)和(b)分别是In625合金和316L不锈钢在600℃熔盐中腐蚀5、10和21 d并经超声水洗后表面的XRD谱图。
由图4可见,腐蚀前In625合金的3个衍射峰的2值和腐蚀前316L不锈钢的3个衍射峰的2值均与Cr0.19Fe0.7Ni0.11的3个衍射主峰2值最为接近。
腐蚀5 d后,In625合金原有的一组衍射峰的峰高下降,旁边出现了低Cr(Fe)的Ni2.9Cr0.7Fe0.36物相的衍射峰。316L不锈钢原有的一组衍射峰的旁边,也出现了2分别是43.84°、51.10°和74.85°的一组衍射峰,该组衍射峰的2值比Cr0.19Fe0.7Ni0.11的3个衍射主峰2值略大,但比Ni2.9Cr0.7Fe0.36的3个衍射主峰2值小,考虑到含Cr合金在氯化物熔盐中腐蚀过程Cr流失的现象[11,27],认为形成低Cr(Fe)的Ni2.9Cr0.7Fe0.36物相的可能性比较大。
腐蚀10 d后,两种金属中表征Cr0.19Fe0.7Ni0.11物相的一组衍射峰消失,表征Ni2.9Cr0.7Fe0.36的一组衍射峰仍然存在,说明腐蚀层在增厚,X射线仅能到达腐蚀层下的低Cr(Fe)金属区。另外,腐蚀10 d后,316L不锈钢的腐蚀层出现了MgO新物相,MgO可能来源于熔盐中MgCl2与空气中水分子的高温水解反应
MgCl2+H2O→MgO+2HCl↑ Δrm⊖(873 K)=−5.6kJ·mol−1(1)
In625合金的腐蚀层出现了MgCr2O4新物相,MgCr2O4可能来源于MgO与Cr2O3的反应
Cr2O3+MgO→MgCr2O4
Δrm⊖(873 K)=−37 kJ·mol−1(2)
随着腐蚀时间延长到21 d,316L不锈钢表面检测出的腐蚀产物主要为MgFe0.2Cr1.8O4和MgO,而在In625合金表面检测出的腐蚀产物主要为MgCr2O4和NiO。
有研究表明[20,25],合金中的Cr可以形成Cr2O3氧化层附着在合金表面,减缓对合金基底的腐蚀。由图4(a)和(b)可知,Cr2O3并没有在316L不锈钢和In625合金表面被检测出,说明在腐蚀的初期,金属表面的Cr2O3膜太薄,普通XRD测量收集不到该物相的信息,腐蚀后期形成Cr2O3与别的氧化物发生了反应生成了新物相。
在腐蚀后的316L不锈钢和In625合金表面也没有检测出Fe2O3、Fe3O4和FeO。这些腐蚀产物可能溶解在了熔盐中或在超声水洗时被除去。
2.2.3 腐蚀形貌
(1)表面腐蚀形貌
图5(a)、(c)和(e)给出的是In625合金在600℃熔盐中分别腐蚀5、10和21 d并经超声水洗后腐蚀层表面的扫描电镜(SEM)形貌图。可以看出,In625合金腐蚀5 d后表面存在很多不规则形状的凸起物和孔洞,腐蚀10 d后孔洞变浅,腐蚀21 d后孔洞消失表面趋于致密。316L不锈钢表面变化与In625合金的基本一致,如图5(b)、(d)和(f)所示。图5中各标识区域的X射线能谱(EDX)分析结果见表2。
In625合金腐蚀5 d后表面区域1的EDX结果显示,表面主要元素为Ni、Cr、O、Mo,少量的Mg推测源于熔盐水解。

表2 EDX分析得到的腐蚀表面元素含量
将O指定给Mg之后剩余的量相对于Ni等较少,说明区域1中的金属有些以单质状态存在。图5(c)所示腐蚀10 d后区域4和5处的孔洞变浅,结合表2所示的区域4的EDX分析结果可见,此处元素主要为O、Cr和Mg,O含量很高表示区域4主要是Cr、Mg氧化物,与图4(a)所示In625合金腐蚀10 d生成MgCr2O4结果一致,结合图3(a)所示In625合金腐蚀10 d后质量损失趋于平缓可知,腐蚀产物MgCr2O4较为致密,可减缓金属的腐蚀速率。In625合金腐蚀21 d后,图5(e)呈现凸起颗粒,结合表2可知,凸起颗粒(8)主要含Ni, O含量较少,说明此处Ni为单质,表明合金中的Ni元素具有较好的耐腐蚀性;而平整的区域(9)主要含Cr、Ni、O、Mg,从元素分析和图4(a)所示In625合金腐蚀21 d的XRD结果可见,该区域主要为MgCr2O4,以及少量Mo和Fe的氧化物。
图5(b)所示316L不锈钢腐蚀5 d后,其表面存在很多凸起的颗粒、孔洞和孔道,其颗粒区2和凹坑区3的EDX分析结果,如表2所示。凸起颗粒区2主要为Fe和Ni的氧化物,凹坑区3主要元素为Fe、Cr、Ni、O,氧元素相对含量明显低于区域2,表明孔道内除了含有氧化物之外仍有部分裸露的金属。与凹坑区3相比,颗粒区2的Cr含量很少,说明腐蚀过程会失去元素Cr,这与文献[10]指出的在氯化物熔盐中存在Cr流失的现象相一致。从图5(d)可以看出,腐蚀10 d后的不锈钢表面平整致密,没有明显的孔洞和孔道。表2显示图5(d)区域6和7主要为Mg和O元素,Fe、Cr、Ni含量极少,图4(b)所示316L不锈钢腐蚀5 d的XRD证明主要生成了MgO。图5(f)显示,316L在腐蚀21 d后金属表面平整,其区域10的EDX分析结果(表2)表明,腐蚀表层的主要元素为Mg和O,表明金属表面被致密的MgO完全覆盖,这与图4(b)所示316L不锈钢腐蚀21 d的XRD结果不一致。这是因为EDX仅能分析表层几微米的元素信息,而XRD收集到的腐蚀层物相信息要厚得多。
(2)腐蚀层剖面形貌
为了解两种金属腐蚀层厚度并探析腐蚀过程Cr含量减少的机理,对腐蚀层剖面进行SEM形貌观察并分析其元素分布。图6(a)、(b)分别为In625合金和316L不锈钢有阻接触接触空气条件下在600℃熔盐中腐蚀21 d后的剖面SEM形貌图。比较图6(a)、(b)腐蚀层厚度可以发现,316L不锈钢的腐蚀层厚度约为50 μm,而In625合金的腐蚀层厚度大约只有10 μm,316L不锈钢腐蚀层厚度约是In625合金的5倍。In625合金的腐蚀层则比316L不锈钢的明显致密。
图6(a)所示In625合金在熔盐中腐蚀21 d后,其腐蚀区域可分为腐蚀外层(区域1)和腐蚀内层(区域2)。在区域2中能明显观察到细小的孔,这可能与Fe和Cr特别是Cr的减少有关。区域3应该是金属的本底区。3个区域的EDX元素分析结果见表3。
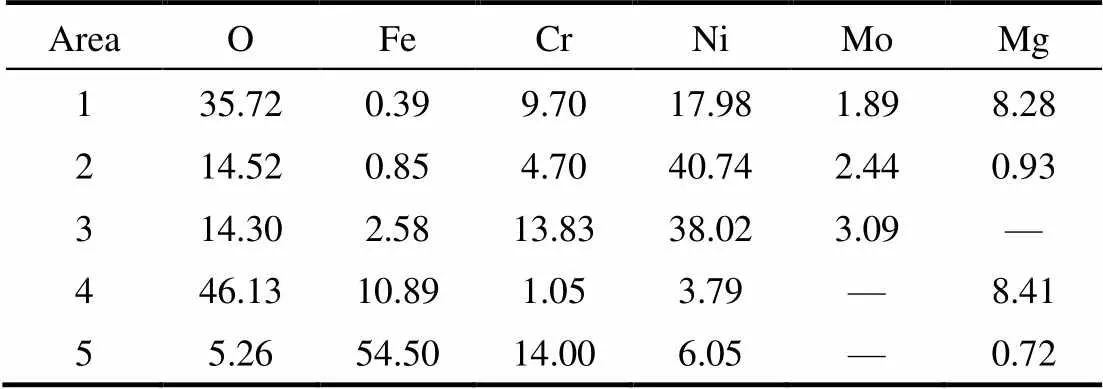
表3 EDX分析得到的腐蚀截面元素含量
由表3可知,图6中所示区域1~5未见Cl元素,说明腐蚀层中没有氯化物;腐蚀层中存在大量O元素,考虑到熔盐为氯化物且腐蚀过程熔盐接触空气,认为熔盐对金属腐蚀的活性物质主要来源于空气中的O2。图6(a)所示In625合金的区域2中各元素含量分析结果证明,该区域Cr含量比外腐蚀层区域1和金属基体区域3都低。腐蚀外层的区域1富含Cr、O、Mg,图4(a)表明In625合金的腐蚀外层主要形成了MgCr2O4,In625合金的腐蚀内层区域2富Ni。腐蚀内层区域2和外腐蚀层区域1中的Fe含量都很低,可能是生成了疏松氧化物在超声水洗过程中失去,也可能与Cl−形成FeCl3挥发扩散到熔盐中,FeCl3的沸点仅为316℃[28]。腐蚀内层区域2和金属基体区域3中的O含量相近都是约14%,但比图6(b)所示316L不锈钢的区域5处约5%的O含量高,说明区域2和3所监测到的O有一部分可能是从腐蚀层扩散而来,还有一部分应该是截取剖面时带入的。区域5含O量低的原因是该区域位于距离腐蚀层外侧约100 μm的深处,O扩散到达不了如此深度,仅来源于截取剖面时带入。区域3则位于距离腐蚀层外侧仅约30 μm处,O元素通过内腐蚀层微孔扩散可以达到,因此该区域O含量较高实属正常。值得注意的是,图6(a)所示的外腐蚀层存在一些类似管状的向上通道,有些通道底部直接与内腐蚀层相通,这些通道似乎为气体产物外逸所留,结合表3所示区域2中Cr含量减少,可以推测腐蚀过程也许生成了Cr的气态化合物,当气态物质外逸到腐蚀外层遇到来自熔盐沉积的致密MgO使得逸出受阻,加上此处O含量较高,在长期高温下与MgO反应形成了图4(a)所示MgCr2O4致密层,因此区域1处的Cr含量又一次增大。查阅文献[28]发现,CrCl4(沸点600℃)、CrO3(沸点250℃)和CrO2Cl2(沸点117℃)在600℃时都是气体,这几种化合物或许是腐蚀过程Cr元素传质输运的关键。
316L不锈钢在熔盐中腐蚀21 d后腐蚀区域呈单一腐蚀层,如图6(b)所示,可以看出,靠近熔盐的腐蚀层外侧,腐蚀产物较为致密,与金属基体接壤的腐蚀层内侧出现明显凹坑,这些凹坑也存在多处向上的通道,而且这些通道还存在横向细小的通道,说明存在气体扩散通道,使得这里的腐蚀产物较为疏松。表3表明,图6(b)所示靠近金属基体区域4的腐蚀产物主要由Fe、Mg和O元素构成,其中Cr含量很低;而区域5的Fe、Cr含量很高,O含量较低,说明该区域是金属基体。
为了进一步了解两种金属腐蚀层和金属基体的元素分布,对图6(a)和(b)所示方框区域进行元素分布分析,如图7所示。
比较图7(a)、(b)发现,两种金属的腐蚀层都出现了一个贫Cr区,表明Cr具有优先脱溶性[27]。导致贫Cr区存在的原因可能是,发生了一系列生成气态化合物的反应
Cr2O3+2MgCl2+2O2+Fe→2CrO2Cl2↑+2MgO+FeO (3)
Cr2O3+2MgCl2+2O2+Ni→2CrO2Cl2↑+2MgO+NiO (4)
Cr + 2MgCl2+ O2→CrCl4↑ + 2MgO (5)
由于腐蚀外层接触熔盐O2含量较高,主要发生反应(3)和(4);靠近金属部位O2含量较低,主要发生反应(5),图7金属区域所示Mg的存在,证明反应(5)的发生。
图7(a)所示的贫Cr区在In625合金的腐蚀内层,与图6(a)所示具有细微小孔的腐蚀内层在同一区域,这些微孔可能是发生反应(5)留下的。图7(a)所示的腐蚀外层,出现了Cr含量增大的区域,这可能是CrCl4从腐蚀内层挥发出来,遇到来自熔盐中水解生成的MgO发生了如下反应
2CrCl4+3MgO→Cr2O3+3MgCl2+Cl2(6)
生成的Cl2再扩散到腐蚀内层金属区,与Cr发生反应
Cr+2Cl2→CrCl4(7)
当腐蚀层逐渐变厚度,腐蚀外层生成的Cr2O3无法接触单质Fe和Ni时,有可能发生反应(8),使腐蚀层消减得以持续。
Cr2O3+2MgCl2+2O2+2FeO→2CrO2Cl2↑+2MgO+Fe2O3(8)
由于In625合金中Fe含量较低,反应(8)发生的概率偏低,因此腐蚀层消减较慢,表现出较好的耐腐蚀性。如图7(a)所示,在In625合金的腐蚀内层,Fe含量也明显比金属本体低,与Cr在腐蚀外层出现增大的现象不同,Fe含量在腐蚀外层没有增大,腐蚀外层和内层的Fe含量较金属基底层要少,这与图4(a)所示没有检测到Fe氧化物的结论一致,FeCl3的低沸点(316℃)特征[28],可能是Fe损失的原因之一。图7(a)所示腐蚀内层的贫Cr区中,Ni相对含量明显较大,这与Fe、Cr相对含量较低有关。In625合金中Mo含量由内到外逐渐降低,说明Mo在最外层逐渐失去。文献[29]认为,在高温下,Mo被O2氧化生成的MoO3氧化膜“在450℃以上就开始挥发,不具有保护性”。但是,Mo的这种反应可以消耗氯化物熔盐中的溶解O2,可起到减缓金属腐蚀的作用。上述反应的标准Gibbs自由能见表4。

表4 相关反应的标准Gibbs自由能
图7(b)所示316L不锈钢的腐蚀层在靠近金属基体的一侧,出现了明显的凹坑暗区,该区域恰好是贫Cr区,但存在O和Mg元素,说明腐蚀过程失去Cr遗留的空间被Mg和O部分填充,结合该区域Fe、Ni、Mo元素分布,该凹坑尚存在其他氧化物。结合图4(a)所示XRD分析,腐蚀层中主要为MgO和MgFe0.2Cr1.8O4。316L不锈钢的各腐蚀反应与In625合金的类似。
尽管在人们的认知中,Cr是增强316L和In625合金耐腐蚀性的重要元素[20,30],其主要作用是形成致密氧化层,但从本实验分析的结果来看,Cr也同时加速两种金属在三元NaCl-CaCl2-MgCl2氯化物熔盐中的腐蚀。真正起到保护作用的应该是氧化铬与氧化镁形成的新物相MgCr2O4或MgFe0.2Cr1.8O4。
3 结 论
(1)空气中的O2和空气中H2O是诱发三元NaCl-CaCl2-MgCl2氯化物熔盐腐蚀In625合金和316L不锈钢的重要因素。升高温度会加快熔盐对金属的腐蚀速率。
(2)钼(Mo)元素是提升316L不锈钢在氯化物熔盐中的抗腐蚀性的重要元素。In625合金的耐腐蚀性明显强于316L不锈钢。21 d腐蚀动力曲线表明,空气氛围下316L不锈钢在600℃下于NaCl-CaCl2-MgCl2熔盐中年腐蚀率为0.2639~0.5407 mm·a−1。同样条件下,In625合金21 d腐蚀速率曲线表明,其年腐蚀率为0.1211~0.1384 mm·a−1。
(3)316L不锈钢和In625合金中所含的Cr元素在氯化物熔盐中具有优先脱溶性。溶解在熔盐中的H2O和O2分子及熔盐中的MgCl2与金属发生反应生成含MgCr2O4、NiO(In625)和MgO、MgFe0.2Cr1.8O4(316L)腐蚀层,可减缓腐蚀的进行;腐蚀过程中CrCl4的生成、扩散、反应是造成合金中贫Cr区域出现的原因;Ni在合金中的耐腐蚀性和稳定性优于Fe。
(4)在NaCl-CaCl2-MgCl2熔盐中,MgCl2通过反应导致MgO及MgCr2O4形成,促进了腐蚀产物层的致密。
References
[1] Vignarooban K, Xu X, Arvay A,. Heat transfer fluids for concentrating solar power systems – a review[J]. Applied Energy, 2015, 146: 383-396.
[2] Hoffschmidt B, Téllez F M, Valverde A,. Performance evaluation of the 200-kWth HiTRec-II open volumetric air receiver[J]. Journal of Solar Energy Engineering, 2003, 125(1): 87-94.
[3] LI P W. Halide and oxy-halide eutectic systems for high performance high temperature heat transfer fluids: report of DOE's office of scientific and technical information[R]. Golden, Colorado: National Renewable Energy Laboratory (NREL), 2012.
[4] WEI X L, SONG M, WANG W L,. Design and thermal properties of a novel ternary chloride eutectics for high-temperature solar energy storage[J]. Applied Energy, 2015, 156: 306-310.
[5] 胡宝华, 丁静, 魏小兰, 等. 高温熔盐的热物性测试及热稳定性分析[J]. 无机盐工业, 2010, 42(1): 22-24.Hu B H, Ding J, Wei X L,. Test of thermal physics and analysis on thermal stability of high temperature molten salt[J]. Inorganic Chemicals Industry, 2010, 42 (1): 22-24.
[6] MYERS Jr P D, Goswami D Y. Thermal energy storage using chloride salts and their eutectics[J]. Applied Thermal Engineering, 2016, 109: 889-900.
[7] Xu Y T, Xia T D, Wang W P,. Hot corrosion failure mechanism of graphite materials in molten solar salt[J]. Solar Energy Materials & Solar Cells, 2015, 132(132): 260-266.
[8] Wang J W, Zhang C Z, Li Z H,. Corrosion behavior of nickel-based superalloys in thermal storage medium of molten eutectic NaCl-MgCl2, in atmosphere[J]. Solar Energy Materials & Solar Cells, 2017, 164: 146-155.
[9] Wang L, Li B, Shen M,. Corrosion resistance of steel materials in LiCl-KCl melts[J]. International Journal of Minerals, Metallurgy, and Materials, 2012, 19(10): 930-933.
[10] Lu Y, Cheng B, Wang J W,. Corrosion behavior of Cr, Fe and Ni based superalloy in molten NaCl[J]. Rare Metal Materials & Engineering, 2014, 43(1): 17-23.
[11] Vignarooban K, Xu X H, Wang K,. Vapor pressure and corrosivity of ternary metal-chloride molten-salt based heat transfer fluids for use in concentrating solar power systems[J]. Applied Energy, 2015, 159: 206-213.
[12] Vignarooban K, Pugazhendhi P, Tucker C,. Corrosion resistance of Hastelloys in molten metal-chloride heat-transfer fluids for concentrating solar power applications[J]. Solar Energy, 2014, 103: 62-69.
[13] Gomez-Vidal J C, Fernandez A G, Tirawat R,. Corrosion resistance of alumina-forming alloys against molten chlorides for energy production (Ⅰ): Pre-oxidation treatment and isothermal corrosion tests[J]. Solar Energy Materials & Solar Cells, 2017, 166: 222-233.
[14] Judith C, Tirawat R,. Corrosion of alloys in a chloride molten salt (NaCl-LiCl) for solar thermal technologies[J]. Solar Energy Materials & Solar Cells, 2016, 157: 234-244.
[15] 宋明. 多元氯化物熔盐体系的构建及性能研究[D]. 广州: 华南理工大学, 2015. SONG M. Construction and performance study of multi-chloride molten salts system[D]. Guangzhou: South China University of Technology, 2015.
[16] Lee Y Y, McNallan M J. Ignition of nickel in environments containing oxygen and chlorine[J]. Metall. Trans. A, 1987, 18A: 1099-1107.
[17] Reese E, Grabke H J. Effect of sodium chloride to the oxidation of high-alloy chromium-nickel steels and chromium[J]. Mater. Corros., 1993, 43: 547-551.
[18] Hofmeister M, Klein L, Miran H,. Corrosion behaviour of stainless steels and a single crystal superalloy in a ternary LiCl-KCl-CsCl molten salt[J]. Corrosion Science, 2015, 90: 46-53.
[19] Grabke H J, Reese E, Spiegel M. The effects of chlorides, hydrogen chloride, and sulfur dioxide in the oxidation of steels below deposits[J]. Corrosion Science, 1995, 37(7): 1023-1043.
[20] Liu S N, Liu Z D, Wang Y L,. A comparative study on the high temperature corrosion of TP347H stainless steel, C22 alloy and laser-cladding C22 coating in molten chloride salts[J]. Corrosion Science, 2014, 83(6): 396-408.
[21] A.约翰.塞德赖克斯. 不锈钢的腐蚀[M]. 北京: 机械工业出版社, 1986: 15-16.Sedriks A J. Corrosion of Stainless Steel[M]. Beijing: China Machine Press, 1986: 15-16.
[22] ASTM. G1-03 Practice for Preparing, Cleaning, and Evaluating Corrosion Test Specimens[S]. 2011.
[23] BARIN I, PLATZKI G. Thermochemical Data of Pure Substances[M]. 3rd ed. Weinheim: Wiley-VCH, 1995: 525-1293.
[24] Groll M, Brost O, Heine D. Corrosion of steels in contact with salt eutectics as latent heat storage materials: influence of water and other impurities[J]. Heat Recovery Systems & Chp., 1990, 10(10): 567-572.
[25] Dorcheh A S, Durham R N, Galetz M C. Corrosion behavior of stainless and low-chromium steels and In625 in molten nitrate salts at 600℃[J]. Solar Energy Materials and Solar Cells, 2016, 144: 109-116.
[26] 梁成浩. 金属腐蚀性导论[M]. 北京: 机械工业出版社, 1999. LIANG C H. Introduction to Corrosion of Metals[M]. Beijing: China Machine Press, 1999.
[27] 彭海健, 金军, 李德富, 等. Ni-Cr-Mo耐蚀合金在CaCl2-CaF2熔盐中的腐蚀行为[J]. 金属学报, 2011, 47(9): 1195-1199.Peng H J, Jin J, Li D F,. Corrosion behavior of Ni-Cr-Mo corrosion resistance alloys in CaCl2-CaF2molten salt[J]. Acta Metallurgica Sinica, 2011, 47(9): 1195-1199.
[28] David R. Handbook of Chemistry and Physics[M]. 84th ed. CRC Press, 2003: 4-39-4-93.
[29] 林玉珍, 杨德钧. 腐蚀和腐蚀控制原理[M]. 2版. 北京: 中国石化出版社, 2014. LIN Y Z, YANG D J. Principles of Corrosion and Corrosion Control[M]. 2nd ed. Beijing: Sinopec Press, 2014.
[30] SOHAL M S, EBNER M A, SABHARWALL P,. Engineering database of liquid salt thermophysical and thermochemical properties[R]. Idaho Falls: Idaho National Laboratory, 2010.
Corrosion behavior of In625 alloy and 316L stainless steel in NaCl-CaCl2-MgCl2ternary eutectic molten salt
LIU Bo1, WEI Xiaolan1, WANG Weilong2, SONG Ming1, DING Jing2
(1School of Chemistry and Chemical Engineering, South China University of Technology, Guangzhou 510640, Guangdong, China;2School of Engineering, Sun Yat-sen University, Guangzhou 510006, Guangdong, China)
Isothermal corrosion of 316L stainless steel and nickel based Inconel 625 alloy was evaluated by total immersion in eutectic NaCl-CaCl2-MgCl2molten salt at 500—700℃.The effect of chromium (Cr), air contact, and temperature on corrosion was studied. Corrosion dynamic and velocity curves of 316L and Inconel 625 alloy at 600℃ molten salt for 21 d were obtained. X-Ray diffraction (XRD), scanning electron microscope (SEM) and X-ray energy spectrometer (EDX) were used to analyze corrosion products and cross section morphologies. The results show that mass loss of the steel and alloy increases with the increase of air contact and corrosion temperature. Element and morphology of metal surface and cross section after 21 d immersion at 600℃ indicate that Cr has a preferential solubility to other elements, which Cr depletion region was observed across cross-section. The dense layer of corrosion products can reduce corrosion rate. Inconel 625 exhibits better corrosion resistance than austenitic stainless steel in NaCl-CaCl2-MgCl2eutectic molten salt.
chloride molten salt; corrosion; stainless steel; nickel based Inconel 625 alloy
10.11949/j.issn.0438-1157.20170131
TQ 050.9+1
A
0438—1157(2017)08—3202—09
魏小兰。第一作者:刘波(1990—),男,硕士研究生。
NSFC-盐湖集团联合基金项目(U1507121);国家自然科学基金重点项目(51436009)。
2017-02-08收到初稿,2017-05-04收到修改稿。
2017-02-08.
Prof. WEI Xiaolan, xlwei@scut.edu.cn
supported by the NSFC-Salt Lake Group Joint Fund (U1507121) and the National Natural Science Foundation of China (51436009).

