改性膨胀石墨对Hg2+吸附性能研究
徐珊,张国春,曹宝月
(商洛学院化学工程与现代材料学院/陕西省尾矿资源综合利用重点实验室,陕西商洛726000)
改性膨胀石墨对Hg2+吸附性能研究
徐珊,张国春,曹宝月
(商洛学院化学工程与现代材料学院/陕西省尾矿资源综合利用重点实验室,陕西商洛726000)
采用化学氧化法,以硝酸为插层剂,分别以马弗炉和微波炉两种不同膨胀方式制备膨胀石墨;并采用超声沉淀法将纳米氢氧化镁负载在膨胀石墨孔隙中,制得改性膨胀石墨。通过正交实验,考察了改性膨胀石墨投加量、Hg2+初始浓度、反应温度和膨胀方式对Hg2+吸附效果的影响;并初步探讨了改性膨胀石墨吸附Hg2+的机理。
膨胀石墨;吸附;汞离子
在重金属污染物中,汞作为一种特殊的、毒性极强的典型重金属元素备受人们关注。常见的汞治理方法主要有化学沉淀法、电解法、生物法和吸附法。其中,吸附法因具有实用、方便、环保等优点而成为最有潜力的汞污染控制方法[1-2]。
膨胀石墨是由天然石墨鳞片经插层剂和氧化剂处理后,高温膨化得到的疏松多孔的蠕虫状物质[3-4]。前期研究和相关文献证明膨胀石墨对Cr6+和含油废水等都具有较好的吸附效果,但对Hg2+吸附效果有待提高,故对其进行表面改性,实验结果表明对Hg2+具有良好的吸附效果[5-7]。
1 材料与方法
1.1 实验材料及仪器
50目天然鳞片石墨(含碳量>99.5%)、HNO3、HCl、KMnO4、SnCl2、C2H5OH、MgCl·26H2O、NaOH所有试剂均为分析纯,实验用水为去离子水。Hg标准贮备液(国家有色金属及电子材料分析测试中心,1000 μg·mL-1逐级稀释到实验所需浓度)。
QM201荧光测汞仪、HJ-1磁力加热搅拌器、101型电热鼓风干燥器、超声清洗器、循环水式真空泵、电热恒温水浴锅、SX2-2.5-10TP马弗炉、HC-83203FB微波炉、KYKY-2800B扫描电镜(SEM)(日本日立)。
1.2 膨胀石墨的制备及改性
按照50目天然鳞片石墨(g):高锰酸钾(g):硝酸(mL)=1.0:0.15:1.5依次称量反应物,并混合,在室温下搅拌75 min后,水洗至中性,于70℃~80℃下干燥,得到可膨胀石墨。再称取一定量的可膨胀石墨,分别于马弗炉(900℃,30 s)和微波炉(800 W,30 s)中,对其进行高温膨胀,得到膨胀石墨。
称取MgCl2·6H2O溶解于C2H5OH中,然后加去离子水配成150 mL混合溶液,称取一定量膨胀容积优的膨胀石墨加入其中,恒速搅拌,同时缓慢滴入NaOH溶液,继续搅拌得到乳浊液,将该乳浊液超声静置3~4 h。结束后,冷却,过滤,用乙醇进行多次洗涤,抽滤后放于电热鼓风干燥箱中于80℃进行干燥过夜。最终得到纳米氢氧化镁改性的膨胀石墨。
1.3 正交试验的设计
在单因素实验的基础上,设计L16(44)正交实验进行改性EG吸附Hg2+的实验研究,采用静态吸附法,探讨EG加入量、Hg2+的初始浓度、反应温度、EG的膨胀方式对膨胀石墨脱除Hg2+的影响。正交实验因素水平表,见表1。
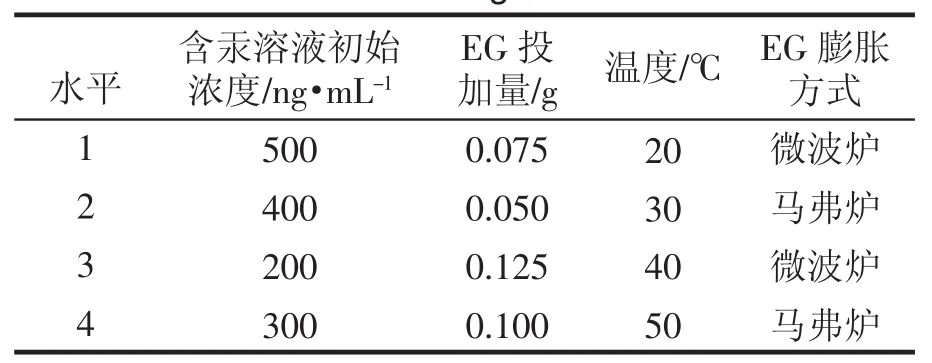
表1 改性EG吸附Hg2+影响因素及水平
根据正交试验,将配制好的含汞溶液400mL和实验所需质量的EG于磁力搅拌器上搅拌180 min,分时间段取样,测其荧光值,参照汞标线和公式计算,考察改性EG对Hg2+的吸附特性[7]。
Hg2+的吸附量:Q=(C0-Ct)·V/m
Hg2+吸附效率:A%=(C0-Ct)/C0×100%
其中Q:吸附Hg2+的量(mg·g-1);m:吸附剂量(g);C0:起始Hg2+浓度(ng·mL-1);Ct:反应时Hg2+浓度(ng·mL-1);V:反应溶液的体积(mL)。
2 结果与讨论
2.1 改性EG投加量对吸附效果的影响
图1显示,随着吸附剂量的增大,脱汞率增大,当改性EG投加量为0.075 g时,Hg2+的去除率达到最大值,为93.3%。初步分析是由于改性EG投加量的增加,使其总比表面积增加,能够吸附Hg2+的活性位点增加,在初始浓度一定的情况下,达到吸附平衡时,溶液中残余Hg2+浓度不断降低,则去除率逐步升高;但当改性EG投加到一定的量时,Hg2+的去除率开始下降,这说明改性EG对Hg2+的吸附已达到饱和,并且有脱附现象发生,因而脱汞率降低[7-8]。
图1还显示,随着改性EG投加量的增大,其对Hg2+的吸附量逐渐降低,当改性EG投加量为0.05 g时,吸附量为最大2.6 mg·g-1。根据吸附平衡规律q=Kc1/n,吸附量随之下降[7]。
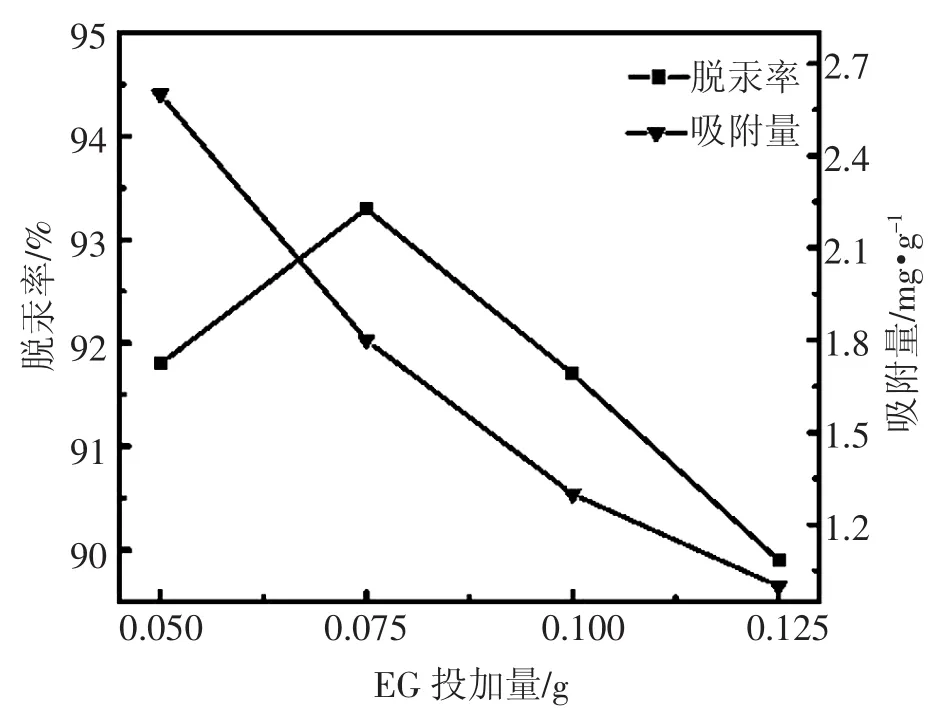
图1 改性EG投加量对吸附效果的影响
2.2 初始浓度对吸附效果的影响
如图2,随着Hg2+浓度增大,去除率和吸附量都逐渐增大。在Hg2+初始浓度为500 ng·mL-1时,改性EG对Hg2+的去除率和吸附量都达到最大值,分别为93.3%和2.4 mg·g-1。因为随着Hg2+浓度的提高,吸附剂与Hg2+的接触几率增加,吸附到吸附剂表面和孔隙中的Hg2+量增加。基于以上实验结果,进行后续实验,考察当浓度继续增加时改性EG对Hg2+的吸附特性,实验结果发现当Hg2+浓度增大到550 ng·mL-1时,EG对Hg2+的吸附量和脱除率都急剧下降,所以,在后续研究改性EG吸附Hg2+的实验中将Hg2+初始浓度定为500 ng·mL-1。
2.3 温度对吸附效果的影响
如图3所示,在30℃时,去除率和吸附量都达到最大值,分别为92.6%和1.8 mg·g-1。但并不是温度越高,吸附效果越好。起初吸附量和脱汞率随着温度的升高而增大,是因为升高温度可以提高Hg2+的迁移速度。但当温度继续升高,同时导致解析速率增加,从而脱汞率和吸附量都降低[7]。
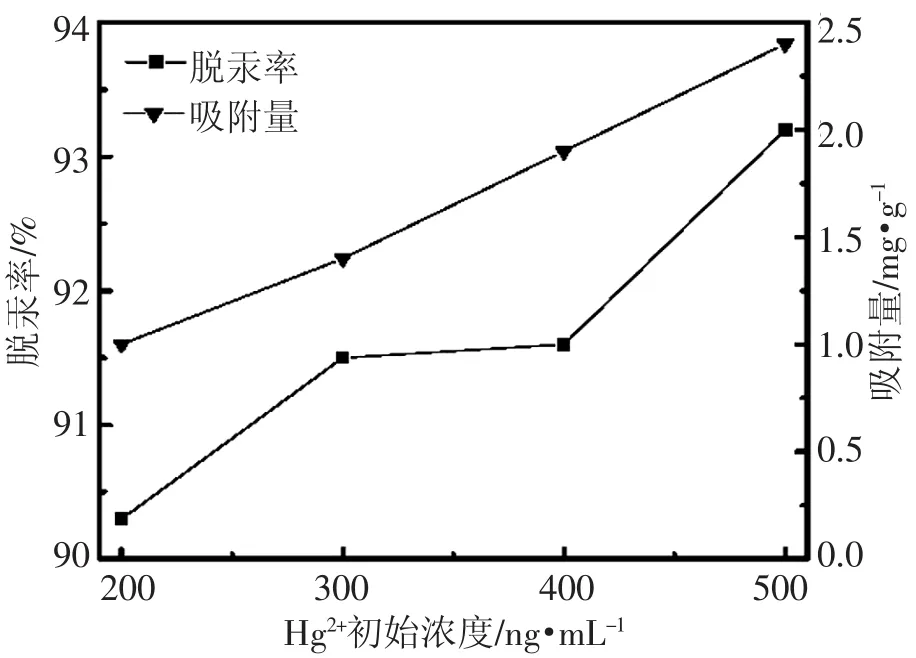
图2 初始浓度对吸附效果的影响
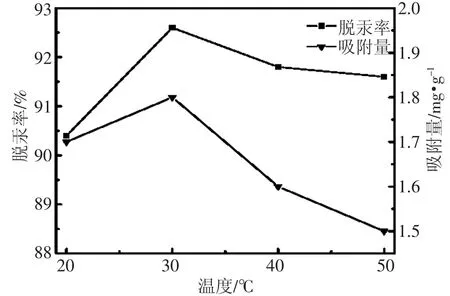
图3 温度对吸附效果的影响
2.4 膨胀方式对吸附效果的影响
由图4可看出,马弗炉膨胀的EG,对Hg2+的去除率和吸附量分别为89%和1.6 mg·g-1;微波炉膨胀的EG对Hg2+的去除率和吸附量分别为94.4%和1.7 mg·g-1。微波法膨胀明显优于马弗炉膨胀所得。
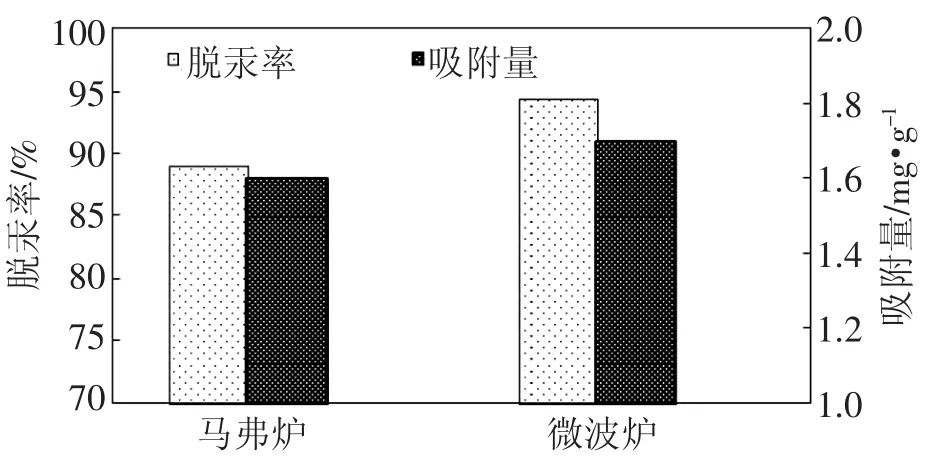
图4 膨胀方式对吸附效果的影响
3 吸附机理分析
3.1 改性膨胀石墨的吸附
3.1.1 物理吸附
图5中,改性EG的形貌同样类似于蠕虫,片层之间形成了许多网状的多边形微细孔。这为吸附Hg2+提供了可能。同时,对于物理吸附,在吸附同时会有解吸现象,参考正交实验数据,发现有脱附现象,所以初步推测有物理吸附作用。

图5 微波膨胀的EG不同倍数下的SEM图
3.1.2 化学吸附
由图6可知,改性EG表面和孔隙中有白色颗粒状物质存在,初步推断是由于强氧化剂浓HNO3存在,导致可能有-OH、-NO2等与Hg2+键合,生成了新的物相[7]。即有化学吸附作用参与。

图6 EG吸附Hg2+后不同倍数下的SEM图
通过EG吸附Hg2+后的EDS能谱,图7可看出:图7中出现的Mg、Mn和Hg吸收峰,证明这三种粒子在膨胀石墨中的存在。Mn吸收峰证明插层反应比较完全,这有利于膨胀石墨在高温膨胀时,有较好的膨胀容积;Mg吸收峰的存在,证明改性时,成功负载纳米氢氧化镁在EG上;Hg吸收峰的存在,说明EG表面吸附了Hg2+。这有可能是Hg2+与EG表面的某些基团发生键合的原因。

图7 EG吸附Hg2+后EDS
3.1.3 膨胀方式的影响
图8和图9分别为马弗炉、微波炉两种膨胀方式制得的EG在相同放大倍数下的SEM图。对比图8与图9可发现,微波炉膨胀制得的EG比马弗炉膨胀的更充分,膨胀容积更大。图8中的石墨的层状结构相对规则,并且显示层间距离较小,而图9中,石墨层间距被最大限度的打开,参考放大后的图片可发现,每一个膨胀石墨微粒都有类似蜂房的结构和很多菱形的小孔,且这些小孔远远大于马弗炉膨胀制得的。这些小孔有利于EG吸附Hg2+。

图9 微波炉膨胀的EG SEM图
3.2 吸附动力学分析
采用准一级、准二级动力学模型对吸附平衡数据进行拟合。结果见图10和图11。
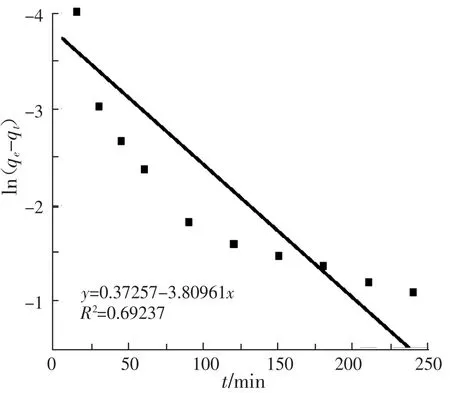
图10 改性EG吸附Hg2+的准一级动力学线性拟合
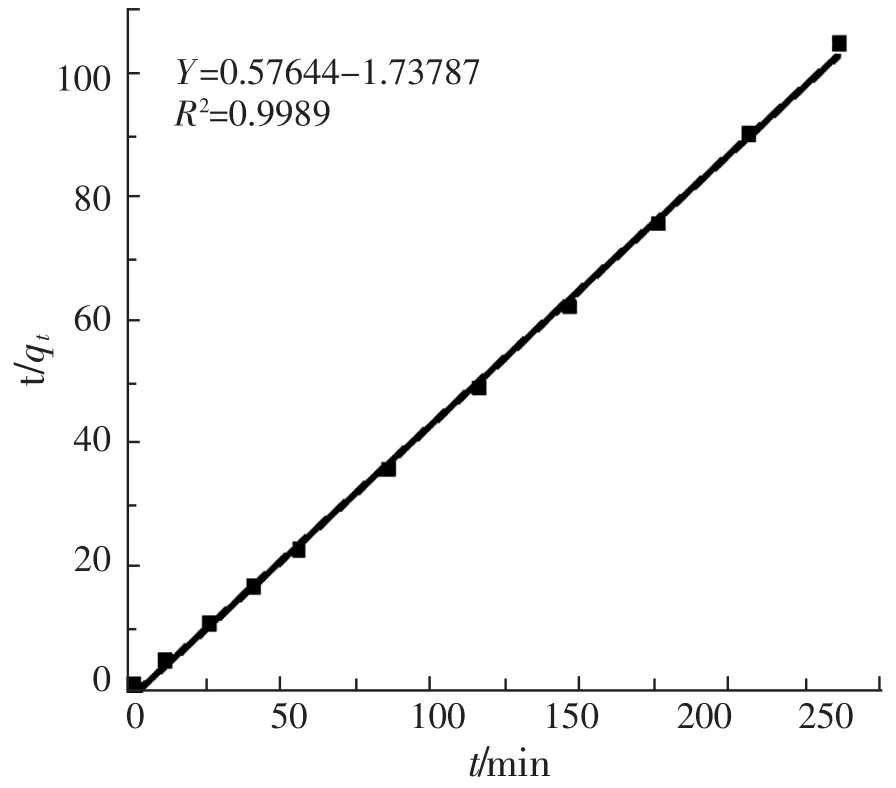
图11 改性EG吸附Hg2+的准二级动力学线性拟合
3.3 吸附等温曲线
采用Langmuir和Freundlich等温方程式对吸附平衡数据进行拟合,结果见图12和图13。
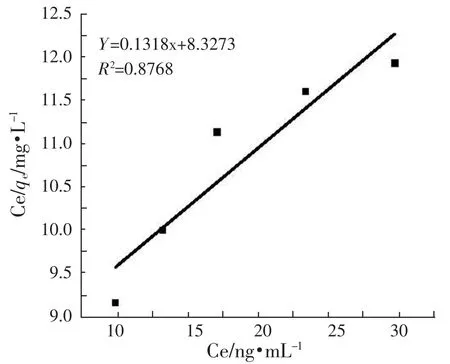
图12 改性EG吸附Hg2+的Langmuir吸附等温线
由线性关系R2可知,改性膨胀石墨对Hg2+的吸附能较好地符合Freundlich等温线,说明改性膨胀石墨吸附剂表面的吸附位点是不均匀的,说明改性膨胀石墨吸附Hg2+不是易吸附过程[10]。
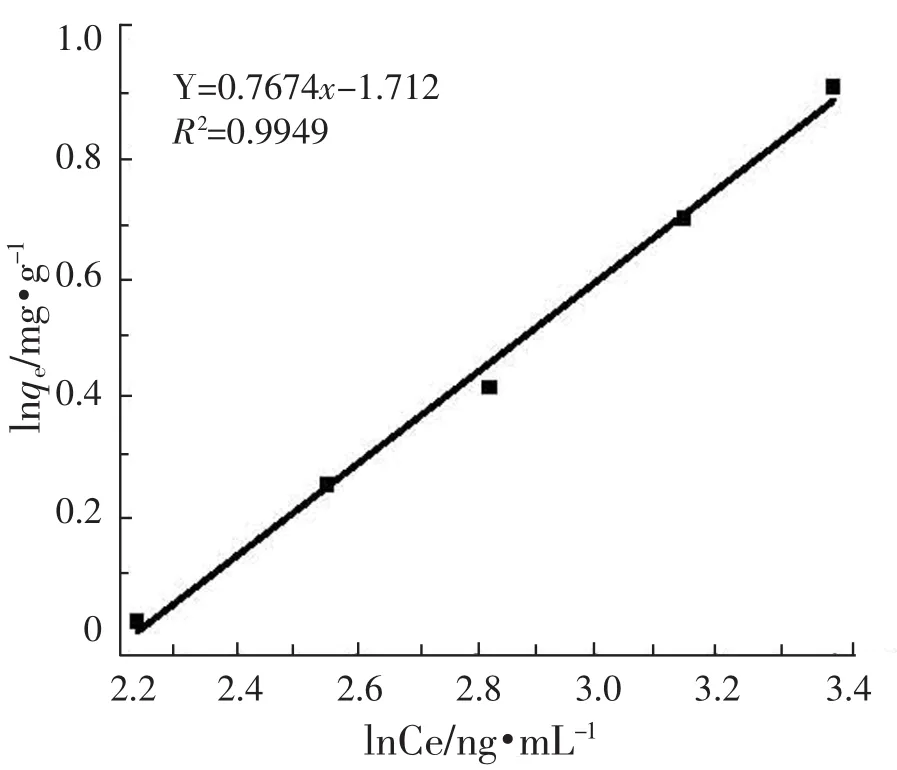
图13 改性EG吸附Hg2+的Freundlich吸附等温线
4 结论
1)正交试验最佳条件为:Hg2+初始浓度:500 ng·mL-1,EG投加量:0.075 g,反应温度:30℃,EG膨胀方式:微波膨胀。此外,改性EG投加量、改性EG膨胀方式、反应温度、Hg2+初始浓度四个因素对脱汞率的影响作用依次减小。
2)通过扫描电镜(SEM)、能量色散谱(EDS)等表征手段的结果初步分析EG吸附Hg2+的机理,应为物理吸附和化学吸附共同作用。
3)改性EG吸附Hg2+过程能更好的符合准二级动力学模型。同时热力学拟合结果表明改性EG吸附Hg2+过程更好的符合Freundlich模型,说明改性膨胀石墨吸附剂表面的吸附位点是不均匀的,其吸附Hg2+不是易吸附过程。
[1]DING X H,WANG R,ZHANG X,et al.A new magnetic expanded graphite for removal of oil leakage[J].Marine Pollution Bulletin,2014,81(12):185-190.
[2]JIN H Y,YUAN J,HAO H Y.The exploration of a new adsorbent as MnO2modified expanded graphite[J].Materials letters,2013,110(7):69-72.
[3]徐珊,曹宝月,牛成吉.无硫膨胀石墨的制备及性能表征[J].硅酸盐通报,2017,3(36):1020-1024.
[4]朱敏聪.膨胀石墨基复合材料的制备、改性及其对水中特定污染物去除的研究[D].上海:东华大学,2012:46-49.
[5]WANG G L,SUN Q R,ZHANG Y Q,et al.Sorption and regeneration of magnetic exfoliated graphite as a new sorbent for oil pollution[J].Desalination,2010,263(7):183-188.
[6]MIEHIO INAGAKI,AKIHIRO KAWAHARA.Recovery of heavy oil from contaminated sand by using exfoliated graphite[J].Desalination.2004,170(8):77-82.
[7]徐珊,曹宝月.无硫膨胀石墨对Cr(VI)的吸附实验研究[J].商洛学院学报,2016,30(6):43-47.
[8]赵颖华,金程,李登新.膨胀石墨对废水中铬的吸附研究[J].环境科学与技术,2012,35(4):149-152.
[9]徐珊,许佩瑶,尹子珺,等.膨胀石墨制备及在环境保护中的应用现状[J].广东化工,2014,41(20):55-56.
[10]李冀辉.以鳞片石墨为原料的多功能碳材料的制备与应用研究[D].保定:河北大学,2009:52-53.
(责任编辑:李堆淑)
Research of Adsorption Performance of Hg2+by Modified Expanded Graphite
XU Shan,ZHANG Guo-chun,CAO Bao-yue
(CollegeofChemicalEngineeringandModernMaterial/ShaanxiKeyLaboratoryofTailings Comprehensive Utilization of Resources,Shangluo University,Shangluo 726000,Shaanxi)
The expanded graphite was prepared by chemical oxidation method with nitric acid as intercalating agent respectively in two different ways:muffle furnace and microwave oven.And the nanosized magnesium hydroxide prepared by the ultrasonic precipitation method is loaded into the expanded graphite pores to obtain the modified expanded graphite.The effects of modified expansive graphite dosage,Hg2+initial concentration,reaction temperature and expansion mode on the absorption of Hg2+by modified expanded graphite were investigated by orthogonal experiment.The adsorption mechanism of Hg2+by expanded graphite was also discussed.
expanded graphite;adsorption;mercury ions
X703
:A
:1674-0033(2017)04-0049-05
10.13440/j.slxy.1674-0033.2017.04.011
2017-05-23
商洛市科学技术研究计划项目(SK2015-20)
徐珊,女,陕西周至人,硕士,助教

