舒洛地特联合坎地沙坦治疗糖尿病肾病4期患者临床疗效观察
龚春水,许树根,胡玉清, 卞小燕,梁 萌
·论 著·
舒洛地特联合坎地沙坦治疗糖尿病肾病4期患者临床疗效观察
龚春水,许树根,胡玉清, 卞小燕,梁 萌
目的 观察舒洛地特联合坎地沙坦治疗糖尿病肾病4期的临床疗效。 方法 选取厦门大学附属成功医院于2014年8月至2015年10月间收治的48例糖尿病肾病4期患者作为研究对象,并将其随机分为舒洛地特组(14例)、坎地沙坦组(17例)及联合治疗组(17例),所有患者均随访12周,比较各组患者的临床有效率、24 h尿蛋白、血浆白蛋白(ALB)、血肌酐(SCr)、总胆固醇(CHOL)、纤维蛋白原(FIB)。 结果 治疗后3组患者尿蛋白水平较治疗前明显改善(P<0.05),舒洛地特组尿蛋白量下降水平与坎地沙坦组比较差异无统计学意义(P>0.05),联合治疗组尿蛋白量下降水平优于单独用药两组(P<0.05),舒洛地特及联合治疗组治疗后FIB有显著下降(P<0.05)。各组患者ALB、SCr、CHOL在治疗前后比较差异无统计学意义(P>0.05)。 结论 舒洛地特联合坎地沙坦能有效减少糖尿病肾病4期患者的尿蛋白水平,效果优于单一用药。
舒洛地特;坎地沙坦;糖尿病肾病;临床疗效
糖尿病肾病(diabetic nephropathy,DN)作为糖尿病患者的重要并发症之一,是导致终末期肾病(ESRD)最重要的原因之一,严重威胁了患者的生命健康。目前临床针对DN的治疗手段有限,主要采用血管紧张素2受体阻滞剂(ARB)类药物,同时配合控制血糖、血压以及限制蛋白尿摄入等基础治疗。舒洛地特是一种天然血管壁糖胺聚糖(glycosaminoglycans,GAG),国外部分临床研究显示它能有效降低DN患者的蛋白尿[1-2]。本研究观察了舒洛地特及坎地沙坦对DN4期患者的临床疗效。
1 资料与方法
1.1 一般资料 随机选取我院于2014年8月至2015年10月间收治的48例DN4期患者作为研究对象,所有患者均符合糖尿病肾病诊断标准[3]。根据糖尿病病史,尿检蛋白尿为主,少或无镜下血尿,结合眼底血管、心脑血管等糖尿病血管损害情况,同时排除其他原因肾病,临床诊断糖尿病肾病,其中3例患者通过肾活检确诊。纳入标准:DN4期即24 h尿蛋白>0.5 g,肾功能正常。排除标准:妊娠期妇女,肝功能异常、肿瘤、严重心脑血管并发症等患者。按照患者编号再用随机数字表的方法分为舒洛地特组(14例)、坎地沙坦组(17例)及联合治疗组(17例)。所有患者平均年龄为(46.48±7.63)岁,平均病程为(17.34±4.38)年,其中男31例,女17例。各组患者在性别、年龄以及病程方面比较差异无统计学意义(P>0.05),见表1。本研究经医院伦理委员会批准(批准号:第s2014-021-02号),患者均签署知情同意书。
表1 各组糖尿病肾病4期患者一般资料比较
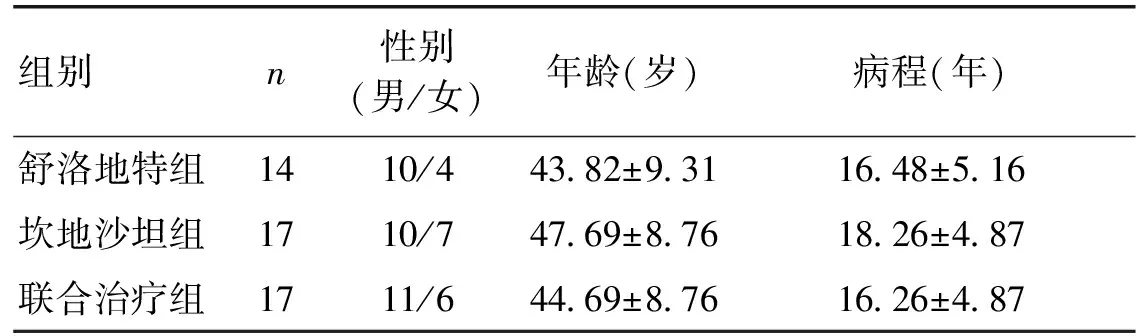
组别n性别(男/女)年龄(岁)病程(年)舒洛地特组1410/443 82±9 3116 48±5 16坎地沙坦组1710/747 69±8 7618 26±4 87联合治疗组1711/644 69±8 7616 26±4 87
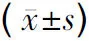
项目舒洛地特组(n=14)坎地沙坦组(n=17)联合治疗组(n=17)治疗前治疗后治疗前治疗后治疗前治疗后尿蛋白(g/24h)2.37±0.842.02±0.53∗#2.27±0.572.01±0.64∗#2.27±0.481.75±0.55∗ALB(g/L)29.5±4.8430.2±3.7828.7±4.7729.3±5.2129.3±4.9830.5±5.24SCr(μmol/L)83.21±7.3281.25±6.7484.38±7.6985.16±6.5386.16±7.2887.06±5.96CHOL(mmol/L)5.84±2.745.84±2.745.84±2.745.84±2.745.84±2.745.84±2.74FIB(g/L)3.24±1.743.27±0.79∗3.24±1.743.24±1.743.24±1.743.24±1.74∗与本组治疗前比较,∗P<0 05;与联合治疗组比较,#P<0 05
1.2 治疗方法 所有患者均给予相同的常规治疗,即给予糖尿病饮食,口服降糖药或者根据患者不同体质皮下注射胰岛素,同时保持适当运动,当空腹血糖(FBG)稳定控制在7 mmol/L以下,同时糖化血红蛋白稳定控制在7%以下时,舒洛地特组患者给予舒洛地特软胶囊(意大利阿尔法韦士曼药厂)1000 LSU/次,2次/d口服,治疗4周后,改舒洛地特软胶囊500 LSU/次,2次/d口服;坎地沙坦组患者给予坎地沙坦片(天津武田药品有限公司)8 mg口服,1次/d;联合治疗组患者在舒洛地特的基础上联用坎地沙坦。3组患者均持续治疗12周。
1.3 观察指标 疗程结束后,观察比较3组患者的临床有效率、24 h尿蛋白、血浆白蛋白(ALB)、血肌酐(SCr)、总胆固醇(CHOL)、纤维蛋白原(FIB)。当患者24 h尿蛋白在0.15 g以下,或者下降幅度超过50%时,则定义为有效[3]。药品不良反应观察:记录3组患者严重恶心、呕吐、牙龈出血、眼底出血、皮下出血等药品不良反应发生情况。

2 结 果
2.1 临床疗效比较 舒洛地特组经治疗后有8例有效,临床有效率为57.1%;坎地沙坦组治疗后有10例有效,临床有效率为58.8%;联合治疗组治疗后有14例有效,临床有效率为82.4%;联合治疗组有效率优于其他2组(P<0.05)。
2.2 治疗前后各项实验室指标检查结果 治疗12周后,3组患者的尿蛋白定量较前均有显著下降(P<0.05),组间比较,联合治疗组尿蛋白定量下降优于单独用药两组(P<0.05)。舒洛地特组与坎地沙坦组比较,尿蛋白定量下降差异无统计学意义(P>0.05)。治疗前后比较,舒洛地特组和联合治疗组FIB有显著下降(P<0.05),各组治疗前后血浆白蛋白、肾功能、总胆固醇差异无统计学意义(P>0.05)。见表2。
2.3 药品不良反应发生情况 坎地沙坦组和联合治疗组各出现1例轻微恶心、呕吐,未予特殊处理,1 d后症状自行缓解。3组患者均未出现牙龈出血、眼底出血等不良反应。
3 讨 论
DN是糖尿病患者最常见的一种严重并发症,其主要的病理表现为肾小球系膜细胞的增生、基底膜的增厚以及肾小球的硬化[4-5]。目前对于DN发病机制的研究也较为广泛,研究显示其是一种多因素综合作用所导致的一种糖尿病微血管并发症,其中糖代谢以及脂质代谢的紊乱,同时肾脏血流动力学、多种细胞因子、肾素-血管紧张素系统的改变等都在DN的发病过程中起到了重要的作用[6-7],其中肾素-血管紧张素系统在患者凝血、纤溶等方面起重要作用[8-9]。在临床上,DN的早期症状为微量的蛋白尿,因此及时有效地减少患者蛋白尿以及蛋白尿存在时间,是治疗或者延缓糖尿病肾病发展的重要手段[10]。
目前临床上采用的ARB类药物在治疗DN方面取得了一定的临床疗效,因为其能够降低肾小球高压,减少蛋白尿;降低系膜细胞吞噬大分子的能力;同时促进基质金属蛋白酶的降解,从而分解已形成的细胞基质[11]。通过本研究结果也表明,ARB类药物能够显著降低DN患者的24 h尿蛋白。
舒洛地特是一种对动脉和静脉均具有强烈抗血栓作用的葡糖胺聚糖。由于糖尿病肾病患者内皮细胞膜、基底膜以及细胞外基质上糖胺聚糖的丢失,从而使患者的血管通透性发生改变,导致白蛋白、纤维蛋白等高分子的渗漏,而这些大分子的渗漏在肾脏则直接表现为蛋白尿[12-13]。既往研究表明舒洛地特作为血管壁的主要成分,能够通过对血管壁上电荷的保留,同时增强血管壁基底膜和细胞外基质功能,抑制凝血酶与胶原的释放,从而使血管壁的通透选择性得以维持,起到减少蛋白尿的作用[14-15]。通过本研究也证实舒洛地特能够显著降低患者血中FIB,说明其能够有效改善肾小球内微血栓形成,具有明显的肾脏保护作用。
通过本研究结果发现,单用舒洛地特可以显著减少DN 4期患者蛋白尿,与坎地沙坦疗效相当。联合应用舒洛地特及坎地沙坦效果优于单一用药,二者在作用机制上是否有协同作用尚不清楚,需要更多的样本数及更进一步的机制研究。
[1] Gambaro G,Kinalska I,Oksa A,etal.Oral sulodexide reduces albuminuria in microalbuminuric and macroalbuminuric type 1 and type 2 diabetic patients:the Di.N.A.S.randomized trial[J]. J Am Soc Nephrol,2002,13(6):1615-1625.
[2] 王扬天,彭 丽,叶小珍,等.舒洛地特治疗糖尿病肾病合并视网膜病变的临床疗效观察[J]. 医学研究生学报,2010,23(12):1269-1272.
[3] 中华中医药学会肾病分会.糖尿病肾病诊断、辨证分型及疗效评定标准(试行方案)[J]. 上海中医药杂志,2007,41(7):7-8.
[4] Jha JC,Gray SP,Barit D,etal.Genetic targeting or pharmacologic inhibition of NADPH oxidase Nox4 provides renoprotection in long-term diabetic nephropathy[J]. J Am Soc Nephrol,2014,25(6):1237-1240.
[5] 陈惠萍.糖尿病肾病患者肾小球滤过膜结构和功能及代谢指标的再认识[J]. 医学研究生学报,2010,23(8):785-791.
[6] 林可意,曾龙驿,舒 冏,等.舒洛地特对糖尿病大鼠尿白蛋白排泄率及肾脏转化生长因子-β1表达的影响[J].中华糖尿病杂志,2009,1(3) : 196-200.
[7] 邵加庆.局部肾素-血管紧张素系统在2型糖尿病中的作用[J]. 医学研究生学报,2011,24(5):449-452.
[8] Tiurenkov IN,Voronkov AV,Slietsans AA,etal. Effects of mexidol and sulodexide on the level of specific markers of endothelial dysfunction in animals with experimental diabetes mellitus [J]. Eksp Klin Farmakol,2012,75(5):14-16.
[9] Masola V, Onisto M,Zaza G,etal.A new mechanism of action of sulodexide in diabetic nephropathy: inhibits heparanase-1 and prevents FGF-2-induced renal epithelial-mesenchymal transition [J]. J Transl Med,2012,10(1):213-216.
[10] 万 倩,张 倩,薛耀明,等. 2型糖尿病肾病患者白蛋白尿的危险因素分析[J]. 实用医学杂志,2015,31(8):1234-1237.
[11] Parving HH, Lehnert H, Brochner-Mortensen J,etal. The effect of Irbesartan on the development of diabetic nephropathy in patients with type 2 diabetes[J]. N Engl J Med,2001,34(5): 870-878.
[12] Packham DK,Wolfe R,Reutens AT,etal.Sulodexide fails to demonstrate renoprotection in overt type 2 diabetic nephropathy[J]. J Am Soc Nephrol,2012,23(1):123-130.
[13] 杨 玲.D-二聚体、纤维蛋白原及抗凝血酶III联合检测对早期2型糖尿病肾病的诊断价值[J]. 东南国防医药,2015,17(4):402-403.
[14] Tak E,Ridyard D,Kim JH,etal.CD73-Dependent generation of adenosine and endothelial adora2b signaling attenuate diabetic nephropathy [J]. J Am Soc Nephrol,2014,25(3):547-563.
[15] 杨绪枫,汪年松.舒洛地特治疗糖尿病肾病作用机制的研究进展[J]. 中国中西医结合肾病杂志,2011,12(4):365-367.
(本文编辑:叶华珍;英文编辑:王建东)
Efficacy observation of sulodexide and candesartan on 48 cases with diabetic nephropathyIV stage
GONG Chun-shui, XU Shu-gen, HU Yu-qing, BIAN Xiao-yan,LIANG Meng
(DepartmentofNephrology,theCheng-gongAffiliatedHospitalofXiamenUniversity,Xiamen361003,Fujian,China)
Objective To explore the clinical effect of sulodexide and candesartan on patients with diabetic nephropathy IV stage. Methods 48 patients with DN-IV stage were randomized divided into sulodexide group (14 cases), candesartan group (17 cases), candesartan and sulodexide group(17 cases) from 2014 August to 2015 October in the Cheng-gong Affiliated Hospital of Xiamen University. The follow-up was 12 weeks. After the treatment, the clinical efficiency, 24 h urinary protein, plasma albumin(ALB),serum creatinine (SCr), total cholesterol(CHOL), fibrinogen(FIB) were compared in three groups. Results Compared with those before treatment, the urinary protein of the three groups after treatment was significantly lower (P<0.05); while the 24 h urinary protein of sulodexide group and candesartan group was not significant different (P>0.05), and the urinary protein of the candesartan and sulodexide group were better than the other two groups (P<0.05); After the treatment the FIB of sulodexide group and candesartan and sulodexide group was significantly decreased (P<0.05); while there was no significant difference in ALB, SCr and CHOL of those groups before and after treatment (P> 0.05). Conclusion Sulodexide and candesartan get a satisfactory result on reducing the urinary protein level in the treatment of diabetic nephropathy IV stage.
Sulodexide; Candesartan; Diabetic nephropathy; Clinical effect
361003厦门,厦门大学附属成功医院肾内科
梁 萌,E-mail:liangmeng666@vip.163.com
龚春水,许树根,胡玉清,等.舒洛地特联合坎地沙坦治疗糖尿病肾病4期患者临床疗效观察[J].东南国防医药,2017,19(3): 248-250.
R587.1;R587.24
A
1672-271X(2017)03-0248-03
10.3969/j.issn.1672-271X.2017.03.006
2016-08-17;
2017-04-23)

