响应面法优化水产品低温保鲜冰配方的研究
,,,,,, ,
(1.中国水产科学研究院南海水产研究所,农业部水产品加工重点实验室,国家水产品加工技术研发中心,广东广州 510300;2.上海海洋大学食品学院,上海 201306)
响应面法优化水产品低温保鲜冰配方的研究
袁小敏1,2,郝淑贤1,*,李来好1,杨贤庆1,林婉玲1,赵永强1,黄卉1,胡晓1
(1.中国水产科学研究院南海水产研究所,农业部水产品加工重点实验室,国家水产品加工技术研发中心,广东广州 510300;2.上海海洋大学食品学院,上海 201306)
为解决保鲜介质温度波动大以及保冷时间短对水产品鲜度的影响,本文以聚丙烯酸钠、氯化钠、丙二醇为主要成分,对水产品低温保鲜冰的配方进行优化。在单因素实验的基础上,依据Box-Behnken实验设计原理,采用响应面进行分析,以优化最佳的低温保鲜冰配方。结果表明:低温保鲜冰的最佳配方为聚丙烯酸钠1.0%、氯化钠0.6%、丙二醇2.1%,此低温保鲜冰可在水产品微冻温度带(-3~-1.5 ℃)维持130 min,与传统盐水介质相比延长约60 min。该低温保鲜冰维持低温时间更长、温度更加稳定,能更有利于水产品的贮藏加工。
保鲜,低温保鲜冰,响应面法,配方优化
水产品由于水分含量高,富含蛋白质与不饱和脂肪酸等营养物质,在运输、贮藏、加工与销售过程中易受到地区和季节等因素的影响,使微生物繁殖过快,加速脂肪氧化等,使水产品的鲜度下降[1-2]。微冻保鲜是将水产品保藏在其冰点及冰点以下1~2 ℃或冻结点附近的一种轻度冷冻保鲜方式[3]。在此温度下,水产品内部水分部分发生冻结,因此对原材料的组织结构影响较小,从而有效抑制微生物的生长繁殖与酶的活性。虽然微冻保鲜的时间较冷冻保鲜时间短,但能有效避免冷冻保藏导致的水产品品质劣化现象,从而较好保持产品品质[4-7]。根据鱼类等水产品冻结点的特征,通常选取微冻温度为-3 ℃左右,在此温度下能有效保证原材料的新鲜品质[8-10]。微冻保鲜中最常见的制冷剂就是冰盐水混合物,但该制冷剂在微冻过程中易出现温度不稳定、冰融化速度快与温度易回升等问题,从而对水产品的鲜度造成影响[9,11]。
目前我国长途贮运流通环节仍以冰鲜[12]为主要保鲜方式,微冻[13]对设备的要求较高,流化冰[14](流化冰超冷却)多用于产品的降温预处理环节,流通过程中的低温控制方面尚属空白。本研究通过降低冰的温度,延长冰融时间,变相实现贮运环节的低温控制,继承传统冰藏保鲜使用方便特点的同时,最大限度延长水产品贮藏和销售过程中的生鲜品质。为进一步满足水产品保鲜的实际要求,解决传统冰鲜介质的不足,本文选用对人体健康无害的聚丙烯酸钠、氯化钠、丙二醇与水作为低温保鲜冰的主要组成成分,可降低传统贮藏介质的冰点到达微冻的温度,通过单因素筛选与响应面分析确定其最佳配比,以有效保持其温度稳定,从而更好应用于水产品的保鲜中。
1 材料与方法
1.1材料与仪器
丙二醇 天津市大茂化学试剂厂;氯化钠 广州化学试剂厂;聚丙烯酸钠 山东西亚化学工业有限公司,以上试剂均为分析纯。
DW-86L626型超低温冰箱 中国山东青岛海尔集团;735-2型温度测量仪 德国德图仪器公司;IN612C型恒温箱 日本YAMATO公司;JJ500Y型电子天平 常熟市双杰测试仪器厂。
1.2实验方法
1.2.1 低温保鲜冰冻结点及融化时间测定 配制低温保鲜冰溶液200 mL于塑料烧杯中,将温度测量仪探头浸入溶液中心点且固定,探头另一端连接温度测量仪的接口,开启温度时间模式,可连续记录一段时间内的温度变化情况。将烧杯放置于-60 ℃冰箱速冻,待其温度降至(-5±1)℃时取出,再放置于20 ℃的恒温箱中测定-3~-1.5 ℃时的温度变化情况,每隔1 min记录一次温度。根据温度测量仪所记录的数据分别绘制出保鲜冰溶液的冻结曲线以及融化曲线。在冻结曲线中最为平滑的一段即为保鲜冰的冻结点[15]。
1.2.2 单因素实验 选取氯化钠浓度1%,丙二醇体积分数2%,配制聚丙烯酸钠浓度分别为0、0.5%、1.0%、1.5%、2.0%的低温保鲜冰溶液,记录在20 ℃的环境中融化保持温度在-3~-1.5 ℃时的时间。
选取聚丙烯酸钠浓度1%,丙二醇体积分数2%时,配制氯化钠浓度分别为0、0.5%、1.0%、1.5%、2.0%的低温保鲜冰溶液,记录在20 ℃的环境中融化保持温度在-3~-1.5 ℃时的时间。
选取聚丙烯酸钠浓度为1%,氯化钠浓度为0.5%,配制丙二醇体积分数分别为1.0%、1.5%、2.0%、2.5%、3.0%的低温保鲜冰溶液,记录在20 ℃的环境中融化保持温度在-3~-1.5℃时的时间。
1.2.3 Box-Behnken实验设计 根据单因素实验所得结果,采用响应面设计并运用Box-Behnken实验设计原理,以温度在-3~-1.5 ℃的融化时间为响应值,选择3个因素聚丙烯酸钠质量分数(A)、氯化钠质量分数(B)、丙二醇体积分数(C)设计三因素三水平响应面分析实验,实验因素水平见表1。

表1 响应面实验因素水平Table 1 The factor level of response surface methodology
1.3数据处理
数据以平均值±标准差(Mean±SD)表示。采用Excel 2003对数据进行分析,利用软件Origin 8.5绘制曲线,利用Design expert 8.0.6.1进行响应面分析。
2 结果与分析
2.1单因素分析结果
2.1.1 聚丙烯酸钠质量分数对低温保鲜冰冻结点及融化时间的影响 聚丙烯酸钠是一种白色粉末,同时具有亲水和疏水基团的高分子化合物,广泛应用于食品制造业,由于其具有增稠特性,常被用作食品胶以及在蓄冷领域的吸水性树脂[16-18]。
由图1可知,聚丙烯酸钠质量分数的增加对冻结点的影响显著(p<0.05),温度在-1.2至-1.4 ℃范围内波动。当聚丙烯酸钠质量分数为1.0%时融化时间最长,后随着聚丙烯酸钠质量分数的增加,低温保鲜冰的融化时间反而下降。这是由于聚丙烯酸钠与水和丙二醇结合形成了凝胶,可以保持水分不流失[19]。当聚丙烯酸钠含量较低时,三者充分融合,但随着其浓度的增大反而不利于与丙二醇和水的融合,从而导致融化时间下降。因此,在氯化钠和丙二醇的质量和体积确定时聚丙烯酸钠质量分数约为1.0%最佳。

图1 聚丙烯酸钠质量分数对冻结点及融化时间的影响Fig.1 Effect of sodium polyacrylate concentration on the freezing point and thawing time
2.1.2 氯化钠质量分数对低温保鲜冰冻结点及融化时间的影响 盐水因其传热系数大,对水产品冷却的速度较快,可有效保证渔获物的鲜度,早被用作保鲜介质进行渔船上水产品制冷保鲜的工艺研究。但由于盐水易腐蚀设备,且易渗透,会对原料的风味与品质造成影响。低温盐水冰保鲜工艺的关键在于需要选择合适的盐水浓度,过高或者过低都会对水产品的鲜度产生影响[20-21]。
由图2得出氯化钠质量分数每增加0.5%,冻结点下降约0.3 ℃。在氯化钠质量分数约为0.5%时,低温保鲜冰融化时间最长。随着氯化钠的质量增加,低温保鲜冰的融化时间反而下降。这主要是由于氯化钠的用量增加,降低了其溶液冰点,从而导致冰在-3~-1.5 ℃时的融化时间缩短。梁昌[22]对氯化钠的冰点以及融化速率进行研究,结果表明冰点与盐的含量成反比关系,同时融化速率会随盐含量的增加而加快,与该实验得到结果一致。因此选择氯化钠的质量分数为0.5%。
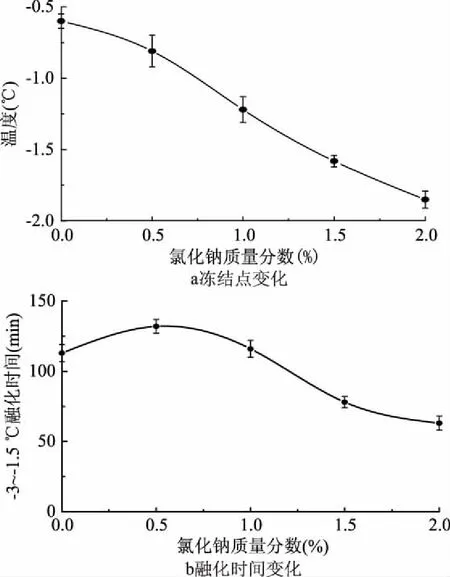
图2 氯化钠质量分数对冻结点及融化时间的影响Fig.2 Effect of sodium chloride concentration on the freezing point and thawing time
2.1.3 丙二醇体积分数对低温保鲜冰冻结点及融化时间的影响 配制低温保鲜冰中聚丙烯酸钠1%、氯化钠0.5%,考察丙二醇体积分数为1.0%~3.0%时的融化时间。
由图3可知,丙二醇的体积分数由1.0%增至3.0%,其低温保鲜冰的冰点下降约0.4 ℃。丙二醇体积分数为2.0%时低温保鲜冰融化时间最长,在其他条件不变的情况下,增减丙二醇的用量都会缩短低温保鲜冰的融化时间。因此,选择丙二醇的体积分数约为2.0%。

图3 丙二醇体积分数对冻结点及融化时间的影响Fig.3 Effect of propylene glycol concentration on the freezing point and thawing time
2.2响应面法优化低温保鲜冰配方
2.2.1 响应面实验结果与分析 在单因素的实验结果基础上,按照表1实验方案进行实验设计,响应面分析与结果见表2。表2中实验1~12为析因实验,13~17为中心实验,以此判断实验误差的大小。利用Design-Expert 8.0.6.1 软件对表2实验数据进行多元回归拟合,得到保鲜冰在-3~-1.5 ℃的融化时间为响应值的回归方程为:
Y=132+6.38A+5.50B+8.13C-6.50AB-5.25AC-6.50BC-18.38A2-11.13B2-19.37C2

表2 响应面实验设计及结果Table 2 Experimental design and the results of response surface methodology

表3 回归方程的方差分析Table 3 Analysis of variance of fitted regression model
注:**,p<0.01,极显著;*,p<0.05,显著。
上述回归方程中各因素与响应值之间的关系见表3,得出模型的p<0.05(显著),失拟项检验的p>0.05(不显著),说明回归方程的拟合程度很好,不存在模型拟合不足的现象,表明残差由随机误差引起。同时R2=0.9804再次表明模型充分拟合实验数据具有可靠的说服力,可利用此回归方程确定保鲜冰融化时间的最佳配比[23]。结果表明,AB、AC、BC对响应值影响显著,A、B、C、A2、B2、C2对响应值影响极显著,各因素对响应值影响大小的排序为C>A>B。
2.2.2 响应曲面分析与优化 根据模型方程得到低温保鲜冰配方的三维空间曲面图见图4~图6。响应面的三维空间图可直观、形象表现出各实验因子之间的相互作用对保鲜冰融化时间的影响。每个响应面都是将其中两个因素对保鲜冰融化时间的影响进行分析比较,另一个因素则固定在零水平,若图形中的曲线陡峭,则表明该因素对保鲜冰融化时间的影响越大[24-25]。从图4可以看出聚丙烯酸钠质量分数和氯化钠质量分数对保鲜冰融化时间的影响,表示聚丙烯酸钠的曲线要比氯化钠的曲线陡峭,因此聚丙烯酸钠对保鲜冰融化时间的影响较大。由图5可得出丙二醇体积分数对保鲜冰融化时间的影响要大于聚丙烯酸钠质量分数。由图6表明氯化钠质量分数的曲线比丙二醇体积分数的曲线较为平滑,因此氯化钠质量分数的增减对保鲜冰融化时间的影响要小于丙二醇体积分数。
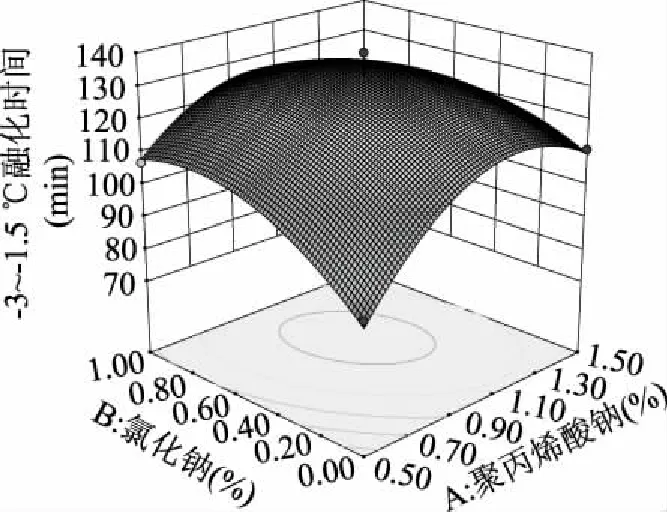
图4 聚丙烯酸钠和氯化钠质量分数对保鲜冰融化时间影响的响应曲面图Fig.4 Response surface plot showing the interactive effects of sodium polyacrylate and sodium chloride concentration on the thawing time of fresh ice
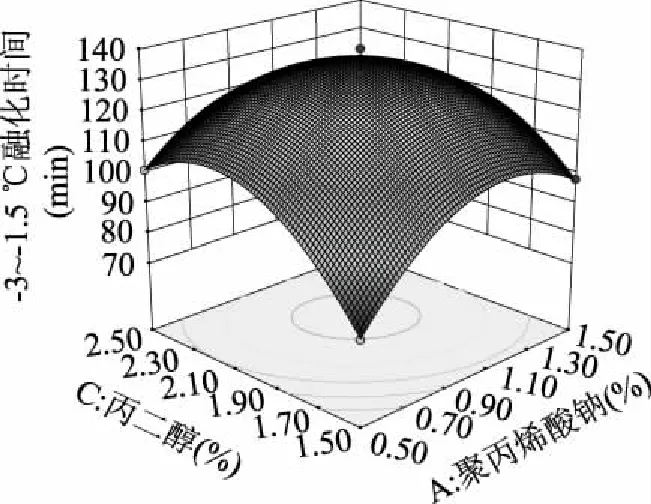
图5 聚丙烯酸钠质量分数和丙二醇体积分数对保鲜冰融化时间影响的响应曲面图Fig.5 Response surface plot showing the interactive effects of sodium polyacrylate and propylene glycol concentration on the thawing time of fresh ice

图6 氯化钠质量分数和丙二醇体积分数对保鲜冰融化时间影响的响应曲面图Fig.6 Response surface plot showing the interactive effects of sodium chloride and propylene glycol concentration on the thawing time of fresh ice
通过模型方程得出最佳低温保鲜冰溶液配比为聚丙烯酸钠1.06%、氯化钠0.58%、丙二醇2.08%,同时预测保鲜冰在-3~-1.5 ℃融化时间为133.5 min。根据实际操作与方便结果计算,最终得出保鲜冰溶液的最佳配方:聚丙烯酸钠1.0%、氯化钠0.6%、丙二醇2.1%。经实验验证保鲜冰在-3~-1.5 ℃融化时间为(130±4) min,与预测结果偏差较小(RSD 1.88%)。因此,响应面法对水产品低温保鲜冰配方的优化是可行的,得到的保鲜冰具有实际应用价值。
2.3低温保鲜冰与传统氯化钠盐水冰比较
传统常用3%左右的冰盐水混合物作为冰藏保鲜的介质[11],图7将传统2%、3%盐水冰与本实验所研究的低温保鲜冰分别进行对比。结果发现,盐的浓度越高越易融化,2%与3%浓度的盐水冰在-3~-1.5 ℃维持时间仅有74与67 min,而本研究配制的微冻保鲜冻结液可维持130 min,融化时间延长了约60 min。有研究表明,使用聚丙烯酸钠为原料得到的高分子吸水树脂制得的冰比普通冰融化时间延长了50 min,有效的延长了相变时间[17]。总之低温保鲜冰能更好的延长温度持续的时间且更加稳定,因此更有利于水产品的保鲜。

图7 不同溶剂的保鲜冰融化时间的影响Fig.7 Effect of different solvents on the thawing time of fresh ice
3 结论
通过进行聚丙烯酸钠、氯化钠、丙二醇对低温保鲜冰融化时间影响的单因素实验,应用Box-Behnken实验设计和响应面分析法对保鲜冰配方进行优化,所得到的模型能较好反映各因素对响应值的影响。最终得到优化的保鲜冰配方为:聚丙烯酸钠1.0%、氯化钠0.6%与丙二醇2.1%。此保鲜冰可维持在水产品微冻温度带-3~-1.5 ℃间约130 min,与传统的以盐水为介质的保鲜冰在相同条件下相比融化时间延长了约60 min。本低温保鲜冰可应用于水产品的微冻保鲜贮藏中,操作方便,安全可靠。
[1]赵良,岑剑伟,李来好,等.高压静电场结合冰温气调保鲜技术对罗非鱼鱼片品质的影响[J].南方水产科学,2016,12(3):91-97.
[2]郝淑贤,何丹,魏涯,等.鱼卵加工产品类型与鱼籽酱保鲜技术研究进展[J].南方水产科学,2014,10(3):104-108.
[3]Bahuaud D,Morkore T,Langsrud O,et al. Effects of -1.5 ℃ super-chilling on quality of Atlantic salmon(Salmosalar)pre-rigor Fillets-Cathepsin activity,muscle histology,texture and liquid leakage[J]. Food Chemistry,2008,111(2):329-339.
[4]Gallart-Jornet L,Rustad T,Barat JM,et al. Effect of superchilled storage on the freshness and salting behavior of Atlantic salmon(Salmosalar)fillets[J]. Food Chemistry,2007,103(4):1268-1281.
[5]罗永康,孔春丽,王回忆.低盐低糖处理鲟鱼片冷藏过程中品质变化规律[J].南方水产科学,2016,12(2):95-101.
[6]Magnussen O M,Haugland A,Torstveit AK,et al. Advances in superchilling of food-process characteristics and product quality[J]. Trends in food Science & Technology,2008,19(8):418-424.
[7]Kaale L D,Eikevik T M. Changes of proteins during superchilled storage of Atlantic salmon muscle(Salmosalar)[J]. Journal of Food Science and Technology,2016,53(1):441-450.
[8]曹荣,薛长湖,刘淇,等.太平洋牡蛎在-3℃微冻贮藏过程中的品质和细菌菌相变化[J]. 南方水产,2010,6(1):49-53.
[9]蔡青文,谢晶.微冻保鲜技术研究进展[J].食品与机械,2013,29(6):248-252.
[10]洪惠,朱思潮,罗永康,等.鳙在冷藏和微冻贮藏下品质变化规律的研究[J].南方水产科学,2011,7(6):7-12.
[11]刘美华,陈丽娇,童金华,等.微冻保鲜在水产品中的应用[J].福建农机,2003,24(4):21-22.
[12]王倩,孙晓红,蓝蔚青,等.保鲜冰在水产品保藏中的应用研究进展[J].食品与机械,2016,32(3):226-230.
[13]胡玥,吴春华,姜晴晴,等.微冻技术在水产品保鲜中的研究进展[J].食品工业科技,2015,36(9):384-390.
[14]郭儒岳,凌建刚,叶宇飞,等.流化冰超冷却对养殖大黄鱼贮藏保鲜效果的影响[J].食品工业科技,2016,37(8):307-312.
[15]杨贤庆,侯彩玲,林婉玲,等.响应面法优化食品浸渍速冻冻结液配方[J].食品科学,2012,33(24):1-5.
[16]周宇光,付国平.食用聚丙烯酸钠的特性及应用[J].中国食品添加剂,2009,20(1):114-117.
[17]冯立品,周孟颖,张奋奋.高分子吸水树脂作为蓄冷材料的性能研究[J].化工新型材料,2012,40(7):55-56.
[18]王静.聚丙烯酸钠增稠剂的合成及工厂设计[D].广州:广东工业大学,2016.
[19]崔静. 聚丙烯酸钠分子量及其分布研究[D].天津:河北工业大学,2015.
[20].Cipolletti J C,Robertson G H,Farkas D F. Freezing of vegetables by direct contact with aqueous solutions of ethanol and sodium chloride[J]. Journal of Food Science,1977,42(4):911-916.
[21]俞静芬.淡水鱼鳙鱼的微冻与冰温保鲜技术研究[D].杭州:浙江工业大学,2007.
[22]梁昌.氯化钠对水冰点及冰融化速率的影响和实验研究[D].青岛:青岛科技大学,2014.
[23]Yue Y,Tan L,Xu Y,et al. Optimization of Combined Drying for Lettuce Using Response Surface Methodology[J]. Journal of Food Processing and Preservation,2016,40(5):1027-1037.
[24]Sin H N,Yusof S,Hamid N S A,et al. Optimization of hot water extraction for sapodilla juice using response surface methodology[J]. Journal of Food Engineering,2006,74(3):352-358.
[25]Asbchin A,Salman. Response surface methodology for cadmium biosorption onPseudomonasaeruginosa[J]. Water Science and Technology,2016,73(11):2608-2615.
Theformulaoptimizationoffreshiceforaquaticproductsbyresponsesurfacemethodology
YUANXiao-min1,2,HAOShu-xian1,*,LILai-hao1,YANGXian-qing1,LINWan-ling1,ZHAOYong-qiang1,HUANGHui1,HUXiao1
(1.South China Sea Fisheries Research Institute,Chinese Academy of Fishery Sciences,National R&D Center For Aquatic Product Processing,Key Laboratory of Aquatic Product Processing,Ministry of Agriculture,Guangzhou 510300,China; 2.College of Food Science and Technology,Shanghai Ocean University,Shanghai 201306,China)
To solve the problem of large temperature fluctuation and short cold-keeping time for aquatic products,the fresh ice formula of partial-frozen for aquatic products,such as sodium polyacrylate,sodium chloride and propanediol,were optimized on the basis of single factor experiments at the point of -3~-1.5 ℃. Box-Behnken experimental design and response surface methodology(RSM)were used to find the optimal formula. The results showed that the optimal fresh ice formula was 1.0% sodium polyacrylate,0.6% sodium chloride and 2.1% propanediol,which could keep the temperature of partial-frozen(-3~-1.5 ℃)of aquatic for 130 min. Compared with traditional fresh ice of sodium chloride,complex fresh ice could prolong for about 60 min. Therefore,fresh ice formula could keep longer low-temperature time,make the temperature more stable and be helpful for the storage and processing of aquatic products.
preservation;fresh ice;response surface methodology(RSM);formula optimization
2016-12-14
袁小敏(1991-),女,硕士研究生,研究方向:水产品加工与质量安全控制,E-mail:yuanxiaominyuan@163.com。
*通讯作者:郝淑贤(1972-),博士,研究员,研究方向:水产品加工与质量安全控制,E-mail:susanhao2001@163.com。
广东省科技计划项目(2016A020210025);国家现代农业(罗非鱼)产业技术体系建设专项(CARS-49);吉林省科技发展计划项目(20170204042NY);国家自然科学基金项目(31601533);中国水产科学研究院基本科研业务费资助(2016TS11)。
TS254.1
:A
:1002-0306(2017)12-0292-06
10.13386/j.issn1002-0306.2017.12.053

