直径≤3 cm肺磨玻璃结节的临床相关研究进展
刘耀波,冯 涛,李京玉,雷 霆
(大连医科大学附属第二医院 胸外二科, 辽宁 大连 116027 )
直径≤3 cm肺磨玻璃结节的临床相关研究进展
刘耀波,冯 涛,李京玉,雷 霆
(大连医科大学附属第二医院 胸外二科, 辽宁 大连 116027 )
近年来由于高分辨率计算机断层扫描(high-resolution CT,HRCT)的发展和普及,肺部磨玻璃结节病灶(ground glass nodules, GGNs)检出率日趋增高。而随着不断对磨玻璃结节的认识增加,处理方式也会有不同的变化。本文对直径≤3 cm的GGNs影像、数量、病理进行分类,自然生长史,年龄、吸烟史、性别、肿瘤史、家族史、影像学特性等相关危险因素及处理策略多方面进行综述,以了解其相关研究的进展状况。
磨玻璃结节;影像学;危险因素;处理策略
近些年来,因高分辨率计算机断层扫描(HRCT)的发展和普及,使得磨玻璃结节(GGNs)检出率越来越高。GGNs是肺磨玻璃样结节在影像学上的一种特征性表现,结节灶以云雾状密度增高为表现,病灶内支气管、血管束影仍能清楚的辨别,但在纵隔窗上则不能显示或只能够显示其实性部分的病灶[1]。虽然对于磨玻璃结节的认识逐渐加深,相关的研究也越来越多,但至今对于GGNs的诊疗尚没有统一的标准。大部分关于肺局灶性病变分类的相关文献均把直径≤3 cm作为区分肺部结节和肺部肿块的界限值[2]。本文将对于直径≤3 cm GGNs的相关临床研究进行综述。
1 GGNs分类
磨玻璃结节的分类可以根据影像学中实性成分、数量多少及病理学基础。在影像学中根据肺部结节实质部分是否能被完全的遮盖,它可以分为实性结节和亚实性结节(SSNs)。而亚实性结节可根据实性成份分为纯磨玻璃样结节(pGGNs)及部分实性结节[3]。部分实性结节同时也称为混合型磨玻璃结节(mGGNs)[4]。依据磨玻璃结节的数量是否≥2个,则可分为多发性磨玻璃结节和孤立性磨玻璃结节。
而在临床中,病理分类显得尤为重要。它不仅可以作为决定手术的方法的依据,还为疾病的后续治疗提供了一定的指导意义。GGNs作为影像学上的一种特征性表现,可以是炎症疾病、纤维化、非典型腺瘤性增生,或者原位腺癌、腺癌等病变[5-8]。根据良恶性质可分为良性、癌前病变、恶性。对于恶性GGNs,除个别报道证实部分GGNs为鳞癌,绝大部分为腺癌[9]。由国际肺癌研究协会、美国胸科学会以及欧洲呼吸学会(IASLC、ATS 、ERS)联合提出有关肺腺癌新分类概念,依据病理类型将其分为:非典型腺瘤样增生、原位腺癌和微浸润腺癌、浸润性腺癌[10]。新的分类为我们提供了临床工作中的诊断标准,也使得不同类型肿瘤有了更细化的区分依据,从而使治疗也更加有针对性。
2 自然生长史
许多的GGNs在随访过程中被手术切除,其自然生长史还未完全被知晓,如何对其进行处理也尚未建立统一标准[11]。而越来越多结节的发现以及更多临床的研究还是让我们对其有了更深一步的认识。磨玻璃结节是一种惰性结节,生长同实性结节相比较慢[12]。GGNs初期形态为pGGNs,后期可发展成为mGGNs[13]。这也揭示了磨玻璃结节进一步可能变为恶性的相应进展规律。而与此相关的研究在国内外也有大量报道。有研究选取了直径≤3 cm的GGNs病例进行分析,其中直径≤1 cm 69例,1.1~2.0 cm 34例,2.1~3.0 cm 5例。pGGNs 82例,实性成分1%~25%GGNs 19例,26%~50%GGNs 7例。随访平均时间4.2年,29例增大。平均增长7 mm(范围2~23 mm),所有29例增长的时间均在3年内,≤1年13例,1.1~2.0年12例,2.1~3.0年4例[14]。Kakinuma 等[15]调查了7294名参与者,通过CT进行筛查,共检测出439例直径≤ 5 mm单发的pGGN,其中1例为新发的pGGN。调查结果示45例(10.3%)(包括新发的pGGN在内)病灶变大,4例(0.9%)发展成为腺癌。在4例腺癌中,进行随访并复查CT,出现了实性成分。病灶开始有实性成分出现的平均年限为3.6年。同时,他们建议对于直径≤ 5 mm单发的pGGN应于3.5年后复查CT,观察是否有实性成分出现。Chang 等[16]评估了直径平均为5.5 mm的122例pGGNs(范围为3~20 mm)。其中有12例变大,比率为9.8%,在这12例中,有5例最大直径在5 mm以下。这12例变大GGNs的中位体积倍增时间是769 d(2.1年),其中的2例在随访中出现部分实性。最后有11例手术证实为原发性肺癌。而Kobayash等[14]评估了82例直径<3 mm的pGGNs,其中21例pGGNs变大,比率为25.6%。这21例均在3年内开始变大,其中13例出现了实性成分。这些研究的结果基本数据有所差异,不排除其它客观因素的影响,但进一步证实了纯磨玻璃结节发展到部分实性磨玻璃结节,再到部分研究中病理结果证实为恶性肿瘤的自然生长规律。
日本发表了一篇关于肺亚实性结节自然生长史的多中心临床前瞻性研究,纳入795名患者,共1229个肺亚实性结节,这些结节被分为3类:1046枚纯磨玻璃结节, 81枚异质性磨玻璃结节(HGGNs)(影像学表现特征:实性成分只在肺窗显示而纵膈窗不显示)、102枚部分实性结节。这些SSNs的直径均≤3 cm,在纵膈窗上显示的实性成分≤5 mm,平均随访时间为(4.3±2.5)年;1046枚纯磨玻璃结节中1.2%发展为异质性磨玻璃结节,而5.4%发展成为混合型磨玻璃结节;81枚异质性磨玻璃结节中16枚(19.8%)发展成为混合型磨玻璃结节。最终统计,有977枚pGGNs、78枚HGGNs、174枚mGGNs。pGGNs发展成为mGGNs平均时间为(3.8±2.0)年,HGGNs发展为mGGNs的平均时间为(2.1±2.3)年[17]。该研究中浸润性腺癌只出现在mGGNs 中。而另外一篇关于GGNs的相关研究结论认为浸润性腺癌在CT上可以为实性结节,也可以表现为pGGNs或mGGNs[18]。这需要更进一步的研究与证实。总之,了解磨玻璃结节的自然生长史对临床的诊疗有一定指导意义,结节发展的各个阶段对不同治疗方法的选择也有参考的价值。
3 相关危险因素
有研究认为肺癌的高风险因素主要包括高龄(>60岁),每天吸烟>20支,吸烟史>30年或戒烟<10年,有恶性病史等,而年龄是其独立危险因素[19]。陈康等[20]对于≤3 cm的单发的肺结节进行相关危险因素分析,通过单因素分析结果显示,患者的年龄、吸烟量对肿瘤性质的鉴定在统计学上有显著性意义;而民族、性别、既往吸烟史、肿瘤史、家族史、临床症状无统计学意义。多因素分析结果示患者年龄、病灶大小是其独立危险因素。
Kim等[11]则对既往行肺切除术患者GGNs调查研究。调查选取了肺术后行CT检查有GGNs的患者92例,共有GGNs 139个,分析了GGNs大小、实性成分、多发性、吸烟和恶性肿瘤病史对于GGNs的增长的影响。平均随访时间为44.4个月,该研究认为在这些因素中GGNs的增长只与实性成分有关(P<0.01)。Lee等[21]对于亚实性结节(实性成分≤5 mm)进行了相关研究,研究共纳入213名患者,共213枚SSNs,研究认为对于亚实性结节,肺癌史、部分实性、结节直径大小是结节变大的重要影响因素,而病灶直径大小是pGGNs的独立危险因素;对于mGGNs,肺癌史是结节变大的重要因素。而相对于pGGNs>或=10 mm、mGGNs>或=8 mm的结节病灶更易变大。有相关研究认为,通过多因素分析年龄≥65岁、初始直径>10 mm、磨玻璃影(GGO)含有实性成分为主要危险因素[22]。而Cho等[23]对GGNs相关研究中多因素分析结果示年龄≥65岁,初始大小≥8 mm,实性成分、支气管空气征是GGNs增长的独立风险因素。
Fan等[24]在研究肺癌相关因素中,针对GGNs影像学特征得出分叶征、毛刺征、边缘模糊、边界不整、充气征、胸膜凹陷征、血管集束征等在恶性GGNs中所占比例要大于良性。分叶征、边缘形态及胸膜凹陷是恶性GGNs的独立危险因素,其中边界清楚但边缘不规整是恶性可能的最重要危险因素。
4 GGNs与PET/CT检查
正电子发射断层显像(PET/CT)则可以通过对病灶FDG摄取量和代谢判断良恶性提供重要的参考。
Higashi等[25]对于<3 cm肺腺癌中研究中认为具有实性成分和PET/CT提示代谢增高是不良预后的相关因素。有研究显示PET/CT对于磨玻璃影≤50%、含实性成分≥10 mm、直径大的肿瘤标准化摄取最大值(SUVmax)越高,其恶性程度也越高[26]。Fleischner学会则建议8~10 mm的部分实性GGNs可进行PET/CT检查,从而更准确评估预后[27]。但由于以GGNs为表现的恶性组织密度比较低,同纯实性的恶性病灶相比SUVmax更低,其与正常的肺组织之间无明显SUV 值差异。Hu等[28]认为PET/CT检查中,支气管肺泡癌(BAC)相对于其它类型肺癌FDG 摄取量显著降低,假阴性率可达60%。同时PET/CT检查费用相对比较昂贵,对于一般家庭来说经济负担比较大。因此运用PET/CT检查GGNs有一定的局限性。
5 处理策略
对于怀疑为恶性的GGNs需要行手术切除,但是最后有20%~25%切除后证明是良性的[29]。如何更好的对不同类型的GGNs进行处置,随访观察还是行手术治疗的判断,还具有一定困难。
2016年8月,由NCCN(National Comprehensive Cancer Network)发表了2017年第1版肺癌筛查指南。并作一相关治疗流程图,见图1~2。
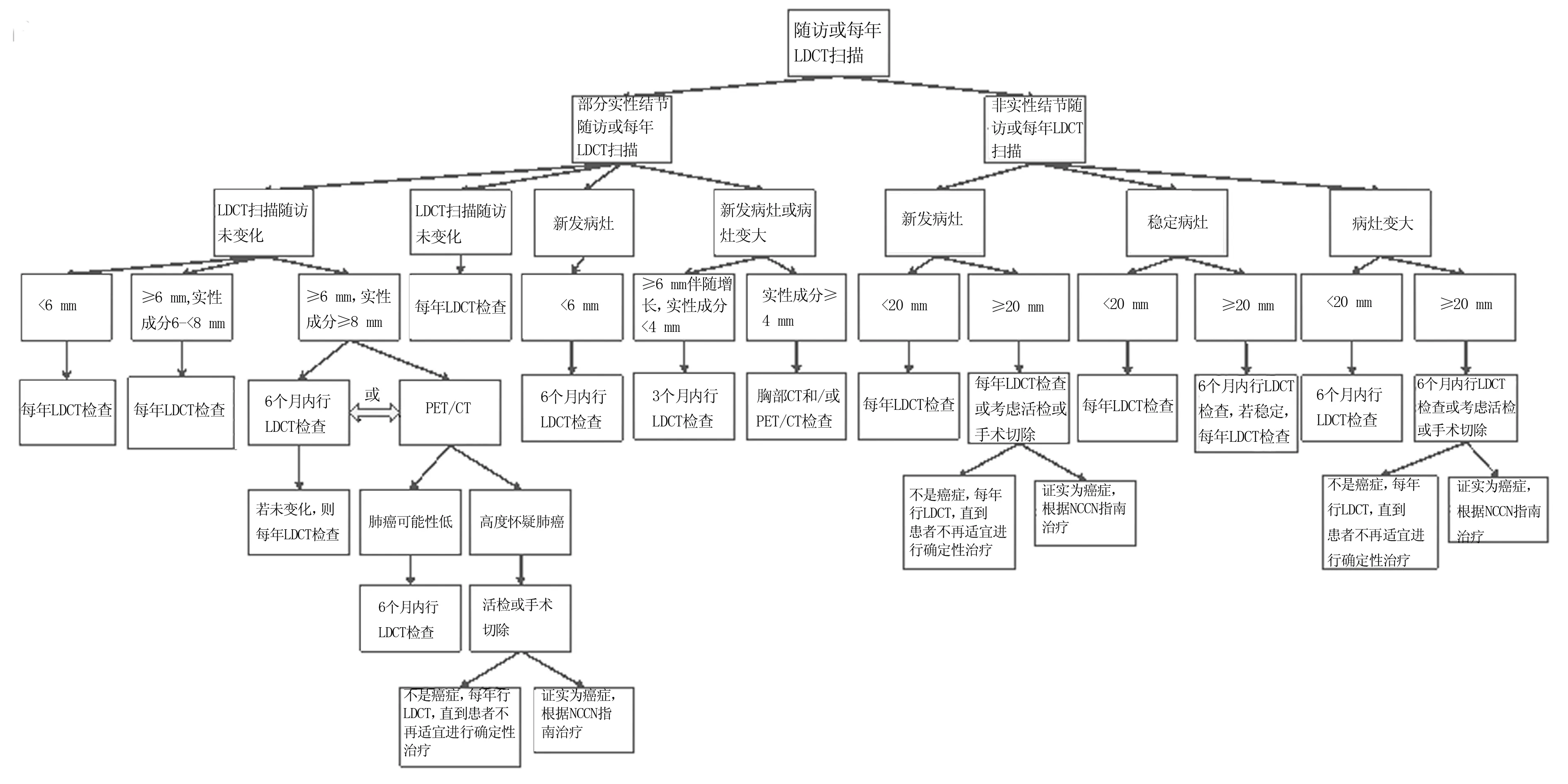
图2 随访或每年低剂量CT(LDCT)检查[30]Fig 2 Follow-up or annual low dose CT (LDCT) [30]
患者行低剂量CT随访或每年低剂量CT检查时,怀疑感染或炎症病灶时,则在1~3个月内进行复查,若变小,3~6个月内再次复查以明确消失或稳定不变。而对于多发pGGNs、mGGNs,则依据最大结节的测量结果进行处理[30]。NCCN指南为不同阶段磨玻璃结节的临床治疗提供了更加详细的科学、规范流程,具有很大的指导意义。
Travis等[10]认为对于pGGNs病理结果为附壁样生长的原位腺癌和以附壁生长为主但≤5 mm的微浸润腺癌,行根治手术切除后有100%或接近于100%的5年生存率。对于此类的患者如进行早期的手术治疗,患者便可以从中得到极大的收益。而近些年一些精准治疗开始用于临床,同过CT检查观察其变化联合更深入的分子学变化更有助于找到一个合理处理方式[31]。在越来越多基因靶向治疗中,EGFR、ALK、p53、HER2、KRAS及ROS1等基因在肺腺癌研究比较多,但在磨玻璃结节中EGFR及ALK的相关研究相对常见[32]。有相关文献指出以磨玻璃结节为主的肺腺癌经常有表皮因子受体(EGFR)突变,实性成分的增加与P53的改变有关[33]。靶向治疗在基因层面阻断疾病的发展机制,从根本上解决疾病的问题,显示了一定的优势,同时也减少了手术的痛苦。但这种治疗尚未成熟,有潜在的未知风险,且目前的靶向治疗费用较昂贵。这有待于进一步研究和认识。
6 存在的问题及展望
GGNs的检出越来越多,根据指南指导意见同时结合我国情况,综合考虑患者的危险因素、影像学特点、GGNs生长变化情况、双肺多发结节等选择合理的处理方式。对于手术的患者,胸腔镜逐渐普及应用在一定程度上减少了患者的创伤,使得越来越多的患者易于接受切除术。而部分实性的GGNs可能存在淋巴结转移情况,根据术中快速冰冻检查选择最优化手术方案,使患者获得良好的收益。但在实际临床工作中,如何准确的判断其良恶性、把握处理时机都还没有完全统一的标准。靶向治疗的新领域开拓,其更加精准的治疗与潜在风险,都还需要进一步的探索。
[1] Suzuki K, Koike T, Asakawa T, et al. A prospective radiologicalstudy of thin-section computed tomography to predict pathologicalnoninvasiveness in peripheral clinical IA lung cancer (Japan Clinical Oncology Group 0201) [J]. Thorac Oncol, 2011, 6(4):751-756.
[2] 高丰,葛虓俊,滑炎卿.肺磨玻璃结节的CT分类及鉴别诊断研究 [J]. 国际医学放射学杂志,2012,35(1):47-49,58.
[3] Henschke CI,Yankelevitz DF,Miacheva R,et al.CT screening for lung cancer:frequency and significance of part-solid and nonsolid nodules [J].AJR,2002,178(5):1053-1057.
[4] Godoy MC, Naidich DP. Overview and strategic management of subsolid pulmonary nodules [J]. Thorac Imaging, 2012, 27(4): 240-248.
[5] Nakata M, Saeki H, Takata I, et al. Focal ground-glass opacity detected by low-dose helical CT [J]. Chest,2002,121(5):1464-1467.
[6] Kodama K, Higashiyama M, Yokouchi H, et al. Natural history of pure ground-glass opacity after long-term follow-up of more than 2 years [J]. Ann Thorac Surg,2002,73(2):386-392.
[7] Kim TJ, Goo JM, Lee KW, et al. Clinical, pathological and thin-section CT features of persistent multiple ground-glass opacity nodules: comparison with solitary ground-glass opacity nodule [J]. Lung Cancer,2009,64(2):171-178.
[8] Nakajima R, Yokose T, Kakinuma R, et al. Localized pure ground-glass opacity on highresolution CT: histologic characteristics [J]. J Comput Assist Tomogr,2002,26(3):323-329.
[9] Sakaizawa T, Yoshizawa A, Nishimura H, et al. A case of pulmonary squamous cell carcinoma revealed ground glass opacity on computed tomography [J]. Thorac Oncol, 2015, 10(8): 1229-1230.
[10] Travis WD,Brambilla E,Noguchi M,et al. International Association for the Study of Lung Cancer/American Thoracic Society/European Respiratory Society: international multidisciplinary classification of lung adenocarcinoma: executive summary [J].Proc Am Thorac Soc,2011,8(5):381-385.
[11] Kim HS, Lee HJ, Jeon JH, et al. Natural History of Ground-Glass Nodules Detected on the Chest Computed Tomography Scan After Major Lung Resection [J] . Ann Thorac Surg,2013,96(6):1952-1957.
[12] Ost DE, Gould MK. Decision making in patients with pulmonary nodules [J].Am J Respir Crit Care Med, 2012, 185(4): 363-372.
[13] 王群,蒋伟,奚俊杰.肺部多发磨玻璃影的外科治疗 [J].中国肺癌杂志,2016,19(6):355-358.
[14] Kobayashi Y, Fukui T, Ito S, et al. How long should small lung lesions of ground-glass opacity be followed? [J].Thorac Oncol,2013,8(3):309-314.
[15] Kakinuma R, Muramatsu Y, Kusumoto M, et al. Solitary Pure Ground-Glass Nodules 5 mm or Smaller: Frequency of Growth [J]. Radiology,2015,276(3):873-882.
[16] Chang B, Hwang JH, Choi YH, et al. Natural history of pure ground-glass opacity lung nodules detected by low-dose CT scan [J]. Chest, 2013,143(1):172-178.
[17] Kakinuma R, Noguchi M, Ashizawa K, et al. Natural history of pulmonary subsolid nodules: a prospective multicenter study [J]. Thorac Oncol, 2016, 11(7):1012-1028.
[18] Godoy MC, Sabloff B, Naidich DP. Subsolid pulmonary nodules: imaging evaluation and strategic management [J]. Curr Opin Pulm Med, 2012,18(4):304-312.
[19] 王涛,陈保俊.肺部≤1.0cm亚厘米结节的临床诊疗策略 [J].中华胸心血管外科杂志, 2012,28(7):387-389.
[20] 陈康,努尔兰·阿汗,马金山.孤立性肺结节的危险因素分析[J/CD].中华临床医师杂志:电子版,2014,8(4): 2602-2607.
[21] Lee JH, Park CM, Lee SM,et a1. Persistent pulmonary subsolid nodules with solid portions of 5 mm or smaller: Their natural course and predictors of interval growth [J]. Eur Radiol,2016,26(6):1529-1537.
[22] Lee SW, Leem CS, Kim TJ, et al. The long- term course of ground-glass opacities detected on thin-section computed tomography [J]. Respir Med, 2013,107(6):904-910.
[23] Cho J, Kim ES, Kim SJ,et al. Long-term Follow-up of Small Pulmonary Ground-Glass Nodules Stable for 3 Years: Implications of the Proper Follow-up Period and Risk Factors for Subsequent Growth [J]. Thorac Oncol,2016,11(9):1453-1459.
[24] Fan L, Liu SY, Li QC, et al. Multidetector CT features of pulmonary focal ground-glass opacity: differences between benign and malignant [J]. Br J Radiol,2012, 85(1015): 897-904.
[25] Higashi K, Sakuma T, Ito K, et al. Combined evaluation of preoperative FDG uptake on PET, ground-glass opacity area on CT, and serum CEA level: identification of both low and high risk of recurrence in patients with resected T1 lung adenocarcinoma [J]. Eur J Nucl Med Mol Imaging,2009, 36(3): 373-381.
[26] Pala K, Serwotka A, Jeleń F, et al. Tumor -specific hyperthermia with aptamer -tagged superparamagnetic nanoparticles [J]. Int J Nanomedicine, 2014,9:67-76.
[27] Naidich DP, Bankier AA, Macmahon H, et al. Recommendations for the management of subsolid pulmonary nodules detected at CT: a statement from the Fleischner Society [J]. Radiology, 2013, 266(1): 304-317.
[28] Hu R,Ma S,Li H,et al.Effect of magnetic fluid hyperthermia on lung cancer nodules in a murine model [J].Oncol Lett,2011,2(6):1161-1164.
[29] Godoy MCB, Naidich DP. Subsolid pulmonary nodules and the spectrum of peripheral adenocarcinomas of the lung: recommended interim guidelines for assessment and management [J].Radiology,2009,253(3):606-622.
[30] Wood DE. National Comprehensive Cancer Network(NCCN) Clinical Practice Guidelines for Lung Cancer Screening[J]. Thorac Surg Clin, 2015,25(2):185-197.
[31] Aoki T.Growth of pure ground-glass lung nodule detected at computed tomography [J]. J Thorac Dis,2015,7(9):E326-E328.
[32] 李镭,刘丹,朱盈盈,等.肺磨玻璃结节临床研究进展 [J].中国肺癌杂志,2016,19(2):102-107.
[33] Aoki T, Hanamiya M, Uramoto H, et al. Adenocarcinomas with predominant ground-glass opacity: correlation of morphology and molecular biomarkers [J]. Radiology, 2012,264(2):590-596.
Clinical progress of pulmonary ground glass nodules of 3 cm or less in diameter
LIU Yaobo, FENG Tao, LI Jingyu, LEI Ting
(DepartmentofThoracicSurgery,theSecondAffiliatedHospitalofDalianMedicalUniversity,Dalian116027,China)
In recent years,due to the high-resolution computed tomography (HRCT) development and extensive application, the relevance ratio of ground glass nodules (GGNs) is rising. With the further understanding of the grinding glass nodules, the treatment will be different. We reviewed GGNs (≤3 cm) imaging and pathological classification, natural history, related risk factors (such as age,smoking history, gender, tumor history, family history), and the treatment strategy by analyzing the related literature at home and abroad.
ground glass nodules;imaging;risk factors; treatment strategies
刘耀波(1990-),男,硕士研究生。E-mail:18842822069@163.com
雷 霆,主任医师。E-mail:1292322786@qq.com
10.11724/jdmu.2017.03.20
R655.3
A
1671-7295(2017)03-0300-05
刘耀波,冯涛,李京玉,等.直径≤3 cm肺磨玻璃结节的临床相关研究进展[J].大连医科大学学报,2017,39(3):300-304.
2016-12-12;
2017-05-10)

