胆管内双极射频消融联合支架植入术治疗恶性胆管梗阻的研究
余辉, 席玮, 武贝, 陆游, 陆逸, 陈世晞, 陈骏
作者单位: 210009 江苏 南京,江苏省肿瘤医院(江苏省肿瘤防治研究所,南京医科大学附属肿瘤医院) 介入科
胆管内双极射频消融联合支架植入术治疗恶性胆管梗阻的研究
余辉, 席玮, 武贝, 陆游, 陆逸, 陈世晞, 陈骏
目的 探讨经皮肝穿刺胆管腔内双极射频消融联合支架植入术治疗恶性胆管梗阻的可行性、安全性及临床疗效。方法 分析江苏省肿瘤医院2012年3月至2016年1月27例经皮肝穿刺治疗恶性胆管梗阻患者临床资料,其中9例行经皮肝穿刺胆管内射频消融联合内支架置入术(胆管射频消融组),18例行单纯内支架置入术(单纯胆管支架组)。观察手术安全性、并发症及近期疗效情况。采用Kaplan-Meier方法比较两组患者的支架通畅率及患者生存时间。结果 27例患者均顺利完成手术。胆管射频消融组手术操作时间平均58.6 min(42.0~70.0 min),较单纯胆管支架组平均手术操作时间45.0 min(35.0~60.0 min)有所增加(P=0.003)。两组患者术中均无并发症发生。术后两组患者的胆管感染、腹痛、恶心呕吐等并发症发生率比较,差异无统计学意义。两组患者术后血清胆红素、转氨酶均明显改善。治疗后3个月胆管射频消融组胆管支架通畅率为100%(8/8),单纯胆管支架组为50%(7/14),P=0.022;6个月时分别为100%(6/6)和0,两组比较,P=0.036。胆管支架中位通畅时间,胆管射频消融组为189 d(Q1,92 d;Q3,279 d),单纯胆管支架组为87 d(Q1,82 d;Q3,161 d),两组比较,P= 0.001。在治疗后6个月,胆管射频消融组生存率为66.7%(6/9),单纯胆管支架组为11.1%(2/18),两组比较,P=0.006。9个月生存率分别为33.3%(3/9)和0,两组比较,P=0.029。患者中位生存时间胆管射频消融组189 d(Q1,100 d;Q3,279 d),单纯胆管支架组118 d(Q1,96 d;Q3,171 d),两组比较,P=0.028。结论 经皮肝穿刺胆管腔内射频消融联合支架植入治疗恶性胆管梗阻安全可行,临床疗效优于单纯支架置入术,可延长支架的通畅期和患者的生存期。
癌; 导管消融术; 支架; 恶性胆管梗阻; 双极射频
经皮肝穿刺胆管引流(percutaneous transhepaticcholangialdrainage,PTCD)联合支架植入术是治疗恶性胆管梗阻的常用手段[1]。支架植入后6~8个月,再狭窄的发生率可达50%[2]。因此,如何控制肿瘤进展,延长支架通畅时间并改善患者生存质量有着重要的意义。胆管腔内射频消融术(radiofrequency ablation,RFA)是在胆管梗阻部位植入支架的同时行肿瘤的射频消融治疗,有望延长支架再狭窄的发生时间。本研究初步探讨胆管腔内射频消融治疗恶性梗阻性黄疸的安全性和可行性,并观察其临床疗效。
1 资料与方法
1.1 一般资料 收集南京医科大学附属肿瘤医院2012年3月至2016年1月收治的27例胆管恶性梗阻性黄疸患者的临床资料(表1)。9例行经皮肝穿刺胆管造影引流支架植入术,同时行胆管腔内射频消融术为胆管射频消融组。18例只行经皮肝穿刺胆管造影引流支架植入术为单纯胆管支架组。
1.2 手术方法 患者平卧,心电监护下,常规消毒术区,2%利多卡因局麻后在DSA机(Phi1ips FD20)透视下采用美国Cook公司PTBD套装经皮肝穿刺胆管造影,明确胆管狭窄或梗阻部位、范围及程度。①射频消融组:患者经交换导丝通过狭窄病变段置入HabibTMEndo HPB双极射频消融导管(英国Emcision公司),设定射频发生器(RITA Model 1500X,美国Angio Dynamics公司)功率为8~10 W,局部消融温度为60 ℃,每一部位的单次消融设置时间为25~60 s,停止60 s后移动导管。根据造影结果,消融治疗从病变远端开始,保证消融范围覆盖病变全长。射频消融后行胆管内自膨式镍钛记忆合金支架植入(Bard E-Luminexx Vascullar stent,德国)。②单纯胆管支架组:患者不做射频消融治疗,其余操作同上。术后予以抗感染、止血、保肝、对症、支持等治疗。
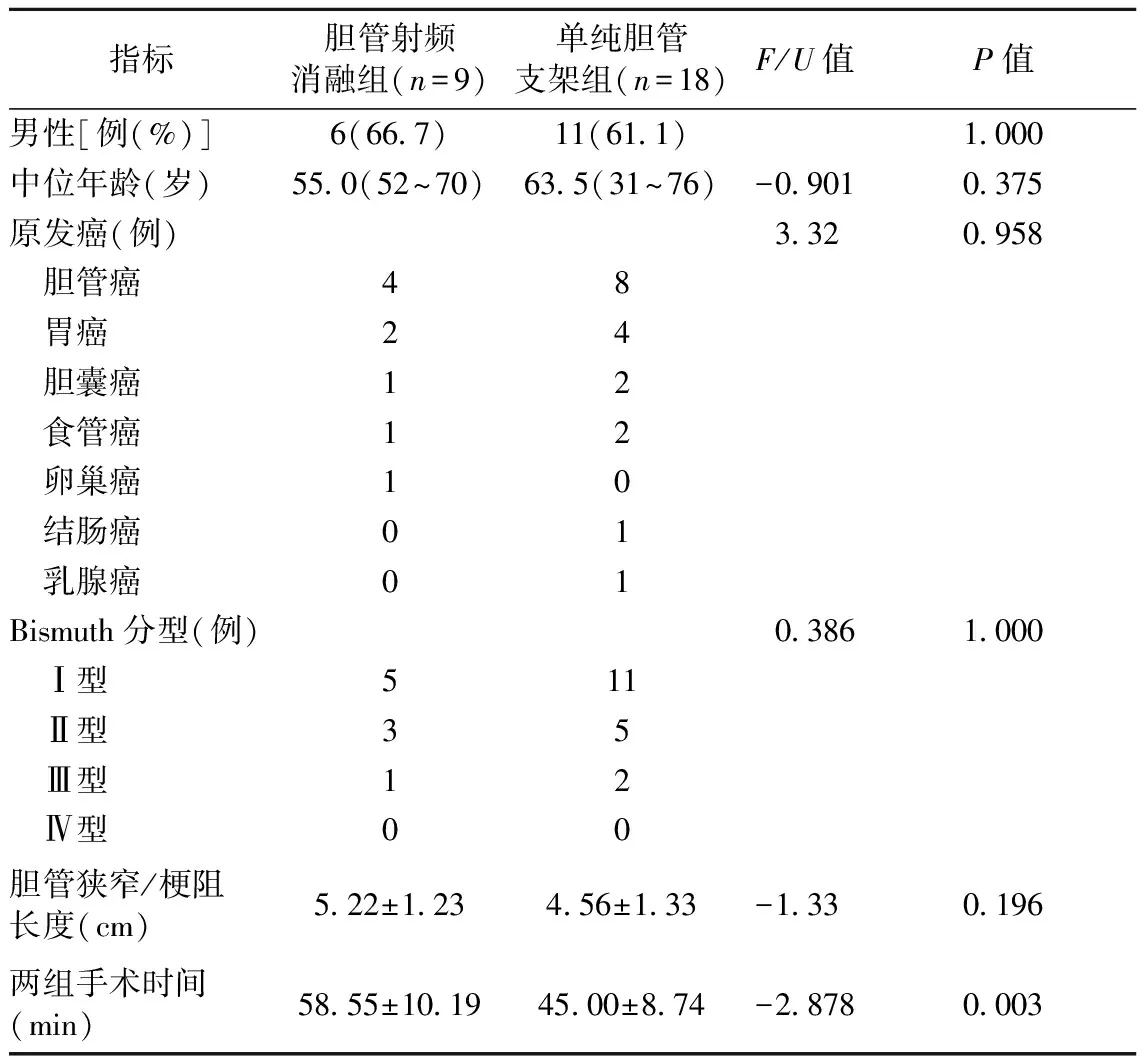
表1 胆管射频消融组和胆管单纯支架组患者一般资料
注:Fisher精确检验或Mann-WhitneyU检验
1.3 疗效评价与随访 采取电话随访及门诊或住院复查的方法了解患者生存情况,定期复查肝功能(术前,术后第7天、14天及术后1个月),结合影像学检查(经引流管胆管造影、肝胆超声、上腹CT、MR检查),观察胆管支架通畅及支架移位或再阻塞等情况。1.4 统计学方法 数据采用SPSS 19.0统计分析软件,两组间基线资料及计数资料采用Fisher精确检验,计量资料采用中位数(25%,75%)表示,两组间比较采用Mann-WhitneyU检验,同组治疗前后采用Wilcoxon符号秩检验。两组患者生存率及支架通畅率采用Kaplan-Meier法及log-rank检验。P<0.05为差异有统计学意义。
2 结果
2.1 手术情况 胆管射频消融组9例均成功接受经皮肝穿刺胆管内射频消融联合内支架植入术治疗,造影显示胆管狭窄或梗阻的平均长度为5.2 cm(3.0~6.5 cm)。根据胆管狭窄或梗阻长度行分段RFA。消融功率平均8.2 W(8.0~10.0 W),单次消融平均时间45.6 s(25.0~60.0 s),消融总持续时间平均166.7 s(75.0~300.0 s)。每例平均消融3.6次(3~5次),有效消融长度平均6.7 cm(4.0~8.0 cm)。射频消融治疗后复查胆管造影可见胆管不规则狭窄消失,边缘光整,胆管恢复通畅,对比剂可缓慢流入十二指肠(图1)。手术操作时间平均58.6 min(42.0~70.0 min)。胆管消融后均放置胆管支架(自膨式金属支架),其中3例为胆管支架再堵塞,消融后支架再通(图2),6例放置支架后使用球囊扩张。
单纯胆管支架组18例患者中,共放置自膨式金属胆管支架18个,其中8例放置支架后使用球囊扩张,平均手术时间45.0 min(35.0~60.0 min),短于胆管射频消融组(P=0.003)。
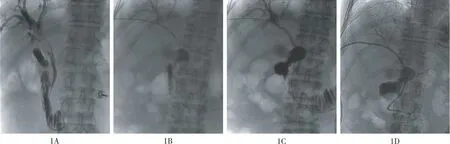
图1 患者男,70岁,肝门部胆管癌,经皮肝穿刺胆管射频消融治疗过程影像图1A:胆管造影显示肝门部胆管狭窄;1B:导丝通过狭窄段并分段行胆管内双极导管射频消融;1C:胆管射频消融后置入自膨式金属支架;1D:置入8.5F胆管内外引流管

图2 患者男,54岁,胃癌手术并化疗后,胆管支架内再狭窄行经皮肝穿刺胆管射频消融治疗过程影像图2A:胆管支架置于胆总管狭窄处;2B:胆管支架内再狭窄;2C:支架内狭窄处分段行胆管内双极导管射频消融;2D:射频消融后狭窄消除,胆管支架再通
2.2 手术并发症 两组患者术中均无特殊不适,心电监护未见异常。胆管射频消融组患者术后出现胆管感染3例(3/9),疼痛5例(5/9),恶心呕吐3例(3/9)。单纯胆管支架组患者术后出现胆管感染4例(4/18),疼痛4例(4/18),恶心呕吐2例(2/18)。两组并发症比较,差异无统计学意义(均P>0.05)。所有并发症经对症处理后缓解,未出现胆管出血、穿孔、胆漏、胰腺炎等严重并发症。
2.3 实验室指标 27例恶性梗阻性黄疸患者介入治疗前后各项生化指标见表2。治疗1、2周及1个月后,两组患者血清胆红素、直接胆红素、丙氨酸转氨酶(ALT)、天冬氨酸转氨酶(AST)水平均较术前逐渐降低,其中治疗前后血清胆红素、直接胆红素比较,差异有统计学意义(P<0.05),且胆管射频消融组较单纯胆管支架组降低更为明显,两组比较,差异有统计学意义(均P<0.05)。两组患者ALT水平,除胆管射频消融组治疗后7 d时与治疗前比较,差异无统计学意义外,其余差异均有统计学意义(P<0.05),胆管射频消融组较单纯胆管支架组降低更明显。同组患者AST水平治疗前后比较,差异均有统计学意义(P<0.05);两组间比较,除治疗后1个月以外,差异均有统计学意义(P<0.05)。白蛋白水平在治疗后略有降低,在胆管射频消融组治疗后7 d及单纯胆管支架组治疗后14 d与治疗前比较,差异有统计学意义(P<0.05),但两组比较,差异无统计学意义。
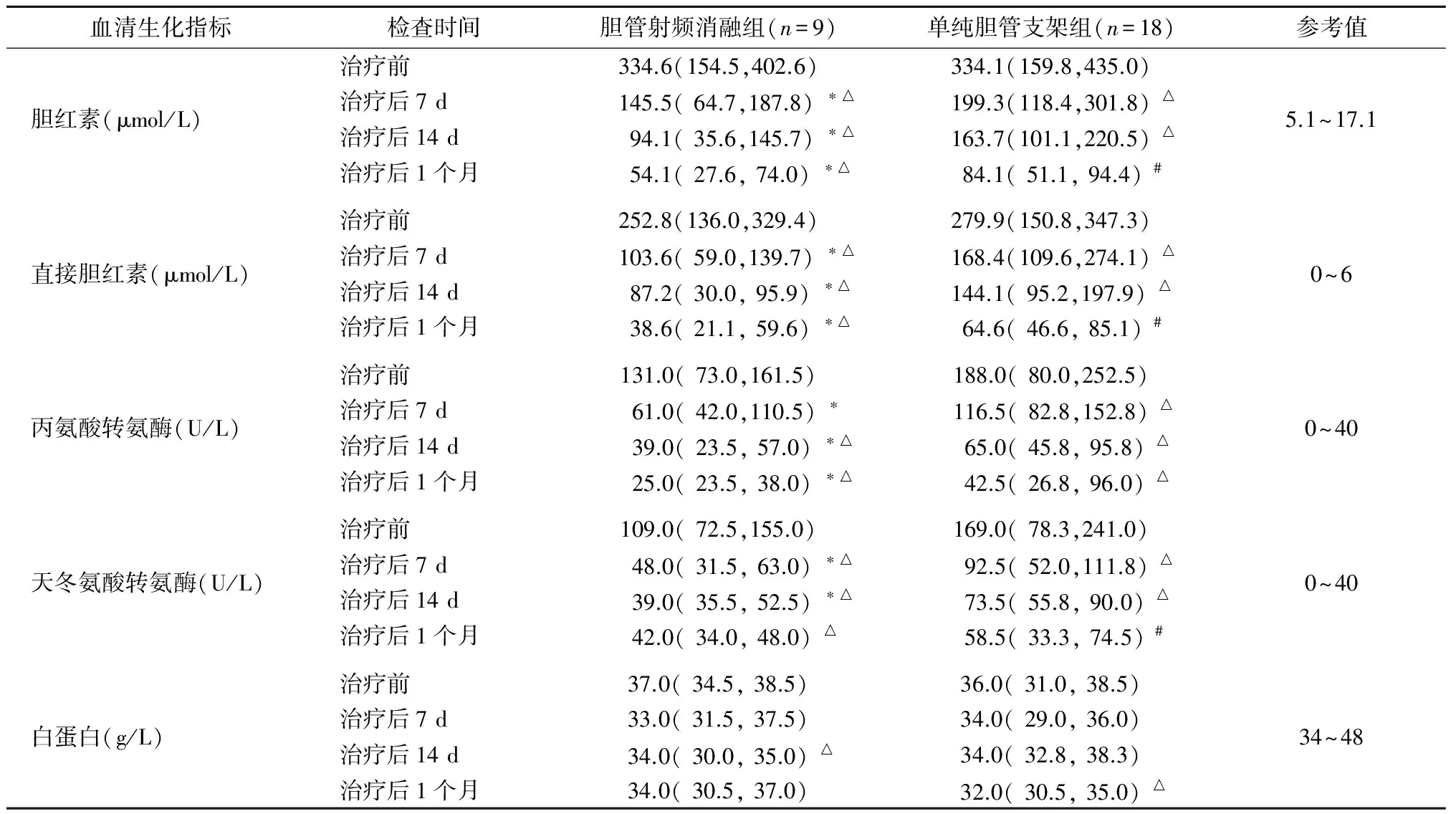
表2 胆管射频消融组和单纯胆管支架组患者治疗前后血清生化指标比较[中位数(25%,75%)]
注:Mann-WhitneyU检验(两组间比较);Wilcoxon符号秩检验(同组间治疗前后比较)。*:与对照组比较,P<0.05;△:与治疗前比较,P<0.05;#:与治疗前比较,P<0.001
2.4 支架通畅情况及患者生存时间 两组患者胆管支架通畅率见表3。两组患者胆管支架中位通畅率在治疗后3个月及6个月时比较,差异有统计学意义(P<0.05)。胆管支架中位通畅时间,胆管射频消融组为189 d(Q1,92 d;Q3,279 d,范围 42~289 d),单纯胆管支架组为87 d(Q1,82 d;Q3,161 d,范围 77~177 d),两组比较,差异有统计学意义(P=0.001)。两组患者支架通畅时间曲线见图3。
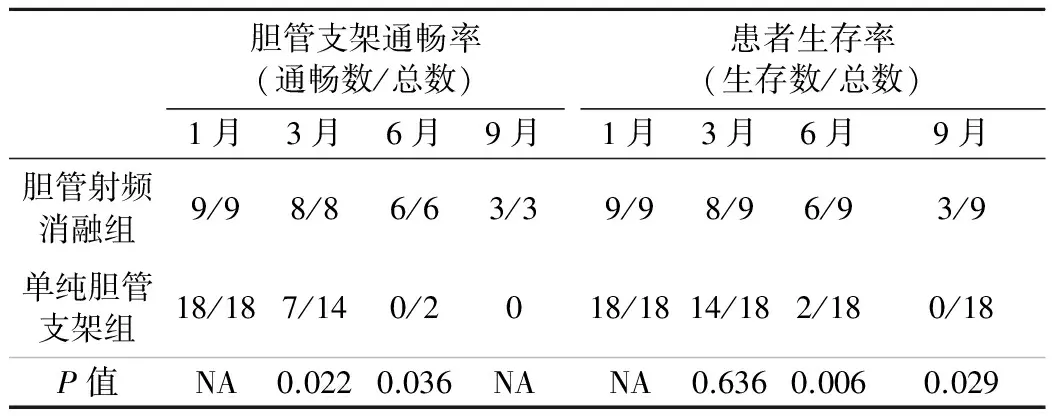
表3 胆管射频消融组和单纯胆管支架组患者胆管支架通畅率及生存率的比较
注:Fisher精确检验

图3 胆管射频消融组和单纯胆管支架组患者胆管支架通畅曲线(Kaplan-Meier法)
所有患者均定期随访直至死亡。两组患者治疗30 d内无1例死亡,患者最终死于肿瘤严重消耗或多器官功能衰竭。在随访期内,胆管射频消融组患者血清胆红素等指标无升高。两组患者生存率见表3,两组患者在治疗后6个月(P=0.006)及9个月(P=0.029)时,两组比较,生存率差异有统计学意义。中位生存时间,胆管射频消融组是181 d(Q1,100 d;Q3,279 d,范围44~289 d),单纯胆管支架组为118 d(Q1,96 d;Q3,171 d,范围79~211 d),胆管射频消融组患者的中位生存时间比单纯胆管支架组稍长,两组比较,差异有统计学意义(P=0.028)。两组患者生存时间曲线见图4。
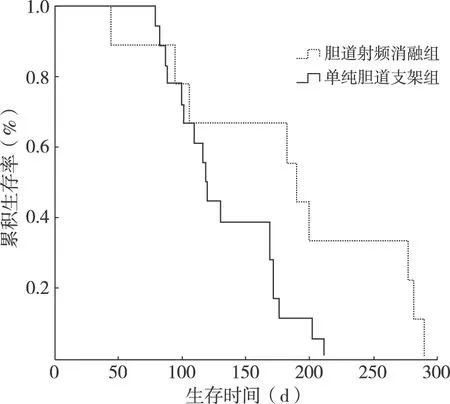
图4 胆管射频消融组和单纯胆管支架组患者生存时间曲线(Kaplan-Meier法)
3 讨论
未治疗的恶性胆管梗阻患者生存期不足3个月[3],生活质量差。PTCD联合胆管支架植入是无法切除的恶性胆管梗阻的重要治疗手段之一[2]。由于胆管支架多为裸支架,无法破坏肿瘤组织,肿瘤组织可经支架网眼向内生长挤压支架,胆管上皮过度增生及支架内沉积物的影响,使得胆管支架中位通畅时间仅为120天[4]。50%患者在6个月内出现支架再狭窄或阻塞[2-3]。
3.1 胆管射频消融术的安全性及可行性 HabibTMEndo HPB双极射频消融导管将射频能量均匀分布在导管两极,由胆管内向外传播热量,引起局部凝固性坏死[5-7]。可产生半径为5 mm,长(25±3) mm的柱形凝固性坏死区。Monga等[8]通过术后复查胆管镜证实,射频导管的确破坏了部分肿瘤组织,并使肿瘤血供减少。然而,Law等[9]对2例继发于胰腺癌的胆管梗阻患者行胆管腔内RFA及金属裸支架植入,随后均接受了胰十二指肠切除术的组织病理结果显示,圆形坏死区域深度仅1.0~1.5 mm,相对于公布的动物实验数据,坏死区明显降低。因此,导管射频消融术尽管能损毁部分肿瘤组织,但范围仍十分有限,无法达到根治性消除肿瘤的目的,仍是一项姑息性局部热疗,因此,适应证的选择有待进一步探讨,而临床疗效主要体现在治疗后胆管支架通畅时间方面。
3.2 胆管射频消融术的并发症 尽管射频消融治疗实体肿瘤已应用较长时间,但胆管内RFA治疗仍处于临床应用的初级阶段,且多为小样本的研究,因此并发症的发生率尚无准确报道[3,5,10-11]。经皮肝胆管内射频消融术的并发症与胆管支架置入的并发症相似,包括出血、疼痛、胆管感染、恶心呕吐、胆管穿孔、胆汁漏、胰腺炎等,其中疼痛、术后低热较常见[5,11]。Uberoi等[6]在833例次的介入治疗中,轻微并发症的发生率为26%,其中术后疼痛(14%)是最常见的,严重并发症的发生率为7.9%,其中败血症(3.5%)最常见。本研究有9例患者出现术后疼痛,均予以吗啡或强痛定镇疼后缓解,其中有5例(5/9)为胆管射频消融组,4例(4/18)为单纯胆管支架组,两组间差异无统计学意义。本研究中共有7例出现胆管感染,5例出现恶心呕吐,均予以抗感染、禁食、止血、对症处理后缓解,两组间差异无统计学意义。胆管感染原因可能与术后留置胆管内外引流管相关。同时,由于肿瘤组织经烧灼后坏死脱落,有可能造成支架引流不畅,从而引起胆管感染[12]。
3.3 胆管内射频消融治疗恶性胆管梗阻的疗效 Mizandari等[5]报道对39例无法手术切除的恶性梗阻性黄疸患者采取经皮经肝导管射频消融治疗,中位生存期为89.5 d(14~260 d),中位支架通畅时间为84.5 d(14~260 d)。国内崔宁等[13]对20例失去手术治疗机会的恶性胆管梗阻患者(其中2例胆管支架再堵塞),采用经皮经肝穿刺胆管路径双极射频消融治疗,患者中位生存期为144 d(13~330 d),支架通畅中位时间为90 d(13~210 d)。我们的结果显示,胆管射频消融组患者中位生存期189 d(44~289 d),支架通畅中位数为189 d(42~289 d),其胆管通畅期和存活期均优于单纯胆管支架组。
3.4 胆管射频消融对胆管支架再狭窄的防治 胆管支架技术失败的主要原因是胆管再狭窄[14],且与患者病死率明显相关[15]。既往支架再堵塞后可选择再次放置支架以疏通胆汁,但此方法效果往往不佳、且费用较高。尽管使用覆膜支架可延长支架通畅时间,但不能明显提高患者生存时间[16]。目前,胆管内射频消融术已用于胆管支架再阻塞的治疗。Pai等[17]对9例胆管支架再堵塞患者的前瞻性研究结果显示,支架通畅中位时间为102.5 d(50~321 d)。其中6例患者在临终前仍保持支架通畅,3例患者的支架分别在术后321 d、290 d和65 d出现再堵塞并再次进行了支架内射频消融术治疗。夏宁等[2]研究结果显示,支架通畅中位时间为129 d。本组有3例恶性胆管阻塞支架再堵塞患者,采用双极射频消融导管消融联合球囊扩张的方法清除支架再堵塞组织,扩张胆管行再通术,留置内外引流管冲洗引流以排除残留在胆管里坏死组织,极大地延长了胆管支架通畅时间。尽管最终所有患者因恶液质、多系统衰竭死亡,但随访期内胆管射频消融组患者血清胆红素等指标无再次升高。提示胆管内双极射频消融联合支架植入术的优势在于可反复多次疏通已经堵塞的胆管支架,从而提高胆管支架通畅时间,延长患者生存时间,此方法安全有效和经济可行。
综上所述,经皮肝穿刺胆管内射频消融联合内支架置入术是一种安全可行并有效的方法,既能对肿瘤进行部分消融从而抑制肿瘤生长,又能联合胆管支架解除晚期恶性胆管梗阻,从而改善患者肝功能状况,延长胆管支架通畅时间,延长患者生存时间。但由于胆管内射频消融破坏的肿瘤范围有限,对于适应证的选择尚待进一步探讨。同时,本研究例数较少是主要的不足。
[1] Jaganmohan S, Lee JH. Self-expandable metal stents in malignant biliary obstruction[J]. Expert Rev Gastroenterol Hepatol, 2012, 6(1): 105-114.
[2] 夏宁, 程永德, 王忠敏. 胆道支架再狭窄的介入治疗进展[J]. 介入放射学杂志, 2014, 23(1): 82-85.
[3] 席玮, 陈骏, 武贝, 等. 经皮经肝双极射频导管处理恶性胆道梗阻及胆道内支架再堵塞的初步临床观察[J]. 中华医学杂志, 2013, 93(9): 698-700.
[4] Loew BJ, Howell DA, Sanders MK, et al. Comparative performance of uncoated, self-expanding metal biliary stents of different designs in 2 diameters: final results of an international multicenter, randomized, controlled trial[J]. Gastrointest Endosc, 2009, 70(3): 445-453.
[5] Mizandari M, Pai M, Xi F, et al. Percutaneous intraductal radiofrequency ablation is a safe treatment for malignant biliary obstruction: feasibility and early results[J]. Cardiovasc Intervent Radiol, 2013, 36(3): 814-819.
[6] Uberoi R, Das N, Moss J, et al. British Society of Interventional Radiology: Biliary Drainage and Stenting Registry(BDSR)[J]. Cardiovasc Intervent Radiol, 2012, 35(1): 127-138.
[7] Krokidis M, Fanelli F, Orgera G, et al. Percutaneous palliation of pancreatic head cancer: randomized comparison of ePTFE/FEP-covered versus uncovered nitinol biliary stents[J]. Cardiovasc Intervent Radiol, 2011, 34(2): 352-361.
[8] Monga A, Gupta R, Ramchandani M, et al. Endoscopic radiofrequency ablation of cholangiocarcinoma: new palliative treatment modality(with videos)[J]. Gastrointest Endosc, 2011, 74(4): 935-937.
[9] Law R, Pai M, Baron TH, et al. The effects of endobiliary radiofrequency ablation in two patients with pancreatic cancer: Gross and microscopic findings[J]. Gastrointestinal Intervention, 2013, 2(2): 124-126.
[10] 鲁东, 吕维富, 肖景坤, 等. 经皮肝穿刺胆道腔内射频消融联合支架植入治疗恶性梗阻性黄疸(附2例报告)[J]. 介入放射学杂志, 2014, 23(7): 593-596.
[11] 何国林, 徐小平, 周陈杰, 等. 一种恶性梗阻性黄疸介入治疗的新方法-经皮肝穿刺胆道内射频消融内支架置入术[J]. 南方医科大学学报, 2011, 31(4): 721-723.
[12] 李志杰, 张洪义, 冯志强, 等. 经皮肝穿刺胆道腔内射频消融联合胆道支架治疗恶性胆道梗阻的初步研究[J]. 中华临床医师杂志(电子版), 2013, 7(12): 5292-5295.
[13] 崔宁, 李晓群. 经皮经肝双极射频消融导管恶性梗阻性黄疸20例[J]. 介入放射学杂志, 2014, 23(8): 693-697.
[14] Zacharoulis D, Lazoura O, Sioka E, et al. Habib EndoHPB: a novel endobiliary radiofrequency ablation device. An experimental study[J]. J Invest Surg, 2013, 26(1): 6-10.
[15] Ridtitid W, Rerknimitr R, Janchai A, et al. Outcome of second interventions for occluded metallic stents in patients with malignant biliary obstruction[J]. Surg Endosc, 2010, 24(9): 2216-2220.
[16] Isayama H. A prospective randomised study of “covered” versus “uncovered” diamond stents for the management of distal malignant biliary obstruction[J]. Gut, 2004, 53(5): 729-734.
[17] Pai M, Valek V, Tomas A, et al. Percutaneous intraductal radiofrequency ablation for clearance of occluded metal stent in malignant biliary obstruction: feasibility and early results[J]. Cardiovasc Intervent Radiol, 2014, 37(1): 235-240.
Clinical application of endobiliary bipolar radiofrequency ablation combined with stenting in treatment for malignant biliary obstruction
YUHui,XIWei,WUBei,LUYou,LUYi,CHENShixi,CHENJun.
(DepartmentofInterventionalRadiology,JiangsuCancerHospital,JiangsuInstituteofCancerResearch,NanjingMedicalUniversityAffiliatedCancerHospital,Nanjing210009,China)
s:CHENJun,Email: 13813939190@139.com
Objective To investigate the feasibility, safety and clinical efficacy of percutaneous transhepatic endobiliary bipolar radiofrequency ablation coupled with biliary metallic stenting for treating malignant biliary obstruction. Methods The clinical data of 27 patients with malignant biliary obstruction who underwent percutaneous transhepatic interventional therapy in Jiangsu Cancer hospital from March 2012 to January 2016 were analyzed retrospectively. Percutaneous endobiliary radiofrequency combined with metal biliary stenting were performed in nine patients(the RFA group), while the other eighteen patients
only metal biliary stenting(the stent group). The safety, procedure-related complications, and short-term clinical efficacy were investigated. Stent patency and patient survival time were compared between the two groups by Kaplan-Meier methods. Results Percutaneous transhepatic treatment was completed in all 27 patients. The average duration of operation was significantly longer in the RFA group(58.6 min, 42~70 min) than that in the stent group(45.0 min, 35~60 min,P=0.003). No immediate procedural complications occurred in patients of both groups. The incidence of postoperative complications including biliary tract infection, abdominal pain and vomiting had no significant differences. The bilirubin and transaminase were significantly improved after treatment. The patency rate for stents at 3 months after treatment was 100%(8/8) in the RFA Group, 50%(7/14) in the stent group(P=0.022), and which at 6 months after treatment was 100%(6/6) in the RFA group, 0%(0/2) in the stent group(P=0.036). The median stent patency was 189 days(quartile 1, 92 days; quartile 3, 279 days) in the RFA Group, which was significantly longer than 87 days(quartile 1, 82 days; quartile 3, 161 days) in the stent group(P= 0.001). The survival rate at 6 months after treatment was 66.7%(6/9) in the RFA group, 11.1%(2/18) in the stent group(P=0.006), and which at 9 months after treatment was 33.3%(3/9) in the RFA group, 0%(0/18) in the stent group(P=0.029). The median survival time was 189 days(quartile 1, 100 days; quartile 3, 279 days) in the RFA group, which was significantly longer than 118 days in the stent group(quartile 1, 96 days; quartile 3, 171 days)(P= 0.028). Conclusions Percutaneous transhepatic endobiliary bipolar radiofrequency ablation combined with biliary metallic stenting is feasible and safe in treating malignant biliary obstruction. Its clinical efficacy is superior to biliary stenting alone, appears to extend stent patency and patient survival.
Carcinoma; Catheter ablation; Stents; Malignant biliary obstruction; Bipolar radiofrequency ablation
江苏省“六大人才高峰”第十一批高层次人才培养入选项目(No.2014-WSW-015)
作者单位: 210009 江苏 南京,江苏省肿瘤医院(江苏省肿瘤防治研究所,南京医科大学附属肿瘤医院) 介入科
陈骏,Email:13813939190@139.com
10.3969/j.issn.1674-4136.2017.02.005
1674-4136(2017)02-0081-06
2016-11-16][本文编辑:李庆]

